博文
磁控镁释放氢气疗法的研究
||
深部组织感染,尤其是由病原菌株引起的感染,已经成为全球人类健康的一个普遍难题。深部组织感染,如与植入物相关的骨髓炎,在临床环境中呈现出重大挑战,其特征是感染和骨破坏,伴随着慢性炎症和反复的感染发作。目前,治疗组织感染的传统方法包括外科清创和给予抗菌药物。不幸的是,不规则的外科干预和不当的抗生素使用导致了对抗生素有抗药性的细菌感染的出现,甚至产生了超级细菌。最近的研究表明,外科手术本身触发了以急性炎症和因高表达活性氧物种(ROS)而导致的细胞死亡为特征的强烈宿主反应。组织中ROS的过度积累不仅引发强烈的炎症反应,使组织易感,而且抑制了内在干细胞和巨噬细胞的活动,刺激破骨细胞和骨损伤。此外,ROS水平的升高通常会引起局部不可逆的氧化损伤,导致炎症加剧和对细菌感染的易感性增加。因此,实施有效的策略来清除ROS、杀灭细菌以及随后的骨组织修复对于治疗难以愈合的骨髓炎至关重要。
气体疗法作为一种新兴的治疗模式,因其在治疗炎症相关疾病中的应用而日益受到关注。特别是氢气(H2),作为一种内源性气体,可以调节各种重要的生理和病理过程,使其在治疗炎症相关疾病(如肿瘤、炎症和感染)中有效。H2具有强大的抗氧化特性,可以有效地中和在炎症组织中高度表达的细胞毒性ROS,例如羟基自由基(•OH)。有趣的是,H2还显示出增强抗感染应用效果的促进作用。然而,由于其水溶性差,通过传统给药途径(如氢水或氢气)富集在病变组织中的H2浓度可能会低于有效清除局部积累ROS的必要水平。最近,已经开发了响应光照或超声波的新型H2供体和输送系统。例如,已开发出新型H2供体(如CaH2、镁电池)、光响应纳米材料(如PdH0.2、TiO2)和超声响应纳米材料(如Pt–Bi2S3、C3N4)。尽管超声波比激光具有更深的穿透深度,但在深层组织(如骨组织)中控制释放H2仍然充满挑战。因此,迫切需要开发新策略以实现在深层组织中按需释放H2气体。
交变磁场(AMF)作为局部治疗工具,最近受到了广泛关注,它不受组织穿透深度的限制,如磁热疗(MHT)。随着新型生物材料和生物技术的发展,由法拉第电磁感应定律产生的涡流热效应使得具有低电阻率和高导电性的宏观导体,例如镁(Mg)植入物,在AMF下能够产生感应电流加热。基于涡流效应,包括我们小组在内的几个研究团队对使用宏观金属进行肿瘤MHT进行了一系列研究工作,包括Mg植入物。令人兴奋的是,Mg作为一种相对活泼的金属,在生理环境中可以产生H2气体,其在AMF下的涡流热效应可以用来增强这一特性。此外,为了对抗抗生素耐药性,基于氧化应激损伤(例如金属离子、ROS生成)的新治疗方法受到了相当的关注和兴趣。通常,ROS的生成以实现抗菌效果与细菌生长环境相矛盾,可能会对局部组织造成二次损伤。令人兴奋的是,碱性阴离子(OH−)可以破坏大多数细菌偏好的酸性生长环境,破坏细菌膜间隙中的质子电化学梯度,并通过过度消耗H+减少ATP的合成,从而导致细菌显著减少。因此,将碱性药物引入细菌微环境可能是一种有效的消除细菌的策略,迫切需要智能地将碱性药物输送到病原菌引起的深部感染中。
在此,针对深部感染如植骨骨髓炎的局限性,应用了Mg植入物在AMF下的涡流热效应来释放H2和中和质子进行抗感染治疗和组织修复(方案1)。由于其涡流热效应,Mg植入物在AMF下表现出优异的H2生成能力,有效清除了细胞毒性ROS并扰乱了细菌感染的敏感环境。此外,释放的OH−阴离子导致碱性环境耗尽质子以抑制细菌增殖,而释放的H2进一步增强了细菌膜的通透性,并加速了OH−进入细菌内部杀死它们。这种协同的AMF诱导的H2和质子耗尽策略不仅杀死了革兰阴性和革兰阳性细菌,还有效治疗了金黄色葡萄球菌引起的脓肿和骨髓炎。在骨髓炎的情况下,从Mg植入物中释放的Mg2+为骨骼生成提供了额外的支持,从而促进了骨组织的再生和生长。总体而言,这项工作巧妙地利用了Mg植入物在AMF下的涡流热效应和化学活性,通过同时释放治疗性H2气体和功能性离子(OH−和Mg2+),逆转炎症环境并抑制细菌增殖,从而促进了感染根除和组织修复的有效干预。这种简单而有效的策略突出了治疗深部组织感染的新方法,因此为临床应用提供了有希望的途径。
本研究作者分别来自澳门苏州和四川等研究机构。
Yang N, Yang X, Cheng S, Gao X, Sun S, Huang X, Ge J, Han Z, Huang C, Wang Y, Cheng C, Cheng L. Magnesium implants with alternating magnetic field-enhanced hydrogen release and proton depletion for anti-infection treatment and tissue repair. Bioact Mater. 2024 May 10;38:374-383.
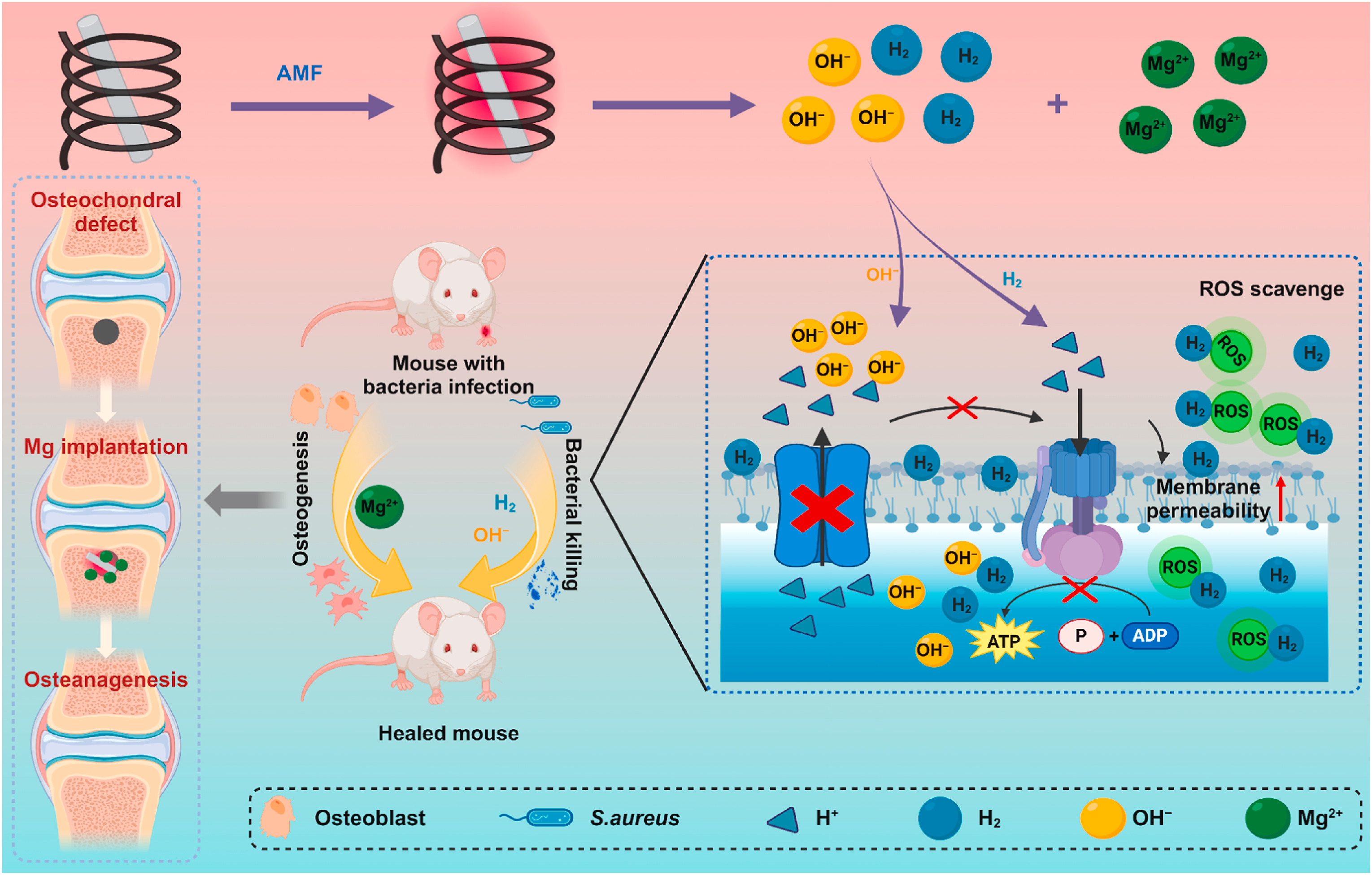
技术方案. 协同Mg介导的H2和质子耗尽疗法的示意图,用于抗感染治疗和组织修复。在AMF下,骨组织中的Mg植入物由于其优异的涡流热效应而释放治疗性气体H2和离子(OH−和Mg2+)。H2有效地清除细胞毒性ROS以抗炎,并破坏细菌的环境。OH−中和细菌微环境中的质子并抑制细菌的能量代谢。随后,Mg2+进一步促进骨组织的愈合,最终实现高效的感染治疗和组织修复。
https://blog.sciencenet.cn/blog-41174-1435232.html
上一篇:毛毛虫们能感知微弱静电电场【PNAS】
下一篇:芬太尼的成瘾由两条不同的神经通路负责