博文
[转载]放疗免疫抑制新机制:YTHDF2为关键免疫检查点
||
放射治疗是恶性肿瘤治疗的核心手段之一,但其临床疗效常受免疫抑制与肿瘤远处转移的制约,如何破解放疗诱导的免疫逃逸难题,提升放免联合治疗效果,是肿瘤免疫领域的研究热点。近日,芝加哥大学Weichselbaum教授、何川教授团队在《Journal of Experimental Medicine》发表重要研究成果,首次鉴定出 YTHDF2 作为树突状细胞(DC)中辐射诱导的新型免疫检查点,系统解析了其介导放疗抵抗与肿瘤转移的分子机制,并证实靶向抑制 YTHDF2 可显著增强放疗的抗肿瘤效果,同时提升树突状细胞疫苗的临床应用潜力,为克服放疗耐药提供了全新的可临床转化策略。

放疗可通过促进树突状细胞的抗原呈递激活CD8+T细胞的抗肿瘤免疫,却也会触发多种免疫抑制通路,导致系统性抗肿瘤免疫功能减弱。此前研究已证实RNA的N⁶-甲基腺苷(m⁶A)修饰是免疫功能的关键调控因子,其中m⁶A阅读蛋白YTHDF2主要介导mRNA降解,参与细胞周期调控、应激反应、免疫细胞分化等重要生物学过程,但其在树突状细胞的放疗应答、抗原呈递功能调控及肿瘤转移中的作用尚未明确。
同时,临床中放疗联合免疫检查点阻断疗法的疗效有限,亟需挖掘树突状细胞中全新的治疗靶点,以增强放疗的免疫激活效应。基于此,研究团队以 YTHDF2为核心研究对象,围绕 “放疗如何调控树突状细胞中YTHDF2的表达”“YTHDF2如何影响树突状细胞的免疫功能”“靶向YTHDF2能否逆转放疗诱导的免疫抑制” 三大科学问题展开系统研究。在本研究中,纽科生物有幸参与并完成了部分生物信息学的分析工作。

多维度验证YTHDF2 与放疗密切相关
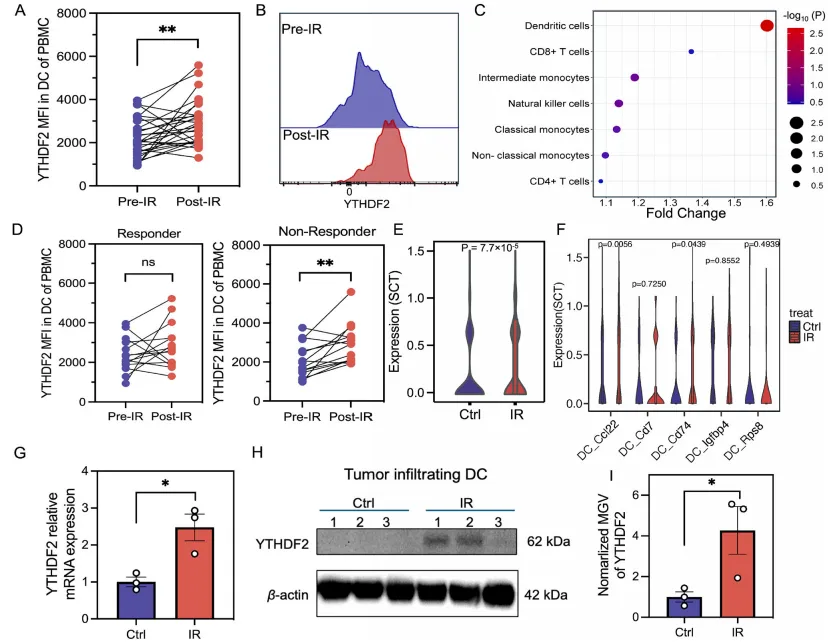
研究团队首先分析了转移性非小细胞肺癌临床试(NCT03223155)患者的活检样本,发现放疗后患者外周血DC中YTHDF2的蛋白表达水平显著升高,且这一变化远高于CD4⁺T细胞、CD8⁺T细胞、单核细胞等其他免疫细胞。
进一步分层分析显示,放疗后疾病进展的无应答患者,其DC中YTHDF2表达显著上调;而治疗有效的应答患者,YTHDF2表达无明显变化。在小鼠肿瘤模型中,单细胞RNA测序和功能实验也验证了放疗可特异性诱导肿瘤浸润DC(尤其是mregDCs和Cd74⁺DC 亚群)中YTHDF2的 mRNA和蛋白表达,且这一诱导依赖于肿瘤细胞与 DC 的直接接触及可溶性信号的共同作用。这一系列临床和预临床证据,直接将DC中YTHDF2的放疗诱导表达与肿瘤治疗失败、转移进展关联起来。
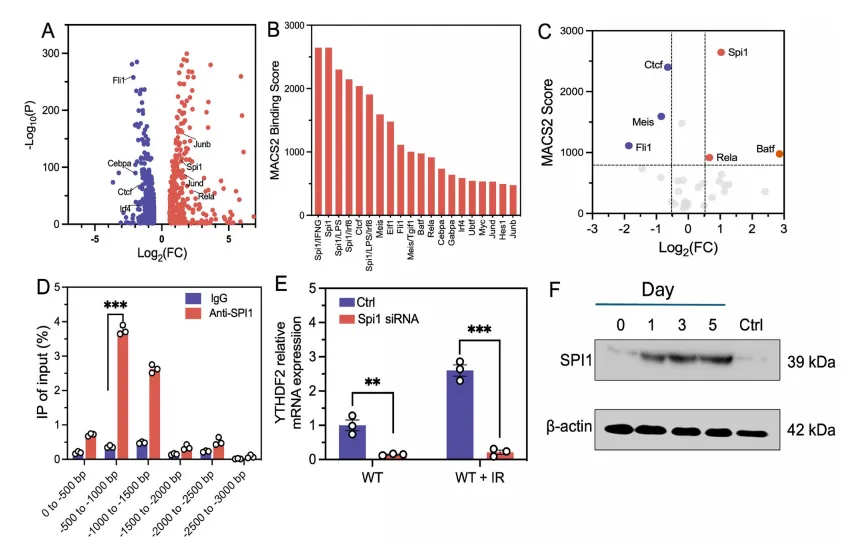
SPI1 为放疗诱导 YTHDF2 表达的关键因子
为明确放疗诱导YTHDF2表达的分子机制,研究通过RNA-seq和 ChIP-seq联合分析,鉴定出转录因子SPI1是调控YTHDF2的关键分子:放疗可时间依赖性上调DC中SPI1蛋白水平,SPI1直接结合Ythdf2启动子区(转录起始位点0.5-1.0kb),驱动其转录表达,而RELA、BATF等其他因子仅短暂结合,并非必需。
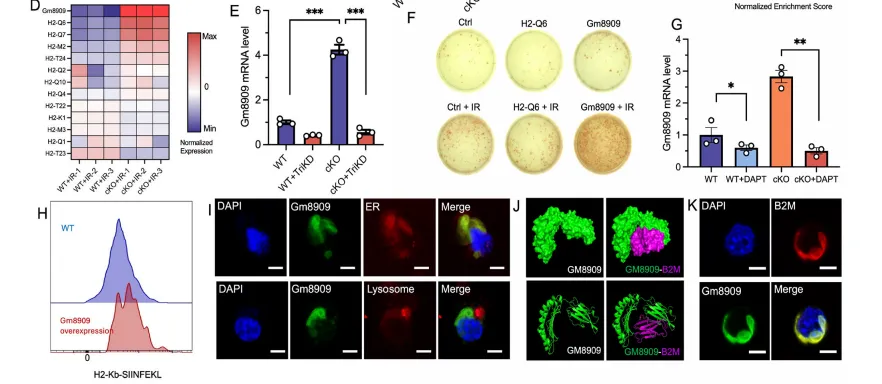
作为m⁶A修饰的核心阅读蛋白,YTHDF2的主要功能是促进m⁶A修饰的mRNA降解。研究通过RIP-seq和MeRIP-seq联合筛选,发现放疗后 YTHDF2 可特异性结合并降解Notch 信号通路的关键正调控因子 Mfng、Aph1b、Aph1c的m⁶A 修饰mRNA。这一降解直接抑制Notch信号通路激活,而Notch通路的失活进一步导致DC中MHC-I家族基因Gm8909表达下调。
Gm8909是本次研究发现的关键MHC-I分子,其定位于内质网,可与 β2微球蛋白结合形成功能性MHC-I复合物,显著增强DC的抗原交叉呈递效率。YTHDF2介导的Notch通路抑制,最终通过下调Gm8909表达,破坏DC的MHC-I交叉呈递功能,导致CD8⁺T细胞活化不足,形成肿瘤免疫抑制微环境。
DC 特异性敲除 YTHDF2 增强放疗抗肿瘤效果
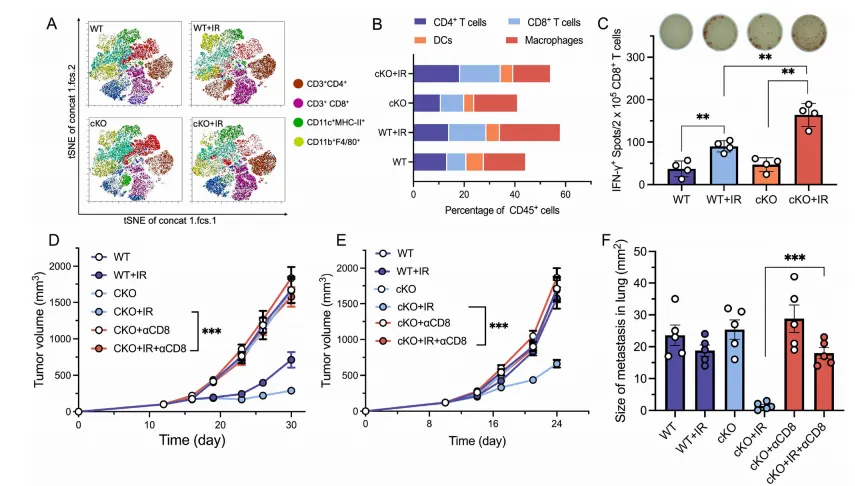
为探究 YTHDF2 在树突状细胞中的功能,研究团队构建了 CD11c-Cre介导的树突状细胞特异性 YTHDF2 条件性敲除(Ythdf2-cKO)小鼠,在MC38 结肠癌、B16F10 黑色素瘤、LLC 肺癌、KPC 胰腺癌等多种小鼠肿瘤模型中开展体内功能实验。
结果显示,无放疗时,Ythdf2-cKO 小鼠与野生型(WT)小鼠的原发肿瘤生长无显著差异;而放疗后,Ythdf2-cKO 小鼠的原发肿瘤生长被显著抑制,且小鼠生存期显著延长。在具有自发肺转移特性的LLC肺癌模型中,放疗联合DC特异性YTHDF2敲除可显著降低小鼠肺部转移灶的面积和数量,实现对远处转移的有效抑制;在KPC胰腺癌原位模型中,放疗对野生型小鼠的肿瘤无明显抑制作用,而在Ythdf2-cKO小鼠中可显著降低肿瘤负荷。
进一步的耗竭实验证实,当利用抗体耗竭CD8+T细胞后,YTHDF2敲除对放疗的增强效应完全消失,说明树突状细胞中YTHDF2的缺失通过激活 CD8+T细胞发挥抗肿瘤作用,CD8+T细胞是该效应的核心执行者。
YTHDF2-Notch-Gm8909 轴调控 DC 抗原交叉呈递
为解析 YTHDF2 调控树突状细胞免疫功能的核心分子通路,研究团队通过 RNA-seq、YTHDF2-RIP-seq 和 m⁶A-seq 联合分析,筛选出放疗下 YTHDF2 的靶基因:结合 “WT + 放疗 vs WT” 的下调基因和 “Ythdf2-cKO + 放疗 vs WT + 放疗” 的上调基因,同时纳入具有 YTHDF2 结合位点和 m⁶A 修饰的基因,最终鉴定出 86 个 YTHDF2 的直接靶基因。
基因功能富集分析发现,这些靶基因显著富集于 Notch 信号通路,其中 Mfng、Aph1b、Aph1c 为 Notch 信号通路的关键正调控因子 ——Mfng 可促进 Notch1 受体的 O - 岩藻糖基化修饰,Aph1b/c 参与 γ- 分泌酶复合物形成,介导 Notch 胞内域的切割与活化。功能实验证实,YTHDF2 以 m⁶A 依赖的方式结合并降解 Mfng、Aph1b、Aph1c 的 mRNA,缩短其半衰期;而敲除 YTHDF2 可恢复放疗后树突状细胞中这三个基因的表达,激活 Notch 信号通路,其中 Notch1-DLL1 轴为核心的配体 - 受体相互作用。
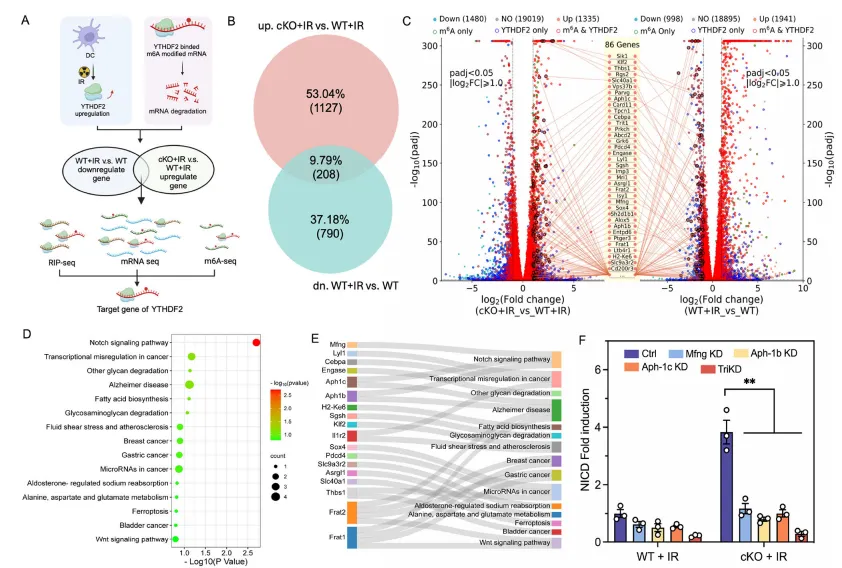
进一步研究发现,Notch 信号通路的活化可上调树突状细胞中 MHC-I 家族基因 Gm8909 的表达。Gm8909 定位于内质网,可与 β2 微球蛋白(β2M)直接结合形成功能性 MHC-I 复合物,增强抗原肽的装载与呈递效率;过表达 Gm8909 可显著增强树突状细胞的抗原交叉呈递功能,而敲低 Gm8909 则会逆转 YTHDF2 敲除对 DC 交叉呈递的增强效应。同时,研究证实 YTHDF2 的缺失不影响树突状细胞的迁移、成熟标志物表达及细胞活力,仅特异性调控抗原交叉呈递功能,明确了YTHDF2-Notch-Gm8909-MHC-I 轴是放疗下树突状细胞抗原呈递功能调控的核心通路。
基于上述机制研究,研究团队探索了靶向 YTHDF2 的临床转化价值,聚焦树突状细胞疫苗的优化与放疗的联合应用。树突状细胞疫苗是肿瘤免疫治疗的重要方向,但临床应答率较低,亟需提升其抗原呈递能力。
研究团队将 YTHDF2 敲除的树突状细胞,或经 YTHDF2 特异性抑制剂(DC-Y13–27)处理的树突状细胞制备为 DC 疫苗,瘤内注射至肿瘤荷瘤小鼠体内,结果显示:单独注射改造后的 DC 疫苗对肿瘤生长的抑制作用有限,而与放疗联合后,可显著抑制 B16F10 黑色素瘤、LLC 肺癌的原发肿瘤生长,并显著降低肺部转移负荷,其效果远优于野生型 DC 疫苗联合放疗。
同时,研究团队在人源细胞中验证了该策略的可行性:从人外周血单核细胞诱导树突状细胞,经 YTHDF2 抑制剂处理后,其对 EBV 阳性肿瘤细胞的抗原交叉呈递能力显著增强,可有效促进人 CD8+T 细胞分泌 IFN-γ,证实 YTHDF2 调控树突状细胞功能的机制在人源细胞中高度保守。此外,抑制剂对 Ythdf2-cKO 小鼠的树突状细胞无额外效应,证明其作用具有 YTHDF2 特异性。
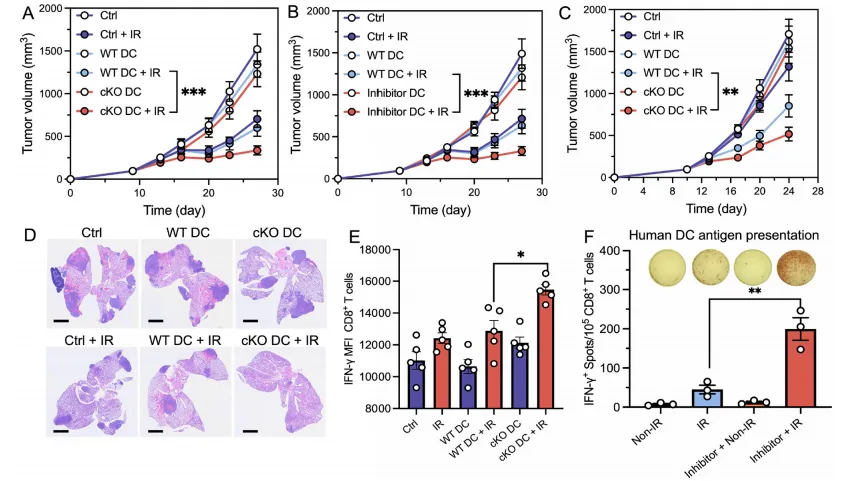
同时,研究团队在人源细胞中验证了该策略的可行性:从人外周血单核细胞诱导树突状细胞,经 YTHDF2 抑制剂处理后,其对 EBV 阳性肿瘤细胞的抗原交叉呈递能力显著增强,可有效促进人 CD8+T 细胞分泌 IFN-γ,证实 YTHDF2 调控树突状细胞功能的机制在人源细胞中高度保守。此外,抑制剂对 Ythdf2-cKO 小鼠的树突状细胞无额外效应,证明其作用具有 YTHDF2 特异性。
该研究的核心创新点在于首次将 YTHDF2 鉴定为树突状细胞中辐射诱导的新型免疫检查点,系统阐明了放疗通过 SPI1-YTHDF2-Notch-Gm8909 轴调控树突状细胞抗原交叉呈递的分子机制,填补了 m⁶A 修饰在放疗诱导 DC 免疫抑制中的研究空白。同时,该研究明确了靶向抑制树突状细胞中的 YTHDF2 可有效逆转放疗诱导的免疫逃逸,与放疗、DC 疫苗协同实现局部肿瘤控制和远处转移抑制,为肿瘤的放免联合治疗提供了全新的靶点和可临床操作的策略。
微生信助力高分文章,谷歌学术9000+
https://blog.sciencenet.cn/blog-707141-1526270.html
上一篇:[转载]【项目文章】空间转录组揭秘EBV相关淋巴瘤微环境差异
下一篇:在线绘制富集分析结果彗星图