博文
氢气缓解癌症放化疗副作用的研究【综述】
||
点评:氢气最重要的应用场景是居家,饮用氢水是普通人最好的使用方法,氢气吸入对于解决某些临床疾病非常具有潜力,氢水洗澡适合高端人群,是美容护肤的理想工具。在氢气的临床应用中,作为减少药物毒副作用是非常有价值非常值得探索的领域。10多年来,氢气在癌症化疗药物毒性对抗,放射治疗损伤等方面有大量研究,但从癌症治疗毒副作用这个角度进行文献综述的并不多见。本文是最近刚刚发表的这方面的论文综述,非常值得对氢气医学感兴趣的同事们阅读品鉴。
Hirano SI, Takefuji Y. Molecular Hydrogen Protects against Various Tissue Injuries from Side Effects of Anticancer Drugs by Reducing Oxidative Stress and Inflammation. Biomedicines. 2024 Jul 17;12(7):1591.
摘要
虽然药物治疗在癌症治疗中发挥着至关重要的作用,但许多抗癌药物,特别是具有细胞毒性和分子靶向的药物,会引起严重的副作用,这通常限制了这些药物的剂量。人们已经通过开发现有抗癌药物的衍生物、类似物和脂质体制剂以及将抗癌药物与减少副作用的物质结合使用来努力减轻这些副作用。然而,这些方法在减少副作用方面并没有取得足够的效果。氢气(H2)在这方面显示出了前景。它直接减少活性氧物种,这些物种具有很强的氧化能力,并间接通过调节基因表达发挥抗氧化、抗炎和抗凋亡作用。它在各种疾病的临床应用已在全球范围内扩展。尽管有报道称氢在动物研究和临床试验中减少了抗癌药物的副作用,但其背后的分子机制仍不清楚。我们全面的文献回顾显示,氢保护免受由顺铂、奥沙利铂、多柔比星、博来霉素和吉非替尼诱导的组织损伤。其背后的机制涉及减少氧化应激和炎症。氢本身表现出抗癌活性。因此,氢和抗癌药物的结合有可能减少抗癌药物的副作用并增强其抗癌活性。这是未来癌症治疗的一个激动人心的前景。

1. 引言
根据世界卫生组织(WHO)的一个外部研究机构国际癌症研究机构(IARC)的统计,2022年全球将有大约2000万新注册的癌症病例和970万癌症死亡[1]。据估计,全球五分之一的人口将在一生中患上某种形式的癌症,九分之一的男性和十二分之一的女性将死于癌症;然而,这些数字因国家和区域而异。尽管最近癌症诊断和治疗技术的进步提高了癌症患者的生存率,但癌症仍然是需要克服的疾病之一。癌症的治疗方法分为三大类:手术、放疗和药物治疗。
药物治疗对于手术和放疗具有补充或替代作用。常用的细胞毒性抗癌药物包括基于铂(Pt)的药物、抗癌抗生素、烷化剂、抗代谢药、拓扑异构酶抑制剂和微管抑制剂,以及分子靶向药物如抗体药物和酪氨酸激酶抑制剂(TKI)。此外,针对乳腺癌和前列腺癌的激素治疗药物也被使用。免疫检查点抑制剂,如抗程序性细胞死亡-1(PD-1)抗体、抗程序性细胞死亡配体-1(PD-L1)抗体和细胞毒性T淋巴细胞相关蛋白-4(CTLA-4)抗体已被广泛使用,被称为癌症免疫治疗药物。此外,最近的研究表明,针对RAD52基因的小分子抑制剂在乳腺癌治疗中的潜力,以及肿瘤抑制因子miR-99b-5p在前列腺癌治疗中的应用。细胞外囊泡是从不同类型的细胞释放出来的,参与细胞间通讯以维持生理和病理过程,也被认为是包括癌症在内的各种疾病病因的潜在治疗候选者[10]。
然而,这些抗癌药物对癌症患者的治疗效果并不令人满意,它们还会引起副作用。细胞毒性抗癌药物和分子靶向药物的副作用是严重的,并且是这些药物剂量限制因素之一。为了减少副作用,已经开发了现有抗癌药物的衍生物、类似物和脂质体制剂,并且还将抗癌药物与减少副作用的抗氧化剂、抗炎药和抗凋亡物质结合使用[18,19]。然而,这些物质在减少副作用方面的有效性有限,因此,出现了具有优越效能和安全性的减少副作用的物质是人们所期望的。
2007年,氢气(氢)被报道为一种抗氧化剂,它能选择性地减少最具氧化性的反应性氧物种(ROS)和反应性氮物种(RNS),分别是羟基自由基(•OH)和过氧亚硝酸盐(ONOO−)[20]。此后,关于氢的生物医学研究在全球范围内展开,超过2000项研究报道了氢的效果[21]。另一方面,由于氢与•OH在水溶液中的反应速率极慢,•OH与氢的体内反应仍然不清楚。2023年,一项研究显示铁卟啉氧化物能在体内催化氢与•OH之间的反应。铁卟啉的氧化物被确定为氢的目标分子;然而,关于氢的目标分子的研究仍处于初期阶段。氢不仅通过直接减少•OH和ONOO−发挥抗氧化作用,还通过调节基因表达间接发挥抗氧化、抗炎和抗凋亡作用。尽管这些间接机制逐渐得到阐明,但仍需要进一步研究。因此,未来对氢的功效及其目标分子的机制研究是必要的。
动物和临床研究表明,氢本身具有抗癌活性,且其与抗癌药物的结合实现了优异的抗癌活性。此外,氢被发现能在动物研究和临床试验中减少抗癌药物的各种副作用。然而,据我们所知,临床试验尚未专注于氢减少副作用的效果或全面审查氢的这些效果及其背后的分子机制。因此,我们假设氢的抗氧化和抗炎作用可能涉及减少抗癌药物的副作用,并进行了全面的文献回顾。我们回顾了动物研究中氢保护免受抗癌药物引起的各种组织损伤的发现,调查了其背后的分子机制,并讨论了氢作为减少抗癌药物副作用物质的潜在临床应用。
2. 方法论
PubMed是一个免费的数据库,主要包括MEDLINE数据库,该数据库包含生命科学和生物医学主题的参考和摘要。美国国家医学图书馆(NLM),作为国家卫生研究院(NIH)的一部分,维护它作为信息检索系统Entrez系统的一个组成部分。为了调查氢减少抗癌药物副作用的效果,我们在2024年1月10日使用PubMed电子数据库进行了文献搜索。搜索使用了医学主题词(MeSH)术语,并结合了使用布尔运算符“AND”和“OR”的关键词。在这次文献搜索中,我们初步使用关键词“氢气”AND“抗癌药”AND“动物实验”进行搜索,得到了几千个参考文献。仔细查看这次搜索结果发现,搜索结果中有很多“噪音”。因为我们感兴趣的文献是显示氢以各种剂量形式对抗抗癌药物作为副作用的组织损伤效果的动物研究或临床研究文献,我们考虑了以下关键词及其组合作为消除这次搜索中“噪音”的对策。搜索中使用的关键词是(“氢气”OR“氢气”OR“氢水”OR“吸入氢”OR“富含氢”)AND(“顺铂”OR“多柔比星”OR“吉非替尼”OR“博来霉素”OR“抗肿瘤药”OR“抗肿瘤剂”OR“抗癌药”OR“抗癌剂”OR“化疗引起的”)。图1中的PRISMA流程图展示了如何选择已经公开可用的信息,遵循Page等人描述的指示。这次文献搜索确定了14项关于铂类制剂顺铂(CIS)和奥沙利铂(OXA)、拓扑异构酶II(Top2)抑制剂多柔比星(DXR)、抗癌抗生素博来霉素(BLM)以及酪氨酸激酶抑制剂(TKI)吉非替尼(GEF)的动物研究(图1)。
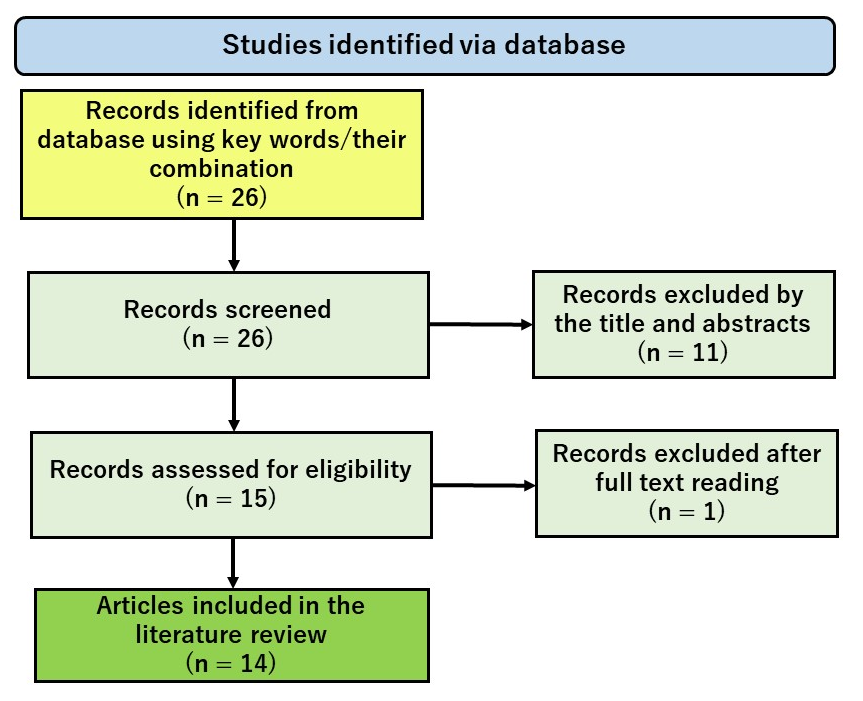
图1. PRISMA流程图显示了文献搜索和选择步骤。
3. 抗癌药物的药理作用和副作用
3.1. 顺铂和奥沙利铂
顺铂和奥沙利铂是铂类药物,这两种药物与铂类药物共享一个共同的化学结构:中心铂被载体配体和离去基团包围。顺铂广泛用于治疗卵巢癌、头颈癌、乳腺癌、子宫癌、胃癌、肺癌、骨肉瘤和恶性淋巴瘤。奥沙利铂用于治疗结肠癌、直肠癌、胰腺癌、胃癌和小肠癌。两种药物中的载体配体都与铂紧密结合,而离去基团则与铂结合较弱,根据周围环境的不同而解离,与细胞内DNA链的嘌呤碱基共价结合。尽管顺铂和奥沙利铂的共价结合方式不同,但形成的铂-DNA加合物抑制了DNA复制和转录,导致细胞凋亡。顺铂引起强烈的肾毒性,这与活性氧物种介导的线粒体功能受损有关。顺铂引起的呕吐和听力损伤也是问题。另一方面,与其他铂类药物相比,奥沙利铂的外周神经病变发生率更高。
3.2. 多柔比星
多柔比星是一种从微生物次级代谢产物中分离出来的蒽环类抗癌抗生素,广泛用于治疗肺癌、乳腺癌、膀胱癌、子宫癌、骨肉瘤和恶性淋巴瘤。多柔比星通过抑制Top2来发挥作用,Top2主要参与双链DNA的切割和结合,从而抑制DNA复制并诱导癌细胞凋亡。多柔比星引起骨髓损伤、肝功能异常、心脏毒性和胃肠道紊乱。心脏毒性依赖于多柔比星的剂量,当累积剂量超过500 mg/m2时,发生率更高。多柔比星引起心脏毒性的机制不仅是因为其化学结构中的苷元部分的醌组充当电子受体产生活性氧物种,还因为多柔比星直接与铁结合,这种复合物产生活性氧物种。此外,已报告一种机制,即多柔比星通过抑制Top2β(Top2的一种同工酶,仅存在于心肌细胞而非癌细胞)来发挥作用。
3.3. 博来霉素
博来霉素是一种从微生物次级代谢产物中分离出来的抗癌抗生素,用于治疗皮肤癌、头颈癌、肺癌、子宫癌、甲状腺癌和食管癌。与多柔比星类似,博来霉素与铁形成复合物。博来霉素引起相对轻微的骨髓损伤,也引起肺和皮肤损伤。博来霉素引起的肺损伤主要是间质性肺炎和肺纤维化,这是严重的并且依赖于给药剂量,当累积剂量≥400 mg/m2时风险增加。虽然在轻微病例中肺损伤仍然可逆,但明确的肺纤维化发病机制是进展性的,对类固醇治疗反应差。博来霉素引起肺损伤的机制包括通过活性氧物种作为急性变化的炎症细胞因子释放诱导凋亡,以及通过胶原蛋白过度产生的慢性变化。
3.4. 吉非替尼
吉非替尼是一种表皮生长因子受体(EGFR)的分子靶向抑制剂,通过口服给药选择性地针对非小细胞肺癌。吉非替尼属于一类EGFR-TKI,它选择性地结合到细胞内EGFR酪氨酸激酶上,并竞争性抑制ATP结合。吉非替尼引起急性肺损伤、间质性肺炎、肝功能异常和皮疹作为副作用。关于吉非替尼引起肺损伤的分子机制,吉非替尼作用于巨噬细胞激活NLRP3炎性体,导致白细胞介素(IL)-1β的释放,还通过激活炎症诱导分子聚(ADP-核糖)聚合酶1(PARP-1)诱导高迁移率族蛋白1(HMGB1)的释放。
4. 抗癌药物副作用的治疗方法和治疗物质的发展
为了减少顺铂的肾毒性和多柔比星的心脏毒性,已经开发了许多治疗方法和治疗物质。然而,尽管有减少博来霉素和吉非替尼肺损伤的治疗方法存在,但很少有新的药物被开发出来以减轻这些抗癌药物的副作用。因此,我们在本章中仅限于讨论为减少顺铂的肾毒性和多柔比星的心脏毒性而开发的治疗方法和治疗物质。
4.1. 顺铂的肾毒性
由于顺铂的肾毒性主要是由于小管损伤,常规的顺铂治疗方法是通过大量水化来缓解这种损伤。尽管大量水化是临床上常见的治疗方法,以促进顺铂从体内排出并减少对肾脏的负担,但它不足以减轻肾毒性。此外,据报道抗氧化剂如维生素E、维生素C、硒、胡萝卜素、褪黑激素、依达拉奉和N-乙酰半胱氨酸可以减少顺铂的肾毒性,但仅在动物模型中进行了评估。另一方面,有机阳离子转运蛋白2抑制剂西咪替丁,它阻断顺铂向肾脏的转运,卡维地洛,它抑制氧化应激,西拉斯坦,它阻断凋亡途径,罗格列酮,它减少炎症,以及氨磷汀,它发挥细胞保护作用,已被应用于减少顺铂的肾毒性。然而,这些药物不仅在减少副作用方面效果较差,而且它们本身也会引起副作用。此外,最近的体外和体内研究表明,天然产物如黄酮类化合物、皂苷、生物碱、多糖和苯丙素类化合物,在顺铂诱导的急性肾损伤中抑制氧化应激、炎症和凋亡。进一步的开发,包括临床试验,正在期待中。
4.2. 多柔比星的心脏毒性
为了减少多柔比星的心脏毒性,已经开发了各种治疗物质。Dexrazoxane是一种铁螯合剂,通过抑制铁-多柔比星复合物的形成来减少心脏毒性,从而减少活性氧物种[87]。这种药物被美国食品和药物管理局(FDA)批准为减少包括多柔比星在内的化疗药物引起的心脏毒性的药物[88]。然而,随后的临床研究对其效果提出了质疑,也有关于该药物可能引起二次致癌的担忧。另一方面,Dexrazoxane还通过蒽环类抗生素抑制DNA-拓扑异构酶复合物的形成,并作为这些抗癌药物的血管外渗漏的治疗药物上市[90]。其他化合物,如降低氧化应激和细胞损伤的地高辛、自噬相关(ATG)7激活剂、减少ROS并激活ATG7的白藜芦醇,以及具有抗氧化特性的草药化合物已被证明可以保护免受多柔比星诱导的心脏毒性;然而,所有这些都有效果和安全性问题。此外,最近关于蒽环类抗生素的分子机制研究揭示了多柔比星抑制血红素合成并插入线粒体DNA(mtDNA),从而诱导铁依赖性细胞死亡——铁死亡,导致心脏毒性。一种氨基酸,5-氨基酮戊酸(5-ALA),已被报道在小鼠中通过抑制负责的分子机制减少多柔比星诱导的心脏毒性,未来关于5-ALA作为多柔比星诱导的心脏毒性保护剂的临床研究备受期待。
5. 氢气减少抗癌药物的副作用
我们的文献回顾显示,氢气减少了顺铂诱导的肾毒性、耳毒性和卵巢损伤,顺铂或奥沙利铂诱导的周围神经病变,多柔比星诱导的心脏毒性和肝毒性,以及博来霉素或吉非替尼诱导的肺损伤。氢气对这些副作用减少的药物特异性总结如表1所示。
表1. 氢气对抗癌症药物在动物模型中诱导的各种组织损伤的保护作用总结。
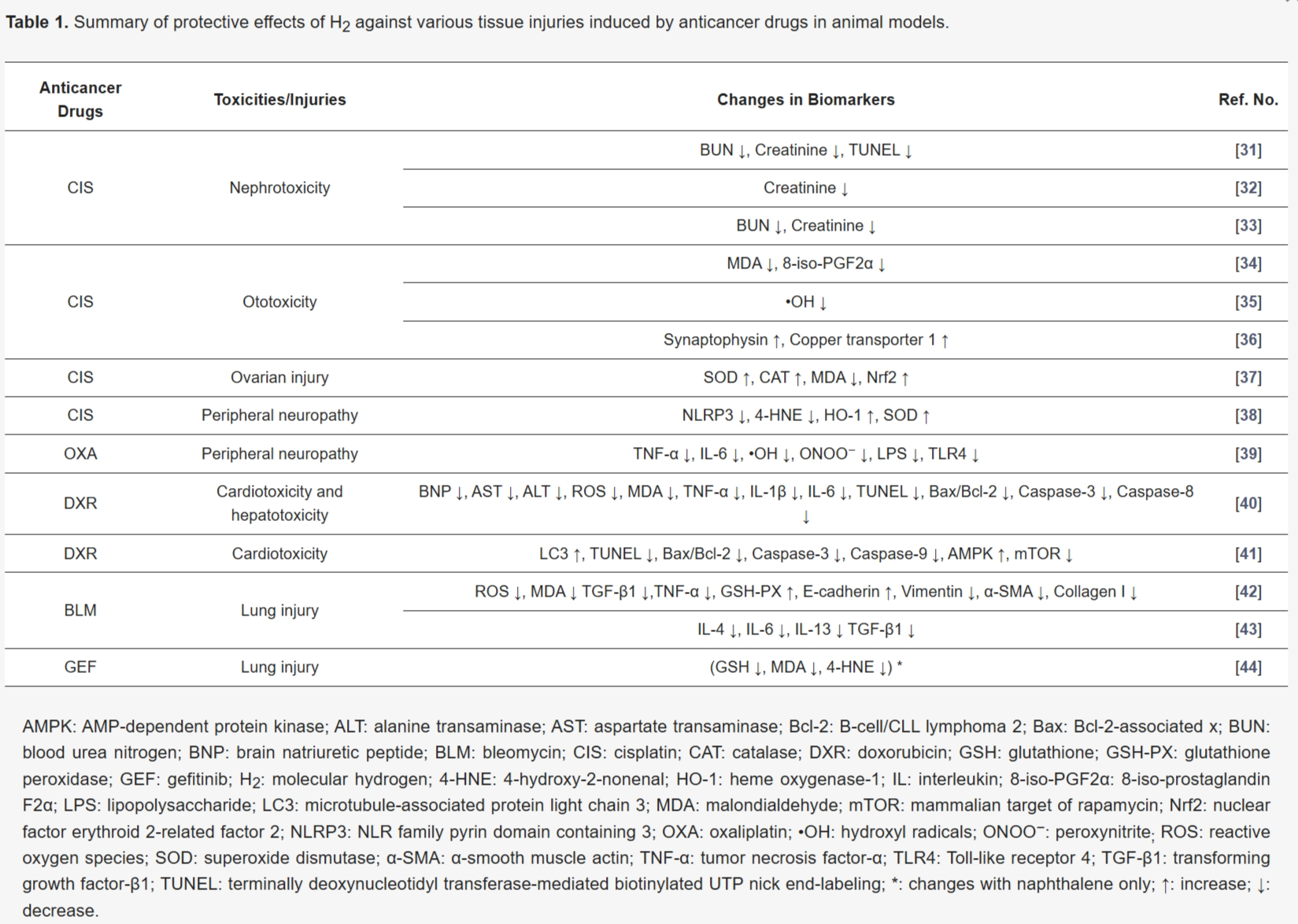
5.1. 对顺铂和奥沙利铂诱导的毒性的影响
5.1.1. 肾毒性
Nakashima-Kamimura等人研究了氢气和富氢水(HRW)对小鼠顺铂诱导的肾毒性的缓解效果,并证明吸入氢气或饮用HRW改善了由顺铂引起的死亡率和体重减轻,以及血清肌酐和血尿素氮(BUN)水平增加。此外,通过对HRW对肾毒性的减弱作用进行组织病理学检查,发现HRW减少了末端脱氧核苷酸转移酶介导的生物素化UTP切口末端标记(TUNEL)阳性细胞的数量。而且,氢气在体外癌细胞系的实验中或在携带癌瘤的小鼠的体内实验中并未削弱顺铂的抗癌活性[31]。这些发现表明,氢气通过减少氧化应激和凋亡来减轻顺铂诱导的肾毒性,而不损害顺铂的抗癌效果。Kitamura等人还使用动态对比增强计算机断层扫描(DCE-CT)研究了HRW对大鼠顺铂诱导的肾毒性的影响,并显示HRW减轻了顺铂诱导的单位肾脏体积对比清除率(K1)和整个肾脏的对比清除率(即K1乘以肾脏体积)的减少。此外,它减少了顺铂诱导的血清肌酐水平的增加和组织病理学损伤。总的来说,这些发现使用DCE-CT证实了氢气对肾毒性的保护作用。Matsushita等人使用血液氧合水平依赖性(BOLD)磁共振成像(MRI)阐明了HRW对大鼠顺铂诱导的肾毒性的保护作用机制。他们证明,HRW显著改善了顺铂诱导的母体横向弛豫率的降低和血清肌酐及BUN水平的增加。这些发现使用BOLD-MRI确认了氢气的肾脏保护作用。
5.1.2. 耳毒性
Qu等人研究了氢气对大鼠顺铂诱导的耳毒性的保护效果。他们发现,吸入氢气显著改善了听性脑干反应(ABR)并从组织病理学上确认了毛细胞损伤。吸入氢气还显著降低了顺铂诱导的血清和耳蜗组织中的丙二醛(MDA)和8-异前列烷F2α(8-iso-PGF2α)水平增加。这些发现表明,氢气通过减少氧化应激减轻了顺铂诱导的耳毒性。Kikkawa等人还研究了含氢培养基对培养的小鼠耳蜗外植体的保护效果,并报告说氢气显著改善了顺铂诱导的毛细胞数量减少,并显著降低了螺旋神经节中·OH的荧光强度。这些发现表明,氢气通过减少ROS诱导的氧化应激来减轻顺铂的耳毒性。此外,Fransson等人研究了氢气对豚鼠顺铂诱导的耳毒性的保护效果,并报告说氢气减轻了顺铂诱导的ABR阈值偏移、毛细胞丢失以及突触小泡蛋白免疫反应性的减少。他们还证明,氢气显著改善了顺铂诱导的内毛细胞和血管带周围突触区域的铜转运蛋白1强度的减少。这些发现表明,氢气在功能、细胞和亚细胞层面上对抗顺铂诱导的耳毒性提供了保护。
5.1.3. 卵巢损伤
Meng等人研究了富氢盐水(HRS)对大鼠顺铂诱导的卵巢损伤的保护效果[37]。他们发现,腹腔注射HRS显著改善了顺铂诱导的卵巢组织中雌激素的减少和促卵泡激素的增加,以及组织病理学确认的卵巢皮质损伤[37]。HRS还显著减轻了顺铂诱导的超氧化物歧化酶(SOD)和过氧化氢酶(CAT)的减少以及MDA的增加。此外,HRS增强了顺铂诱导的卵巢组织中核因子红细胞2相关因子2(Nrf2)表达的增加。这些发现表明,氢气通过调节氧化应激从而激活Nrf2来保护免受顺铂诱导的卵巢损伤。
5.1.4. 周围神经病变
Martínez-Martel等人研究了富氢水(HRW)对顺铂诱导的小鼠触觉异常疼痛以及功能和情绪缺陷的预防效果[38]。所获得的发现表明,HRW改善了顺铂诱导的触觉异常疼痛以及功能和情绪缺陷[38]。HRW还显著减轻了顺铂诱导的背根神经节和前额叶皮层中NLRP3和4-羟基-2-壬烯醛(4-HNE)蛋白水平的增加,以及血红素氧合酶-1(HO-1)和超氧化物歧化酶(SOD)表达的减少。这些发现表明,氢气通过减少氧化应激和炎症来保护免受顺铂诱导的触觉异常疼痛以及功能和情绪缺陷。Lian等人研究了HRW对奥沙利铂诱导的小鼠神经性疼痛的影响,并证明HRW缓解了奥沙利铂诱导的小鼠痛觉过敏,减少了肠道细菌的多样性,并改变了肠道微生物群的结构。HRW还逆转了诸如肿瘤坏死因子(TNF)-α和IL-6等炎症细胞因子以及•OH和ONOO−等氧化应激因子在脊髓段中的不平衡,并降低了脂多糖(LPS)和Toll样受体4(TLR4)的表达。这些发现表明,氢气通过改变肠道微生物群的多样性和结构以及LPS-TLR4途径来减轻神经性疼痛。
5.2. 对多柔比星诱导的心脏毒性和肝脏毒性的影响
Gao等人研究了腹腔注射富氢盐水(HRS)对大鼠多柔比星诱导的心脏毒性和肝脏毒性的影响[40]。所获得的结果显示,HRS改善了多柔比星诱导的大鼠死亡率、心脏功能障碍以及心脏和肝脏的组织病理学损伤。HRS还显著减轻了多柔比星诱导的血清脑钠肽、天门冬氨酸转氨酶和丙氨酸转氨酶的增加以及心脏和肝脏中的ROS和MDA。此外,HRS显著减轻了多柔比星诱导的心脏和肝脏中炎症相关标志物TNF-α、IL-1β和IL-6的增加,以及凋亡相关标志物TUNEL、Bcl-2相关X蛋白(Bax)和B细胞/CLL淋巴瘤2(Bcl-2)比率的增加,并显著减少了caspase-3和caspase-8水平的增加。这些发现表明,氢气通过减轻炎症和凋亡来改善多柔比星诱导的心脏毒性和肝脏毒性。
马等人研究了氢气吸入在大鼠多柔比星诱导的心肌损伤模型中的效果,并展示了心脏功能的改善和心肌组织病理学损伤的减轻。氢气还恢复了多柔比星诱导的心肌细胞中微管相关蛋白轻链3(LC3)表达的减少,LC3是一种自噬相关蛋白,并同时改善了多柔比星诱导的凋亡增加(TUNEL,Bax/Bcl-2比率,caspase-3和caspase-9)。此外,氢气增加了磷酸化腺苷酸依赖性蛋白激酶(p-AMPK)与AMPK的比率,并降低了磷酸化哺乳动物雷帕霉素靶蛋白(p-mTOR)与mTOR的比率。这些发现表明,氢气通过AMPK/mTOR通路激活自噬,并保护免受多柔比星诱导的心肌损伤。
5.3. 对博来霉素诱导的肺损伤的影响
高等人研究了氢气吸入在大鼠博来霉素诱导的肺纤维化模型中的效果,并发现它减少了博来霉素诱导的肺组织中ROS、MDA、转化生长因子(TGF)-β1和TNF-α水平的增加,并减轻了博来霉素诱导的谷胱甘肽过氧化物酶(GSH-PX)活性的降低。氢气还通过增加上皮细胞标记物E-cadherin的表达水平和减少间充质细胞标记物波形蛋白的表达来抑制博来霉素介导的上皮-间质转化。此外,氢气通过下调α-平滑肌肌动蛋白的表达并抑制胶原I的产生来发挥其抗纤维化作用。这些发现表明,氢气通过抑制与纤维化相关的TGF-β1和氧化应激以及抑制上皮-间质转化来减轻博来霉素诱导的肺纤维化。青木等人调查了氢气吸入在小鼠博来霉素诱导的肺纤维化模型中的效果,并发现氢气减少了博来霉素诱导的呼吸功能恶化和组织病理学确认的肺纤维化。他们还展示了氢气抑制了肺泡巨噬细胞中IL-6、IL-4和IL-13水平的增加,减少了在肺纤维化中起作用的M2偏向型巨噬细胞的数量,并减少了诱导纤维化的TGF-β1分泌细胞的数量。这些发现表明,氢气改善了博来霉素诱导的呼吸功能障碍和肺纤维化。
5.4. 对吉西他滨诱导的肺损伤的影响
寺崎等人研究了富氢水(HRW)在小鼠模型中的效果,该模型通过在给予萘(一种与氧化应激相关的有毒物质)预处理后再给予吉西他滨(GEF)来诱导急性肺损伤,并报告说HRW逆转了萘/GEF处理小鼠的体重减轻,延长了存活时间,改善了肺部组织病理学改变,并增加了支气管肺泡灌洗液中的细胞计数。然而,氢气减弱了萘诱导的GSH水平的减少以及MDA和4-HNE水平的增加,并发挥了抗氧化作用,但没有显著影响萘/GEF诱导的变化。另一方面,氢气并未损害GEF在体外肺癌细胞系实验或体内携带癌瘤小鼠实验中的抗癌效果。这些发现表明,氢气减少了GEF诱导的肺损伤,同时没有损害其抗癌活性。
6. 氢气减少抗癌药物副作用的机制
我们的文献回顾显示,氢气减少了顺铂、奥沙利铂、多柔比星、博来霉素和吉西他滨的副作用,主要归因于其抗氧化和抗炎作用,但也通过其抗凋亡和自噬激活作用,以及其调节细胞死亡的作用。这些作用并非孤立存在,而是似乎相互影响,构成了氢气减少副作用的整体能力。这些作用在每个项目中都有描述(图2)。
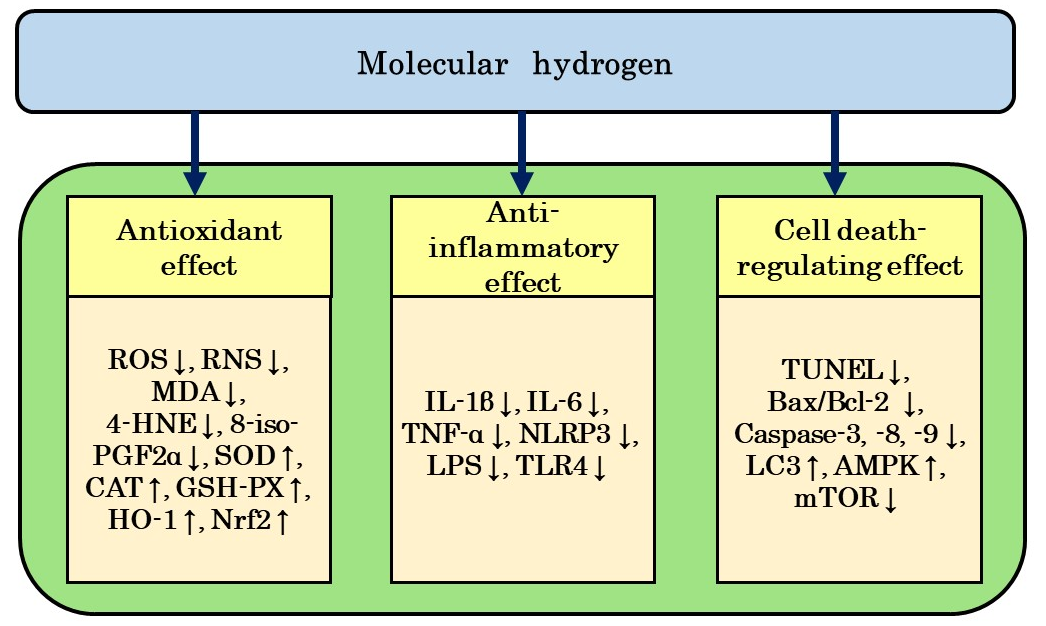
图2. 氢气对抗抗癌药物诱导的组织损伤的保护作用的可能机制。
保护作用主要被归类为抗氧化、抗炎和细胞死亡调节作用。AMPK: AMP依赖性蛋白激酶;Bcl-2: B细胞/CLL淋巴瘤2;Bax: Bcl-2相关x蛋白;CAT: 过氧化氢酶;GSH-PX: 谷胱甘肽过氧化物酶;氢气:氢气;4-HNE: 4-羟基-2-壬烯醛;HO-1: 血红素氧合酶-1;IL: 白介素;8-iso-PGF2α: 8-异前列腺素F2α;LPS: 脂多糖;LC3: 微管相关蛋白轻链3;MDA: 丙二醛;mTOR: 哺乳动物靶标雷帕霉素;Nrf2: 核因子红细胞2相关因子2;NLRP3: NLR家族热蛋白结构域含有3;RNS: 活性氮物种;ROS: 活性氧物种;SOD: 超氧化物歧化酶;TNF-α: 肿瘤坏死因子-α;TLR4: Toll样受体4;TGF-β1: 转化生长因子-β1;TUNEL: 末端脱氧核苷酸转移酶介导的生物素UTP缺口末端标记法;↑: 增加;↓: 减少。
6.1. 抗氧化作用
在研究氢气对抗顺铂诱导的听觉毒性、奥沙利铂诱导的周围神经病变、多柔比星诱导的心脏毒性和肝脏毒性以及博来霉素诱导的肺损伤的效果时,氢气减少了这些抗癌药物副作用引起的ROS和RNS(即•OH和ONOO−)的产生。另一方面,在研究氢气对抗顺铂诱导的耳毒性、卵巢损伤和周围神经病变、多柔比星诱导的心脏毒性和肝脏毒性以及博来霉素诱导的肺损伤的效果时,氢气减少了这些抗癌药物副作用引起的MDA、8-iso-PGF2α和4-HNE水平的增加,并增强了这些抗癌药物降低的SOD、CAT、HO-1和GSH-PX的活性。
这些发现可能归因于氢气不仅直接抑制ROS的产生,还间接调节涉及氧化和抗氧化的酶,从而产生抗氧化作用。ROS参与顺铂、多柔比星和博来霉素在癌细胞中的细胞毒性作用机制。然而,从减少副作用的角度来看,重要的是抑制引起组织损伤的ROS的产生,并防止它们造成二次损伤。
6.2. 抗炎作用
在研究氢气对抗顺铂和奥沙利铂诱导的周围神经病变、多柔比星诱导的心脏毒性和肝脏毒性以及博来霉素诱导的肺损伤的效果时,氢气分别减少了这些抗癌药物增加的NLRP3蛋白水平、LPS和TLR4表达水平以及TNF-α、IL-1β和IL-6水平。这些发现表明,抗炎作用参与了氢气减轻抗癌药物副作用的过程。
氢气还对抗吉西他滨诱导的肺损伤有效;然而,其潜在机制尚不清楚。吉西他滨诱导肺损伤的机制包括其诱导巨噬细胞激活NLRP3并释放IL-1β以及通过PARP-1的异常激活释放HMGB1。因此,在吉西他滨诱导的肺损伤中,氢气可能通过阻断导致炎症细胞因子释放的NLRP3激活途径来减少肺损伤。这一点得到了我们之前综述的支持,该综述显示氢气通过抑制mtDNA氧化可能抑制从NLRP3激活到炎症细胞因子释放的级联反应,从而抑制慢性炎症。
6.3. 调节细胞死亡
在研究氢气对抗顺铂诱导的肾毒性和多柔比星诱导的心脏毒性及肝脏毒性的效果时,氢气分别减少了TUNEL阳性细胞数的增加和TUNEL蛋白水平的升高、Bax/Bcl-2比率以及caspase-3、-8和-9活性的增加。这些发现表明,氢气通过其抗凋亡作用减少了顺铂和多柔比星的毒性。另一方面,在一项关于多柔比星诱导的心脏毒性的研究中,氢气恢复了多柔比星诱导的LC3表达减少,增加了p-AMPK与AMPK的比率,并降低了p-mTOR与mTOR的比率。这些发现表明,氢气通过AMPK/mTOR通路激活自噬,并保护免受多柔比星诱导的心脏毒性。这些发现还表明,如抑制凋亡和激活自噬等细胞死亡调节作用参与了氢气减轻顺铂和多柔比星毒性效应的机制。
7. 氢气的抗癌和放射保护效果
7.1. 抗癌效果
许多体外和体内研究报道了氢气的抗癌效果,最近的临床试验显示吸入氢气治疗对各种癌症有效。Chen等人展示了82名癌症患者经过3个月的氢气吸入治疗后,生活质量得到改善并且癌症进展受到抑制。他们使用氢气吸入与几种小剂量抗癌药物联合治疗大约三分之二的患者,但没有观察到氢气单独使用与药物组合使用在抗癌效果上的显著差异,也没有发现当药物一起使用时副作用有所减少。Akagi等人检查了抗PD-1抗体nivolumab和氢气吸入联合治疗癌症患者≥60个月的效果,并报告说,与单独使用nivolumab治疗的14名患者相比,接受联合治疗的42名患者实现了显著的总体生存优势。
Chen等人将58名非小细胞肺癌患者分成五组:对照组(10名患者)、仅氢气组(10名患者)、氢气加化疗组(10名患者)、氢气加靶向治疗组(18名患者)和氢气加免疫治疗组(10名患者)。联合治疗组接受了包括顺铂或卡铂在内的化疗药物、包括吉西他滨在内的几种靶向治疗药物以及包括nivolumab或pembrolizumab在内的免疫治疗药物。除对照组外,仅氢气组和氢气联合组接受了5个月的氢气吸入治疗。在治疗的前5个月,对照组的症状逐渐增加,而四个治疗组的症状逐渐减少。在16个月的随访中,仅氢气组、氢气加化疗组、氢气加靶向治疗组和氢气加免疫治疗组的无进展生存率明显高于对照组。联合治疗组中大多数抗癌药物的副作用也减少或消除了。这些发现表明,吸入氢气抑制了非小细胞肺癌患者的肿瘤进展。尽管没有描述个别抗癌药物减少副作用的效果,且明确显示氢气缓解了化疗药物、靶向治疗药物和免疫治疗药物的各种副作用,但获得的结果表明,氢气与抗癌效果的组合通常有效地减少了抗癌药物的副作用。
因此,氢气与抗癌药物的组合不仅可能增强抗癌药物的抗癌效果,还可能减轻它们的副作用。显示氢气增强了抗癌药物的抗癌效果而不损害其抗癌效果的发现表明,通过调节基因表达的间接防御机制比直接减少•OH更密切地参与了氢气的抗癌效果。
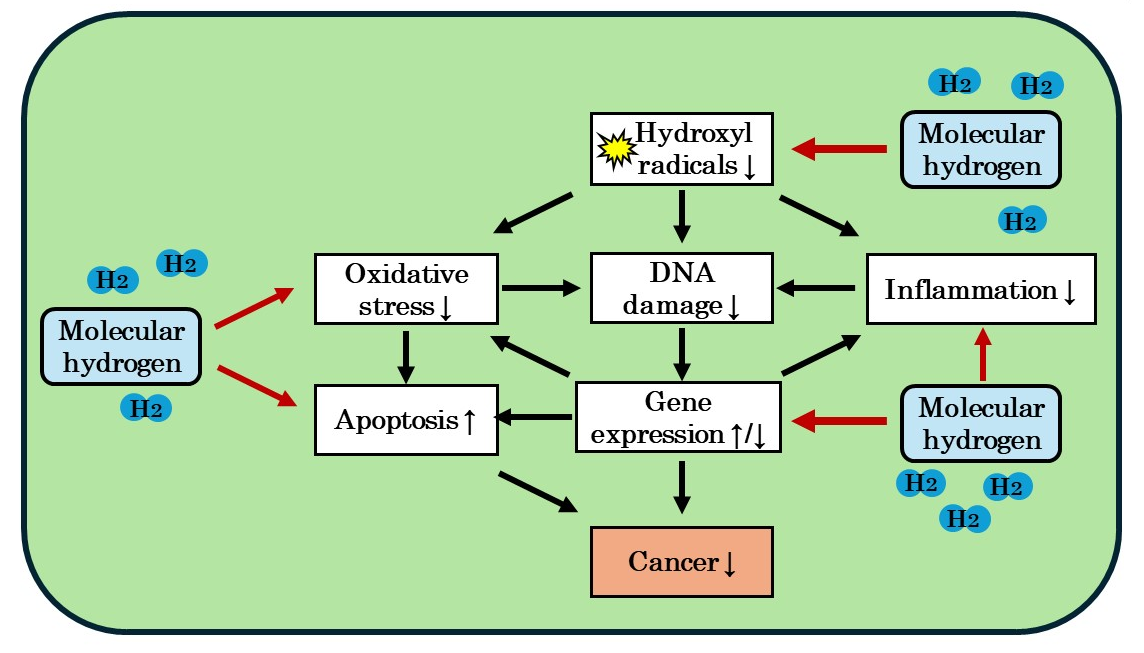
图3. 氢气(氢气)的抗癌作用的可能机制。
氢气直接减少羟基自由基,并通过间接调节基因表达展示出抗氧化、抗炎和促凋亡效果。通过这些作用,氢气可能表现出抗癌效果。详情请参阅[27]。↑:增加;↓:减少;↑/↓:增加或减少。
7.2. 放射保护效果
抗癌药物和辐射对机体造成的损伤机制非常相似。我们之前在一篇综述中报道了氢气对辐射损伤的保护作用及其可能的机制[25]。在本章中,我们将比较氢气对抗抗癌药物引起的损伤与对抗辐射引起的损伤所展现的保护作用机制。
电离辐射对身体的有害影响被分为直接效应和间接效应。直接效应是由辐射能量直接吸收到核酸(DNA)、蛋白质和脂质中引起的。间接效应是由自由基(如•OH)和水射解过程中产生的分子引起的。由于低剂量辐射损伤主要是由这种间接效应引起的,因此作为非DNA靶标的二次损伤比对DNA的直接损伤更为密切。这种二次损伤包括与细胞内反应相关的氧化应激、炎症、凋亡以及对基因表达的影响。
氢气的放射保护效果也在许多体外和体内研究中被报道,最近的临床试验显示吸入氢气减轻了与辐射相关的生活质量降低和骨髓损伤。在我们之前的综述中,我们描述了体外和体内研究中氢气展现放射保护效果和抗癌效果的机制,这些机制不仅归因于氢气直接减少•OH,还包括氢气通过细胞内反应间接调节基因表达以及间接的抗氧化和抗炎作用。氢气通过细胞内反应间接调节基因表达从而可能发挥抗氧化、抗炎和抗凋亡效果的可能性得到了证明(图4)。因此,氢气对辐射和抗癌药物引起的细胞毒性展现保护作用的机制是相似的。
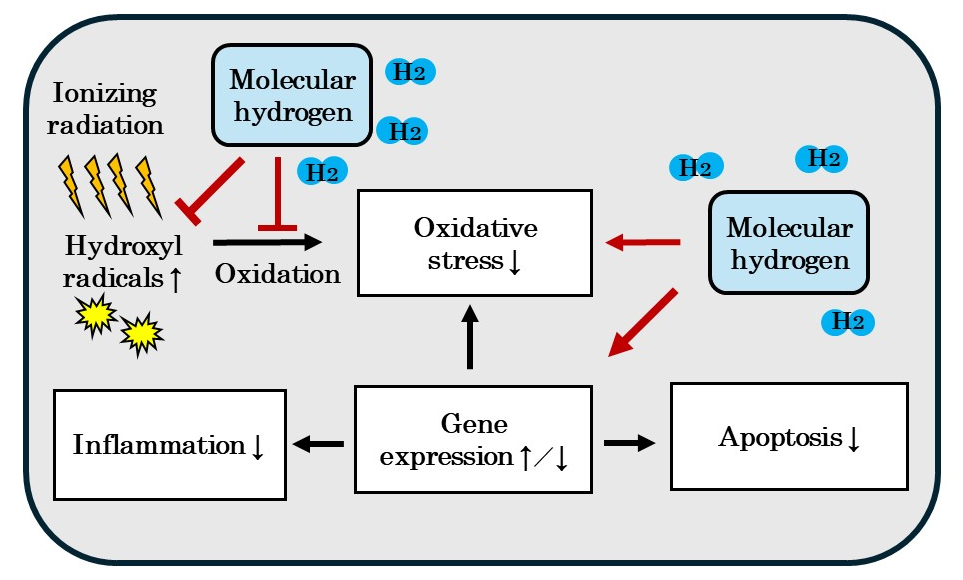
图4. 氢气(氢气)不仅通过减少羟基自由基直接具有放射保护作用,还通过调节基因表达间接地展现抗氧化、抗炎和抗凋亡效果,这可能导致放射保护效果。详情请参阅[25]。↑:增加;↓:减少;↑/↓:增加或减少。
8. 氢气的临床应用前景
这篇文献综述展示了氢气减少了顺铂诱导的肾毒性、耳毒性和卵巢损伤,顺铂或奥沙利铂诱导的周围神经病变,多柔比星诱导的心脏毒性和肝脏毒性,以及博来霉素或吉西他滨诱导的肺损伤。基于生化和分子生物学标记物的变化分析氢气减少副作用的机制揭示了氢气的抗氧化、抗炎和细胞死亡调节作用对抗顺铂和多柔比星诱导的紊乱具有保护作用。此外,氢气的抗氧化和抗炎作用似乎对抗奥沙利铂、博来霉素和吉西他滨诱导的紊乱具有保护作用。这些发现使我们得出结论,氢气主要通过减少氧化应激和炎症在动物研究中保护了各种来自抗癌药物副作用的组织损伤。
为了减少抗癌药物的副作用,已经进行了许多努力。关于开发具有较少副作用的现有抗癌药物的衍生物和类似物的研究,以及关于如脂质体和乳剂等制剂技术的研究已经进行,但没有满意的结果。顺铂的肾毒性和阿霉素的心脏毒性涉及氧化应激、炎症和凋亡。因此,已经联合使用抗氧化、抗炎、抗凋亡物质,并且一些已经应用于临床试验。然而,尚未报告令人满意的发现。
氢气对抗癌药物副作用的减弱作用主要已在动物研究中进行了检验,其背后的机制归因于其抗氧化、抗炎、抗凋亡和自噬激活特性。临床研究确认了氢气对抗癌药物副作用的减弱作用;然而,它们不是针对副作用减少的详细临床研究[46]。此外,在动物研究中,氢气与抗癌药物的组合并未损害抗癌药物的抗癌效果,临床研究展示了氢气与抗癌药物的组合增强了抗癌药物的抗癌效果,超过了单独使用的效果。氢气在治疗各种人类疾病中的功效已在150多项临床研究中被报道,没有不良反应被归因于氢气。因此,氢气与抗癌药物的结合对于癌症患者可能是一种安全有效的治疗方法,可以增强抗癌效果并减少副作用。
另一方面,有许多限制需要解决。本综述仅讨论了五种抗癌药物:顺铂、奥沙利铂、多柔比星、博来霉素和吉西他滨。尽管很可能氢气对许多其他抗癌药物的副作用产生类似效果,但需要进行进一步研究以扩大抗癌药物的范围。此外,已显示氢气通过减少氧化应激和炎症来改善作为抗癌药物副作用的组织损伤;然而,包括负责这些效果的目标分子在内的潜在分子机制仍然未知。最近的研究报道了体内•OH的减少需要铁-卟啉的氧化作为催化剂,而这种铁-卟啉氧化物是氢气的目标分子。然而,包括氢气的目标分子在内的功效及其副作用减弱的分子机制仍不清楚,需要进一步研究。此外,最近的研究报道了生物聚合物作为一类新材料在生物医学应用中具有很好的潜力。因此,将生物聚合物与氢气整合以增强抗癌效果或减轻抗癌药物的副作用的可能性是未来探索的一个有趣方向。
9. 结论
虽然已有报道氢气在动物研究和临床试验中减轻了抗癌药物的副作用,但我们对其分子机制的理解仍然有限。为了解决这一问题,我们进行了广泛的动物研究综述。所获得的发现表明,氢气保护免受顺铂诱导的肾毒性、耳毒性和卵巢损伤,顺铂或奥沙利铂引起的周围神经病变,多柔比星导致的心脏毒性和肝脏毒性,以及博来霉素或吉西他滨造成的肺损伤。涉及的主要机制似乎是减少氧化应激和炎症。在临床研究中,氢气在减少抗癌药物的副作用方面表现出功效。有趣的是,氢气并没有在动物实验中减弱这些药物的抗癌效果。氢气与抗癌药物的组合在临床试验中增强了抗癌效果。因此,氢气与抗癌药物的组合作为一种治疗策略,减少了抗癌药物的副作用并增强了其抗癌效果,这为未来的癌症治疗提供了一个令人兴奋的途径。
https://blog.sciencenet.cn/blog-41174-1444405.html
上一篇:氢气治疗川崎病的动物实验【台湾】
下一篇:脂质参与离子通道家族孔隙的结构成分