博文
大型智能生物反应器【科学】  精选
精选
|
大型智能生物反应器,具有完全集成的无线多变量传感器和电子元件,可对干细胞培养进行长期原位监测
生物反应器是大规模细胞生产的重要设备,但生物反应器非常不智能,特别是和细胞生长密切相关参数,如温度、酸碱度、氧气浓度、葡萄糖浓度、离子浓度等信息,这些参数会随着时间和细胞生长发生改变,如果不及时纠正,可能会严重影响细胞生长质量。对于生长环境要求非常高的干细胞来说,这尤其是重要的问题。在今天智能时代,细胞培养的低智能现状让人担忧,这正是本研究希望解决的问题所在。

封面文章:一个一体化的传感器系统提供了对干细胞培养物的连续监测。为了满足个性化医疗这个新兴领域的需求,干细胞和治疗性细胞必须进行大规模生产,同时保持一致的高质量和低成本。Lee等人通过创建一个可扩展的、低轮廓的和灵活的传感器阵列来解决这一需求。这些阵列允许对干细胞培养物进行无线、多变量、长期的实时监测,并可以与商业上可获得的大细胞培养袋或较小的培养皿相结合。
使用现有设备实现大规模、具有成本效益和可重复的干细胞制造具有挑战性。传统的一次性细胞袋式生物反应器受限于其刚性和单点传感器,难以实现高质量细胞制造的准确性和可扩展性。在这里,我们介绍了一种智能生物反应器系统,该系统可实现多空间传感,以实现实时无线培养监测。这种可扩展的系统包括一个薄型、无标记的薄膜传感器阵列和与柔性细胞袋集成的电子元件,允许同时评估培养特性,如pH值、溶解氧、葡萄糖和温度,以接收长达30天的实时反馈。实验结果表明,从塑料培养皿到2升细胞袋,使用可调节载体可以准确监测干细胞和成肌细胞的时间动态和空间变化。这些进展为智能传感系统开辟了广泛的适用性,用于大规模、低成本、可重复和高质量的工程细胞制造,用于广泛的临床应用。
在干细胞非凡潜力的推动下,个性化医疗的出现正在彻底改变治疗以前无法治疗的神经退行性疾病和遗传性疾病的治疗方法 (1, 2)。干细胞(如原代间充质干细胞)因其再生和多能性的能力而成为强大的治疗工具 (3, 4)。然而,将基于干细胞的疗法整合到主流医疗实践中面临着一个显着的挑战:缺乏可靠的制造平台来确保临床级干细胞的一致生产,同时保持其可重复性和基本细胞特性。虽然扩大培养皿生产规模以满足日益增长的需求是可行的,但在整个制造过程中保持最佳培养皿质量是一个巨大的工程障碍。这一挑战的主要原因之一是细胞培养过程中缺乏连续监测技术 (5–7)。认识到持续监测的重要性,生物医学研究一直强调监测细胞培养的重要性和需求 (8–13)。正如 2019 年诺贝尔奖 (14) 所承认的那样,氧气可用性会影响细胞的适应和反应 (15)。这些参数,如pH,温度和生化分析物的浓度,也会影响细胞生理学(16,17)。 遗憾的是,在 2014 年至 2019 年期间进行的实验中,只有不到 0.5% 显示了培养基 pH 值的测量值,并且没有报告溶解氧 (DO) 水平 (18)。在实验过程中缺乏对培养参数的验证损害了制造后结果的可靠性和有效性(19,20)。 为了解决这个问题,必须通过主动监测和反馈机制建立稳健的标准,以确保稳定的培养条件,同时增强实验与体内生理学的相关性,最终提高可重复性。最近,一次性细胞袋式生物反应器已被广泛认为是产生大量干细胞的理想制造平台 (21–23)。尽管有各种电化学传感器可用 (24),但目前的监测方法依赖于穿透细胞袋的单点检测传感器,仅提供传感器附近的间接信息,无法捕获整个培养环境 (25)。此外,随着规模化生产的尺寸增加,监测整个细胞袋变得非常具有挑战性 (26–28)。尽管已经进行了许多尝试,以使用微纳加工和电化学加工技术制造用于在线监测的传感系统,但结果仍然是初步的,并且不切实际,无法与传感器袋集成(29–36)。总体而言,目前尚无可用于在细胞袋生物反应器中对细胞培养条件进行实时、无线、多空间传感的解决方案。
在这里,本文报道了一种大型智能生物反应器系统的开发,该系统具有完全集成的无线多膜传感器和电子设备,用于干细胞培养的长期、连续、原位监测。我们的技术利用薄型、无标记的纳米膜传感器和超薄电子元件与商业细胞袋无缝集成,用于在线培养监测并提供实时反馈。多功能传感器阵列可测量 pH 值、葡萄糖、溶解氧和温度,具有高灵敏度、可靠性和可重复性。与现有的细胞袋传感器不同,整个传感器系统柔软而灵活,在生物反应器中摇摆运动期间不会中断细胞培养过程和自然流体运动。小型化集成电路能够采集无线实时数据,同时捕获细胞袋内细胞培养质量的空间信息。该系统为高通量培养皿制造提供动态的空间分辨反馈。总的来说,对材料、力学、制造和包装的综合研究为开发先进的传感平台提供了指导,该平台具有确定性、高质量地制造治疗性细胞和干细胞的潜力,用于广泛的临床和工业用途。
研究结果
带传感器和电子元件的智能生物反应器系统概述
智能生物反应器系统包括一系列用于检测pH值、葡萄糖、溶氧和温度的纳米膜多功能传感器,以及用于无线数据监测的小型化柔性电子电路,与市售的一次性一次性细胞袋集成在一起(图1A和视频S1)。使用便携式设备或将在线处理监测仪与我们的系统连接,用户可以无线接收原位干细胞培养信息,例如细胞群的空间分布和具有非理想生长速率或细胞状态的培养区域(表1)。现有的培养皿袋传感器无法向制造商提供此类信息。该多传感器系统旨在通过无线电子系统检测干细胞培养(图1B),提供对培养条件的实时反馈。阵列中的每个传感器都采用独特的信号转导设计,采用电化学、电位和惠斯通电桥电路。一旦信号被模数转换器(ADC)转换为原始电压,带有蓝牙模块的微控制器就会将信号无线传输到外部设备。测量的信号被校准为所需的信息,以实现细胞培养的条件,并以 1 Hz 的采样率实时响应,允许每秒收集一个样本。薄型薄膜传感器封装可集成到任何培养平台中,包括柔性聚合物基板(图 1C)。该封装具有设计灵活性,因为传感器的数量、阵列设计和传感器的放置可以在目标平台或细胞培养体积上自由选择。图1(D和E)显示了几个示例,包括一次性聚苯乙烯培养皿中的传感器和用于生物反应器的不同尺寸的一次性细胞培养袋。
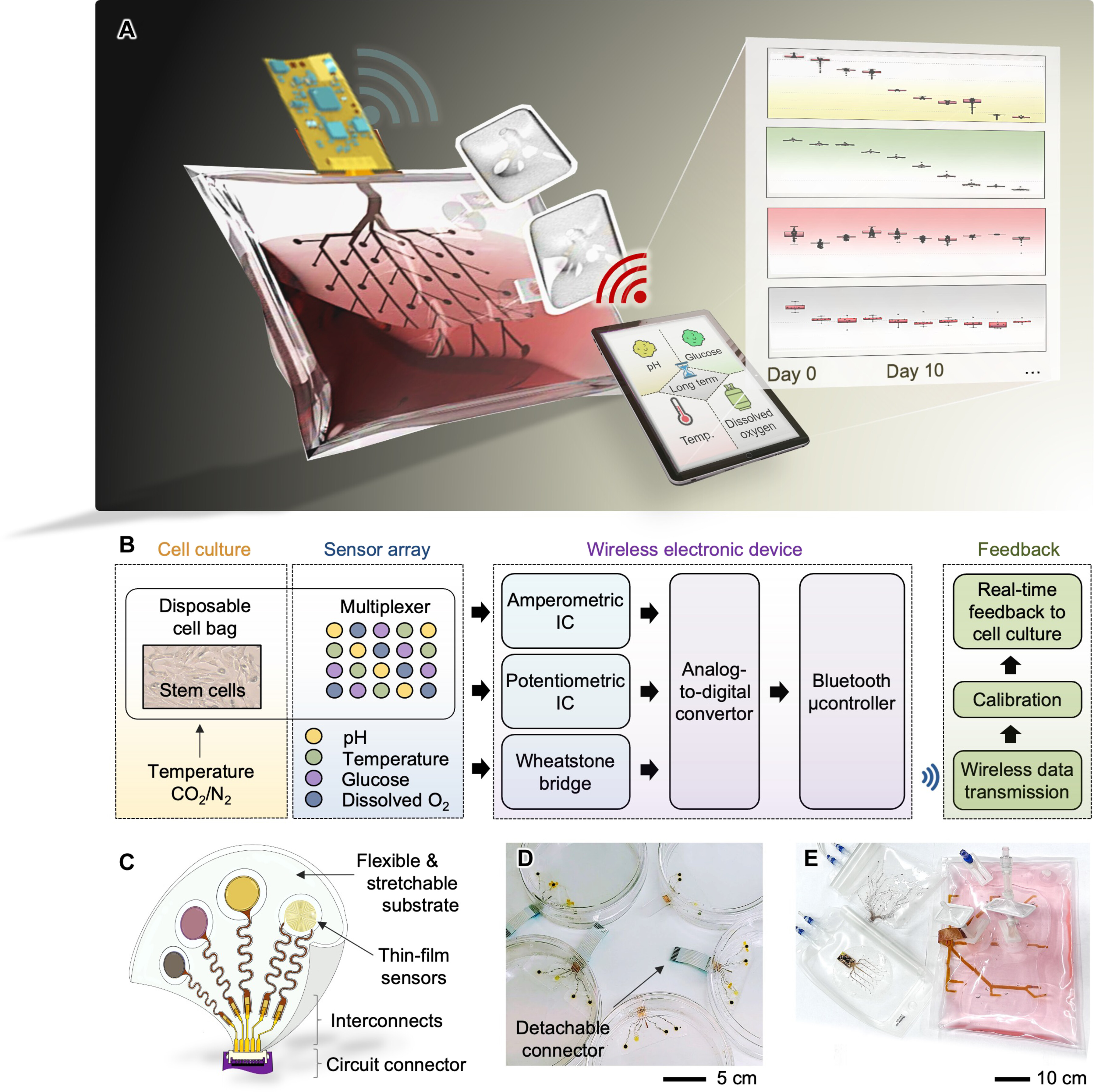
图 1.集成多变量传感器的智能生物反应器概述,用于干细胞培养的长期原位监测。
(A) 集成到一次性细胞袋中的无线多传感系统的示意图,该系统可以连续 30 天实时监测细胞培养环境。传感数据以无线方式传输到移动设备,以基于反馈的方式控制培养参数。(B) 使用智能生物反应器系统捕获干细胞培养过程的流程图。(C) 多传感器集成平台的主要功能,包括软薄膜传感器、互连和用于连接无线电路的电路连接器。(D 和 E) 照片显示了一个完整的细胞培养平台,使用带有传感器包的培养皿 (D) 和一组带有集成薄膜传感器的不同规模的细胞袋,用于在 2 升体积溶液 (E) 中对干细胞培养进行实时、连续、原位监测。
表 1.不同类型细胞监测系统的比较。
hMSCs,人间充质干细胞;iPSCs,人类诱导多能干细胞;mMSCs,小鼠间充质干细胞;C2C12,小鼠成肌细胞;mPMs,小鼠原代成肌细胞;hDFBs,人真皮成纤维细胞;HL-1,小鼠心肌细胞;CHO,中国仓鼠卵巢细胞;MRC-5,人成纤维细胞(ATCC CCL-171)细胞系;T-47D,人乳腺癌细胞系;T98G,人肿瘤细胞系;L929,小鼠成纤维细胞系;adMSCs,人脂肪来源的间充质干细胞;NHDFs,正常人真皮成纤维细胞;HaCaT,人类永生化角质形成细胞;H1 hESCs,人胚胎干细胞;GM12878,人淋巴母细胞样细胞;K562,人慢性粒细胞性白血病细胞;DO, 溶解氧;DCO公司2,溶解的二氧化碳。
*原型生物反应器的尺寸:16.5 mm × 45.5 mm。
†商用光学传感器安装在开流微灌注探头系统中。
‡商用光学传感器反复测量溶氧和DCO的含量2每隔 8 小时一次。
多功能薄膜传感器的制造
为了实现具有成本效益和可扩展的制造,我们开发了一种利用晶圆规模微纳加工、电化学材料沉积和材料转移打印的策略 (37–39)。我们使用了微纳加工技术,允许晶圆级制造固态薄膜传感器(图 2A)。通过这一系列工艺,多个晶圆包括一系列电极,该电极具有蛇形线,具有良好的拉伸性,可焊接接触焊盘可与传感器互连集成,具有出色的撕裂特性。根据传感器的目标功能,多功能电化学传感器是通过传感材料和聚合物涂层的额外沉积来制造的。图2B中的光学显微镜图像和插图描述了结构层的细节,这些结构层提供了检测(i)pH值、(ii)温度、(iii)DO和(iv)葡萄糖的功能。所有传感器(包括参比电极和反电极)的制造步骤及其功能化过程的其他细节如图所示。S1 到 S6。pH检测传感器是在IrO的基础上制造的x通过脉冲循环伏安法沉积的膜(图S7)(40,41)。 单层 IrOx容易分层,因此不能确保长期稳定性。同时,将其浸入溶液中12小时;因此,通过滴涂和薄膜固化工艺的组合制备了Nafion和聚(2-羟乙基甲基丙烯酸酯)(pHEMA)层,以提高对培养环境的传感稳定性(图S8)。薄膜电阻式温度传感器采用图案化Au电阻作为传感方法。微纳加工过程与传感平台程序几乎相同。由于不需要与流体进行物理相互作用,因此电阻器与顶部聚酰亚胺 (PI) 完全密封,除了两个用于电气连接的接触垫。线粗的轮廓如图所示。S9,显示 4 μm 以下的总厚度。葡萄糖传感器在石墨烯层上使用 PtPdPt 纳米颗粒通过安培法监测细胞培养基中的葡萄糖浓度 (42, 43)。通过石墨烯分散油墨的滴铸和随后的电化学沉积在Au表面形成PtPdPtPt纳米颗粒修饰的石墨烯结构,而Nafion则通过旋涂沉积。Pt和Pd纳米材料的各种偶联物用于开发葡萄糖传感器(图S10)。溶氧传感器使用与 NiPt 纳米颗粒掺入的电子束沉积 Pt 层 (44)。尽管Pt的表层经过处理以形成纳米结构以提高氧敏感性,但由于纳米结构的存在可以忽略不计,因此假设Pt在纯度方面始终是纯度的。为了气体分子的运输和表面官能团化,在电极顶部覆盖聚[2-甲基丙烯酰氧乙基磷酰胆碱 (MPC)–co-n–十二烷基甲基丙烯酸酯 (DMA)] [聚(MPC-co-DMA)] 水凝胶 (45)。下行图像是通过扫描电子显微镜捕获的每个传感器的传感材料的表面形态(图2B,底部图像)。它们的横截面图也如图S11所示。这些薄膜传感器使用粘合剂和焊接与准备好的互连器连接(图 2C)。我们使用微纳加工和转移印刷的组合来制造薄膜互连器,该互连器由软弹性体层上的PI封装的Cu迹线组成。顶部 PI 的图案化仅暴露底部 Cu 层的部分,从而可以集成单个传感器。通过微纳加工和激光微加工方法设计和制造了各种互连器,以适应不同类型或不同体积的细胞培养平台(图 S12)。连接安装在传感器上的互连器的无线电路包含多个组件(图 2D),例如低功耗蓝牙芯片(nRF52,Nordic Semiconductors)、前端信号调理(ADS1299,Texas Instruments)、放大器(LM324MX,Texas Instruments)和多路复用器(ADG1606,Analog Devices),以实现多个传感器数据的采集以及无线实时数据传输到连接的移动设备。该器件配备多路复用器,每个多路复用器最多允许八个传感器连接,可以处理来自传感器阵列的多个传感数据的同时传输。传感器连接原理图设计详见图.S13.无线电路可以由锂聚合物培养皿 (3.7 V) 供电,也可以通过 USB 电缆连接进行连续测量,而无需对培养皿进行充电或放电。使用充电线,几乎可以永久使用。如果使用容量为 600 mAh 的培养皿,则该设备可以在 20 小时内记录来自多达 5 个传感器通道的信号。该器件的功耗为 0.43 W。 图 2E 捕获了连接到摇摆式生物反应器用于细胞培养的电路集成细胞袋的示例。智能生物反应器系统的主要特点在影片 S2 中得到了重点介绍。
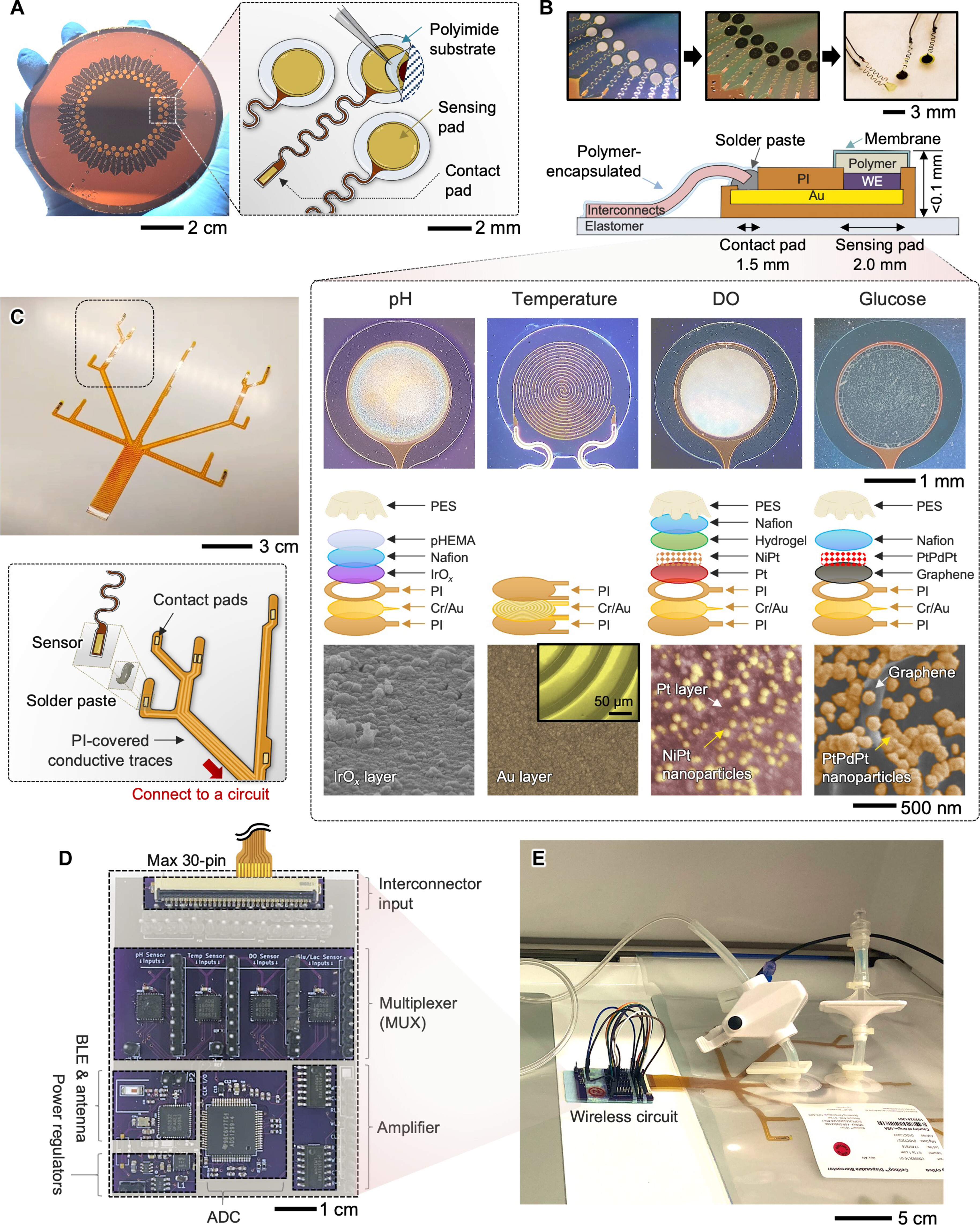
图 2.具有无线电路的可扩展多传感器平台的系统架构。
(A) 在晶圆上制造薄膜电极阵列;除传感焊盘外,所有区域均完全覆盖聚酰亚胺 (PI),可单独转移到不同的基板上。(B)活性材料电化学沉积前后的电极照片(上)和四个传感器的示意图和详细结构设计照片(下);有pH、温度、DO和葡萄糖传感器,具有不同设计的嵌入式层,用于功能化。底部扫描电子显微镜图像显示了每个传感器的顶面。(C) 用于集成四个传感器的制造薄膜互连层的照片(上图)和显示每个传感器连接到互连器的策略分解图(下图)。(D) 完整的无线电路系统的俯视图,该系统包含多个功能组件 [例如,每个传感器的多路复用器、模数转换器 (ADC)、低功耗蓝牙 (BLE) 和天线],可直接与不同类型的生物反应器集成。(E) 使用具有用于数据采集的无线电路的一次性细胞袋的生物反应器的照片。
用于检测pH值、温度、溶氧和葡萄糖的纳米膜传感器的性能验证
准确、灵敏和稳定地监测细胞培养条件要求嵌入式传感器在与生物反应器集成时表现出一致的传感器到传感器特性。在这项研究中,我们进行了一系列实验,以验证每个传感器的性能、可靠性和长期可用性。图3A显示了四个传感器,它们遵循不同的传感原理,包括电位pH传感器、电阻式温度传感器以及电化学溶氧和葡萄糖传感器。除温度传感器外,其他传感器需要参比电极,而电化学传感器则需要额外使用对电极。pH传感器测量溶液中参比电极和工作电极之间的电位差。当传感电极与具有不同pH值的溶液接触时,会产生电势,该电势与Nernst方程(即25°C时的-59.2 mV/pH值)的pH值成正比(46)。图3B总结了薄膜pH传感器在不同pH缓冲液中的特性,验证了pH值在4至10范围内的稳定读数。该传感器的平均灵敏度为−57.12 mV/pH,接近理论值,可以覆盖6.5至7.8的典型细胞培养pH值范围(47,48)。 与商用传感器(游标式)相比,7 天内的长期 pH 记录显示了传感器的稳定性。温度传感器通过测量电极材料电阻的变化来检测温度变化 (49)。电阻的这种变化是由电荷载流子迁移率的温度变化引起的。在这项研究中,使用具有较高导热系数(即317 W/m·K)和较高温度电阻系数(即0.0034/°C)的热稳定Au作为电阻器,能够在温度变化时引起更大和更迅速的电阻变化(50,51)。 图3C显示了使用三个温度传感器的实验结果。由于薄膜电阻器的温度相关电阻变化具有固有的线性特性,因此制造的传感器表现出 4.03 欧姆/°C 的均匀灵敏度。 设计简单,采用完全封装,有助于温度传感器在 7 天的监测过程中具有出色的长期稳健性。溶氧传感器通过检测传感电极 (52) 氧化产生的电流来测量溶液中的氧含量。在参比电极和工作电极之间施加电势,测量反应产生的电流并将其转换为溶解氧值。实验结果Fig. 3D捕捉了传感器在22°C下0至百万分之15(ppm)的不同氧浓度下的性能。 灵敏度超过−80.66 μA/cm2·ppm,覆盖0至15 ppm的宽溶氧范围(53)。此外,该传感器可对溶氧进行 7 天的稳定监测,而不会在传感器表面引入任何气泡。相比之下,在第 7 天,在商用溶氧传感器 (Hamilton Oxysens 120) 的表面上观察到大量气泡,导致传感信号产生噪声。与溶氧传感器一样,葡萄糖传感器检测葡萄糖分子在工作电极上氧化产生的电流。该传感器有一个涂有催化葡萄糖氧化材料的工作电极和一个参比电极。采用电沉积技术(包括循环氯化)制备超薄、稳定性良好的 Ag/AgCl 参比电极。参比电极的附加评估如图S14所示。图3E显示了葡萄糖传感器在磷酸盐缓冲盐水(PBS)中不同葡萄糖浓度(从0到60 mM)的电流信号变化,清楚地显示了不同的电流响应。该传感器的灵敏度性能显示葡萄糖浓度的线性范围为 2 至 60 mM,覆盖正常范围的细胞培养基 (54, 55)。与商用传感器(Care Touch)相比,葡萄糖传感器在7天内的性能显示葡萄糖浓度的一致记录。在设计这些传感器时,我们使用了transwell膜来减少蛋白质引起的污染(例如,与细胞的直接接触和细菌感染),并消除细胞培养过程中传感器表面的机械应力。具有亚微米小孔的亲水性低蛋白结合膜允许选择性地渗透目标材料,如葡萄糖、氧和质子,同时防止较大颗粒通过,如一般间充质干细胞(D = 15 至 30 μm)或细菌。通过使用定制的三维(3D)打印模具,我们制造了膜,如图S15所示。在这项研究中,我们测试了不同膜(包括醋酸纤维素、聚醚砜 (PES)、聚偏二氟乙烯、聚碳酸酯和聚四氟乙烯)对电位变化的影响,以优化传感器稳定性(图 S16)。膜的物理特性分布列于表S2中。其中,PES膜表现出最好的稳定性。因此,该膜安装在表面电极的顶部,并保护传感器免受细胞或任何污染物的渗透(图 S17)。

图 3.细胞培养监测系统中四个传感器的性能验证。
(A) 示意图显示了每个电化学传感器的传感器配置和工作原理,包括参比电极 (RE)、工作电极 (WE) 和对电极 (CE)。Ω,欧姆。(B)电位pH传感器在不同缓冲液中的性能(上图),其灵敏度图(中图;n = 5),薄膜传感器与商用传感器相比,长达 7 天的稳定性图(底部;n = 3)。V, 电压。(C) 电阻式温度传感器的性能,显示与商用温度传感器的比较(上图;两个传感器之间的差异可以忽略不计),灵敏度图(4.03欧姆/°C)(中;n = 3),稳定性图显示 7 天的测量一致性(底部;n = 3)。(D) 薄膜溶氧传感器在0至百万分之十五的不同溶氧浓度下的性能(ppm;上图),传感器的灵敏度图(中;n = 5),以及 7 天的 DO 测量值(底部;n = 5),与 O 低于 8 ppm 的商用氧传感器相比2. (E) 葡萄糖传感器的性能,显示盐水在0至60 mM之间不同葡萄糖浓度下的电流信号变化(上图),传感器的灵敏度图显示线性范围为60 mM(中;n = 5),以及与商业相比,7 天的稳定性图(底部;n = 5)。J, 电流密度。
计算建模结果和传感器的长期稳定性和可靠性
在这项研究中,我们进行了一系列计算和实验研究,以验证该系统的机械稳定性和可靠性,以便长期使用摇摆式生物反应器。有限元分析(FEA)是一种计算研究,用于确定开发电子系统的最佳设计布局和材料(56,57)。 这项工作中开发的四个传感器具有不同厚度的PI。图4A所示的有限元分析结果表明,在高达10 μm的任何PI厚度下,最小弯曲半径足以承受培养皿袋中的流体波动应力。当PI的厚度设置为2μm时,在传感器连续弯曲的432,000次循环中,没有发现任何损坏。在最大循环次数为 5,863,761 时观察到疲劳失效的发生。仿真参数的详细信息在材料和方法中进行了描述。图4B中关于蛇形连接器拉伸性的其他研究表明,在PI封装的Cu迹线中,在降解之前的最大伸长率为~139%。FEA研究还有助于确定为细胞培养开发的传感器中功能材料层的最佳组合。因此,图4C显示了pH、DO和葡萄糖传感器所需的最小弯曲半径。对于具有每个 x-y 坐标的 pH 传感器(例如,pHEMA 和 IrO 的组合x),由观察最大应变确定的最小弯曲半径被指定为 z 坐标。生成的 3D 曲面图显示了柔韧性的总体趋势。更薄的 pHEMA 和 IrOx膜允许更小的弯曲半径,这意味着更高的柔韧性。pHEMA和IrO选择<100 μm和<16 μm的厚度组合x,以确保有效的膜功能,表明在观察到疲劳失效之前,总共可以实现 1,498,110 次弯曲循环。此外,溶解氧传感器的水凝胶(在0至100μm范围内)和Pt(0至3μm)之间以及葡萄糖传感器的Nafion(0至30μm)和PtPdPt-石墨烯(0至100μm)之间的FEA结果表明,当整个曲线位于z平面的1 mm以下时,任何厚度组合都应产生有利的结果。计算分析表明,薄膜传感器可以承受生物反应器中细胞培养过程中连续摇摆运动引起的反复弯曲。其他有限元分析数据集,包括温度传感器和其他参比电极,如表S3至S7所示。图4(D至F)中的实验结果验证了摇摆生物反应器系统力学稳定性的计算研究。为了确保结构和功能的可靠性,传感器集成系统被放置在培养箱的摇摆模块上(图 4D)。对于长期、连续的测试,传感器集成培养皿在相同温度下填充无细胞培养基,无需气体控制。传感结果由移动平板电脑检测,通过蓝牙连接长达 30 天。视频 S3 中展示了在注入溶液发生变化时进行无线、实时和连续数据监控的演示。图 4E 显示了从连接设备检测到的接收信号强度指示器和蓝牙数据速率。这两个数据都代表了连续 7 天连续摇摆的稳定无线连接。在7天开始和结束时获得的四个传感器的光学显微镜和电子显微镜图像表明,在比较两组图像时,即使在微观尺度上也可以忽略不计(图S18)。图 4F 的顶行图表显示了四个膜传感器的电气可靠性,在无细胞介质中连续摇摆 30 天后进行了评估。所有传感器在 30 天的测量中都能保持性能变化的 1% 以内的长期稳健性。四个传感器的测得灵敏度(下行图)在整个期间的变化也可以忽略不计,这验证了在摇摆运动下使用细胞袋生物反应器进行细胞培养的可靠性能(图 S19)。在这个培养皿监测系统中,我们开发的 Android 应用程序提供了具有内置两点校准功能的信号处理。该应用程序的主要功能和校准过程如图所示。分别为 S20 和 S21。为了研究实时无线数据收集过程中可能出现的电力干扰和噪声水平,我们通过将电子设备移动到不同位置(例如,生物反应器内部、插座附近和桌子上)来测量信号,如图 S22 所示。除了靠近插座的区域外,这种干扰引起的噪声影响可以忽略不计。同样,为了确定生物反应器的摇摆运动可能产生的噪声水平,通过改变转速水平(例如,2 至 18 rpm)和角度(例如,2° 至 12°)来进行信号测量。确定进行摇摆运动的最佳条件为10 rpm和3°,可以有效地忽略噪声水平(图S23)。
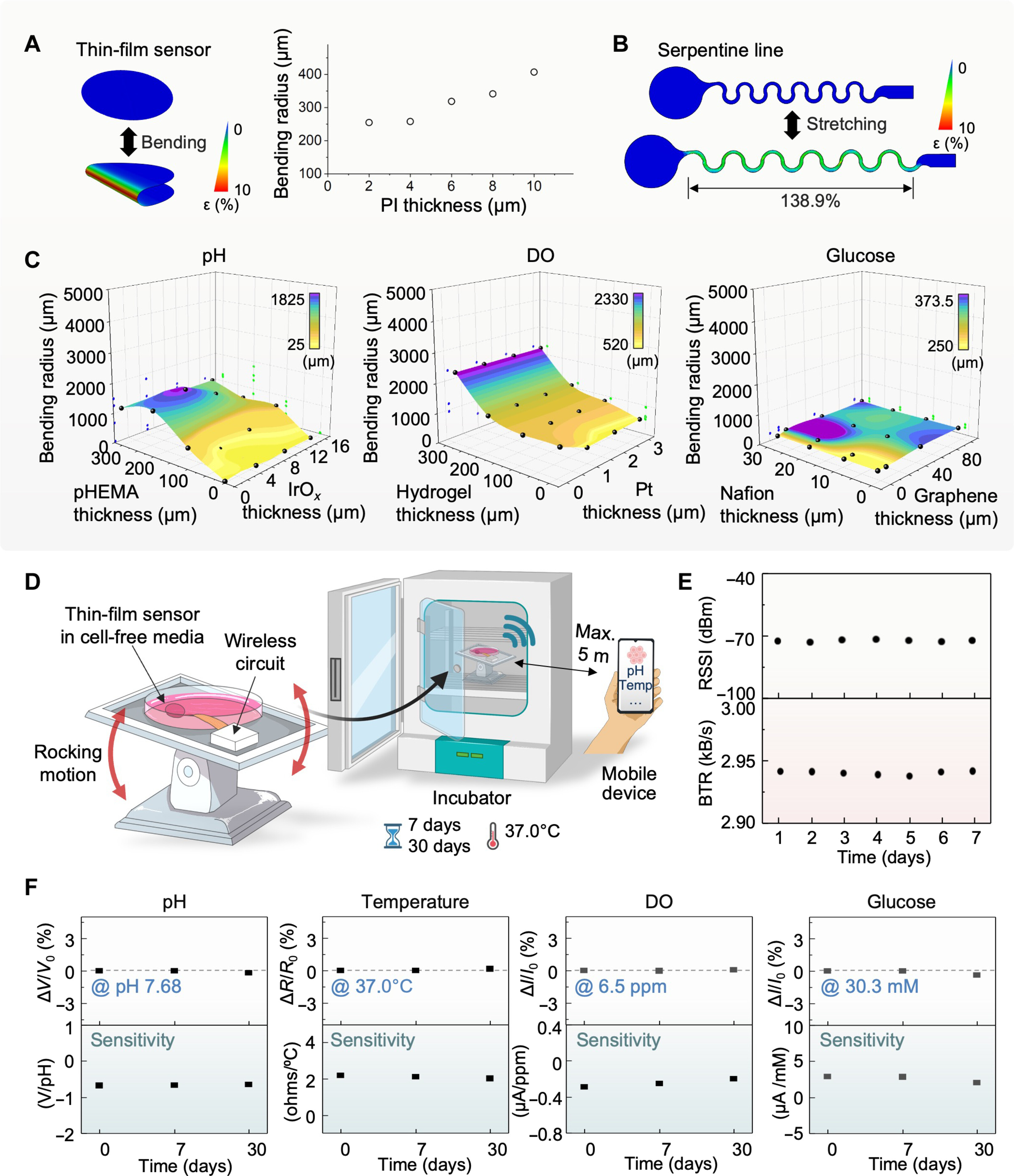
图 4.计算建模结果和传感器的长期稳定性和可靠性。
(A) 弯曲稳定性模拟,根据覆盖的 PI 厚度显示传感器薄膜的最小弯曲半径。(B) 每个传感器设计的可拉伸蛇形线的最大拉伸模拟。(C) 基于三个传感器在给定的可变膜厚度组合下的最小弯曲半径的表面图。在 55,000 次弯曲循环中,半径为 10 mm 以下的任何组合均未观察到薄膜损坏。(D) 生物反应器设置示意图,用于在生物反应器的摇摆条件下确定传感器的长期可靠性。摇摆式生物反应器位于培养箱内长达 30 天。(E) 在摇摆过程中 7 天内来自传感器的信号强度,显示系统和移动设备之间 5 m 距离处接收到的信号强度指示器 (RSSI) 和数据传输速率 (BTR)。(F) 薄膜 pH 值、温度、溶解氧和葡萄糖传感器的可靠性,在连续系统摇摆下评估至 30 天。所有传感器在性能变化的 1% 以内保持长期稳健性 30 天。
用于生物反应器系统中 3D 细胞培养的明胶水凝胶载体工程
以前,2D 培养方法已被广泛用作干细胞的标准技术 (58)。然而,这种细胞培养条件不能提供生理相关的微环境,从而影响细胞活性和功能 (59)。在塑料和玻璃表面上培养细胞通常表现出异常行为,例如扁平形态、异常极化、对治疗剂的反应改变以及分化表型的缺失 (58, 60–62)。因此,对于 3D 细胞培养,本研究使用载有细胞的水凝胶作为生物反应器中细胞培养的支架(图 5)。具体来说,我们开发了生物相容性明胶水凝胶(GHs;GH)由辣根过氧化物酶(HRP)和H原位交联反应形成2O2 (63-65)。水凝胶已被广泛用作组织工程支架,因为它们可以提供模拟体内条件的生物物理和生化特性的微环境(58,59,66)。 在 3D GH 水凝胶(图 5A)中,由于 3D 基质、动态条件和精确控制参数的协同效应,靶标干细胞与生物反应器结合封装,以提高培养质量 (67)。圆柱形GH水凝胶(图5B)具有多孔结构,可将细胞附着在表面(2D)或细胞封装(3D),并精确控制形状和大小(直径550μm,高度400μm)。使用最佳 GH 支架,人间充质干细胞 (hMSC) 可以在静态 3D 体外培养中存活和增殖,而不会产生任何细胞毒性作用 (67)。图5C中的实验结果显示了不同H下形成的GH水凝胶的力学性能和体外蛋白水解降解行为2O2浓度范围从 0.42 mM(表示为 GH-L)到 1.31 mM(表示为 GH-H)。GH水凝胶的弹性(G′)和粘性(G“)模量高度可控,这些值与天然组织的弹性相当。此外,GH水凝胶在胶原酶存在下表现出可控的生物降解特性,胶原酶是细胞在组织重塑过程中用于细胞增殖和迁移的分泌酶。为了给细胞培养提供有利条件,本研究优化了水凝胶的机械和可生物降解性能。图5D中的两个实验装置验证了使用波浪生物反应器进行3D干细胞培养的性能,为细胞生长提供了摇摆运动。本研究制备了含有hMSCs的圆柱形GH水凝胶,并将其转移到50 ml培养板中作为对照组,转移到1 L透气袋中作为实验组。之后,将培养板在常规培养箱中以 37°C、5% CO 孵育2和 95% 的湿度,同时将袋子放在摇杆上以均匀混合介质。外部条件,包括温度和一氧化碳2浓度,保持恒定。在第 5 天,收集负载 hMSC 的 GH 水凝胶,并用钙黄绿素-AM/乙锭同源二聚体-1 (EthD-1) 和 Phalloidin-iFluor 647/Hoechst 试剂对细胞进行染色,以评估细胞活力和形态。图5E中的图像显示了培养的hMSCs的活/死染色和细胞形态学的结果。在静态和搅拌条件下,大多数细胞都是有活力的。已观察到绿色染色的活细胞在水凝胶基质内均匀分布,细胞活力>93%(图5,F和G)。这两种条件都表现出细长良好的 3D 细胞扩散以促进细胞增殖。也就是说,未暴露于机械刺激的收获的 hMSC 与通过生物反应器暴露于连续摇摆的 hMSC 之间没有明显区别。图S24总结了在搅拌下GH水凝胶中收获的hMSCs的时程形态变化和细胞生长。水凝胶内的hMSC细胞发生形态变化,从第1天的圆形转变为第5天的纺锤形。同时,活细胞数量增加,细胞计数试剂盒-8 (CCK-8) 测定证明了这一点。从第 1 天到第 5 天,光密度 (OD) 增加了三倍,表明细胞数量增加。为了证实 3D 水凝胶在提供最佳细胞环境方面的功效,我们使用一种方法来创建 2D 圆盘形水凝胶。使用相同的方法,我们封装了hMSC细胞并促进其生长5天。总结结果如图所示。S25 展示了 3D 水凝胶基质内细胞外围细长突起的显着发展。这一观察结果强调了3D水凝胶为细胞培养建立稳定和有利条件的能力。因此,我们成功地证明了在生物反应器中使用3D水凝胶进行体内细胞培养的优越性。

图 5.在生物反应器系统中进行 3D 细胞培养的 GH 载体工程。
(A 和 B) 通过酶介导的交联反应形成的细胞明胶-羟苯基丙酸 (GH) 水凝胶载体的示意图和照片,用于干细胞培养与生物反应器 [辣根过氧化物酶 (HRP)]。(C) 不同H形成的GH水凝胶的力学性能及体外蛋白水解降解行为2O2浓度[0.42-1.31mM;标记为GH-L(低H2O2)、GH-M(中H2O2)和 GH-H(高 H2O2)].G′和G“分别表示弹性模量和粘性模量。(D) 常规培养箱(左;静态对照组)和摇摆式生物反应器(右;搅拌实验组)中 3D hMSCs 培养的实验设计。详细条件如下表所示。(E) 荧光图像显示收获的 hMSC 的高活力(左)和培养细胞的细胞形态(右)图像。DAPI,4′,6-二脒基-2-苯基吲哚。(F) GH水凝胶中显示的细胞分布。(G) 在对照(培养箱)和实验(生物反应器)中培养的 GH 水凝胶中细胞活力的比较 [不显着 (ns)]。
使用生物反应器系统监测人 iPSC 培养物
人诱导多能干细胞 (iPSC) 可通过对分化的人细胞进行重编程获得 (68)。iPSCs的产生解决了与胚胎干细胞相关的局限性,特别是与伦理问题相关的局限性。使用 iPSC,研究人员可以为再生医学创建各种疾病模型,并培养肝细胞、神经元或其他细胞类型来设计个性化治疗模型 (69)。因此,iPSC的产生成为进一步研究的主要要求。iPSC生产过程中的参数监测可以提高细胞生产效率,并有助于扩大生产规模,因为我们可以通过精确的参数控制保持细胞生长的最佳条件。在iPSC培养的第一天,小菌落粘附在直径为100至200μm的基质胶包被的培养皿上(图S26)。安装生物传感器2天后,iPSC菌落继续生长并扩增了3倍以上。菌落紧凑,边缘清晰,所有细胞都表现出较高的细胞核/细胞质比,这表明 iPSC 的形态正确且无分化 (70)。在第 4 天,iPSC 表现出强劲的生长,达到 80% 以上的汇合度,表明它们已准备好传代和储存。在安装了生物传感器的情况下,达到完全汇合的 iPSC 所需的形态、汇合度和时间与对照 iPSC 相似。这表明生物传感器对iPSC培养没有明显的影响。图S27完整记录了5天内iPSC培养的监测结果。将四种不同类型的传感器(pH、温度、溶解氧和葡萄糖)排列成四组并放置在培养皿中。培养基溶液每隔一天更换一次。在第 5 天,观察到 pH 值、葡萄糖和溶氧显着下降,表明从传感器 4 区域开始存在潜在的污染问题。
使用生物反应器系统监测 mPM 增殖和分化
原代细胞是从特定组织类型中收获的成熟细胞。在组织工程策略中使用原代细胞的主要优点是它们具有潜在的免疫相容性。在病理学研究的实验模型中,另一个优点是它们保留了与体内器官非常相似的功能和表型。然而,寿命有限、密度、快速表型变化、可用性和供体间变异性等挑战阻碍了它们在应用中的进展。为了解决这些局限性,体外原代细胞培养,精确控制定义微环境的变量,被认为是最小化细胞变化的重要程序。在这项研究中,我们培养了从 Pax7/TdTomato 小鼠中分离的小鼠原代成肌细胞 (mPM),并应用生物传感器来监测有关细胞培养条件的各种参数。图6A中的实验装置显示了培养箱中用于静态mPM培养的细胞培养皿,以验证其稳定性。将mPM连接到基质胶包被的培养皿上后,安装了四个生物传感器,类似于图S27所示的设置。在 2 天内,成肌细胞增殖,增强细胞密度并达到 ~80% 汇合度(图 6B)。随后,培养基被切换到分化培养基。mPMs经过分化、迁移和融合形成肌管。此外,成肌细胞和肌管不断融合,导致在第 4 天形成更大的肌管。此外,肌管表现出相互融合的能力。在安装和不安装生物传感器的mPM之间没有观察到显着差异(图S28)。图6C分别显示了使用不同细胞培养基溶液进行增殖和分化的mPM培养过程中的完整记录数据。在细胞分化过程中的pH值变化中观察到一个有趣的结果;四个pH传感器彼此相距至少3厘米,记录了pH值的显着变化,范围从7.0到7.8。然而,每个传感器达到最低pH值的发生发生在不同的时间点,强调了与区域信息相关的本地监测的重要性。同时,商用pH传感电极无法捕捉到精确的变化。

图 6.使用两个代表性系统演示细胞培养。
(A) 在常规培养箱内静态培养小鼠原代成肌细胞 (mPM)。(B) mPM的代表性光学图像,显示细胞随时间推移的渐进性细胞生长(第2天)和随后的分化(第4天)。(C) 监测结果,包括 pH 值变化、温度变化以及细胞培养基中 DO 和葡萄糖的水平随时间的变化。所有图表中的红色填充圆圈表示使用商用传感器或实验室传感器获得的测量值。(D 至 F)使用生物反应器进行大规模、搅拌、GH 封装的干细胞培养。(D) 带有刚性无线电路原型的柔性传感器集成 2 升细胞袋的照片,以及生物反应器内水凝胶中 hMSC 培养的实验条件。(E) 在生物反应器中培养 9 天的代表性细胞形态。(F) 连续9天的监测结果。所有图表中的红色填充圆圈表示使用商用传感器或实验室传感器获得的测量值。
使用生物反应器系统进行 GH 封装细胞培养的演示
本研究的重点是展示两种不同系统的GH封装干细胞培养。培养皿中的传感器集成系统可以对 C2C12 细胞进行 6 天的无线、实时、连续监测(图 S29)。照片见图。S29A 显示培养基中细胞计数增加和细胞形态延长 6 天。细胞培养在线监测实验结果的详细信息见图。S29B,显示两个数据集:一个没有单元格,另一个有单元格。与哺乳动物细胞培养一致,由于细胞代谢引起的培养基酸化和脱氧,测得的 pH 值和葡萄糖水平呈下降趋势 (8)。在四个传感器的性能验证方面,我们的纳米膜无线电子系统与点可测量的商业传感器表现出很好的一致性,无论介质中是否存在细胞。与传统传感器的离散数据记录不同,一体化智能系统可对培养箱内的在线培养过程进行无线、连续、实时监控,而无需多个传感器和单独的数据采集工具。此外,我们的系统避免了在培养箱打开以进行细胞采集或pH测量期间温度波动和氧气供应不足造成的污染和不良后果的风险。图中的数据。S29 在仅包含不含细胞的细胞培养基的环境中呈现监测数据,与从商业传感器获得的数据点相比,显示出高度恒定和连续的进展。此外,我们的研究表明,使用连续摇摆模块成功监测小鼠MSC(mMSC)培养物中的细胞生长(图S30)。随着培养时间的延长,生物反应器系统保持了对温度和溶氧水平的精确控制,而pH值和葡萄糖值与初始值相比下降了50%,表明细胞袋内mMSCs的增殖。传感器集成的波浪生物反应器系统展示了对干细胞的大规模、长期原位监测(图 6D)。本研究使用人类间充质干细胞,并在连续摇摆运动下监测 9 天内的培养过程。商用 2 升一次性培养皿袋集成了膜传感器和电子元件(图 S31)。pH、葡萄糖、溶氧和温度值的实时数据采集示例出现在生物反应器系统的视频 S1 和 S2 中。图6E中的结果显示了hMSCs通过含有细胞负载的GH水凝胶的等分试样的活/死细胞染色测定的活力(参见图S32分别显示每个通道)。这种出色的细胞活力(>95%)证明了传感器集成平台具有完全的生物相容性,能够连续监测所有参数,而不会产生任何细胞毒性作用。此外,与第 0 天的细胞形态相比,培养超过 9 天的 hMSC 表现出高度可拉伸的形态,表明细胞生长良好。干细胞随时间增加的能力证实了我们系统提供的有利培养条件。这一结果证实了一体化系统在提供稳定和连续监测结果方面的有效性和可靠性(图6F)。与其他细胞培养物类似,成功的细胞代谢导致 t 的酸化和脱氧培养基,pH值和葡萄糖水平持续下降证明。在培养过程中,每天通过细胞袋上的收获线收集培养基样品,并使用商业探头进行测量,以比较设备的性能,这会导致温度、pH 值和 DO 读数的轻微波动。多变量传感器平台可以通过每个具有代表性的工作电极集成多达 8 个有源传感器来定制以适应大规模细胞培养。实验结果如图所示。S33 显示从两个传感器阵列获得的 hMSC 培养。传感器阵列 #1 放置在培养皿袋的中间,而传感器阵列 #2 则集成在袋子边缘附近。这些结果显示出一致的趋势,但空间差异很小,这表明这种多变量传感器阵列有可能提供有关细胞分布的准确空间信息,并识别具有异常pH或温度条件的区域。总的来说,这项研究首次展示了一种大型智能生物反应器,该生物反应器具有完全集成的无线多传感器和电子设备,用于干细胞培养的长期原位监测。与以前的工作(表1)相比,该系统的主要优势是高数据采样率、集成无线传感器、长达 30 天的监控以及从培养皿到 2 升细胞袋的可扩展性。通过使用灵活和多变量的传感器阵列,我们的平台实现了对细胞需求的实时和连续监测,捕捉了培养条件的时空变化。高通量细胞制造的这一进步能够精确调整营养喂养策略和优化生物反应器条件,最终提高细胞密度、提高生产率和大规模细胞生产。
讨论
这里介绍的智能生物反应器系统展示了一条在临床和研究环境中实现可扩展、低成本和反馈细胞生产的有前途的途径。完全集成的传感器和电子设备以及摇摆式生物反应器可准确、无线和实时监测不同类型细胞的 pH、温度、DO 和葡萄糖,包括 iPSC、mPM、C2C12、hMSC 和 mMSC。该系统能够持续评估培养环境中的空间和时间变化,为高通量细胞生产提供并行反馈和主动管理功能。柔性电化学和电传感器的纳米膜组表现出出色的灵敏度,传感器尺寸比刚性商用传感器更小。这项实验研究在连续摇摆运动下进行了 30 天,验证了该设备的结构完整性、寿命和柔性无线传感器的可靠性,显示灵敏度在时间跨度内的变化小于 1%。使用生长激素载体,我们的系统展示了使用 2 升细胞袋式生物反应器系统进行干细胞培养的准确性、可重复性和可扩展性。此外,我们的生物传感器可以原位精确监测细胞培养基中的pH值、温度、溶氧和葡萄糖,克服了标准细胞培养的局限性。细胞以不同的速率生长,因此很难理解培养基中变化的日常发生 (8)。因此,精确控制这些参数可以提高体外细胞培养的可重复性,并准确概括生理条件,特别是对于敏感细胞,如iPSC或原代细胞。保持稳定的参数为在各种生物医学研究背景下建立实验结果的相关性提供了更大的机会。未来的工作将集中在其他在线过程监测传感器的工程开发上,并通过更大的细胞袋和多个生物反应器平台验证系统的可扩展性,以实现治疗性细胞和干细胞的确定性、高质量生产,用于广泛的临床和工业用途。
材料与方法
pH传感器的制造
传统的微纳加工工艺用于制造柔性薄膜型pH传感电极。pH传感电极通过电沉积在三电极配置中选择性地功能化。该装置包括一个商用 Ag/AgCl 参比电极、一个由铂化钛网制成的对电极,以及与电化学工作站相连的精制金 (Au) 电极。pH传感器的传感组件涂有氧化铱(IrOx) 通过电沉积。电沉积溶液包括 4.5 mM 四氯化铱 (IrCl4;Thermo Fisher Scientific)、130 mM 过氧化氢 (H2O2;默克公司)和 40 mM 草酸二水合物 (C2H2O4·2H2O;Sigma-Aldrich),使用无水碳酸钾(K2一氧化碳3;西格玛-奥尔德里奇)。将混合物在室温下储存在深琥珀色瓶中 2 天以确保稳定性,然后再在 ~4°C 下冷藏直至进一步使用。将金工作电极浸没在该溶液中,并对商用 Ag/AgCl 电极施加脉冲电位(0.7 V 持续 2 秒,随后 0.0 V 持续 10 秒关闭),总共 300 个脉冲。在 IrO 形成时x在pH敏感层上涂覆了2.5%的Nafion(Sigma-Aldrich)和pHEMA膜,以提高生物相容性并延长传感器的使用寿命。用甲基丙烯酸2-羟乙酯(Sigma-Aldrich)、乙二醇二甲基丙烯酸酯(Sigma-Aldrich)、1-十二醇(Sigma-Aldrich)和2,2′-偶氮双(2-甲基丙腈)(Sigma-Aldrich)制备pHEMA前驱体溶液。随后将膜在130°C下热固化10分钟。将最终确定的薄膜传感器固定在柔性基板(例如PDMS)上,并通过焊接连接电线。为了保护连接,同时将传感器表面暴露在分析物溶液中,连接点用PDMS封装。图 S1 提供了其他制造细节和插图。
温度传感器的制造
薄膜温度传感器是使用光刻图案化的金电阻器制造的,其微纳加工工艺类似于电化学传感器。最初,将聚二甲基硅氧烷 (PDMS)/PI 的复合层旋涂在 100 毫米硅晶圆上以形成衬底。随后,为铜(Cu)层创建了蛇形图案,该图案通过溅射沉积。随后是铬 (Cr) 和 Au 层的顺序层压以形成电阻元件。在金属层沉积后,整个结构被额外的PI层封装,然后对其进行图案化,仅露出电气连接所需的接触垫。该顶部 PI 层的图案化是使用反应离子蚀刻工艺实现的,该工艺选择性地去除 PI 材料以露出下面的接触垫。为了清楚起见和指导,图S2中详细说明了温度传感器制造过程的每个步骤的示意图。
溶氧传感器的制造
柔性溶解氧传感器通过在铂(Pt)层上电沉积,然后在镍(Ni)和Pt纳米颗粒上沉积来生产。图 S3 显示了柔性 Au 电极上溶解氧传感器的制造过程的示意图。使用直流电源进行铂沉积,设置为0.01 mA/cm23分钟。沉积槽中含有0.035 M氯铂酸六水合物(H2氯化铂6·6H2O;Sigma-Aldrich)和0.5M硫酸(H2所以4;J.T.贝克)。随后使用三电极恒电位仪将Ni/Pt纳米颗粒电沉积到Pt层上,将电极浸入相应的前驱体溶液中。电流密度:−3 mA/cm2从电镀液(Sigma-Aldrich)中施加5分钟以沉积Ni,并在100 mV/s下分三段使用−0.4至1.0 V的电位扫描,用于对商业Ag/AgCl参比电极的Pt沉积。然后将Nafion层施加到表面上并风干30分钟。为了表面功能化,引入了由poly(MPC-co-DMA)组成的水凝胶作为透气层。
葡萄糖传感器的制造
在石墨烯片上制造了一系列葡萄糖传感器,上面有电沉积的Pt和钯(Pd)纳米颗粒,以创建基于PtPdPt电催化剂的葡萄糖传感器,旨在用于细胞培养环境。为了解决催化传感器由于环境中的化学和氧气浓度而快速失去活性的问题,我们追求一种无酶传感器设计,以增强细胞培养过程中的传感能力。PtPdPt纳米颗粒沉积在石墨烯片上,有利于纳米催化剂的分散而不聚集。将0.5 wt%石墨烯片状粉末(Sigma-Aldrich)混合在200 ml纯乙醇中,然后进行广泛的超声处理,制备石墨烯分散体。每个具有大量 Au 电极的晶圆都用 O 处理2等离子体~1分钟,使金电极表面更亲水,然后滴铸石墨烯分散体。对于每个单个金电极,使用微量移液管施加0.5μm石墨烯溶液,然后将晶圆置于设置为60°C的热板上完全干燥5分钟。石墨烯片在金导体上滴涂和干燥后,通过循环电沉积实现了纳米颗粒的形成。图 S4 描绘了柔性 Au 电极上的葡萄糖传感器制造步骤。使用前面描述的三电极系统,将PtPdPt纳米颗粒电沉积到石墨烯衬底上。将用于葡萄糖检测的电极浸没在温和的硫酸基溶液中,施加不同的电位:Pt在5个周期内以100 mV/s从−0.4到1.2 V,Pd在100 mV/s下从−0.4到1.0 V,与商用Ag/AgCl电极相比。随后,在顶部加入Nafion层并在空气中干燥30分钟。
参比电极和对电极的制造
参比电极和对电极由金电极通过与其他传感器相同的微纳加工工艺制成。此外,银 (Ag) 沉积、电化学氯化和膜涂层是制备参比电极不可或缺的一部分。通过混合0.02 mM硝酸银(AgNO3;Sigma-Aldrich)和1M硝酸钾(KNO3;西格玛-奥尔德里奇)。将裸露的金电极浸入该制备的溶液中,并在−0.4 V下对商业参比电极进行恒电位扫描5分钟,导致金沉积。对于氯化,由0.1M氯化钾(KCl;Sigma-Aldrich)和0.01M盐酸(HCl;Sigma-Aldrich)准备好了。将银沉积的电极浸入稀释的HCl溶液中后,进行循环伏安法,以50 mV/s的扫描速率在五个段上扫描0.1至0.4 V的电位。要了解Ag/AgCl表面对不同pH值的电压稳定性,聚乙烯醇缩丁醛(PVB;Sigma-Aldrich)基质(含KCl)用作盐桥。将PVB、KCl和甲醇混合制备PVB-KCl膜混合物。将混合物滴涂在Ag/AgCl电极上后,将表面干燥过夜。在Ag/AgCl/PVB-KCl表面加入额外的Nafion膜,以避免KCl盐从Ag/AgCl/PVB-KCl表面浸出,并在空气中干燥30 min。图S5和S6显示了参比电极和对电极的制造过程示意图。
计算分析
分析软件(fe-safe、3DS)与 ABAQUS 结合使用,用于检查机械弯曲模拟的故障。表 S1 列出了用于制造传感器的材料及其各自的特性,例如允许的厚度范围、模量和最大应变 (71–78)。一些层被分配了固定的厚度值,以简化问题并确保传感器功能。为了显示五个传感器的最小弯曲半径,在 ABAQUS 环境中创建模型表示。它们以不同的半径弯曲到 180°,直到在任何层中观察到最大应变。如果观察到大于 45° 的弯曲度,则两种材料的特定组合被认为是具有指定弯曲半径的可弯曲的。所有数据点都标记在 3D 绘图空间中。
电化学传感器的表征
对电化学传感器进行表征,以评估其选择性、灵敏度和重现性。为了简化电路,电位pH传感器使用双电极系统,Ag/AgCl电极既用作参比电极,也用作对电极。将传感器浸没在不同pH值的溶液(如pH 4、pH 7、pH 10和pH 7.4的PBS溶液)中时测量pH电位,以生成校准曲线,并将性能与从商用pH传感器(Vernier Go Direct pH传感器)获得的数据进行比较。为了确定温度监测校准曲线,当溶液在20°至60°C的范围内加热时,测量了用作工作电极和参比电极/对电极的金线圈两个尖端之间的电阻。 为了与商用温度传感器(Go Direct 温度探头、游标)进行比较,将两种类型的传感器置于 60°C 的加热溶液中,并在将相对较冷的溶液添加到温溶液中时监测每个传感器的值。来自电化学传感器(特别是溶氧传感器和葡萄糖传感器)的电流数据分别在−0.4和0.25 V的施加电压下记录。通过充分吹扫N制备具有不同DO水平的校准溶液2/O2使用商用溶氧传感器(Hamilton Oxysens 120)评估气体混合物及其数值。通过将不同量的 d-(+)-葡萄糖粉(99.5%,Sigma-Aldrich)溶解在 PBS 溶液中来制备用于测量葡萄糖水平的校准溶液,以达到 1 至 60 mM 范围内的葡萄糖水平。使用商用传感器(Care Touch)测量每种葡萄糖溶液的葡萄糖水平。在使用无线硬件操作之前,使用有线电化学分析仪(Interface 1010E,Gamry Instrument)对传感器进行表征。
传感器阵列系统的制造
在选择培养平台时,需要考虑两种主要选择:适用于100 ml以下体积的培养皿规模平台和设计用于体积超过500 ml的细胞袋规模平台。平台的选择取决于目标传感阵列的所需尺寸。此外,可以根据所选平台和目标阵列尺寸选择制造方法。两种可能的方法包括晶圆级微纳加工,这是一种更复杂、更精确的工艺,适用于较小的阵列,以及简单的激光切割,这是一种更直接、更具成本效益的选择,适用于更大的阵列。为了在平台规模方面进行比较,图。S12 显示两个不同过程的代表性照片。表S8列出了传感器阵列(总共由36个传感器站点组成)的粗略制造成本,材料成本低于每单位设备0.93美元。
集成一体化传感平台
准备了电化学传感器和传感器阵列,并通过焊接进行了电气互连。随后,所有电极的活性表面都覆盖了3D结构PES膜,以防止环境干扰。为了减轻电信号传输过程中的外部干扰,使用可固化聚合物(如医用级环氧树脂或PDMS)来封装连接。这种封装用于将组分与离子扩散在细胞培养基中引起的子反应或副反应隔离开来。组装完成后,集成传感平台被转移到细胞培养袋或培养皿中。传感平台的底面涂有医用级环氧树脂,以将其固定在基板上。用 70% 乙醇溶液对细胞培养袋或培养皿进行灭菌,然后暴露在紫外线 (UV) 下超过 12 小时,以确保彻底灭菌。使用前,用 Dulbecco 的 PBS(DPBS,1× 对平台进行了大量冲洗;Gibco) 去除任何残留的灰尘。
无细胞培养试验
为了验证传感平台的长期稳定性和完整性,通过连续摇摆运动进行无细胞培养。通过混合Dulbecco改良的Eagle培养基(DMEM;Gibco)和 10% 胎牛血清 (FBS;Gibco)和1%青霉素-链霉素(PS;Gibco)。将集成传感平台浸没在无细胞培养基中,并放置在培养箱中的单轴摇杆上。在连续摇摆的第 7 天和第 30 天定期检查机械故障、电气连接和传感器/电子性能。数据被无线传输到距离孵化器5米的移动设备。实验装置示意图如图4D所示。
摇摆式培养箱系统的准备
为确保对细胞袋内的内部空间进行彻底消毒,实施了细致的两步流程。首先,该系统经过严格的清洁程序,包括用 70% 乙醇溶液进行三轮处理。随后,该系统在紫外线下暴露了 12 小时。紫外线灭菌后,用PBS轻轻清洗内部的整个细胞袋,以消除任何残留的乙醇痕迹。与传感器集成的细胞袋被固定在摇摆式生物反应器系统(WAVE Bioreactors,GE Healthcare)上,该系统被编程为以 3° 角和 10 rpm 的速度振荡。该装置维持了长达 10 天的时间,确保了 37°C 的恒定温度和 CO2浓度为5%。在整个摇摆运动过程中,培养基完全浸没了整个传感器系统,为细胞生长和评估提供了最佳条件。评估了电化学传感器的稳定性和连续运行。因此,没有对培养基进行任何更改,仅观察干细胞增殖过程中电化学传感器的性能。通过将DMEM(Gibco)与10%FBS(Gibco)和1%PS(Gibco)混合来制备C2C12生长培养基。类似地,mMSC生长培养基是通过将DMEM与10%FBS和1%PS组合来配制的。此外,使用间充质干细胞基础培养基(MSCBM;龙沙)。
在细胞培养板中制备人 iPSC 和 mPMS
人iPSCs购自STEMCELL Technologies(加拿大不列颠哥伦比亚省温哥华市)。在这项研究中,在70ml mTeSR Plus培养基中,在基质胶包被的150-mm组织培养皿上培养第5次传代的iPSC。在1天内实现完全附着后,安装生物传感器以监测各种参数。培养基交换每 2 天进行一次,直到致密菌落和/或扩大区域达到 ~80% 汇合。对于对照样品,在不安装生物传感器的情况下以类似的方式培养iPSC。通过使用 ECHO 旋转显微镜第 2 代(美国加利福尼亚州圣地亚哥的 BICO 公司)进行观察,鉴定了 iPSC 的形态。使用预铺板方法从Pax7 / TdTomato小鼠(3.06个月大)中分离mPM。对两只小鼠分别实施安乐死以分离mPMs;一只小鼠被指定用于生物传感器安装,另一只用作对照。对于每只小鼠,解剖来自两个后肢的肌肉并收集在PBS中。去除可见的脂肪、神经沉积物和肌腱后,使用手术剪刀在灭菌的塑料板上切碎肌肉,形成糊状物。用在DMEM中制备的5ml 0.2%II型胶原酶(LS004177,Worthington Biochemical,Freehold,NJ,USA)消化糊状物。在 37°C 下孵育 60 分钟后,使用 20 号注射器针头混合消化的肌肉溶液,然后加入 40 ml DPBS。然后通过40μm尼龙网过滤器过滤切碎的肌肉悬浮液,并将离心后获得的细胞沉淀重悬于10ml生长培养基(DMEM,20%FBS和1%PS)中。将含有细胞的生长培养基在胶原包被的 100 毫米培养皿中孵育 16 小时,然后转移到另一个涂有胶原蛋白的 100 毫米培养皿中。3小时后,将含有细胞的生长培养基移至基质胶包被的100mm培养皿中,并加入碱性成纤维细胞生长因子(bFGF;10ng / ml)。24小时后,弃去有碎片的培养基,更换补充有bFGF(10ng / ml)的新鲜生长培养基。接下来的 24 小时后,将附着的细胞胰蛋白酶化、离心并重悬于含有 bFGF (10 ng/ml) 的 10 ml 新鲜生长培养基中。将这种含有细胞的生长培养基在胶原包被的培养皿中孵育5分钟,轻轻摇动以悬浮未附着的细胞,并重复孵育和摇动步骤五次。然后将溶液移至基质胶包被的 150 mm 培养皿中,并加入 60 ml 含 bFGF 的生长培养基。在细胞附着一天后,在更换含有bFGF(10 ng / ml)的新鲜生长培养基后安装生物传感器。对于对照样品,使用来自第二只小鼠的mPM,无需安装生物传感器,并且所有步骤都保持不变。培养2天后,将细胞切换到分化培养基(DMEM,2%马血清和1%PS),2天后交换分化培养基。通过使用 ECHO 旋转显微镜第 2 代(美国加利福尼亚州圣地亚哥的 BICO 公司)进行观察,鉴定了 mPM 和肌管的形态。
细胞水凝胶的制备
使用苯酚含量为144 μmol/g的明胶-羟基苯基丙酸(GH)制备了包裹靶细胞的水凝胶。在HRP(VI型,250至330U / mg)和H2O2(Sigma-Aldrich,美国密苏里州圣路易斯)。水凝胶刚度由流变仪(MCR 302e,Anton Paar USA Inc.,Houston, TX, USA)在振荡模式(锥板,应变的1%,角频率为5 rad/s)下测定。选择 C2C12 成肌细胞(第 9 代)、小鼠骨髓来源的 mMSC(从 C57BL/6 小鼠的股骨中分离)和 hMSC(第 4 代,Lonza)作为实验的细胞来源。将细胞与明胶-羟基苯基丙酸(GH;5.0 wt %)以106个细胞/ml的密度均匀混合。在微管A中,GH/细胞混合物(90μl)和H2O2溶液(10μl,0.09%)轻轻涡旋。在微管B中,分别制备GH/细胞混合物(90μl)和HRP溶液(10μl,0.015mg / ml)。为了形成充满细胞的GH水凝胶,将溶液A和溶液B混合并加入PDMS(Corning Sylgard 184)模具中。凝胶形成15分钟后,GH/细胞水凝胶立方体,具有3.0×105每立方体的细胞,被转移到含有1升细胞培养基的灭菌细胞袋中。对于GH/C2C12水凝胶,采用含有10%FBS和1%PS的DMEM制备生长培养基。对于GH / hMSC水凝胶,通过混合MSCBM基础培养基(PT-3238,Lonza)和MSCGM SingleQuots添加试剂盒(PT-4105,Lonza)制备生长培养基。
培养细胞的表征
描述了监测细胞培养各个方面的方法,包括细胞活力、活细胞/死细胞比例、细胞形态和蛋白质含量,为细胞行为和整体培养质量提供了有价值的见解。用光学显微镜(Axioscope 5,蔡司)进行细胞形态观察。细胞接种 5 × 105每个培养皿的细胞在直径为 100 mm 的所需培养板中,并在 5% CO 中孵育2和 37°C。 细胞接种后,监测细胞形态,每天获得图像。在细胞袋中培养后的 GH/细胞水凝胶用 LIVE/DEAD 活力/细胞毒性试剂盒染色以评估细胞活力。为了定量活细胞,根据制造商的说明进行CCK-8(ALX-850-039-KI01,Enzo Life Sciences Inc.,Farmingdale,NY,USA)。此外,还用鬼笔环肽-iFluor 647 (ab176750) 和 Hoechst 33342、三盐酸盐三水合物 (10 mg/ml) 溶液对一些 GH/细胞水凝胶进行染色,以观察细胞形态。对于CCK-8测定,将每种GH / hMSC水凝胶在含有900μl细胞培养基和100μlCCK-8试剂的混合物中在培养箱中孵育2小时。通过酶标仪在450nm处测定OD,并根据吸光度值计算细胞活力。对于活染色和死染色,GH/hMSC水凝胶在DPBS中洗涤两次。然后将样品浸入含有0.8μl钙黄绿素-AM和1.6μlEthD-1的800μlDPBS中1小时。染色后,用DPBS洗涤样品三次,并用ECHO Revolve显微镜(BICO公司,San Diego,CA,USA)以荧光模式观察(激发和发射波长分别为528/617nm和495/515nm)。在鬼笔环肽和Hoechst染色的情况下,GH/hMSC水凝胶在室温下用4%多聚甲醛固定过夜。然后用DPBS洗涤这些样品至少三次。向每个样品中加入含有1μl鬼笔环肽-iFluor 647的1ml封闭溶液(2%牛血清白蛋白,0.5%山羊血清和0.5%Triton X-100的DPBS溶液)。细胞固定后,将样品用DPBS洗涤两次,每次1小时,然后浸入含有10μlHoechst的1ml DPBS中1小时。用DPBS洗涤过夜后,通过共聚焦显微镜(DMi8 型自动化,Leica Microsystems CMS GmbH,德国曼海姆)观察这些染色的 GH/hMSC 水凝胶,以产生现场视图中整个样品结构的 Z 堆图像。
https://blog.sciencenet.cn/blog-41174-1421738.html
上一篇:戒烟也无法避免吸烟对免疫系统损伤
下一篇:自身抗体的健康和疾病价值