博文
Cancer Research:天津医科大学牛瑞芳/张飞团队发现果糖促进胰腺癌进展的分子机制
|
2023年12月15日,天津医科大学牛瑞芳/张飞团队在期刊Cancer Research 期刊上发表题为“Fructose-Induced mTORC1 Activation Promotes Pancreatic Cancer Progression through Inhibition of Autophagy ”的研究论文,研究数据表明,在葡萄糖不足时,Glut5介导的果糖摄取和利用有助于胰腺癌的进展。果糖不仅是葡萄糖的简单替代燃料,除了提供ATP产生和碳源外,果糖还调节关键的细胞内信号通路和代谢可塑性。果糖调控的AMPK-mTORC1信号通路抑制自噬诱导的细胞死亡,使胰腺癌细胞更有利于生长和进展。Glut5-AMPK/mTORC1信号通路可能是治疗胰腺癌的潜在靶点。
研究背景
胰腺导管腺癌(PDAC)占据了所有胰腺癌的约90%,是最具侵袭性的实体肿瘤之一。尽管近年来在诊断和治疗方面取得了进展,但由于早期转移和耐药性,胰腺癌的累计5年生存率仍不到9%,使得PDAC患者的治疗极具挑战性。迫切需要验证的预防策略、早期诊断和有效的系统治疗,以降低PDAC的发病率、抑制其恶性进展并改善患者的生存率。因此,揭示导致PDAC发生和进展的机制将有助于确定该恶性肿瘤的新诊断标志物和新的治疗靶点。
果糖是一种单糖,化学式与葡萄糖相同,但结构不同。它广泛存在于天然食物中,如水果和蜂蜜,并且也是高果糖玉米糖浆的主要成分之一。作为天然糖中最甜的一种,果糖被广泛用作加工食品的甜味剂,在近几十年里其消费量大幅增加。然而,过量的果糖摄入可以促进多种肿瘤的发展和恶性进展,并导致癌症患者预后不佳。然而,果糖促进肿瘤发生和进展的详细机制仍有待阐明。
研究结果
果糖在体内外促进胰腺导管腺癌(PDAC)细胞的侵袭和转移
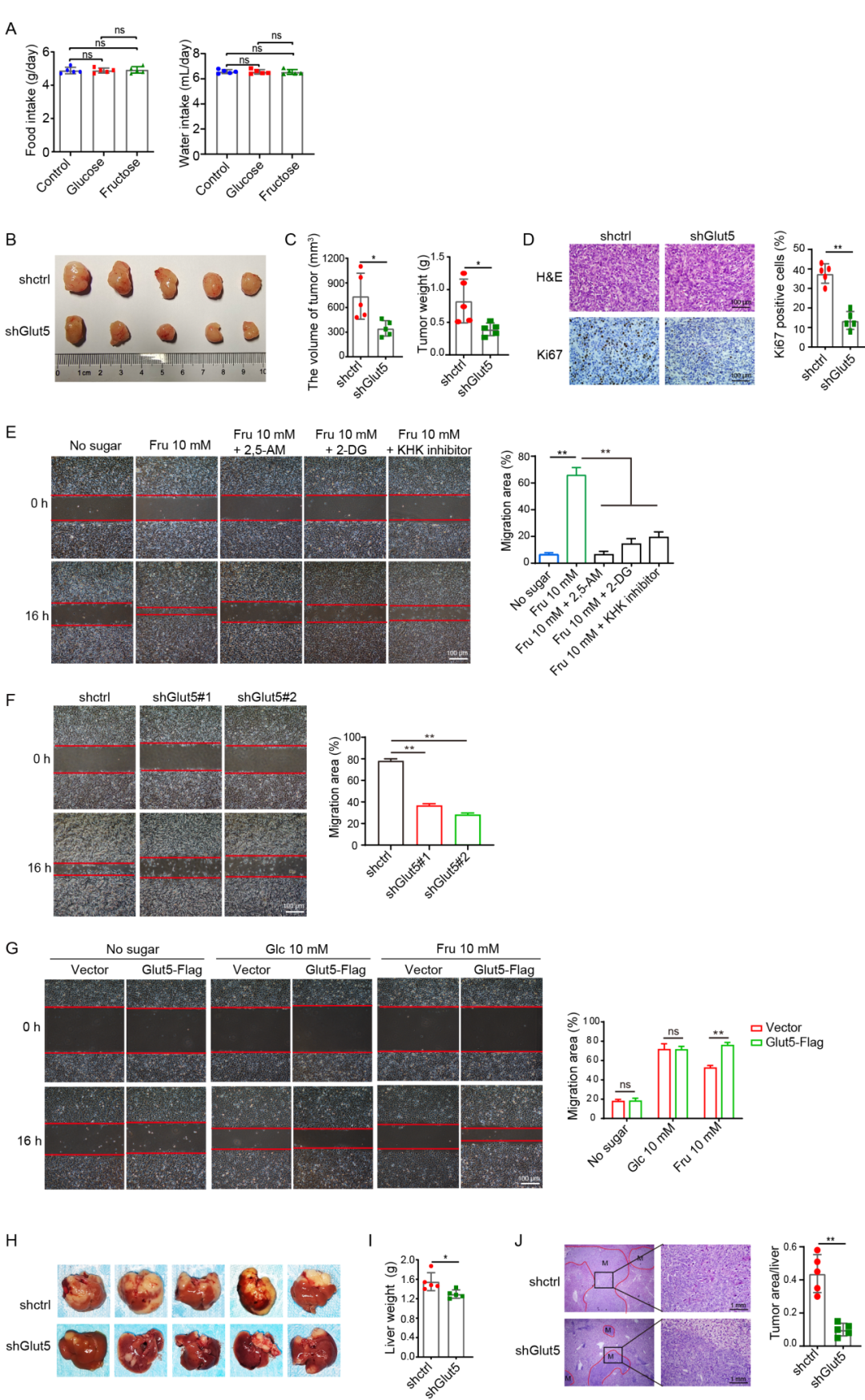
早期转移是胰腺导管腺癌(PDAC)的特征之一。本研究发现,在果糖培养基中,SU86.86和Capan2细胞的迁移和侵袭能力显著高于无葡萄糖培养基,而双糖培养基中的细胞迁移和侵袭能力最强。在SW1990和Panc02细胞的划痕愈合实验中也得到了类似的结果,表明果糖显著促进了PDAC细胞的迁移。此外,抑制Glut5或果糖代谢抑制剂存在时,SW1990细胞在果糖培养基中的迁移能力极弱,而在PDAC细胞中过表达Glut5则增强了其迁移能力。
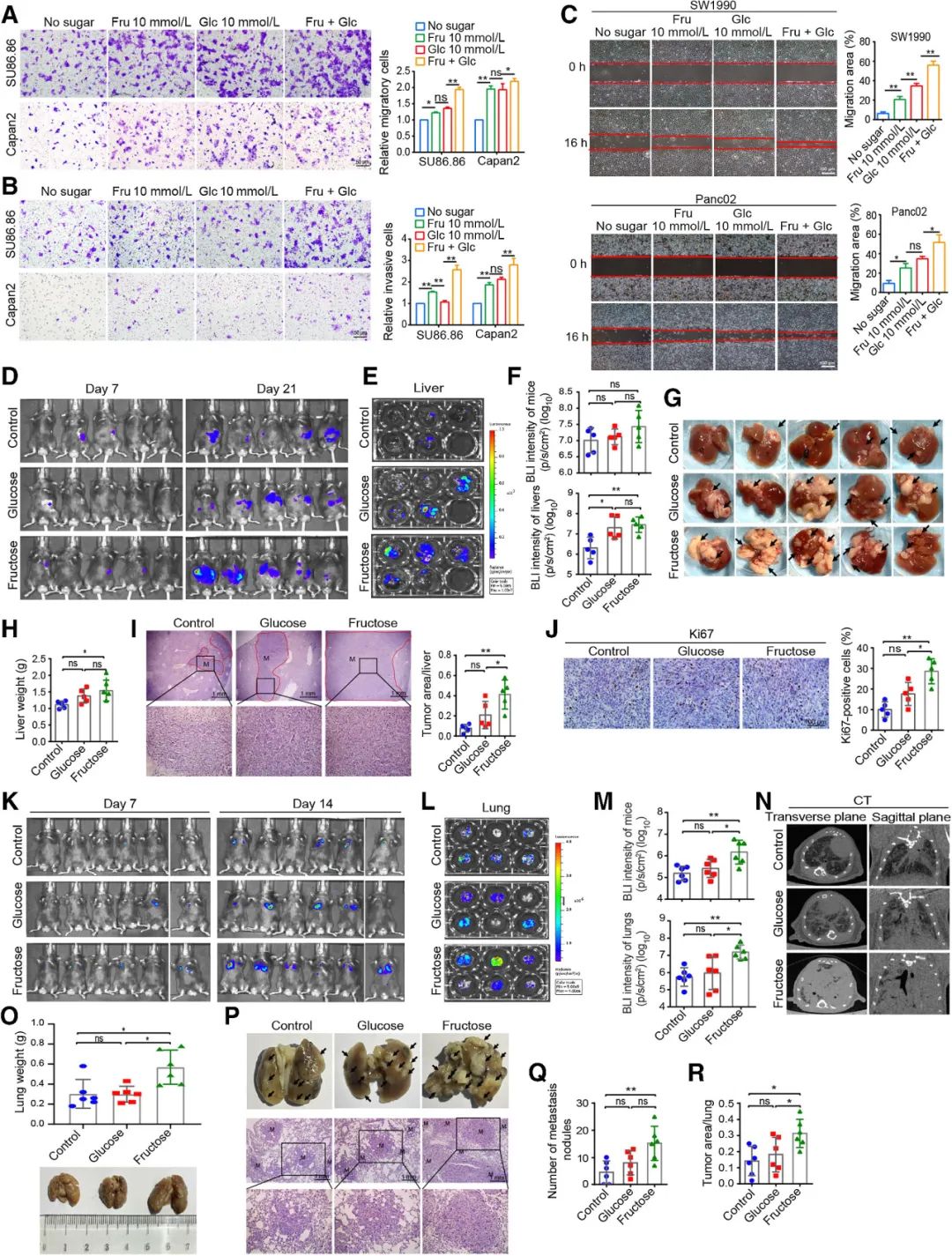
研究人员通过脾注射Panc02/luciferase细胞构建了肝转移的小鼠模型,并通过尾静脉注射Panc02/luciferase细胞构建了肺转移的小鼠模型。与前面的模型一样,根据喂养方式将小鼠随机分为三组。
在肝转移模型中,虽然这三组小鼠的生物荧光强度没有明显差异,但隔离肝脏的生物荧光强度和重量在果糖组和葡萄糖组中显著高于对照组。此外,在果糖组和葡萄糖组中出现了更多的肝表面转移和更重的肝脏,并且H&E染色也证实果糖和葡萄糖促进了Panc02细胞的肝转移,在果糖组中发现了比葡萄糖组更多的转移灶。另外,转移物中的细胞增殖指数在果糖组中也更高。虽然Glut5的沉默明显抑制了果糖喂养小鼠中的肿瘤转移。
在肺转移模型中,果糖组小鼠和分离的肺中的生物荧光强度明显高于其他两组,表明果糖显著促进了PDAC细胞的转移。CT成像也证实了以上结果。同时,果糖组小鼠的肺部最大且最重,H&E染色还显示果糖组中肺部有更多的转移结节和肿瘤区域,比其他两组更多。
总结
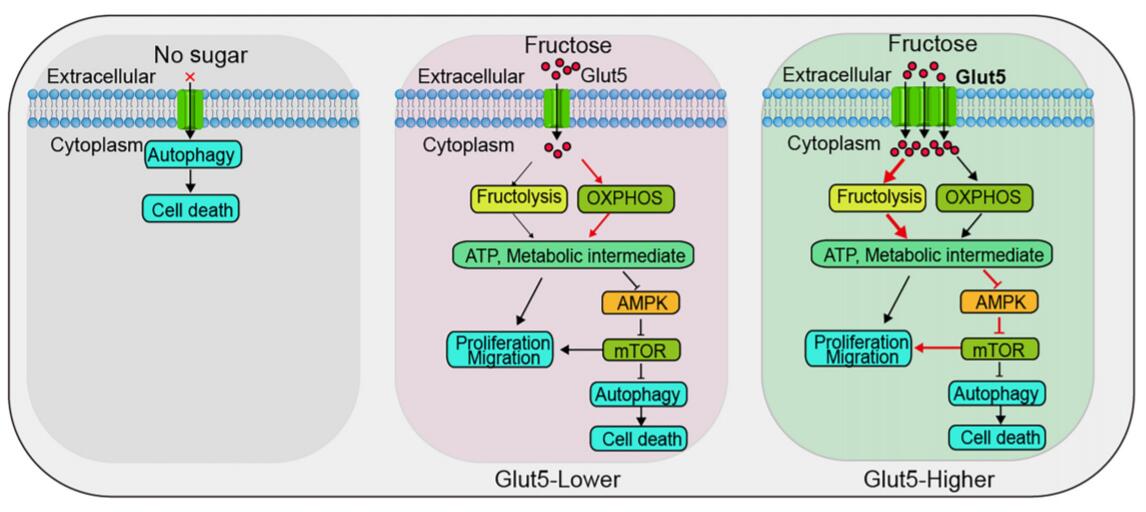
综上所述,研究数据表明,在葡萄糖不足时,Glut5介导的果糖摄取和利用有助于胰腺癌的进展。果糖不仅是葡萄糖的简单替代燃料,除了提供ATP产生和碳源外,果糖还调节关键的细胞内信号通路和代谢可塑性。果糖调控的AMPK-mTORC1信号通路抑制自噬诱导的细胞死亡,使胰腺癌细胞更有利于生长和进展。Glut5-AMPK/mTORC1信号通路可能是治疗胰腺癌的潜在靶点。
摘要 Abstract
Excessive fructose intake is associated with the occurrence, progression, and poor prognosis of various tumors. A better understanding of the mechanisms underlying the functions of fructose in cancer could facilitate the development of better treatment and prevention strategies. In this study, we investigated the functional association between fructose utilization and pancreatic ductal adenocarcinoma (PDAC) progression. Fructose could be taken up and metabolized by PDAC cells and provided an adaptive survival mechanism for PDAC cells under glucose-deficient conditions. GLUT5-mediated fructose metabolism maintained the survival, proliferation, and invasion capacities of PDAC cells in vivo and in vitro. Fructose metabolism not only provided ATP and biomass to PDAC cells but also conferred metabolic plasticity to the cells, making them more adaptable to the tumor microenvironment. Mechanistically, fructose activated the AMP-activated protein kinase (AMPK)–mTORC1 signaling pathway to inhibit glucose deficiency-induced autophagic cell death. Moreover, the fructose-specific transporter GLUT5 was highly expressed in PDAC tissues and was an independent marker of disease progression in patients with PDAC. These findings provide mechanistic insights into the role of fructose in promoting PDAC progression and offer potential strategies for targeting metabolism to treat PDAC.
意义 Significance:
Fructose activates AMPK–mTORC1 signaling to inhibit autophagy-mediated cell death in pancreatic cancer cells caused by glucose deficiency, facilitating metabolic adaptation to the tumor microenvironment and supporting tumor growth.
DOI: https://doi.org/10.1158/0008-5472.CAN-23-0464
全文PDF:https://aacrjournals.org/cancerres/article-pdf/83/24/4063/3390985/4063.pdf
参考文献:https://aacrjournals.org/cancerres/article/83/24/4063/731563/Fructose-Induced-mTORC1-Activation-Promotes
果糖相关研究:
1.Cell Metabolism:重庆医科大学揭示高果糖饮食促进肝癌进展的新机制
2. Cancer Research:中山大学庄诗美/方坚鸿发现肿瘤内皮细胞的果糖代谢促进肝癌转移
3. Cell Metab:上海交通大学医学院团队揭示果糖代谢促进CD8+ T细胞抗肿瘤机制
https://blog.sciencenet.cn/blog-446272-1414569.html
上一篇:引物和探针的设计原则及技巧
下一篇:周末在嘉陵江畔跑了12.25公里