博文
重塑银屑病治疗:持续氢化调控“氧化还原-代谢稳态”实现高效缓解与复发干预
||
重塑银屑病治疗:持续氢化调控“氧化还原-代谢稳态”实现高效缓解与复发干预
论文作者主要来自上海交通大学氢科学中心。
氢化微泡凝胶制剂可实现氢气(H₂)在局部充足、持久释放。
机制研究揭示:氢气可选择性下调角质形成细胞能量代谢。
外用氢气介导银屑病能量疗法(HPET)生物相容性高,可减轻银屑病发生与复发。
摘要
银屑病是全球高发的慢性皮肤病,以持续性角化过度、自我维持的炎症循环与频繁复发为特征。传统疗法疗效有限、生物安全性不足,面临严峻挑战。本研究提出一种氢气介导的外用银屑病革新治疗策略:构建原位成型微泡水凝胶,实现高效产氢与长效递送。
通过在盐水中自组装,将氢化镁(MgH₂)纳米颗粒包载于两亲性温敏水凝胶中,可精准调控析氢反应、微泡形貌与储氢性能,在饱和浓度(~0.8 mM)下实现数天持续释氢。体外与体内实验证实,该局部氢气治疗可显著改善银屑病样病理改变,疗效优于咪喹莫特小鼠模型与临床药物卡泊三醇。
机制上,持续氢化通过PKM2介导通路发挥抗瓦博格效应与能量代谢重编程,直接抑制银屑病角质形成细胞过度增殖;同时恢复氧化还原稳态,进一步阻断炎症-免疫反馈环路。本研究还证实该氢气调控能量代谢策略可预防银屑病复发。
综上,本研究为氢气介导银屑病能量疗法(HPET)提供概念验证,为银屑病长期管理提供可转化的新方向。
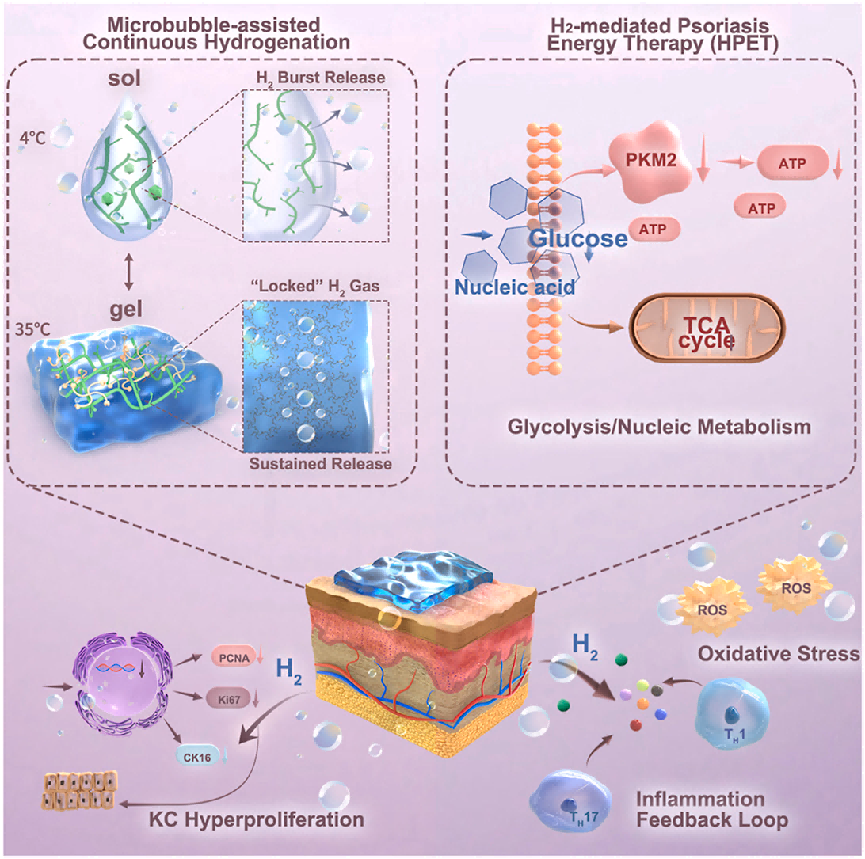
---
1 引言
银屑病是常见的终身性自身炎症性疾病,全球受累人口约1.25亿[1]。以慢性、难治性、对称性分布的红斑鳞屑、丘疹、斑块为主要表现,可致关节畸形、红皮病型与脓疱型银屑病,甚至危及生命[1]。
当前基于病情严重程度的治疗包括传统系统治疗、生物制剂与辅助外用药物[2]。外用制剂(以糖皮质激素与维生素D₃类似物卡泊三醇为主)仍是轻中度银屑病一线药物,但长期使用受限于皮肤刺激、萎缩、毛细血管扩张、全身钙代谢紊乱等副作用[3,4]。更严峻的是,生物制剂虽清除皮损高效,但停药后复发率极高,使银屑病长期管理愈加困难。因此,亟需开发生物安全性更高、疗效更优的替代疗法,兼顾治疗与防复发。
银屑病发病核心为角质形成细胞(KC)异常活化与过度增殖[5],并与氧化应激、糖代谢异常、多因子炎症细胞因子网络(如TNF‑α、IL‑12/23、IL‑17)密切相关[1]。总氧化应激升高、抗氧化酶(CAT、SOD)活性降低会加重病情[6]。ROS影响TNF‑α等免疫通路,是调控角质形成细胞增殖的关键[7,8]。抗氧化酶(CAT、SOD)可干预银屑病皮损形成[9],提示抗氧化应激药物有望用于寻常银屑病治疗。
在新型抗氧化剂中,氢气(H₂)因选择性清除毒性ROS(·OH)与抗炎特性脱颖而出,最早见于《Nature Medicine》[9]。氢气对炎症性肠病、胰腺炎、COVID‑19、肿瘤等炎症疾病的治疗作用已被广泛证实,临床试验日益增多[[10‑12]]。氢浴可缓解患者皮损与瘙痒、提高皮瓣存活率[13]。
但气态H₂生物利用度低、治疗机制未完全阐明,严重限制临床转化。传统全身给药(高压吸氢、富氢水)因H₂高扩散、低溶解度效果有限。近年研究者开始开发载氢/产氢生物材料以实现可控释氢,如氢化钯(PdH₀.₂)纳米晶[14]、镁改性微球(Mg@PLPE MSs)[15]、金属镁植入体(MgG)[16]等用于肿瘤氢气治疗。然而,在皮损局部实现安全、高效、长效释氢仍未解决。
微泡是被固体/液体包裹的气核空腔,在医药领域因尺寸小、结构独特,广泛用作医学造影剂与药物/基因/气体递送载体。但根据拉普拉斯定律,微泡形成后承受巨大附加压力,数秒内即可破裂。高稳定、均一、高生物相容性微泡已用于O₂、NO、Xe递送[[17‑20]],但成本高、制备工艺精细。且氢气分子量最小、扩散最快,进一步加剧气体逃逸,难以实现高效长效递送。
本研究开发原位成型微泡水凝胶体系,实现持续氢化,建立新型高效氢气介导银屑病能量疗法(HPET)(图1)。通过合成储氢MgH₂纳米颗粒,包载于两亲性温敏快凝水凝胶:
- 高纯MgH₂生物相容性好、储氢量极高;
- 两亲性Pluronic凝胶基质为MgH₂水解提供湿润环境,持续产氢;
- 同时作为稳定剂,抑制微泡破裂、延缓氢气逃逸,实现局部长效释氢。
该MgH₂‑Gel氢化微泡体系可在皮肤生理温度(32–35 ℃)下原位自组装,通过喷涂/浸涂简便施用于皮损。本研究系统揭示持续氢化对角质形成细胞的显著生物学效应,证实MgH₂‑Gel外用治疗寻常银屑病生物安全性高、疗效优异,并阐明其基于氧化还原与能量调控的全新治疗机制:首次发现H₂可使糖代谢从瓦博格效应转向三羧酸循环,提示H₂诱导的能量代谢重编程是核心机制。
本研究开创氢气介导能量疗法的原理性验证,为银屑病及其复发提供以能量调控为核心的全新管理策略。
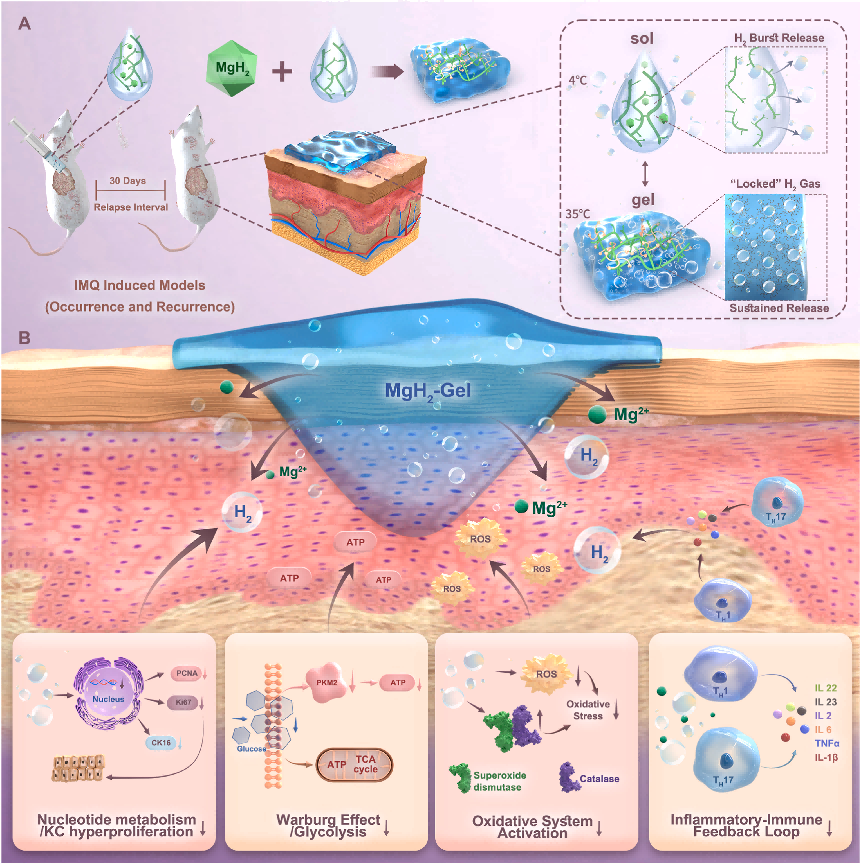
图1 原位成型长效释氢体系(MgH₂‑Gel)用于外用氢气治疗银屑病(HPET疗法)的构建示意图,覆盖发病与复发小鼠模型。
(A)高储氢MgH₂纳米颗粒在银屑病皮损处同步自组装,进入两亲性温敏水凝胶。与溶液态气体快速逃逸不同,凝胶网络中原位生成并稳定大量微泡,实现数天高效持续释氢。
(B)与临床药物卡泊三醇相比,外用MgH₂‑Gel在银屑病样与复发小鼠模型中疗效更优、生物安全性更高,并阐明氢气介导的核心作用机制。
---
2 结果
2.1 持续释氢气凝胶的制备与表征
镁是极具前景的可降解生物医用金属,生物相容性优异、储氢量高、热稳定性好,尤其在纳米尺度[21]。本研究采用电弧等离子体蒸发法合成高纯亚微米级氢化镁颗粒(MgH₂,记为HydroMg)[22]。
透射电镜(TEM)显示纳米MgH₂呈球形/多面体,平均粒径~280 nm(图2B、C)。XRD证实晶体结构与标准卡片(JCPDS 12‑0697)一致(图2D),镁粉几乎完全氢化为MgH₂,残留未反应Mg与氧化MgO极少。TGA/DSC表征热稳定性(图S1‑2)。在450 ℃下储氢量约7.1 wt%,接近理论最大值7.6 wt%,储氢性能优异。该气相合成法可规模化量产高质量、粒径可控的MgH₂。使用前MgH₂纳米颗粒于室温干燥真空密封保存,保证长期稳定与批次一致性。
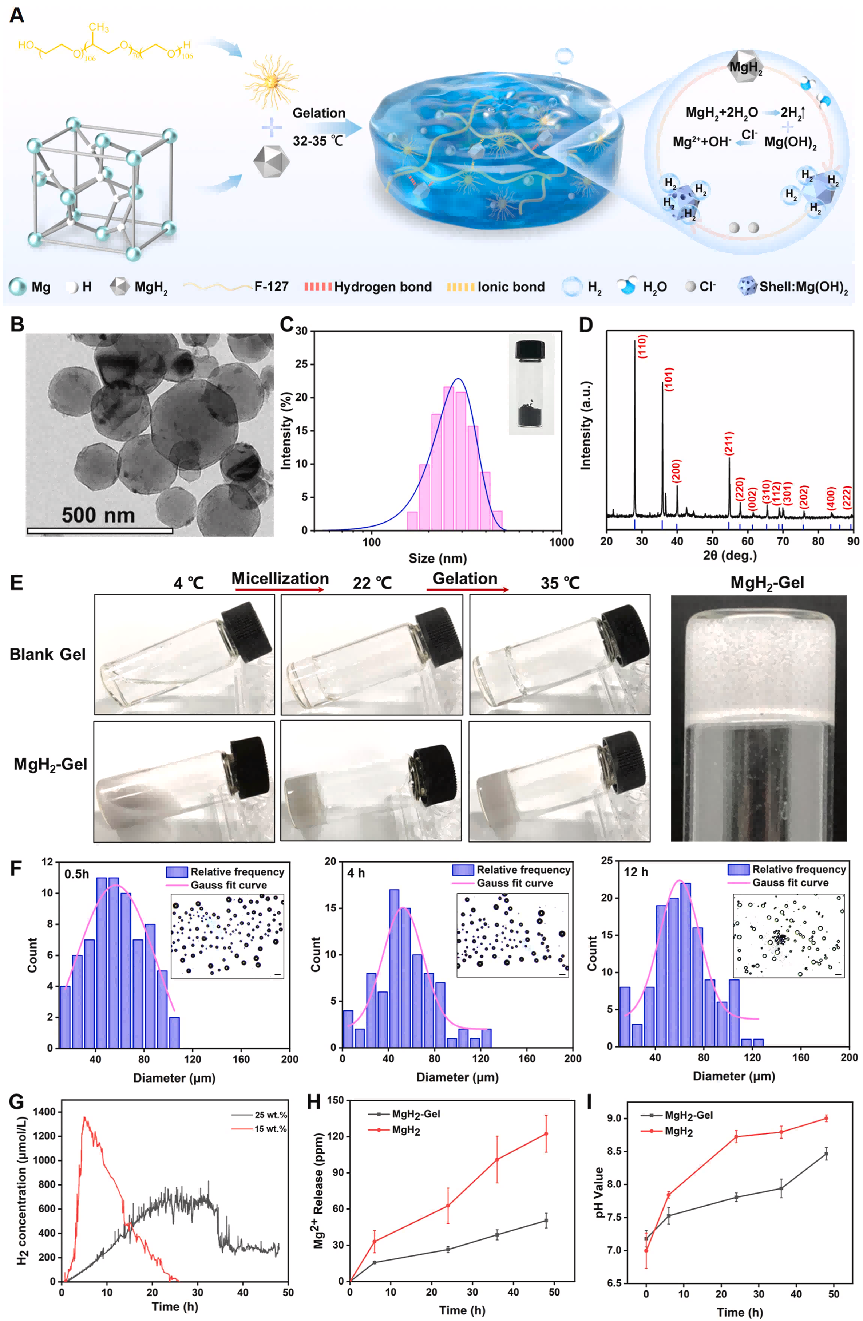
图2 MgH₂与MgH₂‑Gel的制备、结构表征、微泡生成及释氢曲线。
(A)MgH₂原位析氢示意图。
(B)MgH₂的TEM图。
(C)MgH₂的DLS粒径分布(插图:MgH₂颗粒实物图)。
(D)MgH₂的XRD图谱。
(E)不同温度下各类凝胶形貌及制备12 h后稳定微泡MgH₂‑Gel。
(F)不同时间MgH₂‑Gel生成H₂微泡的尺寸分布与显微图(标尺=50 μm)。
(G)不同两亲性凝胶剂浓度下MgH₂‑Gel局部H₂浓度曲线。
(H)MgH₂颗粒与MgH₂‑Gel在0.9% NaCl溶液中Mg²⁺累积释放(n=3)。
(I)MgH₂颗粒与MgH₂‑Gel在0.9% NaCl溶液中pH变化(n=3)。
为将储氢MgH₂递送至银屑病皮损持续产氢,室温下将MgH₂纳米颗粒与生理盐水(0.90% w/v NaCl)简单混合,制备温敏快凝复合水凝胶。凝胶剂采用聚氧乙烯‑聚氧丙烯嵌段共聚物(POE–POP–POE,Pluronic F‑127),为FDA批准无毒两亲性三嵌段共聚物,高于最低临界溶解温度(LCST)可发生胶束化与凝胶化。
MgH₂‑Gel体系的水凝胶制备、产氢与递送过程如图2A所示,凝胶形貌见图2E。体系在22–35 ℃发生明显溶胶‑凝胶相变,黏度与温敏性随凝胶剂浓度变化(图S3)。流变学证实水凝胶在4 ℃为低黏度液体,25 ℃与35 ℃形成凝胶(图S4、表S1)。25 wt%凝胶在35 ℃20 s内快速固化,半流体状态涂抹于皮肤后迅速成型,增强H₂局部递送与患者依从性。
MgH₂纳米颗粒通过氢键与离子键与Pluronic F‑127醚基结合,均匀分布于凝胶网络,在皮肤生理温度下自组装快速成胶。红外光谱(图S5)显示MgH₂‑Gel包含MgH₂(500–850 cm⁻¹,Mg–H振动)、Mg(OH)₂(945.97 cm⁻¹,Mg–OH振动)与F‑127(1083.15 cm⁻¹,C–O–C振动)特征峰。
凝胶基质在原位氢化体系中发挥双重作用:
1. 提供水环境,促进MgH₂水解持续产氢;
2. 两亲性凝胶剂作为表面活性剂稳定氢气微泡,降低表面张力、抑制气体扩散,实现微泡凝胶体系持续释氢。
微泡凝胶被两亲性胶束固定,减少氢泡破裂与融合;凝胶网络为物理屏障,进一步减缓气体扩散。新鲜凝胶微泡显微图(图2F、S6)显示大量分布均一的微泡,平均直径~45 μm,表明凝胶体系可快速大量“锁定”氢气。4 h与12 h后平均粒径分别约50 μm与70 μm,仍保留大量完整气体微泡。微泡载药水凝胶中出现特征H₂峰(图S7),直接证实MgH₂‑Gel包载与释放气体为氢气。
氢气微传感器多表计测定体外释氢动力学:MgH₂纳米颗粒在水溶液中快速水解爆释,因高扩散低溶解度难以长效(图S8);而优化配方MgH₂‑Gel(25 wt/v%)可持续稳定释氢约2天,显著长于水溶液。通过调节F‑127浓度可精准调控释氢曲线,25 wt/v%高浓度凝胶流变性能适宜,稳定自发生成微泡,释氢效率远高于15 wt/v%低浓度凝胶。
图2H、I结果与H₂释放趋势一致:优化凝胶配方显著抑制水解副产物(Mg²⁺、OH⁻)过量释放,利于提升生物安全性与相容性。体内皮肤刺激性实验(图S9‑11)、主要脏器组织学分析(图S12)及人体志愿者斑贴试验(图S13)均证实MgH₂‑Gel无刺激性、对人体皮肤安全,符合中国国家标准(GB/T 16886.23/ISO 10993‑23)医疗器械生物学评价要求,并获CMA认证报告(补充材料_GB/T 16886.23报告)。
2.2 氢化在体外抑制HaCaT细胞过度增殖与糖酵解
银屑病发病中,角质形成细胞(KC)异常活化与过度增殖是症状发生的关键环节。采用Transwell体系,将不同剂量MgH₂纳米颗粒与角质形成细胞(HaCaT)共培养(图3A),评估其对细胞活力与增殖的影响。
图3B、C显示:HaCaT细胞活力随MgH₂浓度升高逐渐降低。体外抑制50%角质形成细胞活力的干预浓度为519.6 μg/ml。
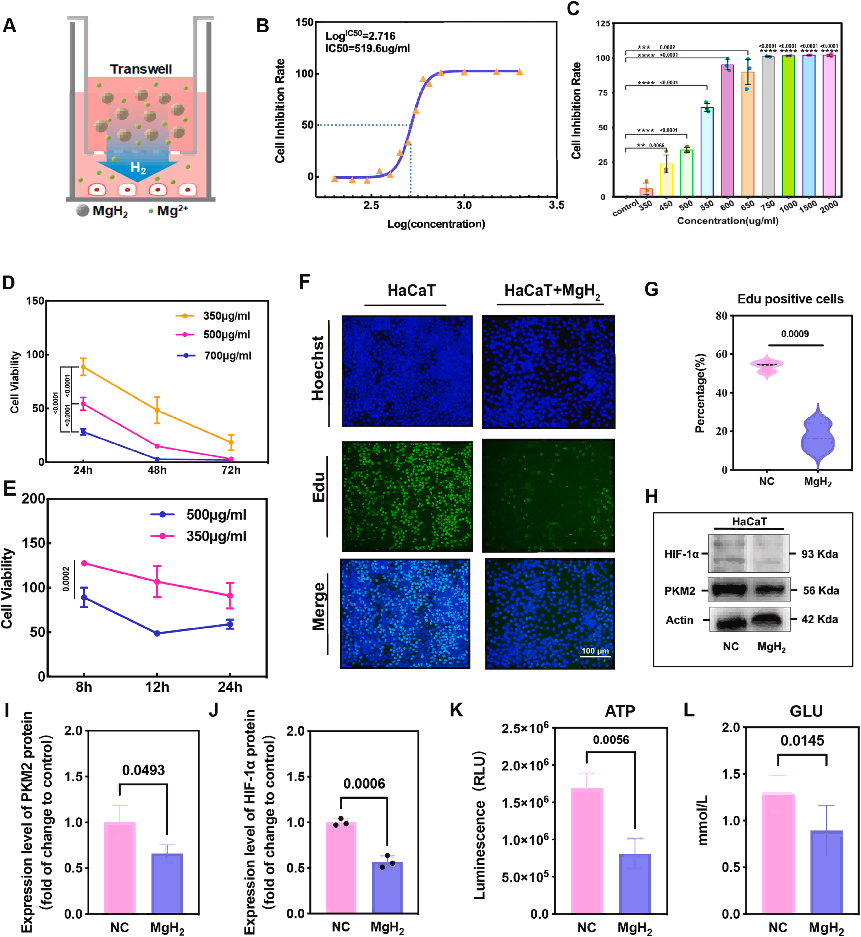
图3 MgH₂孵育抑制HaCaT细胞增殖、糖代谢、氧化应激与炎症反应。
(A)MgH₂干预细胞示意图。
(B‑C)不同浓度氢化镁处理24 h后HaCaT抑制率。
细胞抑制率(%)= [1 − (OD实验组 − OD空白)/(OD对照组 − OD空白)] × 100。
(D‑E)MgH₂孵育后HaCaT细胞活力。
细胞活力(%)= (OD实验组 − OD对照组)/(OD对照组 − OD空白) × 100。
(F‑G)EdU法测定EdU阳性细胞比例(%)。
(H‑J)HaCaT细胞中HIF‑1α(I)与PKM2(J)表达的Western blot及定量分析。NC:正常对照组。
(K‑L)MgH₂处理后HaCaT细胞葡萄糖与ATP含量变化(n=3)。NC:正常对照组。
选取350、500、700 μg/ml MgH₂浓度,在24、48、72 h检测细胞活力。随干预时间延长,三组均呈显著活力下降(图3D、E)。500 μg/ml可有效抑制HaCaT细胞DNA合成与增殖(图3F‑G、S14)。
证实MgH₂纳米颗粒在体外显著抑制角质形成细胞活力与过度增殖,主要源于水介质中MgH₂反应产生大量氢气长期作用,可能伴随少量副产物影响。
糖酵解与氧化应激可协同影响角质形成细胞增殖。银屑病皮损中角质形成细胞过度增殖、异常分化与代谢亢进类似肿瘤细胞:即使有氧条件下也依赖有氧糖酵解(瓦博格效应)而非三羧酸循环产生ATP[24,25]。干预角质形成细胞糖酵解与代谢过程是银屑病潜在治疗靶点。特异性抑制糖酵解关键酶(如丙酮酸激酶M2亚型PKM2),可通过促进巨噬细胞活化、增加TNF‑α分泌削弱KC增殖能力[26]。
为验证MgH₂是否影响KC糖酵解,采用Western blot检测PKM2(促炎通路关键限速酶)表达。银屑病皮损中PKM2表达升高,而经500 μg/ml MgH₂处理24 h后,PKM2表达大幅下调(图3H、I)。
利用STRING数据库构建PKM2蛋白互作(PPI)网络,生物信息学分析显示HIF‑1α(关键上游调控因子)与LDHA(丙酮酸最终转化为乳酸的酶)为最接近互作节点(图S15)。Western blot证实:MgH₂显著抑制HaCaT细胞中HIF‑1α表达,而LDHA蛋白水平基本不变(图3H、J、S16)。
尽管LDHA表达稳定,下游乳酸生成、胞内ATP与葡萄糖利用均显著下降(图3K、L),提示糖酵解终产物减少主要源于上游底物耗竭——即PKM2环节阻断,而非LDHA蛋白直接下调。综上数据表明:MgH₂特异性破坏角质形成细胞中亢进的HIF‑1α/PKM2通路。
为进一步证实PKM2抑制的下游代谢效应,采用非靶向LC‑MS分析MgH₂干预前后代谢物变化。KEGG通路分类(图4A)显示差异代谢物主要富集于碳水化合物代谢与能量代谢。KEGG富集分析(图4B)突出与葡萄糖利用密切相关通路显著改变:碳代谢、三羧酸循环、氧化磷酸化。下游代谢组变化与PKM2抑制、ATP生成减少高度一致。LC‑MS数据从代谢层面证实:MgH₂限制银屑病角质形成细胞亢进的糖酵解流。
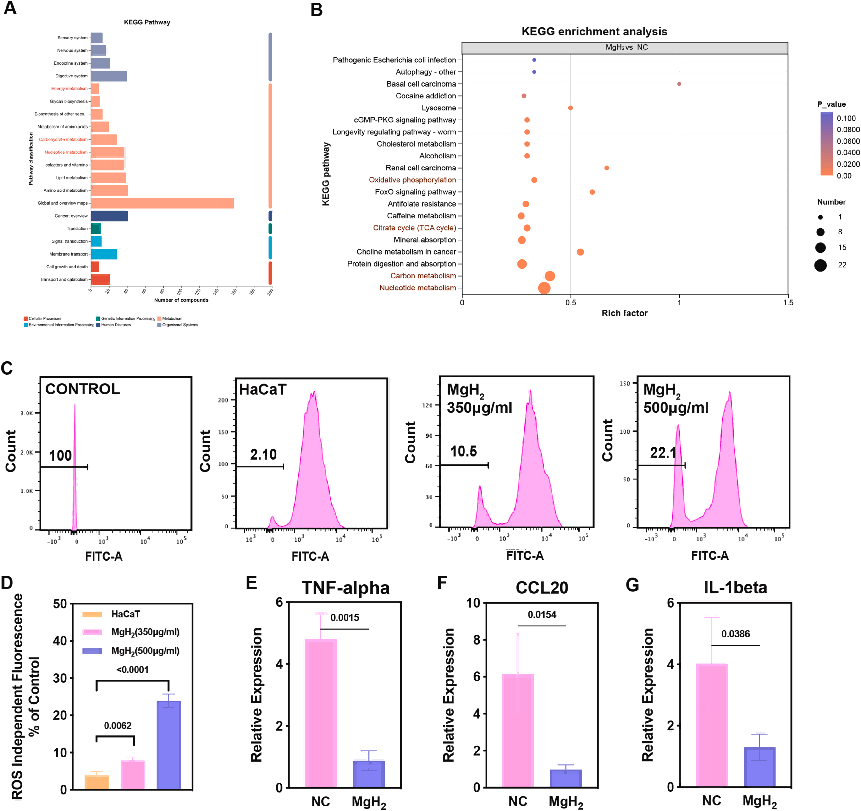
图4 MgH₂在银屑病模型中的代谢通路分析与生物学效应。
(A‑B)MgH₂组与NC组差异代谢物的KEGG通路分类与富集分析,突出能量与核苷酸代谢显著改变。
(C‑D)不同浓度MgH₂处理HaCaT细胞后ROS水平流式分析与定量。
(E‑G)MgH₂处理后HaCaT细胞炎症因子TNF‑α(E)、CCL20(F)、IL‑1β(G)mRNA表达RT‑qPCR分析(n=3)。
2.3 体外清除ROS与重塑免疫炎症
ROS与氧化应激在银屑病发生发展中作用关键,尤其参与角质形成细胞转录因子活化[7]。为阐明MgH₂抗氧化效应,检测350、500 μg/ml MgH₂纳米颗粒与HaCaT共培养后胞内ROS水平。
ROS(·OH、ONOO⁻等)是细胞代谢产生的活性自由基,过量蓄积导致组织氧化损伤[28]。MgH₂干预后HaCaT细胞ROS水平显著下降,利于恢复胞内氧化还原稳态;500 μg/ml MgH₂处理组ROS降低更显著(图4C、D)。
ROS升高在炎症发生、进展与消退中起核心作用,并伴随多因子炎症细胞因子[1,29]。为探究炎症调控效应,LPS预处理HaCaT细胞30 min后给予500 μg/ml MgH₂颗粒,24 h后收集样本。RT‑qPCR显示:MgH₂预处理可降低LPS刺激下银屑病关键促炎因子TNF‑α、IL‑1β、CCL20的转录水平(图4E‑G),证实MgH₂颗粒对HaCaT细胞具有强效清除ROS与抗炎特性。
2.4 持续释氢气凝胶对IMQ诱导银屑病小鼠实现安全高效皮损缓解
本研究构建的MgH₂‑Gel可原位生成大量微泡锁定氢气,实现局部持续释氢,体内有效性实验前已证实无皮肤刺激性。
将不同剂量(1 mg/ml、5 mg/ml)MgH₂‑Gel外用于咪喹莫特(IMQ)诱导银屑病小鼠模型,以IMQ空白对照组(未治疗)为对照(图5A、B、S17)。另设空白凝胶、MgCl₂‑Gel、NaOH‑Gel组,区分MgH₂‑Gel应用中反应副产物(Mg²⁺释放、碱性升高)的作用(图5B、S18)。
体内结果清晰显示:两种浓度MgH₂‑Gel均显著改善银屑病样皮损。短期治疗中,氢化镁凝胶皮损缓解速度快于临床药物卡泊三醇,提示其在快速缓解银屑病方面具显著优势。
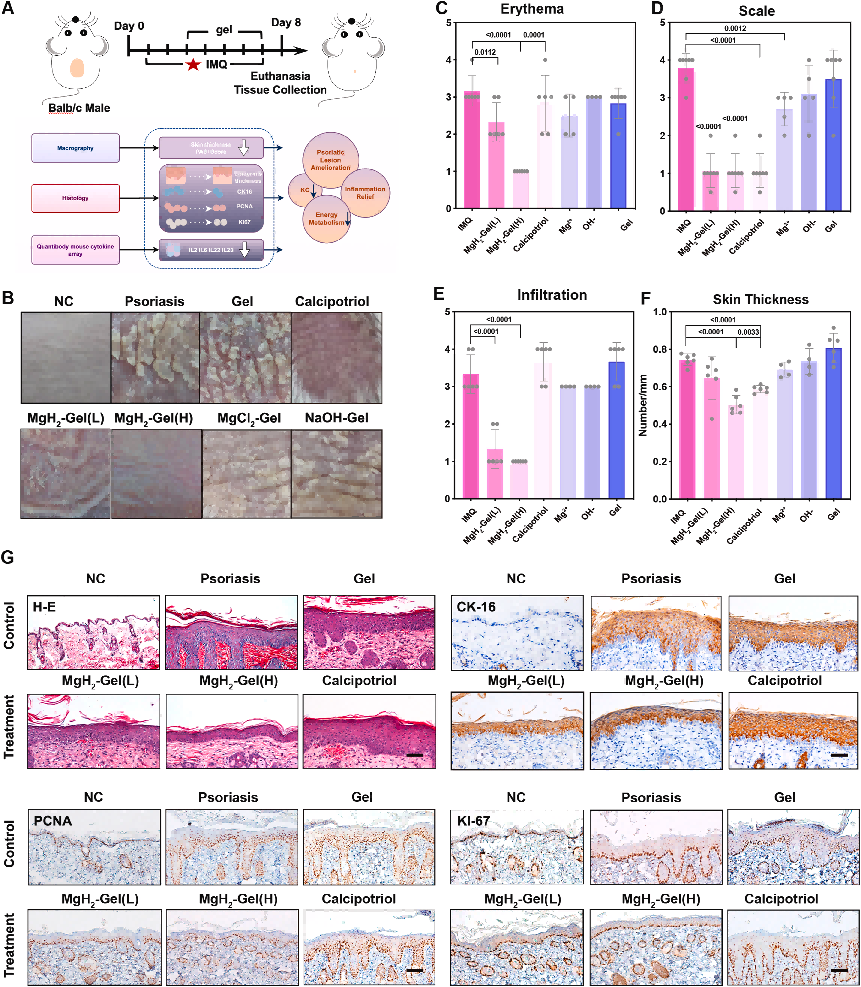
图5 MgH₂‑Gel外用治疗IMQ诱导小鼠银屑病皮损的疗效。
(A)MgH₂‑Gel治疗银屑病样小鼠模型示意图。
(B)第8天不同治疗组小鼠银屑病皮损形态变化(n=4‑6)。
(C‑F)不同组小鼠PASI评分(C‑E)与皮肤厚度(F)。
MgH₂‑Gel(L):1 mg/ml,MgH₂‑Gel(H):5 mg/ml。
(G)各组小鼠HE染色;CK‑16、PCNA、Ki‑67免疫组化染色。标尺=100 μm。
低剂量MgH₂‑Gel(1 mg/ml)即可改善银屑病样皮损红斑(PASI:3.16→2.33)、鳞屑(PASI:3.83→1.16),并降低浸润评分(PASI:3.33→1.33)。高剂量MgH₂‑Gel(5 mg/ml)改善更显著:红斑(3.16→1.00)、鳞屑(3.83→1.16)、浸润(3.33→1.00)。
经1 mg/ml与5 mg/ml MgH₂‑Gel治疗后,表皮厚度分别由0.735 mm降至0.627 mm与0.517 mm。对比可见:卡泊三醇组仅轻‑中度改善;空白凝胶、NaOH‑Gel组无明显皮损变化,排除凝胶基质与碱性pH的影响。MgCl₂‑Gel组鳞屑评分略有改善,可能与Mg²⁺抗炎作用相关[30]。
采用HE与CK‑16免疫组化评估各组病理改变:IMQ诱导小鼠皮肤呈现典型银屑病改变——角化过度伴角化不全、棘层肥厚、真皮乳头延长、炎症细胞浸润,证实模型构建成功。CK‑16为角质形成细胞角化过度标志物,正常皮肤低表达[31],IMQ组显著升高。
MgH₂‑Gel(5 mg/ml、1 mg/ml)治疗后角化过度、炎症浸润、棘层肥厚与CK‑16表达均显著降低,且改善程度与MgH₂‑Gel浓度正相关。卡泊三醇组、空白凝胶、MgCl₂‑Gel、NaOH‑Gel组虽有改善,但未完全恢复(图5G、S19)。
以上结果证实:MgH₂‑Gel有效改善银屑病皮损症状;体内对照明确主要治疗效应源于局部持续释氢,而非空白水凝胶或pH升高,Mg²⁺仅对皮损缓解发挥轻微抗炎作用。
2.5 体内局部氢化通过下调PKM2表达抑制角质形成细胞过度增殖与瓦博格效应
通过皮损PCNA与Ki‑67免疫组化进一步证实MgH₂‑Gel生物学效应。PCNA与Ki‑67为细胞增殖标志物,IMQ诱导银屑病组小鼠角质形成细胞中二者表达显著升高[32,33]。MgH₂‑Gel治疗后,角质形成细胞中两种蛋白表达同步降低(图5G)。
卡泊三醇、MgCl₂‑Gel、NaOH‑Gel与空白凝胶组未观察到PCNA、Ki‑67类似变化(图5G、S20),证实MgH₂‑Gel抗增殖能力仅源于充足氢气释放。
此外,MgH₂‑Gel可下调银屑病核苷酸代谢。核苷酸代谢对细胞增殖分化至关重要,参与碳水化合物代谢调控。增殖细胞对核苷酸需求剧增(用于rRNA合成、基因组复制、转录组维持),使核苷酸合成在增殖细胞代谢中占据特殊地位[34]。
采用LS/MS代谢组学分析MgH₂‑Gel(5 mg/ml)干预前后皮损代谢物变化(图6A)。与正常对照相比,IMQ诱导小鼠核苷酸代谢相关代谢物水平升高;MgH₂‑Gel治疗后显著下降,其中尿嘧啶/腺嘌呤/dCMP/dAMP/UDP‑GlcNAc代谢水平变化具统计学意义(图6B)。
综上推测:MgH₂‑Gel抑制角质形成细胞生长活性,至少部分通过下调核苷酸代谢实现。
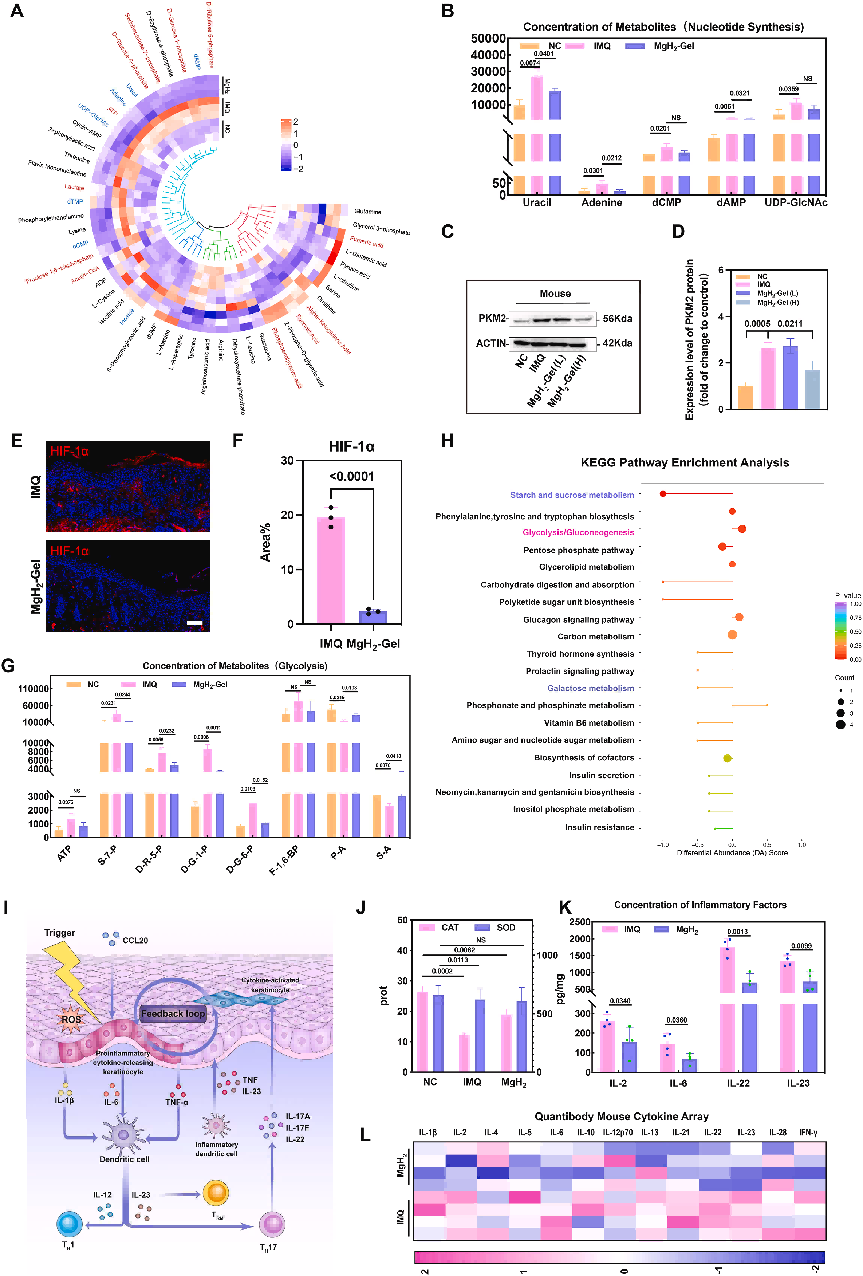
图6. MgH₂‑凝胶体内治疗抑制银屑病样小鼠皮损角质形成细胞增殖、调控糖代谢及改善氧化应激与炎症水平的机制分析(治疗前后)。
(A)LC‑MS/MS分析MgH₂‑凝胶干预前后银屑病皮损中能量代谢物变化。
(B)LC‑MS/MS分析MgH₂‑凝胶治疗后银屑病皮损中核苷酸代谢相关代谢物水平。单位:ng/g。
(C‑D)MgH₂‑凝胶干预后银屑病皮损中PKM2蛋白表达水平。
(E‑F)IMQ诱导银屑病模型与MgH₂‑凝胶治疗组皮肤组织HIF‑1α免疫荧光代表性图像(E)及面积百分比定量分析(F)。标尺=100 μm。
(G)LC‑MS/MS分析MgH₂‑凝胶治疗后银屑病皮损中糖酵解水平。
S‑7‑P:景天庚酮糖‑7‑磷酸;D‑R‑5‑P:D‑核酮糖‑5‑磷酸;D‑G‑6‑P:D‑葡萄糖‑6‑磷酸;D‑G‑1‑P:D‑葡萄糖‑1‑磷酸;F‑1,6‑BP:果糖‑1,6‑二磷酸;P‑A:磷酸烯醇式丙酮酸;S‑A:琥珀酸。单位:ng/g。
(H)基于LC‑MS/MS代谢组学数据的KEGG通路差异丰度(DA)评分分析。
(I)角质形成细胞炎症反馈环路作用示意图。
(J)MgH₂‑凝胶干预后皮损中SOD与CAT水平。
(K‑L)MgH₂‑凝胶治疗后皮损中炎症因子表达。
代谢特征与活性是决定角质形成细胞增殖速率的关键因素[25]。为探究MgH₂‑凝胶对银屑病皮损糖酵解的影响,采用Western blot检测PKM2蛋白表达。与正常对照相比,银屑病小鼠PKM2表达升高,经MgH₂‑凝胶治疗后显著降低,与细胞水平结果一致(图6C、D)。进一步检测HIF‑1α与LDHA表达:与体外细胞结果一致,MgH₂‑凝胶组组织中HIF‑1α显著下调,而LDHA表达基本不变(图6E、F,图S21)。上述体内结果与细胞实验高度吻合,进一步证实MgH₂‑凝胶可调控糖酵解通路。
为进一步阐明MgH₂对糖代谢的生物学效应,以5 mg/mL MgH₂‑凝胶治疗组为对象,分析干预前后相关代谢物改变。与正常对照相比,IMQ小鼠糖代谢相关代谢物升高,经MgH₂‑凝胶治疗后恢复至稳态水平。代谢组学分析显示,三羧酸循环(TCA)关键中间产物琥珀酸[35]在IMQ诱导皮损中显著降低,而MgH₂‑凝胶治疗后明显上调(图6G)。另一种TCA循环中间产物α‑酮戊二酸(AKG)呈现相似的恢复趋势。相反,糖酵解终产物乳酸在IMQ干预后上调,经MgH₂‑凝胶治疗后显著下调[36]。
基于LC‑MS/MS代谢组学数据的KEGG通路差异丰度(DA)评分分析显示:与MgH₂‑凝胶治疗组相比,银屑病样皮损中差异代谢物在糖酵解通路显著富集;而淀粉蔗糖代谢、半乳糖代谢等其他糖代谢通路富集程度显著降低(图6H)。值得注意的是,半乳糖代谢通路可作为糖酵解的替代途径,乳酸生成更低[37]。结合观察到的糖酵解限速酶PKM2下调,上述结果表明IMQ诱导皮损中存在有氧瓦博格效应——即在有氧条件下仍优先通过糖酵解代谢葡萄糖以支持增殖。MgH₂干预可有效重编程该代谢表型。
2.6 体内局部氢化诱导内源性抗氧化表达并阻断炎症反馈环路
银屑病中总氧化应激水平显著升高,伴随CAT与SOD降低[6]。本研究发现IMQ小鼠皮损中SOD(716.3 vs 538.4 U/mg)与CAT(26.55 vs 12.27 U/mg)表达显著降低,经MgH₂‑凝胶治疗后可恢复至对照组水平(图6J),表明持续可控释氢的MgH₂‑凝胶可有效降低银屑病皮损氧化应激水平,重建体内氧化还原稳态。
为进一步验证,检测IMQ组、MgCl₂‑凝胶组与MgH₂‑凝胶组皮损中4‑羟基壬烯醛(4‑HNE)(公认的组织氧化损伤标志物)[38]水平。图S22显示:MgH₂‑凝胶干预显著降低组织中4‑HNE蓄积;而MgCl₂‑凝胶治疗未出现类似降低,凸显MgH₂凝胶作为镁基释氢治疗体系的综合优势。
在氧化应激应答下,角质形成细胞(KC)分泌细胞因子(TNF‑α、IL‑1β、IL‑6)刺激树突状细胞(DC)分泌IL‑23,促进Th17细胞分化与活化。KC作为启动与放大因子,被Th17细胞(IL‑17、IL‑22)与炎症树突状细胞(IL‑23、NO、TNF)分泌的炎症因子激活并过度增殖,启动并维持炎症恶性循环(图6I[6,39])。
采用Quantibody小鼠细胞因子阵列高通量测序,评估MgH₂‑凝胶干预前后炎症因子水平(图6K、L)。MgH₂‑凝胶干预后炎症因子整体表达急剧下降,证实体内强效抗炎效应。值得注意的是,KC驱动炎症恶性循环的核心因子——包括IL‑6、IL‑22、IL‑23——经MgH₂‑凝胶治疗后表达均显著降低[40]。促炎介质的全面抑制凸显局部氢气治疗的强效抗炎能力。
2.7 持续释氢凝胶通过靶向组织驻留记忆T细胞定植与代谢重编程减轻银屑病小鼠复发
按照图7A、B所示方案,在小鼠复发模型中验证MgH₂‑凝胶对银屑病复发的干预作用。IMQ诱导阶段,免疫荧光染色显示组织驻留记忆T细胞(TRM)表面标志物CD69与CD103表达显著降低,而TRM是驱动原位复发的关键细胞(图7C‑F)。MgH₂‑凝胶治疗显著减轻银屑病样皮损复发,表现为PASI评分显著改善(图7G‑I)与表皮厚度降低(图7J)。
外用MgH₂‑凝胶可显著改善H&E染色中银屑病核心组织病理学特征,包括角化不全、棘层肥厚与Munro微脓肿同步减轻(图7K)。
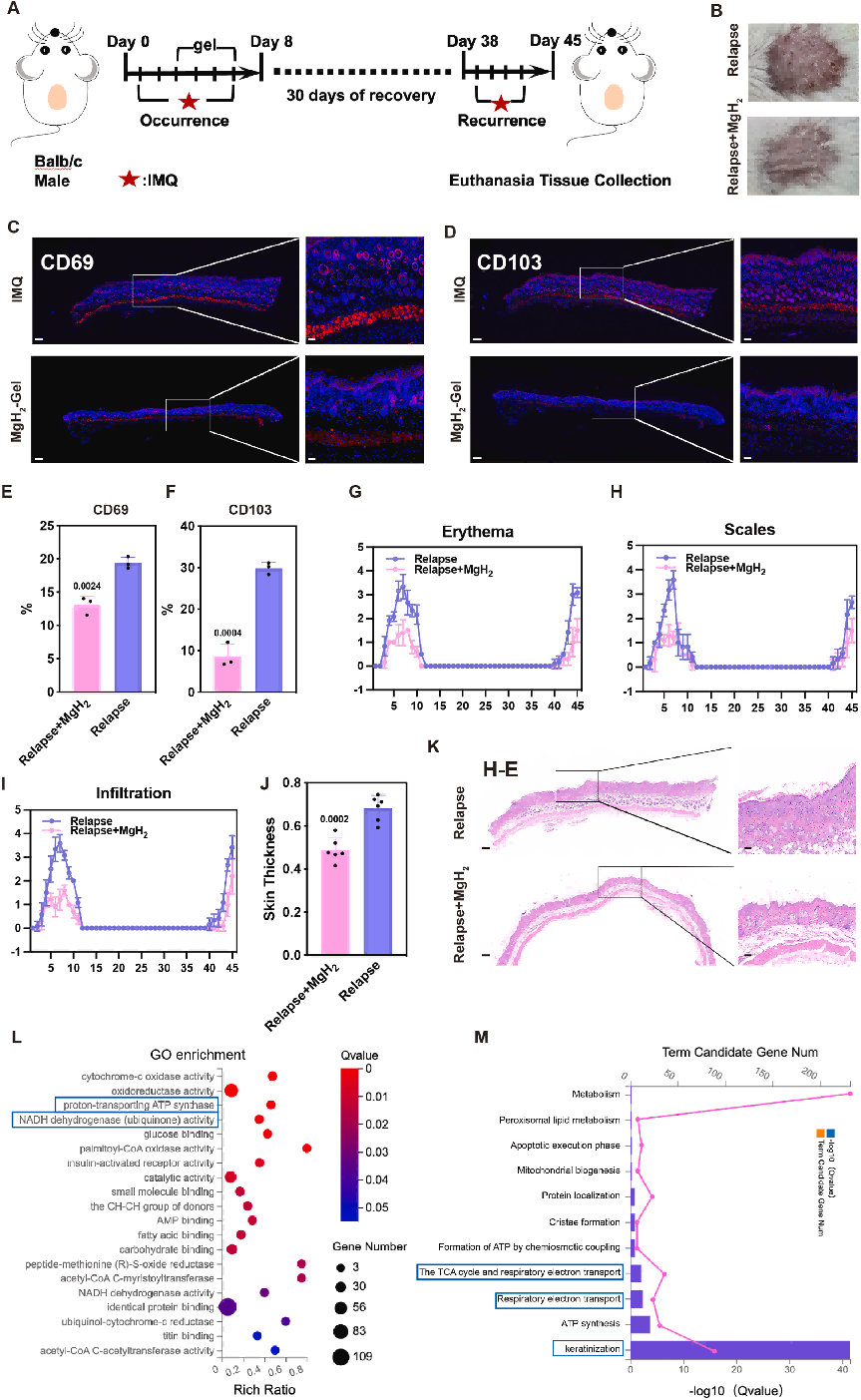
图7. MgH₂‑凝胶外用长期调控皮损严重程度以减轻IMQ诱导银屑病复发小鼠模型复发。
(A‑B)实验全程皮肤外观代表性图像:IMQ诱导炎症(1‑7天)、间歇期(8‑37天)、复发期(38‑44天),分别给予MgH₂‑凝胶+IMQ或单纯IMQ处理(n=6)。
(C‑D)IMQ复发组与MgH₂‑凝胶治疗组CD69(C)、CD103(D)免疫荧光染色。标尺=1 mm;放大图标尺=100 μm。
(E‑F)CD69(E)、CD103(F)阳性面积百分比定量,MgH₂‑凝胶组表达降低。
(G‑I)IMQ组与MgH₂‑凝胶组红斑(G)、鳞屑(H)、浸润(I)定量。
(J)第40天皮肤厚度测量。
(K)第40天皮肤H&E染色。标尺=1 mm;放大图标尺=100 μm。
(L)基因本体(GO)富集分析,显示各类生物学过程富集率与基因数,突出关键通路。
(M)相关代谢过程候选基因分析,与角化通路显著关联。
为阐明长效治疗效应与预防复发的分子机制,对复发组与复发+MgH₂组皮损进行RNA测序。差异表达基因GO富集分析显示:线粒体质子转运ATP合酶活性、NADH脱氢酶活性相关生物学过程显著富集(图7L)。相应地,Reactome富集分析进一步证实三羧酸循环、线粒体呼吸电子传递、角化相关通路受到显著协同调控(图7M)。综上,MgH₂‑凝胶可同时靶向银屑病复发中的TRM定植与代谢调控。
3 讨论与结论
银屑病是由角质形成细胞(KC)免疫‑炎症轴失调驱动的慢性免疫介导疾病,打破该致病恶性循环是实现持续缓解的关键[1]。氧化应激、炎症细胞因子与能量代谢在银屑病发生中发挥重要致病作用[6,24,25,39]。尽管生物制剂与小分子药物治疗取得进展,原皮损部位仍频繁复发。TRM定植与银屑病原位复发密切相关,表面标志物为CD69与CD103[41,42]。因此,临床仍亟需同时靶向三大致病机制、高效安全耐受的外用药物,实现皮损清除与复发预防。
近期临床报道中,Ping等首次证实电解水产生氢气联合浴疗可有效改善银屑病患者瘙痒与皮损[39]。但高昂成本、制备复杂、用药依从性差等问题严重限制氢水浴疗法进一步应用。实现充足、长效氢气递送是疗效核心与临床转化关键。然而,传统给药途径受限于氢气高扩散、低溶解度特性。尽管近年释氢生物材料取得进展,仍普遍存在局部供氢不足或生物安全性问题,成为当前未解决的障碍。
本研究开发创新型氢化微泡凝胶,实现银屑病局部充足、长效氢气递送,并阐明其核心治疗机制。MgH₂在含盐水凝胶中自发水解持续产氢,凝胶基质内形成大量稳定微泡,可立即“储存”与“锁定”这种轻质易逃逸气体,抑制氢气爆释。值得注意的是,银屑病病理环境呈弱酸性。本研究生理盐水体外释氢结果为基线数据,而局部酸性环境可能轻微加速MgH₂初始水解。此外,氢气高扩散性可穿透增厚皮肤屏障,在真皮深层发挥抗炎作用。
但本研究难以在体内直接定量皮肤中氢气分布,主要源于氢气本征特性:极高扩散性与光学不可见性,现有技术无法实现活体皮肤实时检测。因此,气体疗法中氢气滞留评估通常依赖间接证据,如持续释氢动力学与长效生物学效应。本研究体内观察到的长效疗效支持局部氢气有效性,而氢气空间分布有待未来技术突破。
此外,水凝胶递送是成熟且高生物相容性技术,无创、无皮肤创伤、外用安全性优异[43,44]。
机制上,局部氢气治疗并非通过单一通路,而是协同调控氧化、炎症与代谢微环境发挥深远生物学效应:
1. 首次证实MgH₂‑凝胶有效破坏银屑病角质形成细胞亢进代谢状态。基于STRING数据库预测,MgH₂干预显著下调HIF‑1α与PKM2。有趣的是,尽管下游酶LDHA表达不变,胞内乳酸与ATP生成显著降低,提示糖酵解终产物减少主要源于PKM2阻断后上游底物耗竭。
2. LC‑MS与KEGG富集分析证实,该干预触发更广泛系统性代谢转变,影响中心碳代谢与TCA循环,逆转银屑病特征性类瓦博格代谢重编程。
同时,MgH₂‑凝胶强效抑制表皮过度增殖(PCNA、Ki67降低)并重建内源性氧化还原稳态(4‑HNE减少)。尽管Mg²⁺基础抗炎作用已被证实[45,46],但MgCl₂‑凝胶对照组平行评估显示:单纯Mg²⁺无法显著降低PCNA、Ki67或4‑HNE,也无法驱动广泛代谢纠正。这一鲜明对比表明,观察到的强效治疗效应本质上由镁基平台中持续释氢的协同作用驱动。
除急性皮损清除外,MgH₂‑凝胶在复发干预中亦展现显著潜力,可减轻复发并下调驱动复发的T细胞定植。
尽管结果极具前景,本研究仍存在一定局限性:
1. 多组学与体外数据证实氢气干预、糖酵解下调与表型改善强相关,但主要为相关性而非严格因果性。MgH₂‑凝胶干预银屑病样皮损发生与复发的具体分子因果机制(如基因扰动)仍需进一步研究。
2. 与卡泊三醇单药探索性对比显示短期皮损改善显著,但需开展更长时间、符合临床维持剂量方案的对比研究,全面评估长期综合优势。
重要的是,标准慢性皮肤刺激性试验(GB/T 16886.23/ISO 10993‑23)与脏器组织学分析已证实制剂生物安全性,支持其转化潜力。
综上,本研究构建局部、持续产氢与释氢体系,生物安全性高,可显著改善小鼠银屑病样症状并降低复发。该原位氢化微泡凝胶治疗策略具备制备简便、成本低廉、使用便捷优势,有望成为银屑病外用管理的优选方案,临床转化前仍需开展大规模长期临床试验综合验证。本概念验证研究不仅强化镁基生物材料治疗潜力,更为氢气医学在各类炎症性皮肤病与氧化应激相关疾病中的多元化应用奠定基础。
4 材料与方法
4.1 MgH₂颗粒制备
采用电弧等离子体蒸发装置制备均匀亚微米级分散MgH₂粉末(命名为HydroMg)。如前期报道[22],采用纯镁电弧蒸发与原位氢化工艺。具体:市售99.9%纯镁粉室温下经25 MPa单轴压机制备圆柱坯体。反应腔抽真空至5×10⁻² Pa以下,充入Ar(0.75 atm)与H₂(0.05 atm)混合气体,将圆柱坯体作为阳极置入。电弧蒸发直流电流设为140 A。最终,制备的HydroMg颗粒在空气中钝化后取出。
4.2 颗粒表征
采用TEM(120 KV, Talos L120C G2, 美国)观察MgH₂形貌;Nano ZS90系列粒度分析仪分析粒径分布;D8 DaVinci衍射仪(布鲁克,德国)在40 kV下采集XRD数据。
4.3 MgH₂‑凝胶体系制备
4 ℃下将15 g、20 g、25 g F127(15 wt%、20 wt%、25 wt%)加入生理盐水(0.9% NaCl, 100 mL)充分溶解,获得温敏水凝胶前驱液。采用试管倾斜法测定凝胶化温度(GFT):取1 mL样品溶液加入试管,20‑37 ℃水浴缓慢加热,每温度点平衡后倾斜观察。
MgH₂‑凝胶采用简易混合自组装法制备:将不同量F127(Sigma‑Aldrich, 美国)加入生理盐水(0.9% NaCl)制备空白凝胶,4 ℃冰箱磁力搅拌至透明溶胶。按设计浓度分别加入MgH₂颗粒、MgSO₄溶液或NaOH溶液混合成胶,空白凝胶液4 ℃保存备用。
4.4 氢气、镁离子与碱性体外释放动力学
广口圆柱瓶中加入1 mL水凝胶(MgH₂浓度1 mg/mL)完全覆盖底部,再加2 mL 0.9% NaCl溶液。校准氢气微传感器多表计(MMS‑903995, UNISENSE, 丹麦)经微操纵器精准垂直插入瓶口,位于凝胶上方1 cm处(图S23)。
采用配备阻挡放电离子化检测器(BID)的气相色谱仪(Nexi GC 2030, 岛津,日本)分析水凝胶包埋气体组分。分别采用氢气测量仪(ENH‑2000, TRUSTLEX, 日本)、便携式pH计(LAQUAtwin‑pH‑22, 堀场先进技术,日本)与电感耦合等离子体分析(iCAP6300, 赛默飞,美国)记录不同时间点生理盐水溶解氢气浓度、pH值与Mg²⁺浓度。
4.5 细胞活力检测
人永生化角质形成细胞(HaCaT)购自美国模式培养物收藏所(ATCC),培养于含10% FBS、100 U/mL青霉素‑链霉素的DMEM培养基(Gibco, 美国),37 ℃、5% CO₂培养。采用CCK8试剂盒(日本同仁)按说明书评估细胞活力。
HaCaT细胞接种于96孔板,培养至40‑50%汇合度,分别用MgH₂颗粒处理8、12、24、48、72 h。每孔加入10 μL CCK‑8溶液与90 μL新鲜培养基,37 ℃孵育1 h。酶标仪(Multiskan GO, 赛默飞,美国)450 nm波长检测。
4.6 EdU检测
EdU(5‑乙炔基‑2'‑脱氧尿苷)488成像试剂盒购自中国锐博。细胞经50 μM EdU 37 ℃标记2 h,4%多聚甲醛固定15 min,0.5% Triton X‑100透膜10 min,Apollo 488与Hoechst 33342染色。EdU阳性细胞(绿色)与总Hoechst阳性细胞(蓝色)比值代表DNA合成能力。
4.7 ATP生成检测
采用增强ATP检测试剂盒(碧云天,中国)评估ATP含量。细胞经ATP裂解液裂解,12,000 g离心5 min取上清,与ATP检测工作液反应。发光光谱仪(EnSpire, 美国)检测发光活性,ATP水平以细胞蛋白浓度归一化。
4.8 ROS检测
采用流式细胞仪与2',7'‑二氯二氢荧光素二乙酸酯(DCFH‑DA, Sigma‑Aldrich)检测ROS生成。HaCaT细胞(10⁵细胞/孔)经不同剂量MgH₂(350 μg/mL、500 μg/mL)处理24 h。收集细胞,1000 rpm离心5 min,1 mL PBS洗涤,加入20 μM DCFH‑DA孵育20 min。流式细胞仪(BD LSRFortessa, 美国)检测荧光:激发/发射波长488 nm/525 nm。
4.9 蛋白提取与Western blot
分离表皮或预处理细胞采用含1 mM苯甲基磺酰氟的RIPA裂解液(碧云天,中国)提取总蛋白,BCA试剂盒测定蛋白浓度。样品经天能预制胶电泳分离,转印至PVDF膜。一抗β‑actin、PKM2(1:1000)4 ℃孵育过夜,二抗(1:1000, 碧云天)室温孵育50 min。TBST洗涤3次后,增强化学发光法显影。
4.10 qPCR
PCR引物由上海生工合成。采用SYBR Premix EX TaqII(Takara)在7500实时PCR系统(Applied Biosystems, 美国)扩增。以β‑actin为内参,2⁻ΔΔCt法计算基因表达倍数差异。
引物序列:
- β‑actin:F 5'-TAAGGTGACAGCAGTCGGTT-3',R 5'-TGTGTGGACTTGGGAGAGG-3'
- TNF‑α:F 5'-CAGGACTTGAGAAGACCTCAC-3',R 5'-GTCTGGAAACATCTGGAGAGA-3'
- CCL20:F 5'-GACATAGCCCAAGAACAGAAA-3',R 5'-CCAGTGAGGCACAAATTAGAT-3'
- IL‑1β:F 5'-GATATGGAGCAACAAGTGGT-3',R 5'-AGGACAGGTACAGATTCTTTTC-3'
- CD69:F 5'-GTACGAGAAGTTGGAATCATCTG-3',R 5'-GTTGTGGTGGAGAAGAAGTAACAT-3'
- CD103:F 5'-TCTCCAGATGTTCAGTGTGATG-3',R 5'-CTTGAGTATGGGGTGACCAAT-3'
4.11 IMQ诱导银屑病样小鼠模型
7周龄雄性BALB/c小鼠购自上海吉辉实验动物饲养有限公司,在复旦大学实验动物科学部无特定病原体(SPF)环境饲养。所有动物实验严格遵循《实验动物护理与使用指南》,经复旦大学实验动物科学部动物福利与伦理小组批准(许可号:2020‑华山医院‑JS‑294),全程遵循实验动物福利伦理原则,最大限度减少动物痛苦。
适应饲养1周后,小鼠背部剃毛2×3 cm以诱导皮肤炎症。连续7天,每24 h在剃毛区涂抹5% IMQ乳膏(50 mg/只),第8天拍照观察并进行PASI评分,数显千分尺(三丰)测量背部皮肤厚度(随机3点取平均)。
小鼠分为8组:
1. 正常组
2. 单纯IMQ模型组
3. 1 mg/mL MgH₂‑凝胶治疗组
4. 5 mg/mL MgH₂‑凝胶治疗组
5. 卡泊三醇治疗组
6. 空白凝胶对照组
7. MgCl₂‑凝胶对照组
8. NaOH‑凝胶对照组
银屑病复发小鼠模型参照Shi等[48]建立:背部剃毛区连续7天涂抹62.5 mg IMQ,间歇30天后,连续7天涂抹20.8 mg IMQ诱导复发。
4.12 PASI评分
参照临床PASI标准,对小鼠背部皮损炎症程度与严重度进行客观评分。红斑、鳞屑按0‑4级评分(0=无,1=轻度,2=中度,3=重度,4=极重度)。
4.13 组织病理学与免疫荧光
第8天(发病)/第48天(复发)收集各组背部皮损,4%多聚甲醛固定,石蜡包埋、脱水、脱蜡、复水后H&E染色。采用CK‑16(GB12804)、PCNA(GB13010‑1)、Ki67(GB111141)抗体检测,HRP标记二抗反应,DAB显色,苏木素复染。
4.14 免疫组化
组织4%多聚甲醛固定,一抗兔抗CD69(Absinbio, abs136297)、兔抗CD103(Absinbio, abs118732)4 ℃孵育过夜,Alexa Fluor 555抗兔IgG与Alexa Fluor 488抗鼠IgG二抗(1:2000, CST)室温染色,DAPI核复染。共聚焦激光扫描显微镜(FV‑1000, 奥林巴斯,日本)观察。
4.15 液相色谱‑串联质谱(LC‑MS/MS)
精密称取50 mg解冻样品至2 mL EP管,加入500 μL预冷提取液(70%甲醇水溶液)与小钢珠,30 Hz均质4次,每次30 s。1500 r/min振荡5 min,冰浴静置15 min,4 ℃、12000 r/min离心10 min。取200 μL上清至进样瓶用于LC‑MS/MS分析。
4.16 RNA测序分析
TRIzol试剂提取小鼠全层皮肤总RNA,oligo(dT)磁珠纯化mRNA,构建文库在Illumina HiSeq 2000平台测序,生成50 nt单端读长。Agilent 2100生物分析仪评估文库质量,Trimmomatic软件处理原始数据。
4.17 葡萄糖生成及SOD、CAT活性检测
采用SOD、CAT试剂盒(碧云天,中国)分别检测SOD、CAT活性;葡萄糖检测试剂盒(南京建成,中国)按说明书定量分析葡萄糖生成。
4.18 炎症因子水平定量
按蛋白阵列手册(Ray Biotech, 美国)处理银屑病小鼠、正常小鼠与MgH₂‑凝胶组皮损并提取蛋白,采用定制Quantibody小鼠细胞因子阵列检测。该阵列采用多重夹心ELISA系统,膜上包埋特异性细胞因子/趋化因子抗体,每种因子抗体4点重复,设阳性、阴性与内参对照。RayBio QAM‑TH17‑1软件提取分析数据,低于检测限因子以0计。
4.19 皮肤刺激性试验与体内生物安全性评估
4只Balb/c小鼠评估MgH₂皮肤刺激性。刺激实验前24 h剪毛器剃除背部毛发。MgH₂均匀涂抹于无毛皮肤区(A、D区)5天,B、C区不处理作为对照(图S10)。观察皮肤反应(主要为红斑),参照ISO‑10993‑10评分标准(刺激指数),记录红斑与水肿评分(0‑4)。刺激指数<0.4为无明显刺激。
为进一步评估全身生物安全性,取主要脏器(心、肝、脾、肺、肾)进行组织学分析。小鼠分为对照组、空白凝胶组、MgH₂‑凝胶组,标准H&E染色观察全身毒性与病理损伤。
4.20 KEGG通路富集分析
采用KOBAS软件平台检测差异基因KEGG通路统计富集,Cluster Profiler R工具筛选基因组背景下高度富集通路。Q值<0.05为差异基因高度富集通路。
4.21 统计学分析
数据以平均值±标准差(SD)表示,SPSS 18.0(IBM, 美国)统计分析。两组比较采用非配对双尾t检验,多组比较采用单因素方差分析(ANOVA),事后Tukey检验校正多重比较。P<0.05为具有统计学差异。
https://blog.sciencenet.cn/blog-41174-1527727.html
上一篇:红光疗法的科学原理《自然》
下一篇:误食过氧化氢导致脑血管气栓塞案例