博文
GLP‑1 减重药物心脏保护作用巨大《自然·通讯》
|
GLP‑1 减重药物心脏保护作用巨大《自然·通讯》
尽管急诊救治成功,仍有多达半数的心脏病发作患者出现微血管血流受损。一项新研究表明,现已广泛用于糖尿病和肥胖症治疗的 GLP‑1 类药物,有望被重新用于解决这一问题。
一项新研究显示,广泛使用的 GLP‑1 减重药物不仅能改善代谢健康,还可能在心脏病发作后保护心脏。
医生通常可以重新开通引发心梗的堵塞动脉,但这并不意味着心肌内部的危机就此结束。
布里斯托大学与伦敦大学学院(UCL)的一项新研究表明,GLP‑1 类减重药物,例如司美格鲁肽(商品名:Ozempic、Wegovy)和利拉鲁肽(商品名:Victoza、Saxenda),可在心梗发作后的数小时至数天内,通过改善心脏最微小血管的供血,帮助保护脆弱的心肌组织。研究人员表示,这可降低与持续性损伤相关的严重并发症风险,而这一问题影响着多达半数患者。
这项发表在《自然·通讯》(Nature Communications)上的研究,为心梗救治提供了新方向:利用临床上已广泛用于代谢疾病的一类药物,针对标准急诊救治未必能解决的顽固性循环障碍。
已有大型研究表明,GLP‑1 减重药物与主要不良心血管事件风险降低相关,即便患者健康背景不同、减重幅度各异。这项新研究则聚焦于这些益处在微观层面可能的机制。
探究“无复流”现象的成因
研究团队重点关注了“无复流”(no‑reflow)——一种危险状况:即使主要冠状动脉已被疏通,部分心肌的血流仍无法完全恢复。这种并发症尤其令人棘手,因为它可能发生在血管造影显示手术成功的情况下。
团队此前的研究指出,周细胞(包裹毛细血管的小型收缩细胞)是关键元凶。在缺血状态下,心脏缺乏富氧血液供应,这些细胞会收缩并使毛细血管变窄,形成持续的血流瓶颈,即便动脉已重新开通也依然存在。
布里斯托医学院转化健康科学系心血管再生医学高级讲师、该研究第一作者 Svetlana Mastitskaya 博士解释道:
“在近半数心梗患者中,即便急诊治疗已开通主要动脉,心肌内的微小血管仍处于狭窄状态。这会导致一种被称为‘无复流’的并发症,血液无法抵达部分心肌组织。”
“我们此前的研究已表明,这种血管狭窄是‘无复流’的重要原因,而该并发症会增加心梗一年内死亡或因心力衰竭住院的风险。但我们最新的发现令人意外:GLP‑1 类药物或可预防这一问题。”
GLP‑1 药物如何改善血流
在动物模型中,研究人员发现 GLP‑1 药物能够解除微血管的“ choke point(瓶颈/堵塞点)”。这类药物可激活钾离子通道,使周细胞松弛,让收缩的血管重新扩张。毛细血管更通畅后,心梗后的心脏血流得到改善,从而降低进一步损伤的风险。
这一机制意义重大,因为它瞄准了当前治疗难以解决的环节。恢复大血管血流至关重要,但“无复流”主要是小血管问题,即便主要堵塞已解除,仍可能导致部分心肌供血不足。
伦敦大学学院乔德雷尔生理学教授、该研究共同负责人 David Attwell 教授补充道:
“如今越来越多同类 GLP‑1 药物应用于临床,用于治疗 2 型糖尿病、肥胖症乃至肾病等多种疾病。我们的研究结果凸显了这类现有药物被重新用于治疗心梗患者‘无复流’风险的潜力,有望提供挽救生命的解决方案。”
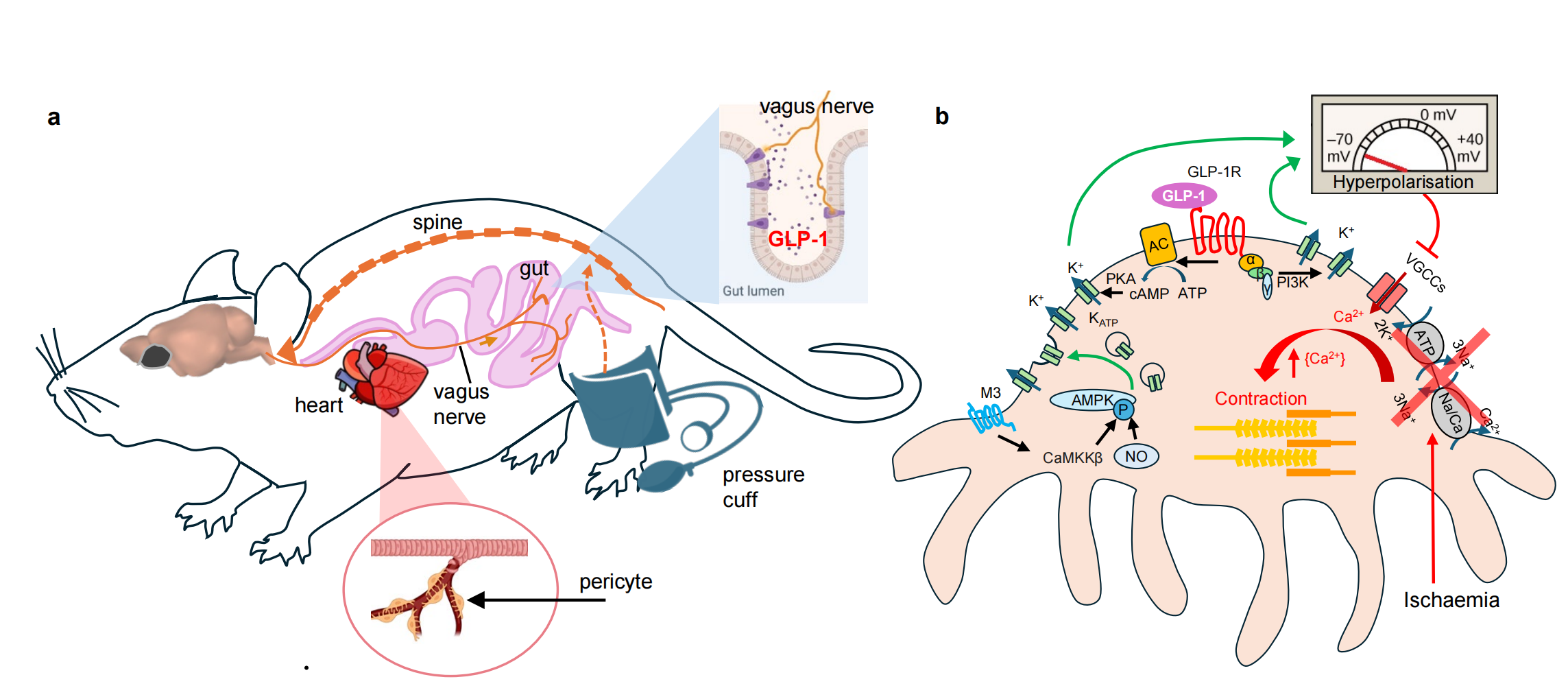
图 本文阐明的信号通路
a 远程缺血预处理(RPc)心脏保护作用中的脑‑肠‑心脏神经体液通路示意图
下肢缺血通过脊柱激活远程缺血预处理(RPc)反射,该信号在脑干层面进行处理。随后神经信号经迷走神经传递至肠道,由肠道内分泌L细胞分泌GLP‑1(插图:L细胞——紫色;迷走神经——橙棕色)。GLP‑1随血液/淋巴进入体循环并到达心脏,作用于微血管系统,使周细胞舒张。
b 心脏周细胞上GLP‑1受体激活后的下游分子机制
在体缺血或离体氧糖剥夺(OGD)会耗竭细胞内ATP,抑制Ca²⁺泵出周细胞,进而激活周细胞收缩、导致毛细血管狭窄。
缺血预处理促使肠道释放GLP‑1,激活周细胞上的GLP‑1受体,使cAMP浓度升高或激活PI3激酶,进而激活KATP通道(前提是AMPK已将其插入细胞膜)。
K⁺外流使周细胞膜发生超极化,抑制电压门控Ca²⁺通道的Ca²⁺内流,最终使周细胞舒张。
AMPK的活性依赖于毒蕈碱(M3)受体及一氧化氮(NO)相关机制。
https://blog.sciencenet.cn/blog-41174-1525139.html
上一篇:红细胞作为主要葡萄糖汇,改善高海拔环境下的葡萄糖耐量
下一篇:从肠道逆转认知能力下降