博文
为什么心脏肿瘤如此罕见?不断泵血的心肌“击退”了癌症
|
为什么心脏肿瘤如此罕见?不断泵血的心肌“击退”了癌症
心脏泵血时产生的压力,能阻止癌细胞在小鼠心脏内增殖。

一排用于医学教学的心脏解剖模型。
今日发表于《科学》(Science)的一项研究指出,心脏的持续跳动能够阻止癌症在小鼠心脏内生长。这或许可以解释,为何包括人类在内的所有哺乳动物中,心脏肿瘤都极为罕见。
人体内几乎所有器官和组织都可能发生肿瘤,但心脏肿瘤却极少出现。在人类中,仅有不到1%的尸检病例发现原发性心脏肿瘤;而继发性肿瘤(原发癌位于身体其他部位)在尸检中的检出率也仅为18%。
澳大利亚悉尼大学心脏病学家、研究员詹姆斯·庄表示,迄今为止,对于心脏肿瘤为何如此罕见,科学界一直没有令人满意的解释。他说,这项最新研究提出了一个极具说服力的观点:心脏受到的机械张力可能是关键原因。
意大利的里雅斯特大学临床科学家塞雷娜·扎奇尼亚带领团队,将心脏移植到基因改造小鼠的颈部。这些“外置心脏”不会跳动,但仍能获得血液供应并保持功能。
随后,研究团队分别向小鼠颈部的移植心脏和体内的原生心脏注射癌细胞。短短两周内,移植心脏中的癌细胞大量增殖,取代了大部分健康细胞;相比之下,原生心脏中仅有约20%的组织发生癌变。
工程化心脏组织
研究团队还在培养皿中利用大鼠细胞培育了工程化心肌组织。只有在研究人员向组织中加入钙离子(钙离子在体内驱动心脏跳动)时,这些细胞才会产生搏动。
团队随后向这些心肌组织中注射肺癌细胞。结果发现:静止不动的心肌组织中,癌细胞数量更多、侵占范围更大。此外,癌细胞在静止组织中均匀分布,却只聚集在搏动组织的外层。
扎奇尼亚团队长期致力于研究“为何心脏组织无法再生”。此前研究已发现,心脏跳动时产生的压力在其中发挥作用。“我们不禁思考:阻止心脏自发性再生的机制,是否也在保护心脏免受癌症侵袭?”扎奇尼亚说,“很高兴看到我们的假设得到了验证。”
扎奇尼亚表示,团队目前正在研究:能否在身体其他部位(如皮肤、乳腺)模拟心脏受到的机械压力,以阻止肿瘤生长。研究人员还在探索高血压等会增加心脏压力的疾病,是否同样具有抑制癌症生长的保护作用。
澳大利亚墨尔本贝克心脏与糖尿病研究所的心脏细胞生物学家亚历山大·平托认为,这项研究对纤维化等其他心脏病也具有启示意义——纤维化会导致心肌过度瘢痕形成。他表示,心脏受到的机械张力,或许可以解释为何瘢痕组织只出现在心脏特定区域,就像癌细胞只聚集在搏动心肌组织的外层一样。
Mechanical load inhibits cancer growth in mouse and human hearts | Science
编者摘要
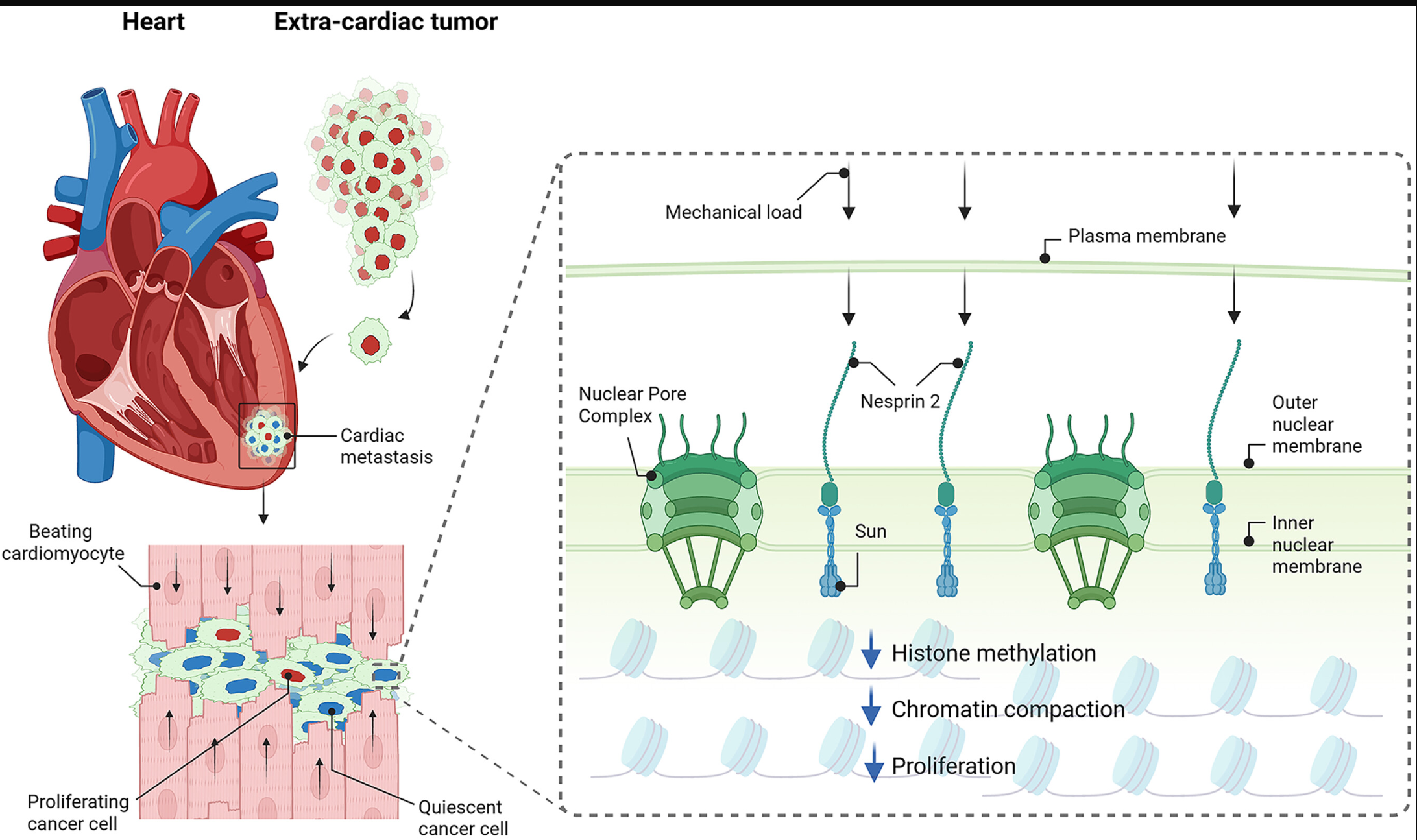
心脏原发癌变或癌细胞转移至心脏的情况极为罕见,这表明心脏微环境中存在某种抑制肿瘤生长的机制。机械负荷是最具可能性的核心解释。丘奇(Ciucci)团队对此假说开展验证:将癌细胞植入啮齿动物心脏,并在体外构建存在/缺失正常机械负荷的心脏工程模型;同时对比分析罕见心脏转移癌患者的人体组织样本,及其对应的心外肿瘤组织。研究证实:机械负荷升高会激活核膜蛋白2(Nesprin-2) 信号通路,进而引发染色质浓缩与组蛋白甲基化修饰改变,最终抑制癌细胞增殖(详见帕尔策与马丁的观点评述文章)。——叶夫根尼娅·努西诺维奇
结构化摘要
研究背景
心脏极少发生癌变;尽管心肌组织血管分布极为丰富,但心脏原发肿瘤与心脏转移瘤均十分罕见。心脏的抗癌屏障机制,目前尚不明确。
研究依据
已有研究表明,机械负荷是哺乳动物出生后早期心肌细胞停止增殖的关键诱因,直接限制成年心脏的再生修复能力。本研究提出科学假说:心脏的机械负荷,同样能够抑制心脏内癌细胞的增殖。
研究结果
1. 研究首先构建小鼠体内癌症遗传模型,通过Cre重组酶技术实现突变K-Ras基因过表达、p53基因敲除,验证心脏的抗肿瘤特性。结果显示:肝脏、心脏、骨骼肌的基因重组效率相近,但小鼠全身多部位均出现肿瘤,唯独心脏无肿瘤发生。
2. 构建小鼠异位心脏移植模型,实现活体心脏去机械负荷处理:通过外科手术,将移植心脏的主动脉、肺动脉分别与受体动物的颈动脉、颈外静脉吻合,保证心脏血液灌注,但使左心室脱离正常机械负荷。
3. 同步构建可精准调控机械负荷的体外人工心脏组织模型。动物实验与体外模型共同证实:机械负荷可显著抑制心肌内肺腺癌、结肠癌、黑色素瘤细胞的增殖;反之,心脏去负荷则会促进癌细胞增殖。
4. 利用空间转录组技术,分析同时发生心脏转移与心外转移的人类肿瘤样本。发现:无论原发肿瘤类型如何,心脏转移癌均存在统一的转录组特征,且组蛋白去甲基化酶显著高表达。
5. 心脏转移癌组织中,组蛋白H3第9位赖氨酸三甲基化水平降低、染色质浓缩程度下降。单细胞转座酶可及染色质测序、染色质免疫共沉淀测序结果证实:调控心脏机械负荷,会改变癌细胞增殖关键基因位点的染色质开放程度与组蛋白甲基化状态。
6. 核膜蛋白2(Nesprin-2) 是核心机械信号传导分子,可感知心脏搏动产生的机械力,并将机械信号传导至细胞核,最终抑制细胞增殖。动物实验进一步验证:敲低肺癌细胞的Nesprin-2基因后,再将癌细胞植入活体心脏,即便存在生理水平的机械负荷,癌细胞仍可大量增殖并形成巨大肿瘤。
研究结论
本研究系统阐明了机械力在心脏天然抗癌过程中的关键作用,为基于机械刺激的新型肿瘤治疗策略提供了理论基础与全新方向。
心脏抑制癌细胞增殖的核心机制
定植于心肌组织的癌细胞,会持续暴露在心肌收缩、压力-容积负荷共同产生的机械力环境中。Nesprin-2作为核心机械感受器,感知机械信号后,会降低癌细胞内组蛋白甲基化水平、减弱染色质浓缩,从表观遗传层面全面阻断癌细胞增殖。
常规摘要
心脏自身极少癌变,同时再生能力极度匮乏——哺乳动物出生后,心肌细胞便永久停止分裂增殖。这提示:限制心脏再生的生理机制,同时也是心脏抵御癌症的天然屏障。
本研究围绕机械负荷展开机制探究,结合活体动物肿瘤模型、体外人工心脏组织模型证实:机械负荷可有效抑制心肌内癌细胞增殖。
人类心脏转移癌的空间转录组分析显示,肿瘤组织存在组蛋白甲基化下调、染色质松散化等表观遗传特征;该改变会直接影响增殖相关基因的染色质开放状态,而Nesprin-2是介导这一系列机械-表观遗传调控的核心感应蛋白。
本研究揭示了机械力保护心脏抵御癌症的分子机制,为开发机械干预类抗肿瘤疗法提供了全新思路。
https://blog.sciencenet.cn/blog-41174-1531858.html
上一篇:革命性技术:将健康线粒体精准输送至需要的部位