博文
科学家患自己研究的帕金森病什么感觉?
|
自患自己研究的病帕金森病什么感觉?
这个故事的一个版本出现在《科学》杂志,第380卷,第6644期。
Twist of fate: What happens when a top Parkinson’s researcher gets the disease? | Science | AAAS
几年前,匹兹堡大学匹兹堡神经退行性疾病研究所所长蒂姆·格林纳米尔(Tim Greenamyre)开始注意到自己身体的令人不安的症状。他逐渐开始闻不到东西,便秘,在睡梦中大喊大叫,踢腿。走路时左臂没有摆动。


2021 年 7 月,格林纳米尔求助于一位神经科医生同事,以确认他已经怀疑的诊断。他患有帕金森病,他一直致力于治疗和试图治愈这种疾病。在他漫长而富有成效的职业生涯中,这位67岁的老人不仅赢得了患者和临床同事的钦佩,而且还开发了广泛使用的帕金森氏症动物模型,并对环境触发因素提供了关键见解。这项工作使他接触到在啮齿动物中诱发疾病的化学物质,这可能是他自己疾病的一个因素。
“讽刺是显而易见的,”格林纳米尔说,他是一个害羞的人,有着枯燥的幽默感,喜欢开玩笑,在未经实践的眼睛看来,他几乎没有表现出这种疾病的迹象。
对于同事们来说,这个消息令人震惊和心碎。“我受到了如此深的影响,以至于无法立即做出反应,”杜克大学医学院研究帕金森氏症的神经科学家劳里·桑德斯(Laurie Sanders)说,他曾经是格林纳米尔博士后。“老实说,我真正想做的只是开车去匹兹堡,给他一个拥抱。”
格林纳米尔的200名左右的帕金森病患者中,几乎所有的人,其中一些他已经被照顾了十多年,都会从这篇文章中得知他的诊断,他在这篇文章中不情愿地公开了他的病情,因为它正在成为谣言的主题。他担心这会分散他们的注意力。“我希望他们更关注在自己身上,而不是我,”他说。
具有讽刺意味的是,格林纳米尔的诊断是在帕金森氏症研究人员重新乐观的时候做出的,他们认为他们可能最终接近可以减缓或阻止阿尔茨海默氏症之后第二常见的神经退行性疾病进展的治疗方法。美国约有100万人患帕金森病,每年诊断出近9万例新病例。据估计,全球有超过800万人患有帕金森病,是世界上增长最快的神经系统疾病。
英国外科医生詹姆斯·帕金森(James Parkinson)于1817年描述了帕金森病的典型运动症状,这是由于在黑质(参与运动控制的中脑区域)中产生神经递质多巴胺的细胞退化所致。这会导致各种症状,包括最常见的震颤、肌肉僵硬以及平衡和协调困难。随着疾病的进展,人们可能难以说话和开始运动。许多人后期发展为痴呆。帕金森氏症本身不会杀死患者,但它的并发症,特别是由于吞咽困难引起的吸入性肺炎,经常会致命。
以左旋多巴和卡比多巴的口服药物组合给药补充多巴胺,自1970年代在美国获得批准以来一直是一线疗法,尽管全球许多人仍然无法获得或负担不起。这种药物改善了运动症状,但随着时间的推移,它开始更快地消失,有时无法忍受的副作用 - 包括称为运动障碍的不自主抽搐运动 - 经常发展。五十年过去了,科学未能开发出一种阻止疾病而不是针对其症状的疗法,这对患者及其家人来说是痛苦和沮丧的。
日益严重的问题
美国的老龄化帮助推动了帕金森病患病率的大幅增加,但唯一批准的疗法针对的是症状而不是疾病进展。
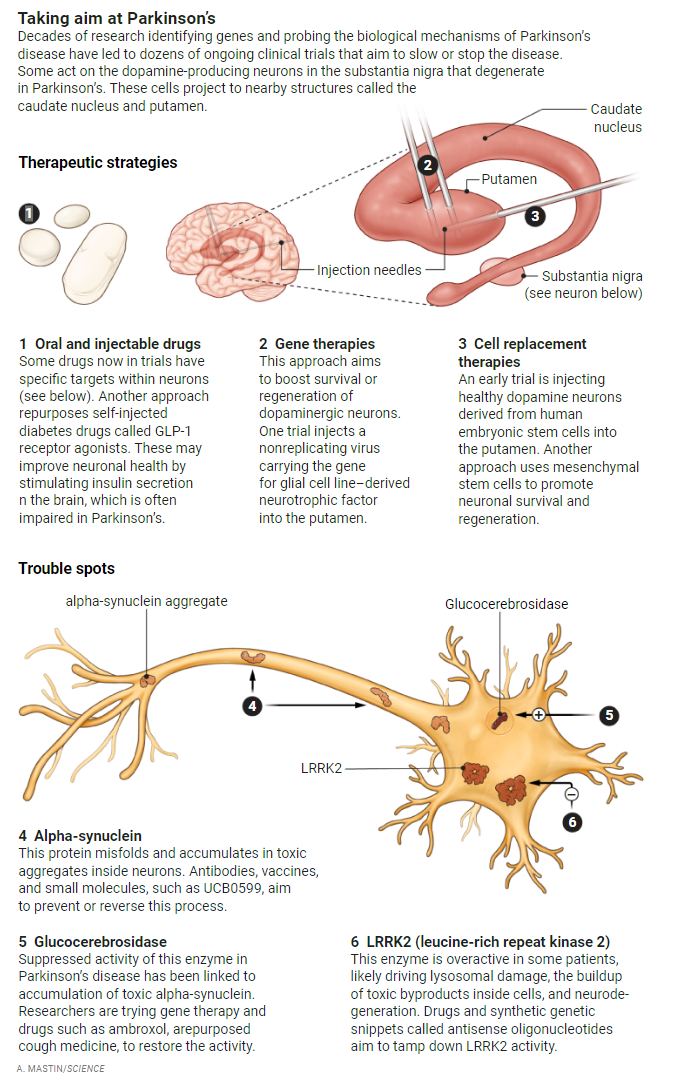
但现在,“我们正处于一个转折点,”格林纳米尔前博士后托德·谢勒(Todd Sherer)说,他管理迈克尔·J·福克斯帕金森氏症研究基金会,现在是其首席任务官。这种乐观情绪是数十年研究的结果,从1997年开始,与该疾病相关的基因突变的揭示加速了这项研究。这些发现为包括格林纳米尔在内的科学家探索该疾病的分子机制打开了大门,并发表了大量出版物(见图表)。新知识反过来又使公司能够开发旨在减缓,阻止甚至预防疾病的药物和其他实验性疗法(见图)。今天,这些疗法正以惊人的速度进入临床试验。
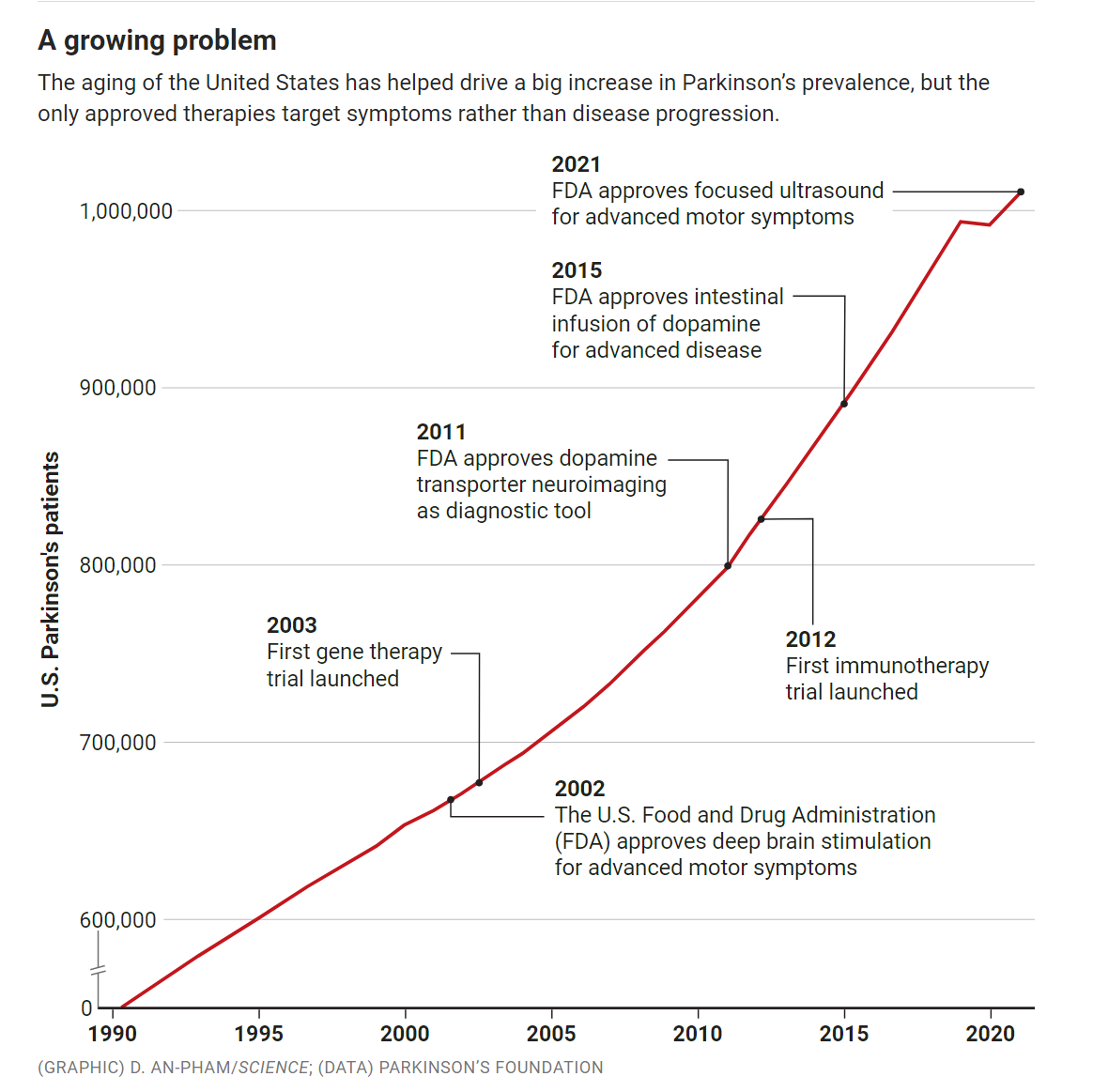
“已经发生了转变,因为我们更好地了解了疾病和目标,”桑德斯说,并指出有50多项针对疾病根源的临床试验正在进行中。她说,与15年前她刚开始涉足该领域时正在进行的少数几个相比,这是一个非凡的增长。
尽管有这些充满希望的迹象,但对于格林纳米尔和他的帕金森病患者来说,预期的突破可能为时已晚。当通过颤抖的手或拖拽的脚诊断出这种疾病时,它被认为已经在雷达下活跃了几十年,导致格林纳米尔经历的便秘和嗅觉丧失等更安静的症状 - 并破坏黑质中大约一半的多巴胺产生神经元。但格林纳米尔仍然决心打破这种疾病的后盾。
“现在没有被诊断出患有帕金森病的好时机,”他去年秋天说,当时他赢得了福克斯基金会颁发的100万美元研究领导奖。“但这是历史上被诊断出患有帕金森病的最佳时机。”
格林纳米尔在纽约威彻斯特县长大,是一位化学工程师和家庭主妇的儿子。在密歇根大学医学院,格林纳米尔成为医生安妮·白金汉·杨(Anne Buckingham Young)新团队的一员。Young是一位热情的新助理教授,格林纳米尔回忆说她是“自然的力量”。当Young描述她的博士工作时,阐明了毒药士的宁如何在脊髓中神经递质甘氨酸的受体上发挥作用,格林纳米尔被迷住了。“我觉得这太酷了,在她那里可以谈论具有临床意义的基本药理学和生理机制,”他说。他加入了她的实验室,并开发了一种可视化大脑中神经递质受体的技术,他和杨用它来研究阿尔茨海默氏症和亨廷顿病的机制。他获得了医学博士和博士学位,到1990年,当他开始经营自己的实验室并在罗切斯特大学一流的运动障碍诊所看病人时,他与人合著了20篇论文,其中两篇发表在《科学》杂志上。
他还开始研究帕金森病。与该领域的其他人一样,他的灵感来自1983年《科学》杂志上的一篇论文,该论文描述了一群突然发作的帕金森氏症年轻人,他们出现在北加州的医院。所有人都服用了一种被一种叫做MPTP的化学物质污染的街头毒品。它的有毒代谢物MPP+破坏了黑质中的多巴胺能神经元,科学家们很快表明,MPP+存在于并抑制线粒体复合物I,复合物I是关键生化链中的第一个酶,在线粒体中将食物转化为能量,线粒体是细胞内的微小动力源。这是一个诱人的线索,线粒体损伤可能在疾病中发挥作用。
格林纳米尔等知道MPP +并不是线粒体复合物I的唯一抑制剂。还有很多,包括一些化学物质,研究开始与帕金森病有关。但这种重要的线粒体酶的经典抑制剂是家庭蔬菜园丁使用的一种名为鱼藤酮的杀虫剂。
鱼藤酮被认为是一种天然“有机”杀虫剂,因为它来自某些植物的根部;人们还用它来杀死宠物身上的跳蚤和蜱虫,野生动物机构用它来控制入侵鱼类种群。但对于格林纳米尔来说,这是探索帕金森氏症奥秘的一种工具。到1990年,他开始使用放射性标记的鱼藤酮,这是一种喜欢脂肪的化学物质,很容易穿过生物膜,包括血脑屏障,来绘制复合物I大脑中的位置。
大约在同一时间,几个实验室在死后大脑样本以及患者的血小板中发现了帕金森病患者线粒体中存在缺陷的复合物I活性的证据。格林纳米尔意识到他可以通过让大鼠接触鱼藤酮来模仿这种疾病。他预计这种化学物质会在每个器官中影响线粒体,研究证明确实是这样。但鱼藤酮只对一种细胞类型有巨大的毒性作用。
2000年,当时在埃默里大学的格林纳米尔和他的团队在《自然神经科学》上发表了一篇开创性的论文。他们报告说,给大鼠长期静脉输注鱼藤酮选择性地破坏了帕金森病患者退化的黑质中产生多巴胺的相同神经元。此外,幸存的神经元含有α突触核蛋白的原纤维或细线,聚集成团。这些聚集体非常类似于路易体的结构,是人类大脑中帕金森氏症的标志。更重要的是,大鼠出现了帕金森病症状:运动不稳,驼背姿势,爪子颤抖和严重僵硬。
这项工作为研究人员提供了第一个捕捉到经典运动症状和疾病标志性病理学的动物模型。这也增加了对鱼藤酮和其他杀虫剂可能引发帕金森氏症的怀疑。
今天,格林纳米尔想知道他几十年来对鱼藤酮和类似化合物的研究是否可能导致他的疾病。“因为开始对这个危险知道的不多,所以没有那么小心,”他说。“而且我接触了很多化合物,尤其是鱼藤酮。”
二月的一天,格林纳米尔正在他阳光明媚的办公室里大声沉思着一碗米饭、菠菜和山羊奶酪的午餐,办公室毗邻他在皮特市中心医学园区中心的实验室。他刚刚参加了一次实验室会议,神经科学家艾米丽·罗查(Emily Rocha)是一名前博士后,她提出了她在研究中遇到的一个严峻挑战,并停下来与研究生马修·基尼(Matthew Keeney)一起查看了一些新收集的多巴胺神经元图像。前研究生和博士后说,格林纳米尔有一种令人鼓舞但不干涉的指导风格。“他有很强的能力让你探索,但当你误入歧途时,他知道什么时候把你拉回来,”Sherer回忆道。
午餐时,格林纳米尔解释说,鱼藤酮必须溶解在二甲基亚砜(DMSO)等溶剂中才能制成溶液。这种溶液会不时地溅到他的手套上,“DMSO会把它直接穿过手套,进入你的皮肤,然后直接穿过皮肤。他说,当时他并没有做太多事情,因为他和他的同事并不认为有太大的危险。“直到我们对此进行了一些研究,”他补充道。(2011年发表的一项高质量流行病学研究将鱼藤酮的使用与农民及其配偶患帕金森病的风险增加2.5倍联系起来。)
如果鱼藤酮确实在导致格林纳米尔病中起作用,它可能会增加潜在的遗传脆弱性。他是90%的所谓特发性疾病患者之一:他们的帕金森氏症没有明确的遗传原因,但几乎可以肯定是由定义不明确的遗传易感性和环境触发因素的某种组合造成的。例如,格林纳米尔曾经有过红头发,流行病学研究将其与帕金森氏症的风险升高有关。
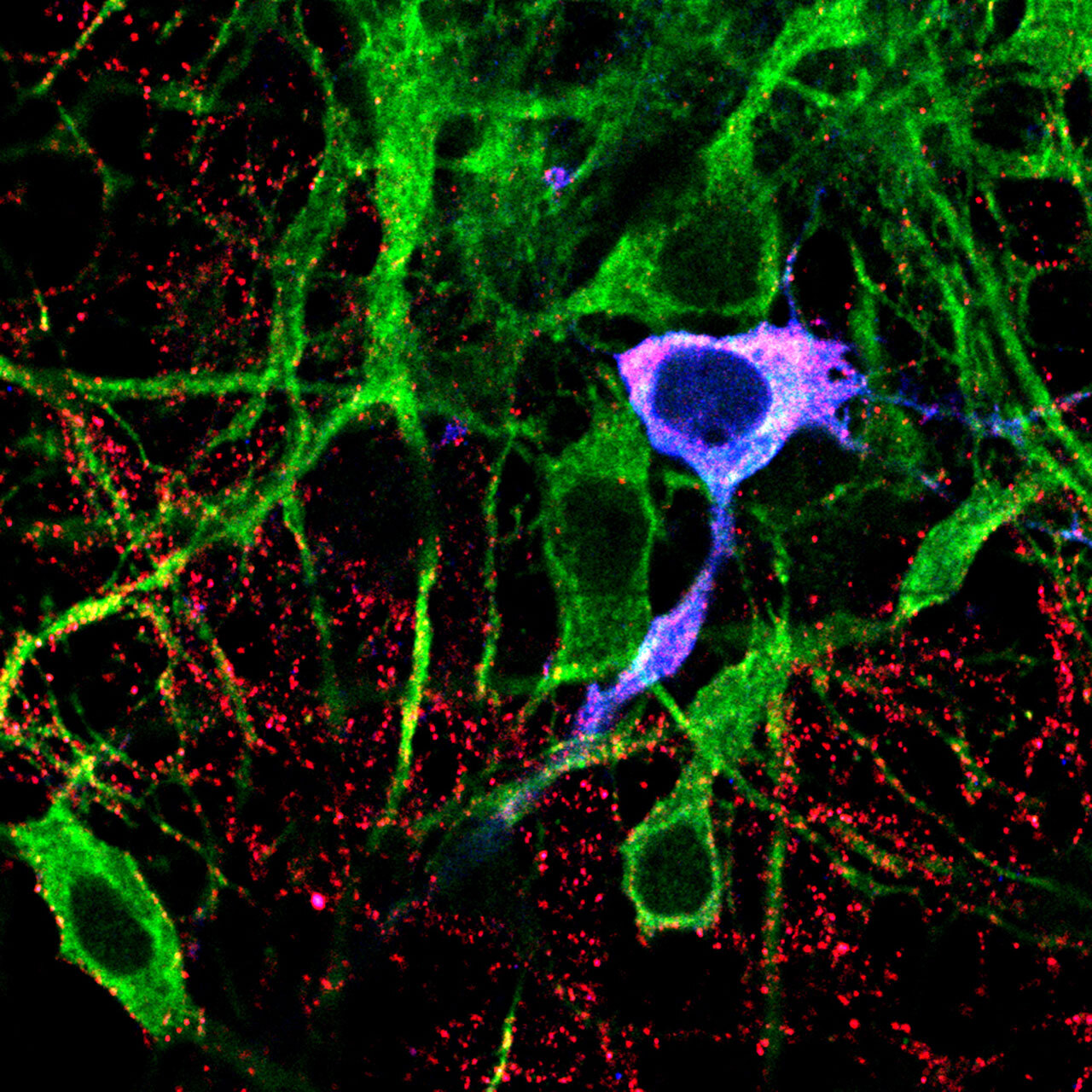
用农药鱼藤酮处理后大鼠多巴胺能神经元(蓝色)的氧化损伤(洋红色)
然而,大约10%的帕金森病病例显然是由于特定基因的突变。在1997年《科学》杂志的一篇论文中发现了第一个α突触核蛋白基因后,许多科学家只关注基因。很快,他们发现了更多的遗传突变——在编码一种叫做Parkin的蛋白质、一种叫做LRRK2的酶和另一种叫做葡萄糖脑苷脂酶的酶的基因中。研究人员开始深入研究突变基因是如何造成损害的。
这些发现恰逢格林纳米尔个人生活中的一段棘手时期。艰难的离婚导致他在2004年从埃默里搬到匹兹堡大学,他还面临资金困境。格林纳米尔当时的主要资助者皮考尔基金会(Picower Foundation)与臭名昭著的庞氏骗局运营商伯尼·麦道夫(Bernie Madoff)投资了数千万美元,一切都失去了。
尽管存在这些障碍,格林纳米尔在过去的20年里一直在试图定义破坏帕金森氏症神经元的关键机制,而不是像许多其他人那样追逐新的致病基因。他一直关注基因与环境之间的复杂关系,重点是与帕金森氏症相关基因相互作用的杀虫剂等物质。
近年来,格林纳米尔已经专注于LRRK2(发音为“lark 2”),它代表富含亮氨酸的重复激酶2。它编码的酶是一个主通路控制器,调节细胞内称为囊泡的蛋白质和隔室的运动。基因中的几个突变使酶的活性进入激活状态。这最终会损害溶酶体的功能,溶酶体是降解不需要的蛋白质的细胞垃圾收集器,并且这种损害被认为会导致这种疾病。
LRRK2突变约占所有帕金森氏症病例的3%至4%。但在 2021 年,由现任阿拉巴马大学伯明翰分校助理教授的博士后 Briana de Miranda 领导的格林纳米尔 小组发现毒素可以模仿它们的效果。他们报告说,溶剂三氯乙烯是一种用于干洗和脱脂金属的线粒体毒素,可提高LRRK2酶活性,并在老年大鼠的大脑中诱导帕金森样病理。这项工作为几十年前在北卡罗来纳州Lejeune营地的海军陆战队基地饮用受污染水的人的初步集体诉讼提供了素材。他们声称水中的三氯乙烯导致了他们的帕金森病。
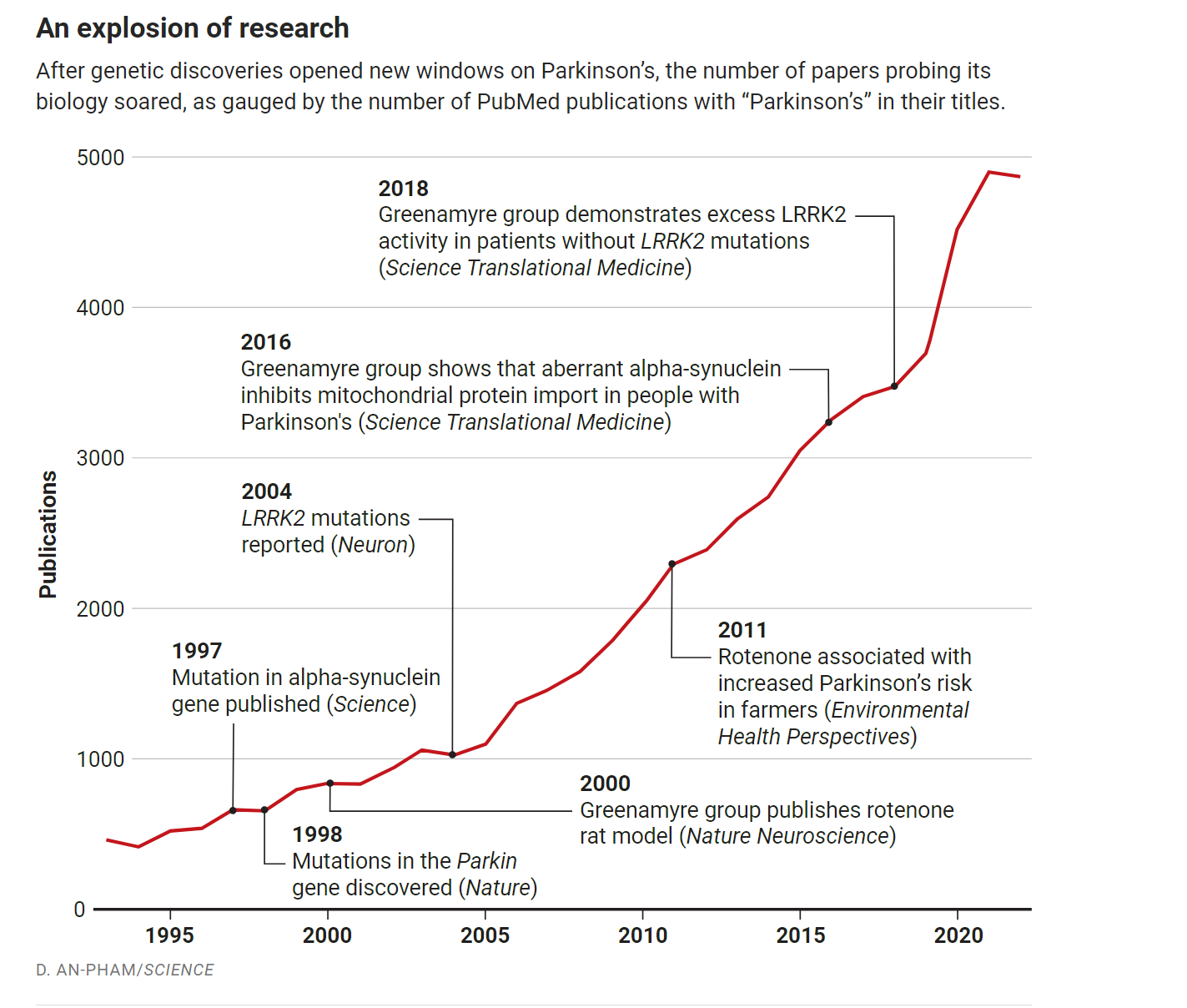
研究的爆炸式增长
格林纳米尔数十年来在环境毒素方面的工作也为福克斯基金会和其他机构对美国环境保护署 (EPA) 提起诉讼奠定了基础,此前该机构于 2021 年重新批准了广泛使用的除草剂百草枯。与鱼藤酮一样,百草枯会导致啮齿动物出现帕金森病症状和病理,其他研究人员也用它来制作该疾病的动物模型。美国环保署认为,随着安全措施的到位,百草枯对农业的好处超过了其对人类健康的风险,并表示已发现“流行病学证据不足”表明百草枯与帕金森氏症之间存在因果关系。格林纳米尔在此案中提交了一份法庭之友简报,谴责EPA忽视了将百草枯暴露与帕金森氏症联系起来的众多流行病学和动物研究。
自从格林纳米尔在2000年使用鱼藤酮在大鼠中产生帕金森样疾病的开创性论文以来,EPA也两次检查了该杀虫剂的安全性。2007年,它限制鱼藤酮的使用,以控制入侵鱼类 - 制造商自愿将其从住宅和花园使用市场上撤出。去年,美国环保署对其在鱼类杀戮中的使用实施了进一步的安全限制,并重申由皮肤暴露驱动的鱼藤酮暴露的职业风险“令人担忧”。但该机构在 2022 年也审查了文献,并得出结论,“证据不足”表明鱼藤酮与帕金森氏症之间存在因果关系。
其他科学家表示,格林纳米尔和其他人的流行病学研究和实验室工作是有说服力的。“他提出了一个非常令人信服的理由,即鱼藤酮和其他杀虫剂是特发性帕金森病非常重要和相关触发因素,”佛罗里达大学医学院的神经科学家Malú Gámez Tansey说。“这是一个非常重要的贡献。”
在实验室隔壁大楼的一家诊所里,格林纳米尔穿上了白大褂,在精神上为71岁的芭芭拉·弗里兹(Barbara Frieze)准备了问题清单,芭芭拉·弗里兹(Barbara Frieze)是一名帕金森病患者,他已经照顾了近10年。“你的小狗怎么样?”他问,一个简单的开场白。她吐露说,当她痴呆的丈夫在疗养院衰落时,小狗一直保持着精神。弗里兹每天都来看他,这使得锻炼变得困难,当他温柔地催促她关于她的活动时,她解释说。(有氧运动可能会减缓运动症状的进展,格林纳米尔本人每周锻炼7天。”
他继续问弗里兹关于她的睡眠,她的平衡,她的情绪和她的震颤。当她将双臂伸直在身前时,后者是痛苦可见的;她的左手继续颤抖,因为她应格林纳米尔的要求走下附近的大厅。
他说:“11年来,你做得很好。你的走路真的很好。我知道你患有帕金森氏症的唯一方法是震颤。”
“当我离开这里时,我感到充满希望,”弗里兹说。“如果我对帕金森氏症感到怀疑,我来到这里,我总是感觉很好离开。
下一位患者卡尔·马斯基维奇(Carl Maskiewicz)是一名60多岁的退休会计师,每周参加六次拳击和瑜伽课。他赞扬格林纳米尔的耐心和解释事情的能力。“我认为有时他比患有帕金森氏症的人更了解我正在经历的事情,”Maskiewicz说。
第三名患者罗伯特·汉南(Robert Hannan)从佛罗里达州通过Zoom打来电话。这位84岁的连锁药店前首席执行官已经患有这种疾病25年了。他现在每2小时服用一次左旋多巴,但随着药物的消失,他的话变得含糊不清,左手的震颤再次出现。
在二月的这一天,格林纳米尔没有告诉他的病人他自己也患有这个病。不过,他很快就给他们发了电子邮件,不想让他们在消息出来时被蒙蔽。“我告诉他们在我的思想和祈祷中,”Maskiewicz说,他已经是格林纳米尔的病人9年了。“我提出聊天,'如果你只是想找人说话'——因为有时这是这种疾病的困难部分。
像其他数百万患有帕金森氏症的美国人一样,格林纳米尔的患者都在等待多巴胺以外的东西。“这仍然是一种无法治愈的疾病,”汉南说。“我每次来都会问:'有接近的东西吗?'”
2018年,由研究科学家罗伯托·迪·马约(Roberto di Maio)领导的格林纳米尔小组的一篇新论文指出了前进的方向。他们开发了一种测定方法来测量不同类型脑细胞中的LRRK2酶活性,并用它来证明该酶在黑质中产生多巴胺的神经元中过度活跃 - 即使在基因没有突变的患者中也是如此。
进一步的实验揭示了分子事件的潜在级联,最终导致细胞垃圾处理系统的瘫痪。研究小组认为,这导致了异常α-突触核蛋白的积累。
“这是实际患者组织中的第一个数据,表明......在特发性帕金森病患者中,他们确实增加了LRRK2激酶活性,“Denali Therapeutics首席医疗官兼开发主管Carole Ho说。
该论文强烈建议抑制这种活动可能有助于许多患者 - 而不仅仅是携带遗传LRRK3突变的4%至2%。研究人员发现,在给予鱼藤酮的大鼠中,LRRK2抑制剂阻断了通常由杀虫剂引起的所有异常事件。这一发现为公司在人体中测试LRRK2抑制剂的努力提供了新的动力;德纳利的候选人走得最远。它与Biogen合作,Biogen现在正在招募1000多名有和没有LRRK2突变的帕金森病患者,看看这种酶的抑制剂是否会减缓疾病的进展。
世界各地的实验室和临床试验正在寻求其他药物、基因疗法和干细胞来替代丢失的多巴胺神经元。一些靶标显示出生物学罪魁祸首,例如提高葡萄糖脑苷脂酶的活性,该酶可以在帕金森氏症中被抑制,或阻断有毒α-突触核蛋白的聚集。其他人的目标是为大脑提供一般弹药,例如更好地修复和维护多巴胺能神经元的药理学工具。
早期也有失望。分别在 2021 年和 2022 年,Biogen 和 AbbVie 停止了攻击 α突触核蛋白的抗体的临床试验。罗氏和Prothena Biosciences正在向前推进,尽管去年夏天同样令人失望的试验结果表明,他们的单克隆抗体prasinezumab对疾病进展没有有意义的影响。
许多研究人员希望这种明显的失败将变得更加罕见。帕金森氏症的潜在生物学在患者亚群之间差异很大,并且正在努力将正确的人与正确的试验相匹配,以便每种疗法在最有可能对其产生反应的人中进行测试。
在运动症状出现之前很久就识别出高危人群也会有所帮助。α-突触核蛋白抗体可能仍然有效,例如,如果足够早地给予,在广泛的神经元丢失之前。福克斯基金会正在进行一项庞大的长期研究,寻找可以在疾病早期阶段捕获人们的成像,生物和遗传标记。这项研究在上个月产生了具有里程碑意义的结果:《柳叶刀神经病学》(The Lancet Neurology)的一份报告发现,脊髓穿刺测试对沐浴脊髓的液体中错误折叠的α突触核蛋白进行了准确诊断,88%的时间准确诊断了帕金森氏症,包括在人们开始出现运动症状之前识别它。科学家说,尽管该测试的侵入性使其不太可能常规使用,但它将成为对患者进行临床试验分类和探索疾病生物学的宝贵工具。如果有希望的早期结果得到证实,类似的血液测试可能会在治疗早期疾病时可用。
在担心自己缺乏嗅觉和其他症状几个月后,格林纳米尔终于求助于一位值得信赖的同事爱德华伯顿,他是研究帕金森氏症的皮特神经学家和神经科学家。伯顿说,他有时会因训练而感到负担;他无意中分析人,用熟练的眼光观察运动中最微妙的异常。
2019年夏天,伯顿从格林纳米尔主持的戈登帕金森病研究会议回来,两人坐在机场休息室里。别人问了格林纳米尔一个问题,伯顿觉得他朋友的头转向提问者只是太慢了。
https://blog.sciencenet.cn/blog-41174-1386877.html
上一篇:恶性胶质瘤为自己生长劫持神经可塑性信号
下一篇:自体干细胞移植治疗自身免疫疾病【科学】