博文
安慰剂效应缓解疼痛的中枢机制  精选
精选
|
安慰剂效应——仅仅对生物效应的期望就能产生该效应——是历史最悠久且至今仍是最有效的医疗干预手段之一。因此,科学家们对其背后的神经机制知之甚少,这颇为令人好奇。陈及其同事在《自然》杂志上撰文,报告了使用一种简单但可靠的方法在小鼠中产生安慰剂疼痛缓解效应,并由此定义了支撑这一现象的神经回路。他们展示了疼痛缓解的期望是由大脑边缘系统中一部分神经元介导的,这个系统已被充分证实与疼痛有关。然而,出人意料的是,这些神经元向脑干和小脑的部分区域发送信号。考虑到这些区域通常与更基础的功能相关联,如协调运动,这确实是一个大惊喜。
安慰剂效应从一开始就备受争议,特别是因为通过疾病的自然进展或患者随时间恢复的统计趋势也能产生类似的症状减轻。但现在已广泛达成共识,认为安慰剂效应是真实存在的。安慰剂引起的疼痛缓解,或称为安慰剂镇痛,是对安慰剂效应研究最深入、可能也是最稳健的例子,主要由疼痛缓解的期望产生。许多形式的安慰剂镇痛可以通过抑制阿片受体的药物纳洛酮(也被称为Narcan)来阻断,这意味着体内产生的阿片肽,如β-内啡肽和脑啡肽,有其作用。
科学家们经常使用大脑扫描或神经成像技术来评估人类大脑活动。2021年关于安慰剂镇痛在人类神经成像研究中识别的大脑区域的元分析包括了许多已知介导疼痛本身的区域。这项元分析的一个令人惊讶的发现是小脑活动的显著减少——一个被认为主要负责运动和协调的大脑区域。尽管小脑以前已与疼痛联系起来(疼痛成像的一个长期“肮脏的小秘密”是小脑经常被激活),但其角色仍然“神秘”。
成像研究尽管很有用,但无法提供现代方法所提供的分辨率,这些现代方法能够追踪小鼠中的神经回路,而这种技术尚未应用于安慰剂镇痛。当然,不能通过口头指令使小鼠产生期望,但通过条件反射(即通过关联学习)很容易在小鼠中生成期望。陈等人开发了一个为期7天的安慰剂镇痛条件反射实验,涉及一个有两个视觉上不同的腔室的设备,其地板被加热至舒适的30°C或有害的48°C。一个为期3天的习惯阶段之后是一个为期3天的条件反射阶段,在此期间一些小鼠学会了48°C的腔室行走时会感到疼痛。
在测试日,经过条件反射的小鼠以及未经过条件反射的小鼠都被放置在设备中,但现在两个地板都被加热到48°C。尽管对所有小鼠来说有害刺激是相同的,但经过条件反射的小鼠更喜欢在之前“安全”的腔室中度过时间,并且,重要的是,表现出更少的疼痛相关行为(如舔舐、挺身和跳跃),就好像它们期望那个腔室中的疼痛更少一样(图1a)。这种镇痛的期望在条件反射阶段后至少持续了一周,并且只要测试在该设备内进行,就会泛化到除热以外的其他疼痛来源。
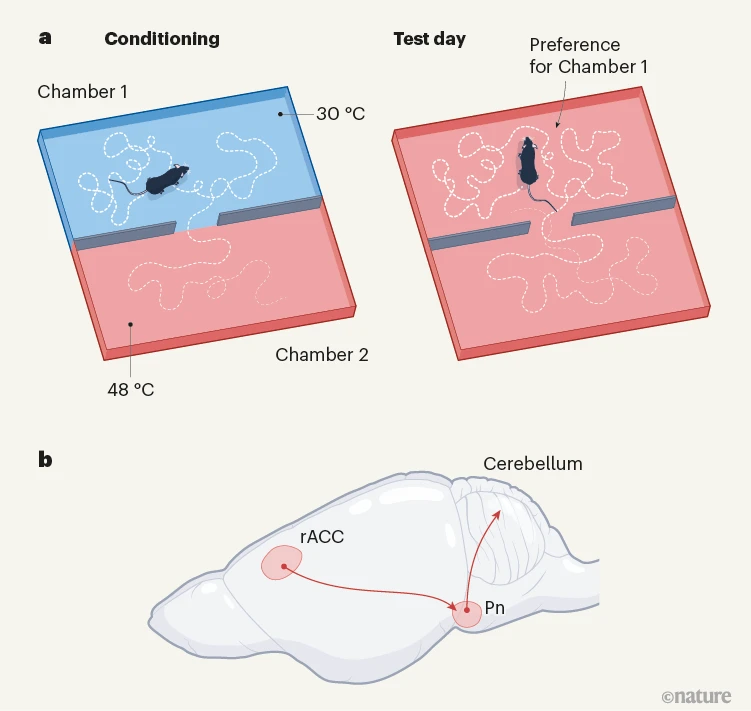
图1 | 安慰剂效应的神经机制。a, 陈等人通过将小鼠放置在一个有两个视觉上不同腔室的设备中——一个温暖(30°C)和一个有害地热(48°C)——产生了疼痛缓解的期望(即安慰剂镇痛)。3天后,两个腔室都被加热到48°C。经过条件反射的小鼠在之前为30°C的腔室中花费更多时间,并且比未经条件反射的小鼠(未显示)表现出更少的疼痛迹象。b, 使用神经回路追踪方法,作者发现这种安慰剂镇痛是由涉及前扣带皮层前端(rACC)、脑干的桥脑核(Pn)和小脑的通路介导的。
陈及其同事利用这一稳健的行为测试,并基于早期证据——即前扣带皮层前端(rACC)——边缘系统的一部分——在安慰剂镇痛中起作用,开始在小鼠大脑中寻找既接收来自rACC的神经投射又在镇痛期望期间表现出神经活动的区域。为此,他们使用了一种名为靶向活跃群体中的重组(TRAP)的基因技术来识别神经元活跃后发生的Fos基因表达。确定了三个大脑区域:纹状体、丘脑和下丘脑核,以及让研究人员惊讶的是,位于脑干中的一对结构,称为桥脑核(Pn)。
使用钙成像(检查清醒行为小鼠中的神经元活动)、电生理学(记录脑切片中的神经元放电)以及通过光控蛋白对rACC-to-Pn回路进行人工“光遗传”激活和抑制,建立了rACC-to-Pn通路在安慰剂中的因果作用。研究人员还使用了单细胞RNA测序方法来查看基因表达,并显示相关的Pn神经元是兴奋性的,并且表达了编码δ-阿片受体的基因,这支持了安慰剂镇痛确实是由阿片介导的观点。
Pn充当大脑皮层和小脑之间的联络者。尽管已观察到Pn因疼痛而激活,但它们并不被认为是通常响应和处理疼痛的大脑区域网络——被称为疼痛矩阵——的一部分。由于小脑是Pn神经元的主要目标,加上一位坚持的审稿人推动了这项工作,作者接下来检查了经历镇痛期望的小鼠中小脑皮层的主要神经元——普肯野细胞的活动。陈等人鉴定出了一组特定的普肯野细胞,这些细胞编码了疼痛缓解的期望,并发现这一组的活动是由rACC-to-Pn回路驱动的(图1b)。
这并不是第一个安慰剂镇痛的动物模型;也不是第一次使用条件反射来研究疼痛。但是,陈等人肯定提供了迄今为止最深入的安慰剂镇痛的神经解释,基本上使用了目前所有可用于定义小鼠中神经回路的现代高分辨率技术。由于安慰剂效应及其邪恶的双胞胎“反安慰剂”——个体对治疗的负面期望导致其症状恶化——在疾病和治疗的中介中无处不在且非常稳健,因此对于此类解释至关重要。值得注意的是,安慰剂效应在人类中可能比在小鼠中更为复杂,因为在人类中,它涉及基于口头指示和社会影响的期待,除了条件反射之外。
这里真正有趣的发现是,在所有可能的大脑区域中,正是Pn和小脑负责产生期望,这一概念可能会被假定为由协调复杂认知功能的中枢神经系统的“更高”级别介导。这一展示,连同其他最近的电路追踪努力,可能导致对疼痛神经解剖学的重新评估。
https://blog.sciencenet.cn/blog-41174-1447993.html
上一篇:大脑衰老的五种模式
下一篇:氢果冻治疗抑郁症的小鼠研究2024