博文
内源性生物抗氧化系统  精选
精选
|
氧化损伤可能疾病的原因,更可能是疾病的结果。氧化还原反应是生命能量代谢的化学基础,生物体主要成分是生物大分子组成的超复杂结构,几乎所有生物大分子,在生物化学反应中都可充当还原性底物,氧化底物的源头是来自空气中的氧气。生物大分子合成的能量源头来自光合作用的光子,光合作用从水和二氧化碳出发,产生复杂生物分子的基础,并释放出氧气。本质上,能量代谢是还原性生物大分子,被氧气氧化,分解为二氧化碳和水的过程。因此,组成生物体的一切生物大分子,是生物化学能源的存储者,也可以作为其他物种的食物,通过能量代谢释放出能量。生物组成成分被氧化是能量代谢的本质,所以一切生物分子被氧化损伤就成为最大可能。这也正是生物分子氧化损伤之所以普遍存在的前提。但生物分子氧化损伤不一定是疾病的原因,也有可能是疾病发生的结果,因为只有生物系统发生紊乱或障碍,生物分子氧化损伤的水平一定会提高,这是在分子水平上体现出生物系统紊乱的特征,但这是表型层面的必然性,不一定是原因层面的标志。
一切复杂系统都是物质能量和信息控制下的稳态,生物体系的维持也必然如此。氧化是能量代谢的基础,生物分子是生物结构,也是能量存储的形式,生物分子被氧化是生物核心现象,维持氧化还原平衡就必然是在物质能量信息控制下最重要的任务。
自由基生物学研究认为,生物体内氧化还原稳态主要决定于两个方面的因素,一是产生活性氧的因素,另一个是控制活性氧的力量。产生活性氧的因素主要来自于电子传递的无序,正常情况下,来自生物分子的相对活泼的电子,以电子传递体为载体进行跨分子传递,其中最经典的电子传递过程就是线粒体内氧化磷酸化过程,电子跨分子复合物传递,能量逐渐下降,释放的化学能将质子跨细胞膜转运,质子梯度产生的电化学能经过ATP合成酶,也是质子回流通道,合成ATP和降低质子梯度。电子最终传递给氧气分子,结合质子产生水,完成全部生物能量代谢过程。在安全正常的电子传递过程能保证完全还原氧气分子,如果这个系统出现故障,电子传递不流畅,中间发生了电子的泄漏,导致电子还原氧气不彻底的现象发生,就会产生超氧自由基,这也就是自由基生成的最常见情景。
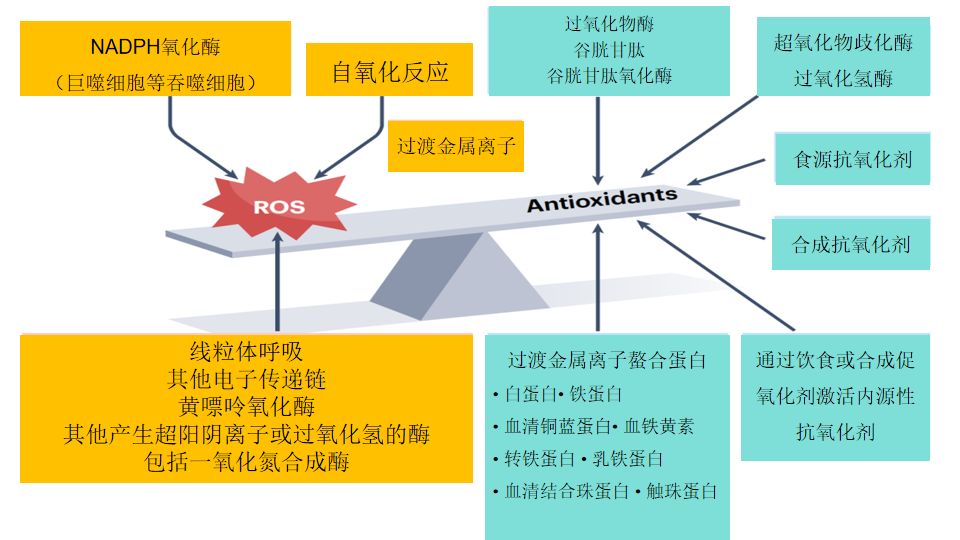
由于自由基活性氧具有生理功能,生物体系被迫或主动保留了自由基产生基础,同时建立控制自由基水平过高的机制。主动产生自由基的途径还包括NADPH氧化酶、黄嘌呤氧化酶、一氧化氮合成酶等多种生化反应过程。其中NADPH氧化酶是免疫吞噬细胞产生自由基杀伤病原体生理基础,具有明显的主动性。为了避免自由基水平过高失去控制,导致生物分子被活性氧攻击破坏,导致生物体系失去平衡,生物体演化出一套控制活性氧水平的工具和方法。这就是生物抗氧化系统。生物抗氧化系统包括内源性抗氧化系统和外源性抗氧化物质,外源性抗氧化物质主要来自食物营养素,如各种植物抗氧化物、维生素和矿物质。其中某些矿物质是内源性抗氧化酶的活性成分。这里主要介绍生物内源性抗氧化系统,生物内源性抗氧化系统由三部分组成,抗氧化酶、非酶抗氧化物、金属离子螯合剂。
一、抗氧化酶
抗氧化酶主要有超氧化物歧化酶、 过氧化物还原酶、谷胱甘肽 过氧化物还原酶和过氧化氢酶等。
1.超氧化物歧化酶(SODs)
超氧阴离子歧化反应
2O2•−+2H+→H2O2+O2
歧化是一种化学反应,其中同一物质既被氧化又被还原;超氧自由基(O2-•)既被氧化为O2,又被还原为过氧化氢。生物体系一般需要SOD催化,没有SOD情况下,超氧化物也会分解,在pH 7.4时要慢一个数量级。
O2•−活性不强,但可以从含有[Fe-S]簇的蛋白质(如克雷布斯循环酶乌头酸酶)中释放Fe2+,从而从铁储存蛋白铁蛋白中促进Fenton化学(见下文)。超氧化物与一氧化氮(NO)快速反应生成过氧亚硝酸盐,过氧亚硝酸盐快速质子化为过氧亚硝酸。
O2-•+NO•→ONOO+H+→ONOOH
过氧亚硝酸盐(ONOO−)、ONOOH及其进一步的反应产物(例如,与二氧化碳)对生物分子造成氧化损伤;EC-SOD在减缓血管系统和其他地方的O2-•与NO的反应中起着重要作用。HO2•(超氧化氢)的质子化形式可以启动脂质过氧化,但这在体内的重要性尚不清楚.
PUFA−H+HO2•→ PUFA• +H2O2
超氧化物歧化酶(Superoxide Dismutase,SOD)是生物体内存在的一种抗氧化金属酶,它能够催化超氧阴离子自由基歧化生成氧和过氧化氢,在机体氧化与抗氧化平衡中起到至关重要的作用,与很多疾病的发生、发展密不可分。
按照 SOD 中金属辅基的不同,大致可将 SOD 分为三大类,分别为 Cu/Zn-SOD、Mn-SOD、 Fe-SOD 。①Cu/Zn-SOD: 呈蓝绿色,主要存在于真核细胞的细胞质内,被认为存在于比较原始的生物类群中且分布最广的一种。②Mn-SOD:呈粉红色,主要存在于原核生物和真核生物的线粒体中。③Fe-SOD:呈黄褐色,主要存在于原核细胞中 。它们可以有效地清除超氧阴离子自由基(带有 1 个未成对电子的同时,还带有 1 个负电荷),避免其对细胞过度的损伤,具有抗氧化、抗辐射及抗衰老等功能。
根据分布部位,有线粒体(一些含铜和锌的SOD(CuZnSOD),SOD1,但线粒体基质中含锰SOD(MnSOD));细胞质、细胞核,可能所有细胞室(CuZnSOD);另一种CuZnSOD分布在细胞外基质(胞外SOD) 。
①大多数原始的无脊椎动物细胞中都存在Cu/Zn-SOD,脊椎动物则一般含有Cu/Zn-SOD和Mn-SOD。人、鼠、猪、牛等红细胞和肝细胞中含Cu/Zn-SOD,且其主要存在于细胞质,同时也存在于线粒体内外膜之间。而从人和动物肝细胞中也纯化了Mn-SOD,其一般存在于线粒体基质中。②植物细胞中的Fe-SOD主要存在于叶绿体中。③真菌里一般含Mn-SOD和Cu/Zn-SOD。大多数真核藻类在其叶绿体基质中存在Fe-SOD,类囊体膜上结合着Mn-SOD,而多数藻类中不含Cu/Zn-SOD。
2.过氧化物还原酶Peroxiredoxins
过氧化物还原酶(peroxiredoxin)是近年来新发现的一个抗氧化酶家族,在所有生物体内普遍存在,其蛋白质相对分子质量为2.2-3万,是机体抗氧化系统的重要组成部分。1988年,过氧化物还原酶最初在酿酒酵母中被发现,可保护谷氨酰胺合成酶免受氧化而失活,曾被命名为硫醇特异性抗氧化剂(thiol-specific antioxidant)和硫氧还蛋白过氧化物酶(thioredoxinperoxidase)。随着对各物种该家族成员认识的不断加深,2016年国际生物化学和分子生物学联合会命名委员会将该家族命“peroxiredoxin”(过氧化物还原酶)。
过氧化物还原酶的突出特点是,这类分子不含任何传统的氧化还原辅因子(如金属离子、血红素等),而是通过其保守的Cys残基参与催化,发挥其抗氧化的功能。过氧化物还原酶催化过程大致分为过氧化、分解和再循环三个阶段。第一阶段过氧化:FF构象中亲核的CP-S– 对H2O2发起双分子亲核取代反应(SN2)型攻 击,自身生成CP-SOH;第二阶段分解:FF构象中 的活性位点局部展开,CP-SOH移出活性口袋,多个残基进行重排,形成 “局部展开”构象,CP-SOH与CR-SH反应生成二硫键CP-S-S-CR;第三阶段再循环:CP-S-S-CR再由硫氧还蛋白系统还原回到初始状态,活性位点重新折叠恢复FF构象,为下一轮催化氧化做好准备。过氧化物还原酶的特点是自身催化过氧化氢,硫氧还蛋白系统是恢复其初始状态的作用。
过氧化物还原酶能催化硫氧还蛋白去除过氧化氢:
Thioredoxin(SH)2+H2O2→Thioredoxin(S)2+2H2O
硫氧还蛋白上的两个硫醇基团形成二硫化硫氧还蛋白(S)2,通过含有硒的硫氧还蛋白还原酶(TR)转化为还原的硫氧还蛋白
Thioredoxin(S)2+NADPH+H+→NADP++Thioredoxin(SH)2
过氧化物还原酶也可能有助于去除脂质过氧化物和过氧亚硝酸盐.
过氧化物还原酶分布在所有细胞部位,其生理功能是调节过氧化氢水平。
过氧化物还原酶活性的调节允许过氧化氢水平短暂升高,用于信号转导目的,然后恢复正常;许多 过氧化物还原酶还有其他重要的作用,例如作为伴侣蛋白; 过氧化物还原酶6具有磷脂酶活性。
3.谷胱甘肽过氧化物酶。
以还原型谷胱甘肽作为电子供体,还原过氧化氢为水。这种酶在细胞内外各种部位,也能协助过氧化物还原酶发挥作用,其中一种类型GPx4,由于在铁死亡过程发挥重要作用,近年来受到特别大的关注。
4.过氧化氢酶。
这种酶和SOD都是传统研究比较充分的酶,其根本作用就是催化过氧化氢为水。
二、非酶活性氧清除剂
非活性氧清除剂是可以直接中和自由基或清除活性氧的生物分子,主要包括还原型谷胱甘肽、缩醛磷脂和辅酶Q。
1.还原型谷胱甘肽
谷胱甘肽是由谷氨酸、胱氨酸和甘氨酸组成的三肽,氧化型谷胱甘肽是两个还原性谷胱甘肽通过二硫键结合起来。谷胱甘肽还原酶是一种含黄素腺嘌呤二核苷酸(FAD)的酶,能利用NADPH将氧化型谷胱甘肽还原成还原型谷胱甘肽。
GSSG+NADPH+H+→2GSH+NADP+
谷胱甘肽含量可到达mM水平,在多种组织内分布。谷胱甘肽是许多特别是酶谷胱甘肽还原酶的辅基。能直接中和次氯酸、过氧化氢和羟基自由基,也具有辐射保护作用。细胞缺乏谷胱甘肽容易发生氧化损伤。
2.缩醛磷脂
缩醛磷脂是一种甘油磷脂,其特征在于在甘油骨架的 sn-1 位置存在乙烯基-醚键。缩醛磷脂是细胞膜的主要成分,主要通过从头合成产生,而不是通过饮食摄入产生。红细胞、心脏、精子、大脑等大多数膜含有缩醛磷脂,能快速清除某些ROS,例如次氯酸和单线态氧(1O2) ,活性氧清除作用有助于保护其他膜脂质免受氧化。
3.CoQ
CoQ,也叫泛醌,可以还原为自由基CoQH•,进一步还原为CoQH2(泛素醇);CoQ的氧化还原使其参与线粒体电子传递链线粒体内膜电子传递链中的必要电子载体,也存在于脂蛋白和质膜中。CoQ主要分布在线粒体内膜,也存在于脂蛋白和质膜中。CoQH2可以清除脂质过氧自由基PUFAO2•为PUFAO2H,自己变成自由基CoQH•。避免脂质过氧化在线粒体和脂蛋白中很重要。CoQH2抗氧化作用也能减少铁死亡的发生。CoQH2能将ɑ生育酚自由基还原为ɑ生育酚。
三、过渡金属离子螯合剂
过渡金属离子是自由基反应的天然催化剂,是生物体系氧化还原反应的重要方式。过渡金属离子在生物氧化还原反应过程发挥重要催化作用,过渡金属离子有游离方式,更多是结合方式,如血红素蛋白。一般情况下,过渡金属离子发挥促进氧化损伤的作用。螯合剂由于可以俘获过渡金属离子,从而产生限制氧化损伤的作用。
铁和铜离子、血红素和血红素蛋白释放到组织或体液时可以促氧化;最常提到的反应是金属离子,特别是铁和铜离子与过氧化氢反应生成更高活性的羟基自由基(OH•)。
Fe2++H2O2→Fe3++OH•+OH-
Cu++H2O2→Cu2++OH•+OH-
铁离子或游离铜离子也会加速其他一些具有破坏性的自由基反应。包括产生ros的自氧化反应和血红素铁酰的产生。小心隔离血红素、血红素蛋白、铁和铜离子成非氧化还原活性形式是抗氧化防御的重要组成部分,例如在预防铁死亡。由NRF2调控的血红素加氧酶(HO-1)酶可以去除血红素。
过渡金属离子螯合剂抗氧化机制在所有的区域都很重要,特别是在细胞外液中。有助于减少氧化损伤,也有利于限制病原体的生长,因为能减少病原体获得金属离子营养素。正常细胞内存在一定浓度的具有催化作用的金属离子和游离血红素。降低过氧化氢水平或者通过隔离减少其扩散,可以控制其造成的氧化损伤。
铁超载疾病如血色素沉着症(包括肝癌、关节炎和糖尿病等)、颅内出血(释放血红蛋白)和肌肉损伤导致的肾衰竭(释放肌红蛋白)的病理说明金属离子通过氧化反应引起组织严重损伤。
1.珠蛋白/血红蛋白
珠蛋白/血红蛋白主要分布在细胞外,属于急性期蛋白,在炎症反应过程释放到血液。它们能结合释放的血红素,阻断其促氧化作用,加速从体液中清除。能降低过渡金属水平,减少过渡金属导致的氧化损伤。
2.转铁蛋白/乳铁蛋白
转铁蛋白/乳铁蛋白主要分布在细胞外,其作用主要是控制铁离子水平,将铁运输到需要铁的细胞中,与这些蛋白质结合的铁离子(如Fe3+)不具有催化氧化损伤的作用,健康人血浆中的“催化”铁水平基本上为零,有多余的铁结合能力,以阻止细菌生长和氧化损伤。组织损伤可导致铁和铜离子的释放,从而促进氧化损伤,例如肝功能衰竭。
3.白蛋白
白蛋白能结合血红素、游离铜离子和游离铁离子。过渡金属离子即使与过氧化氢反应,产生的任何ROS(OH•)都能被白蛋白清除。白蛋白有一个巯基组和其他可以清除ROS的结构,能清除细胞外的OH•、次氯酸和ONOOH。血液中白蛋白水平高达0.5 mM,具有多种生理作用,如抗氧化、渗透平衡,也是胆红素、游离脂肪酸、激素和药物等的血液内共享载体。肝脏是合成白蛋白的器官。氧化白蛋白从循环中去除并降解,氧化白蛋白的水平已被用作氧化损伤的生物标志物。
4.铜蓝蛋白
铜蓝蛋白是一种含铜酶,能氧化Fe2+而不释放ROS。铜蓝蛋白急性期反应蛋白,在炎症反应期间血浆水平增加。
这种“铁氧化酶”活性抑制Fe2+刺激OH•的生成和脂质过氧化。铁氧化酶活性不产生破坏性的氧自由基,不像Fe2+的非酶氧化,Fe2+能催化产生O2•−和OH•。铜蓝蛋白主要分布在细胞外,也存在某些组织细胞内,如大脑、肝脏、眼睛。铜蓝蛋白主要功能是通过安全地将Fe2+氧化为Fe3+并加载到转铁蛋白,确保巨噬细胞和组织正确的铁输出,实现控制铁离子的促氧化作用。
参考文献
Halliwell B. Understanding mechanisms of antioxidant action in health and disease. Nat Rev Mol Cell Biol. 2024 Jan;25(1):13-33. doi: 10.1038/s41580-023-00645-4. Epub 2023 Sep 15. PMID: 37714962.
https://blog.sciencenet.cn/blog-41174-1416970.html
上一篇:强效迷幻药可消除创伤后应激障碍
下一篇:良性氧化应激和氧化还原稳态