博文
Green Carbon│中国科学院大连化物所周雍进研究员、青岛农业大学杨建明教授:合成生物学助力疫苗佐剂的全生物合成
||

英文原题:Toward sustainable supply of vaccine adjuvant via synthetic biology
作者:Meijie Li, Xinglin Jiang, Yongjin J. Zhou*, Jianming Yang*
01 论文信息
论文信息
Li M, Jiang X, Zhou Y J, et al. Toward sustainable supply of vaccine adjuvant via synthetic biology[J]. Green Carbon, 2024 2(4) 421-422.
论文网址
https://doi.org/10.1016/j.greenca.2024.07.001
论文下载
Toward sustainable supply of vaccine adjuvant via synthetic biology
中文解读原链接
Green Carbon文章│中国科学院大连化物所周雍进研究员、青岛农业大学杨建明教授:合成生物学助力疫苗佐剂的全生物合成
02 背景简介
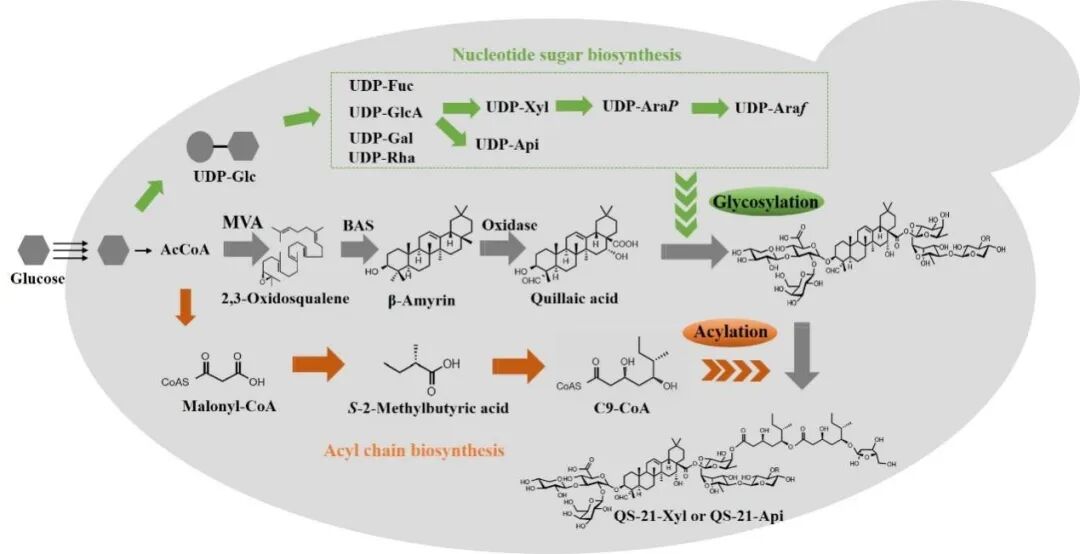
疫苗佐剂通过刺激或增强人体免疫反应来提高疫苗的疗效。QS-21是一种从智利皂树(QS)树皮中提取的强效疫苗佐剂,是目前唯一获批用于人类疫苗的皂苷基佐剂。在过去的25年里,QS-21已经在120多项临床试验中进行了测试和验证,目前已被批准用于儿童预防恶性疟原虫的疟疾疫苗(Mosquirix)、老年人接种的带状疱疹(Shingrix)疫苗和Novavax COVID-19。目前,QS-21主要依赖于从智利皂树的树皮中提取,但是QS-21分离纯化工艺复杂,而且皂皮树种植被GSK公司垄断。另一种途径是通过中间体皂苷的全化学合成,这需要76个步骤,效率极低,使得每公斤QS-21的成本高达数十亿美元。在烟草中通过重构20个步骤可以实现完全生物合成,但是这不适合大规模的生产。因此,QS-21的可持续生产和供应仍然是合成生物学领域的挑战。
近日,青岛农业大学李美洁副教授、丹麦技术大学姜兴林教授、中国科学院大连化学物理研究所周雍进研究员以及青岛农业大学杨建明教授在Green Carbon上发表题为“Toward sustainable supply of vaccine adjuvant via synthetic Biology” 文章,针对Jay D. Keasling团队在Nature上发表的文章“Complete biosynthesis of QS-21 in engineered yeast”,进行了系统性分析和点评。
03 文章简介
为了实现QS-21的全生物合成,Jay D. Keasling团队利用合成生物学技术,先后将来自六种生物的38种不同基因插入酵母中,成功在酵母中合成QS-21分子。首先,酵母的甲羟戊酸途径被上调以提高合成2,3环氧角鲨烯的碳通量,然后由异源 β-香树素合酶(BAS)环化成β-香树脂醇。引入含有细胞色素P450s以及细胞色素P450还原酶(CPR)的表达盒,以实现皂皮酸(QA),即 QS-21 的苷元,的生物合成。此外,引入植物核苷酸糖合成途径合成七种非天然尿苷二磷酸糖(UDP-糖),通过糖基转移酶(GT)共表达,用于在QA的C3羟基和C28羧基官能团上添加糖基。最后,研究人员完成了QS-21生物合成中的酰化和末端糖基化过程。通过过表达I型聚酮合酶(PKSs)、两种III型PKSs和两种酮还原酶(KRs),形成二聚酰基单元C9-CoA。接下来,糖基化中间体被C9-CoA酰基化,加入末端阿拉伯呋喃糖基,得到QS-21,包括QS-21-Xyl和QS-21-Api。在酵母中模拟植物从内质网膜的亚细胞区室化到细胞质。最终菌株YL-46的QS-21产量达到0.0012% w/w/DCW。目前,1 L发酵的生物工程酵母可以在三天内产生约100 μg的QS-21,市场价值约为200美元,生物合成方法在经济上是可行的。
这项研究是从单糖开始在细胞工厂中完全合成复杂化合物的成功案例。38种异源酶在酵母中的表达,这是有史以来构建的最长的生物合成途径之一。先前报道的最长代谢途径是在酵母中过表达来自植物的34个异源基因,用于抗癌药物长春碱的生物合成。另外,QS-21在工程酵母中的成功生物合成也有助于了解皂树中复杂的QS-21生物合成途径。虽然QS-21产量(0.0012% DCW)低于天然皂树(0.0032% DCW),但酵母中QS-21的生产速度仍远快于天然皂树的生产是速度(约1000倍),而且皂树只有在30-50岁时才会产生QS-21。QS-21在工程酵母菌株中的成功生物合成表明,大规模工业发酵有可能取代基于种植园的皂苷供应。此外,构建的酵母生物合成平台还可以用于合成QS-21的结构类似物,这有助于合理设计更有效的疫苗佐剂和QS-21的构效关系的研究。本研究为QS-21的商业化生产提供了强有力的技术支持,通过后续的优化,QS-21产量可以进一步提高,达到到工业规模。通过工程酵母生产QS-21不仅可以显著降低成本,还可以提高产量,避免对自然资源的过度依赖和破坏。这一成就有望对全球疫苗研究和生产方法产生深远影响。
虽然QS-21在酵母中的生产速度比天然皂树快得多,但距离大规模工业化还有很长的路要走,需要进行菌株优化以提高生物合成效率。尤其需要关注的是合成 C9-Keto-CoA的PKS途径,合成皂皮酸的氧化途径和糖基转移途径。此外,将生物合成和化学催化结合起来生产QS-21可能是一种替代方案。另外,发酵工艺和下游提取和纯化工艺的优化对于大规模生产是必要的,这将影响其商业和工业应用。此外,应确认工程酵母产生的QS-21作为疫苗佐剂的效果,并确保QS-21的安全性和可控性,以避免健康问题。此外,使用构建的酵母生物合成平台,通过表达替代酶,利用酶的杂合性,设计和筛选更有效的QS-21类似物作为强效疫苗佐剂。例如,通过表达鼠李糖转移酶(UGT73CX2)来取代木糖基转移酶,C3三糖链中的木糖可以被鼠李糖取代,含三糖的鼠李糖也是下游途径酶的底物,产生QS-21的甲基化衍生物。糖基转移酶GTs可以被修饰以产生截短的低聚糖,这有助于研究QS-21的糖基功能。此外,构建的酵母平台还可以应用于合成其他复杂的天然产物,为药物开发提供了新的途径。
总结及展望
总之,QS-21的全生物合成可以媲美合成生物学领域的里程碑式的成就,例如抗疟疾药物前体青蒿素的生物合成。QS-21的全生物合成证明了过去20年来合成生物学领域取得了很大进展。QS-21的全生物合成只是一个开始,展示了合成生物学在解决复杂化学问题方面的潜力。通过结合化学和合成生物学的优势,将可以实现更多的科学突破。
04 作者简介

杨建明 教授
杨建明,青岛农业大学生命科学学院教授,Green Carbon青年编委。主要从事微生物生理学及微生物代谢工程研究,在微生物催化合成萜烯类化合物开展了一系列基础和应用研究工作。曾先后主持中央军委装备发展部“慧眼行动”项目、中央军委科技委国防科技创新特区重点探索项目、国防科工委项目、国家自然科学基金面上项目、国家外国专家局引智项目、山东省自然科学基金面上项目、青岛市民生科技计划项目及企业横向等课题20余项,申请专利53件,授权37件。已在Biotechnology Advances, Biosensor and Bioelectronics, Green Chemistry, mBIO, Environmental Microbiology, Applied and Environmental Microbiology等国内外期刊共发表论文72篇,其中SCI收录63篇。担任Microbial Cell Factories期刊副主编。获省部级科技奖项1项(排名第2),获山东省教育厅自然科学科技进步一等奖1项(排名第1),获青岛市自然科学奖二等奖1项(排名第1),发布山东省地方行业标准2项。曾获“山东省优秀研究生指导教师”、青岛农业大学“最美教师”等荣誉称号。

周雍进 研究员
周雍进,博士,研究员,博士生导师,中国科学院大连化学物理研究所合成微生物学研究组组长,国家自然科学基金委杰出青年基金、张大煜优秀学者、国家自然科学基金委优秀青年基金项目获得者、国家引进人才青年项目入选者、中国科学院引进人才、Green Carbon青年编委。曾于江南大学获得食品科学与工程学士学位(2006);天津大学获得生物化工硕士学位(2008);大连化学物理研究所获得生物化工博士学位(2012);2012-2016年在瑞典查尔姆斯理工大学从事博士后研究。2017年1月回到中国科学院大连化物所组建合成生物学与生物催化课题创新特区研究组,受聘为课题组长,研究组于2022年1月进入正式研究组序列,更名为“合成微生物学研究组”。曾在Cell、Nature Energy、Nature Metabolism、Nature Chemical Biology、Nature Communications、JACS、PNAS等期刊发表论文100余篇,被引用6300余次。曾获得2015年度中国药学会科学技术奖一等奖,2016年国际代谢科学会议青年科学家奖,2018年‘伦世仪’基金会杰出青年学者奖,2019年全国生物技术创新大会“最具发展潜力奖”。目前担任Biotechnology Journal主编,Synthetic and Systems Biotechnology,BioDesign Research副主编,FEMS Yeast Research等多个学术期刊编委。
05 Green Carbon
期刊官网:Green Carbon官网
投稿网址:Green Carbon投稿
公众号:Green Carbon公众号

https://blog.sciencenet.cn/blog-3620330-1509349.html
上一篇:Green Carbon绿碳文章 │ 东北师范大学常进法和邢子豪、劳伦斯伯克利国家实验室王冠芝:六价铱提高析氧性能
下一篇:Green Carbon│意大利佩鲁贾大学Castellani副教授:置换法实现天然气水合物开发协同二氧化碳海底封存