博文
阿尔茨海默病的突破性进展:脂肪代谢是新疗法的关键  精选
精选
||
阿尔茨海默病的突破性进展:脂肪代谢是新疗法的关键
诸平

Fig. 2 Professor Marcus Grimm. Credit: SRH Hochschule für Gesundheit
据德国萨尔大学(Saarland University / Universität des Saarlandes)2024年1月14日提供的消息,阿尔茨海默病的突破性进展:脂肪代谢是新疗法的关键(Alzheimer’s Breakthrough: Fat Metabolism Key to New Treatments)。
德国勒沃库森SRH应用健康科学大学莱茵兰校区(Rhineland Campus of SRH University of Applied Health Sciences in Leverkusen)和萨尔大学的马库斯·格林姆(Marcus Grimm)教授和托拜厄斯·哈特曼(Tobias Hartmann)教授最近的研究为阿尔茨海默病(Alzheimer’s disease)提供了新的见解,可能为创新治疗和预防方法铺平道路。
他们的研究强调了身体脂肪代谢的双向相互作用在阿尔茨海默氏症发展中的重要作用,此外,它强调了饮食和吸烟等生活方式因素的影响。研究小组将淀粉样前体蛋白(amyloid precursor protein)与脂肪代谢(fat metabolism)之间的联系发表在《细胞化学生物学》(Cell Chemical Biology)杂志网站——Valerie Christin Zimmer, Anna Andrea Lauer, Viola Haupenthal, Christoph Peter Stahlmann, Janine Mett, Sven Grösgen, Benjamin Hundsdörfer, Tatjana Rothhaar, Kristina Endres, Matthias Eckhardt, Tobias Hartmann, Heike Sabine Grimm, Marcus Otto Walter Grimm. A bidirectional link between sulfatide and Alzheimer’s disease. Cell Chemical Biology, 2023, DOI: 10.1016/j.chembiol.2023.10.021. Available online: 15 November 2023. https://doi.org/10.1016/j.chembiol.2023.10.021
参与此项研究的有来自德国萨尔大学(Saarland University, Homburg/Saar, Germany)、德国勒沃库森SRH应用健康科学大学(SRH University of Applied Health Sciences, Leverkusen, Germany)、德国约翰内斯·古腾堡大学医学中心(University Medical Center Johannes Gutenberg-University, Mainz, Germany)以及德国波恩大学(University of Bonn, Bonn, Germany)的研究人员。
阿尔茨海默病(Alzheimer’s disease)是最常见的痴呆症之一,影响着全世界数百万人。阿尔茨海默氏症患者随着病情的发展,记忆力减退、定向障碍、语言障碍、思维混乱等症状也会逐渐加重。这种疾病会导致大脑中的神经细胞受损和死亡,目前是无法治愈的。
随着疾病的发展,人体细胞内发生了无数的生化过程,其中包括高度复杂的指令和信号序列。世界各地的科学家目前都在研究这些复杂的神经通路。了解阿尔茨海默氏症发展时身体发生了什么,就有机会进行干预,减缓或理想地停止相关过程。
淀粉样-β蛋白在老年痴呆症中的作用(Amyloid-Beta Protein’s Role in Alzheimer’s)
在阿尔茨海默病中起关键作用的蛋白质是淀粉样-β肽(amyloid-beta peptide)。在一个健康的人体内,这些蛋白质可以被简单地分解。但是,在老年痴呆症患者中,它们聚集在一起形成斑块,沉积在大脑神经细胞之间。
这种小的淀粉样-β蛋白(amyloid-beta protein)以硬化斑块的形式在患者的大脑中积累。营养专家马库斯·格林姆教授解释说,淀粉样-β蛋白是阿尔茨海默氏症发展的关键因素,导致神经变性。马库斯·格林姆教授在德国勒沃库森的SRH应用健康科学大学莱茵兰校区(Rhineland Campus of the SRH University of Applied Health Sciences in Leverkusen)和萨尔大学任教和研究,在那里他与位于萨尔州洪堡的萨尔大学医学院的德国痴呆症预防研究所(German Institute for Dementia Prevention)所长托拜厄斯· 哈特曼教授密切合作。马库斯·格林姆是洪堡研究所分子和细胞生物学研究实验室的负责人。
老年痴呆症与饮食的关系(The Connection Between Alzheimer’s and Diet)
托拜厄斯· 哈特曼教授和马库斯·格林姆教授长期以来一直在研究阿尔茨海默病和饮食之间的联系,他们的研究小组现在发现了支持这种联系的新证据。研究小组成功地发现了导致阿尔茨海默氏症的人体脂肪代谢过程中一个此前未知的机制。
他们发现淀粉样-β蛋白的产生影响某些脂肪的合成,特别是一类被称为硫脂类(sulfatides)的脂质,相反,硫脂类的数量调节淀粉样-β蛋白的数量。这种双向相互作用在阿尔茨海默氏症的研究中具有潜在的重要意义,因为已知阿尔茨海默氏症患者的大脑中硫酯类含量减少而淀粉样-β蛋白含量升高。
研究结果及启示(The Study’s Findings and Implications)
我们的研究已经确定了淀粉样前体蛋白(amyloid precursor protein简称APP)如何加工的一个以前未知的生理方面,这是重要的,因为APP在调节大脑中脂质代谢,特别是硫脂类的代谢中起着关键作用。SRH应用健康科学大学负责营养治疗和营养咨询学士学位课程和医学营养科学和营养治疗硕士学位课程的马库斯·格林姆解释说:“硫脂类是一种存在于我们吃的食物中的特殊脂肪,但它也可以由身体自身产生。”
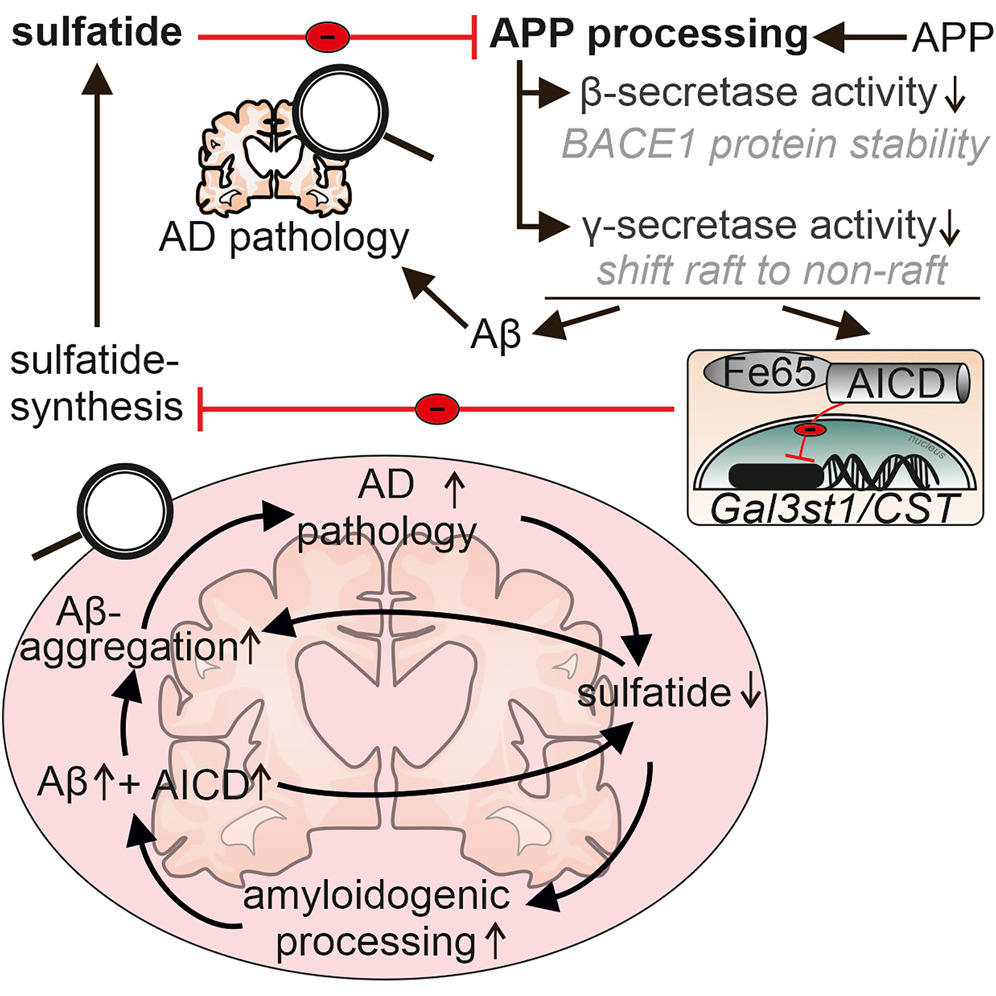
马库斯·格林姆说:“我们已经能够通过实验证明淀粉样-β蛋白的产生会影响硫脂类的数量,反之亦然。我们的研究结果表明,前体蛋白的裂解产生淀粉样-β蛋白也导致另一种称为AICD的蛋白质片段的释放。AICD反过来抑制Gal3st1/CST酶的表达,而Gal3st1/CST酶在人体自身的硫脂类合成中起着核心作用。”这解释了阿尔茨海默病患者细胞中发生的复杂代谢过程。
研究人员特别感兴趣的是饮食和生活方式对这种疾病的影响。吸烟等因素会对硫脂类水平产生负面影响,而确保身体有足够的维生素K供应或食用某些类型的海鲜则会产生积极影响。实验神经学教授托拜厄斯•哈特曼表示:“这些研究结果为阿尔茨海默病的预防和治疗策略的开发提供了可能的途径。”
“我们的研究强调了一个完整的生化回路的重要性,它调节着硫脂类物质的体内平衡和淀粉样-β蛋白的产生,并表明这种调节回路在阿尔茨海默病患者中被破坏。”这项研究对阿尔茨海默氏症的生理过程提供了新的见解,可能会为治疗这种疾病开辟新的途径。
这项研究由德国MWG莱茵兰-普法尔茨 (MWG Rhineland-Palatinate, Germany)、NeurodegX、欧洲委员会(European Commission under the framework programme of the European Union grant agreement no. 211696)、欧盟联合计划神经退行性疾病研究(EU Joint Programme – Neurodegenerative Disease Research简称JPND)以及德国联邦教育与研究部{BMBF grants Multi-MeMo (01ED2306) and EURO-FINGERS (01ED2003) }的资助。
上述介绍,仅供参考。欲了解更多信息,敬请注意浏览原文或者相关报道。
Reduced sulfatide level is found in Alzheimer’s disease (AD) patients. Here, we demonstrate that amyloid precursor protein (APP) processing regulates sulfatide synthesis and vice versa. Different cell culture models and transgenic mice models devoid of APP processing or in particular the APP intracellular domain (AICD) reveal that AICD decreases Gal3st1/CST expression and subsequently sulfatide synthesis. In return, sulfatide supplementation decreases Aβ generation by reducing β-secretase (BACE1) and γ-secretase processing of APP. Increased BACE1 lysosomal degradation leads to reduced BACE1 protein level in endosomes. Reduced γ-secretase activity is caused by a direct effect on γ-secretase activity and reduced amounts of γ-secretase components in lipid rafts. Similar changes were observed by analyzing cells and mice brain samples deficient of arylsulfatase A responsible for sulfatide degradation or knocked down in Gal3st1/CST. In line with these findings, addition of sulfatides to brain homogenates of AD patients resulted in reduced γ-secretase activity. Human brain APP level shows a significant negative correlation with GAL3ST1/CST expression underlining the in vivo relevance of sulfatide homeostasis in AD.
https://blog.sciencenet.cn/blog-212210-1418073.html
上一篇:[转载]我是这样证明√2不是有理数的
下一篇:打破物理学:对宇宙缺失碎片的激进探索