博文
《自然—结构与分子生物学》:周丛照/张余合作揭示双转录因子协同调控蓝藻硝酸盐同化通路转录激活的分子机制
||
中国科学技术大学周丛照研究组与中国科学院分子植物科学卓越创新中心/植物生理生态研究所张余研究组通过冷冻电镜单颗粒技术解析了鱼腥蓝细菌 Anabaena sp. PCC 7120转录激活复合物NtcA-TAC以及NtcA-NtcB-TAC的三维结构,揭示了双转录因子NtcA和NtcB协同激活转录的分子机制。
北京时间2024年1月4日18时,该研究成果以“DNA looping mediates cooperative transcription activation”为题在线发表在Nature Structural & Molecular Biology上。

基因转录是中心法则的核心环节,是遗传信息精准传递的基本条件,也是维持有序生命活动的关键。基因转录的精细调控对于生物适应不同环境是必需的,也是细菌应对环境压力的重要手段。蓝细菌是地球上最古老的光合自养生物,是地球早期大气中氧气的主要来源。同时蓝细菌能利用各种形式的无机氮源,以氨盐作为优先利用的氮源;当环境中氨盐不足时,蓝细菌会激活相应的同化通路以利用其他形式的氮源。例如,蓝细菌可以利用硝酸盐同化通路将硝酸盐从胞外转运到胞内并还原成可直接供菌体利用的氨盐。研究表明,硝酸盐同化通路相关基因(nirA operon)的激活受到转录因子NtcA和NtcB的协同调控。
NtcA是蓝藻的全局性调控因子,属于CRP/FNR家族转录因子,可以响应氮缺乏信号2-oxoglutarate (2-OG)的积累而调控与氮代谢相关的基因。NtcB属于LysR家族转录因子(LysR-type transcriptional regulator, LTTR),是原核生物中最大且分布最广泛的转录因子家族之一,能够调控细菌内多种代谢过程,包括细胞分裂、群体感应、细胞毒性及运动性、氮固定、氧化应激反应、细胞黏连及蛋白分泌等。尽管单个转录因子对转录调控的功能和机制已被深入研究,但多转录因子协同转录调控的分子机制尚不明确。
在周丛照教授、张余研究员和江永亮副教授的指导下,博士研究生韩书婧等通过大量实验,成功表达和纯化了鱼腥蓝细菌RNA聚合酶全酶、NtcA和NtcB,并与优化后的硝酸盐同化通路启动子区域的双链DNA骨架(PnirA)成功组装,得到稳定的转录激活复合物(TAC)。作者通过体外转录(图1)和分子信标实验证实NtcA和NtcB的具有协同激活转录能力。随后作者通过不断优化冷冻制样条件,获得状态均一稳定的冷冻电镜样品,通过单颗粒技术解析了分辨率分别为3.6 Å和4.5 Å的两个转录激活复合物NtcA-TAC和NtcA-NtcB-TAC的三维结构。
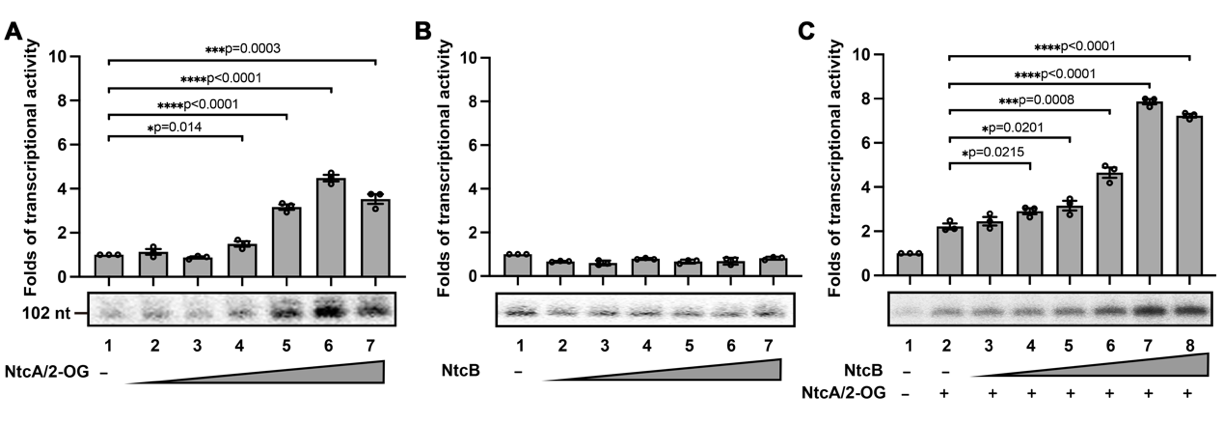
图1:NtcA和NtcB协同激活nirA operon的转录
生化和结构分析表明,NtcA首先结合到启动子DNA上,与RNA聚合酶直接互作,诱导启动子DNA发生弯曲。这种弯曲促使上游的NtcB的DNA结合位点更加接近RNA聚合酶,使得RNA聚合酶的αNTD结构域与NtcB的效应分子结合结构域EBD发生相互作用,进一步稳定转录激活复合物。通过DNA环折(DNA looping)的方式,NtcA和NtcB相继结合并诱导上游启动子DNA发生大幅度弯曲,最终形成完全激活的转录复合物。
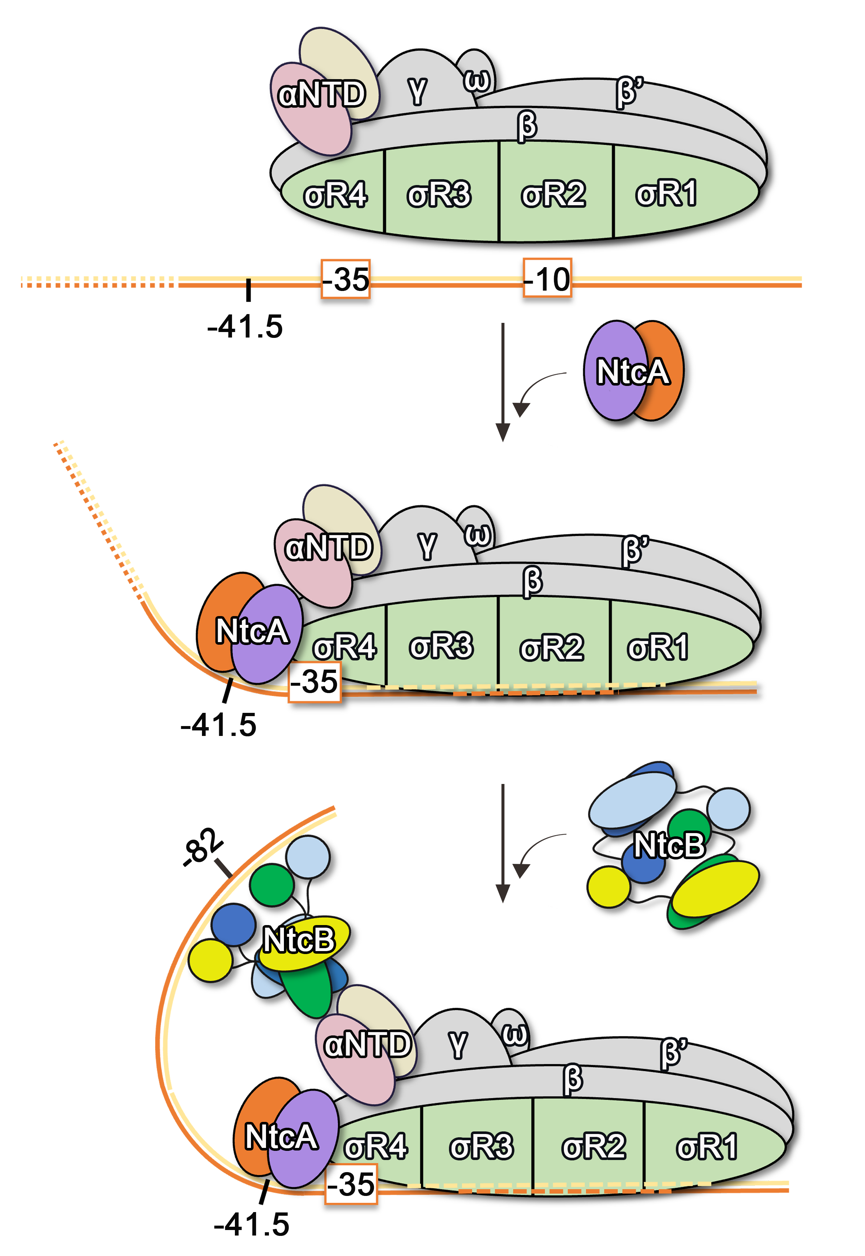
图2:“DNA环折”机制模式图
该研究首次阐明双转录因子协同调控转录激活的分子机制,进一步加深了我们对细菌基因转录及其调控的认识,为这一类广泛存在原核和真核生物中的多转录因子协同调控转录的研究提供了新的范式。
相关论文信息:
https://www.nature.com/articles/s41594-023-01149-7
https://blog.sciencenet.cn/blog-3423233-1416775.html
上一篇:《自然—结构与分子生物学》:许代超团队揭示衰老引起细胞稳态水平降低的分子机制
下一篇:《自然—结构与分子生物学》:清华大学陈柱成团队阐明染色质重塑复合物滑动核小体关闭启动子的机理