博文
[转载]hLife:中国科学院钟劲团队揭示O-GlcNAc糖基化调控外泌体释放新机制
||
外泌体(Exosomes)是细胞间传递信息的重要载体,在肿瘤发生发展、免疫调控以及病毒感染等过程中发挥关键作用。然而,对于外泌体从细胞内产生、运输到最终释放,这一系列过程究竟如何被调控,目前认识仍然理解有限。
近日,中国科学院上海药物研究所钟劲研究团队在hLife中发表题为"Hexosamine biosynthetic pathway regulates exosome secretion by promoting O-GlcNAcylation of SNAP25"的研究论文。该研究揭示了细胞糖代谢旁路——己糖胺生物合成通路(HBP)可以通过促进SNAP25蛋白的O-GlcNAc糖基化,从而增强SNARE复合体的装配效率,推动外泌体向细胞外释放。这一发现为理解肿瘤细胞外泌体高分泌背后的代谢基础提供了重要线索(图1)。
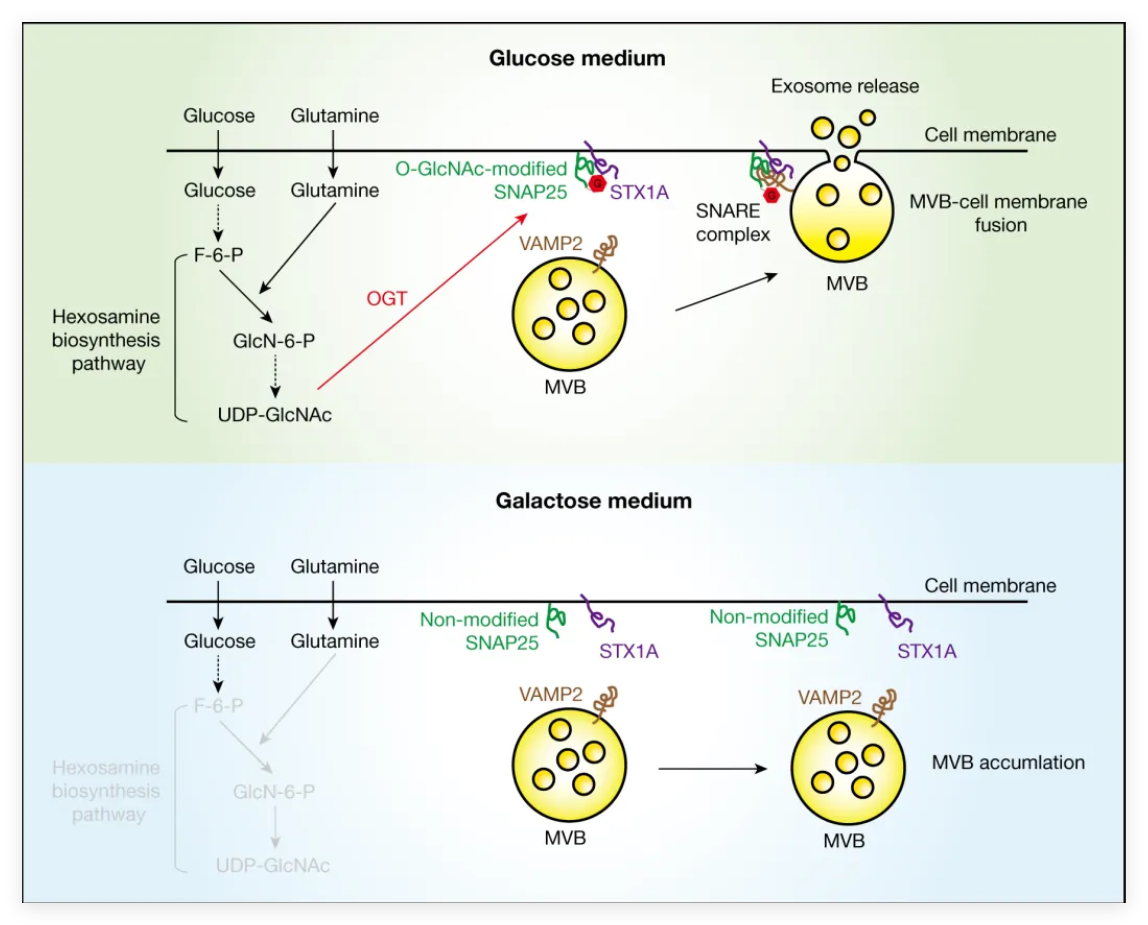
HBP通过调节SNAP25的O-GlcNAc糖基化修饰调控外泌体释放的示意图
肿瘤细胞普遍代谢旺盛,同时表现出更强的外泌体分泌能力,这是一个众所周知但尚未被系统解释的现象。该研究发现使用半乳糖替代葡萄糖进行细胞培养时,糖酵解被显著抑制,外泌体释放量也明显下降;而降低葡萄糖浓度或使用2-DG抑制糖酵解也产生相同结果。团队通过实验发现,使用半乳糖替代葡萄糖进行肝癌细胞系Huh7细胞培养时,这一现象不仅出现在肝癌细胞Huh7中,在胚胎肾细胞系HEK293T、肺腺癌细胞系A549等细胞模型中均可观察到,说明糖代谢水平本身对外泌体释放具有普遍性调控作用。
接下来,为了探究糖代谢是通过什么途径影响这一过程的,研究人员关注到了细胞糖代谢旁路——己糖胺生物合成通路。该通路将糖代谢中间产物转化为UDP-GlcNAc,为细胞提供蛋白O-GlcNAc糖基化修饰的底物。实验显示,无论是敲低HBP限速酶GFPT1、抑制O-GlcNAc转移酶OGT,还是去除培养基中的谷氨酰胺,都能够降低细胞整体的O-GlcNAc水平,并导致外泌体释放量下降;而提升O-GlcNAc水平则可以部分恢复外泌体分泌能力。由此,研究明确了HBP及O-GlcNAc修饰在外泌体分泌调控中的关键作用(图2)。
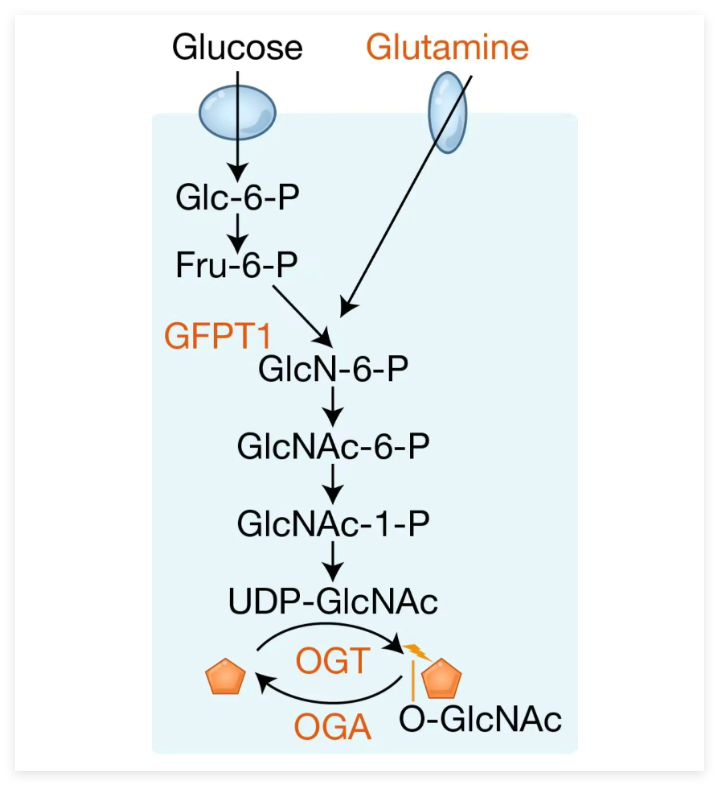
HBP通路及其关键调控因素
进一步分析显示,这种调控并非发生在外泌体生成最早的阶段,因为细胞内多泡体(MVB)形成及内涵体内泡(ILV)数量并未明显减少。相反,研究人员观察到多泡体更容易堆积在细胞核周围区域,并表现出运动性下降,提示问题可能出现在“多泡体的运输及膜融合”环节。
在具体靶蛋白筛查中,研究人员重点关注了已知参与囊泡膜融合的SNARE复合体。实验发现,作为SNARE核心成员之一的SNAP25随着葡萄糖浓度升高,其O-GlcNAc修饰水平明显增加;而提升SNAP25的糖基化会增强其与STX1A、VAMP2等SNARE蛋白的相互作用,促进SNARE复合体的装配效率,最终推动多泡体与质膜更顺利的融合,从而促进外泌体的释放。
这一研究不仅解释了为何肿瘤细胞在高代谢状态下表现出更强的外泌体释放能力,也为理解肿瘤微环境调控等提供了新的研究视角。未来,围绕HBP及O-GlcNAc糖基化修饰的更多关键节点有望成为新的调控靶标,为干预肿瘤生长和细胞通讯提供新的策略。
原文链接:https://www.sciencedirect.com/science/article/pii/S2949928325001129
作者简介
杨乾坤 博士 第一作者
机构:中国科学院上海药物研究所(原中国科学院上海免疫与感染研究所)
研究方向:细胞外泌体释放的调控机制探究
邢一帆 博士 第一作者
机构:中国科学院上海药物研究所(原中国科学院上海免疫与感染研究所)
研究方向:病毒感染的细胞生物学和细胞内囊泡运输
钟劲 研究员 通讯作者
机构:中国科学院上海药物研究所(原中国科学院上海免疫与感染研究所)
研究方向:RNA病毒的分子病毒学、病毒宿主相互作用
参考文献:Yang Q, Xing Y, Tian F, et al. Hexosamine biosynthetic pathway regulates exosome secretion by promoting O-GlcNAcylation of SNAP25. hLife 2025. https://doi.org/10.1016/j.hlife.2025.11.002
https://blog.sciencenet.cn/blog-446272-1516524.html
上一篇:Gut :重庆医科大学发现克服MASH相关肝癌免疫治疗耐药的新策略
下一篇:Gut:郝继辉/刘静团队揭示KRAS突变驱动CLDN18.2 O-GlcNAc糖基化修饰调控胰腺癌进展及耐药的新机制
