博文
氢气一氧化碳等气体治疗肝硬化综述
||
氢气等气体治疗肝硬化综述
研究亮点
- 肝纤维化治疗迫切需要创新策略与全新方法。
- 医用气体天然具备多靶点协同治疗效应。
- 需要先进递送系统与载体实现剂量可控与靶向递送。
- 本文综述医用气体治疗肝纤维化的研究现状。
摘要
肝纤维化是全球性重大健康问题,由肝脏持续性损伤引发,以肝脏进行性损害为特征。由于纤维化难以逆转,且常与复杂慢性肝损伤相伴,肝纤维化治疗面临巨大挑战。近年来,医用气体疗法成为治疗肝纤维化的新兴方向。主要涉及气体包括:一氧化碳(CO)、氢气(H₂)、一氧化氮(NO)、硫化氢(H₂S)、二氧化硫(SO₂)和氧气(O₂)。其中多种气体属于内源性气体信号分子,可天然参与已知细胞信号通路,具备治疗应用潜力。
这类气体的核心治疗优势在于改善肝纤维化关键病理特征:发挥抗氧化、抗炎作用,抑制肝星状细胞(HSC)活化与细胞因子产生,清除活性氧(ROS),阻止肝细胞凋亡。基于医用气体的独特优势,本文综述当前研究进展,探讨分子供体、纳米递送系统等先进递送方式,以提升气体疗法治疗肝纤维化的靶向性。
---
1 引言
1.1 肝纤维化的全球疾病负担
肝纤维化由慢性肝病引发,具有动态变化特征,在进一步进展前存在潜在可逆性。其病因包括慢性病毒性肝炎(乙肝、丙肝)、酒精性肝病(ALD)、代谢功能障碍相关脂肪性肝病(MASLD)、自身免疫性肝炎或胆汁淤积性损伤。活化肝星状细胞(HSCs)引起的慢性持续性炎症损伤,是肝纤维化进展的核心环节。活化后的HSCs脱离静息状态,转化为收缩型肌成纤维样细胞,数量增多并分泌细胞外基质(ECM)蛋白。活化巨噬细胞与受损肝细胞也会释放信号,促进ECM沉积与纤维化进程。过量ECM沉积导致纤维组织增生,破坏肝脏结构、改变血流、降低代谢功能。交联胶原蛋白还会形成支架,进一步促进HSC活化。失控的炎症与纤维化最终可进展为肝硬化,显著增加肝衰竭、肝细胞癌和门静脉高压血管并发症风险。进展至晚期纤维化与肝硬化还会引发明显血管改变、再生结节形成与门静脉高压。
当前肝纤维化治疗以阻断HSC活化与ECM沉积循环为主,仅能延缓疾病进展,凸显出研发针对纤维化核心机制的新型疗法的迫切需求。尽管针对病因(如病毒性肝炎)的治疗可部分逆转或延缓纤维化,但目前可直接抑制纤维化进程的药物极少。因此,肝纤维化新疗法研究重点聚焦于阻断瘢痕组织形成机制。
近年来,靶向TGF-β信号通路、LOXL2酶活性及HSC特异性递送抗纤维化药物等策略取得阶段性突破;部分小分子抑制剂与单抗已在临床前模型中显著减少胶原沉积并促进瘢痕降解;然而,如何实现病灶精准干预、避免系统性免疫抑制、维持长期抗纤维化效应,仍是转化落地的关键瓶颈。
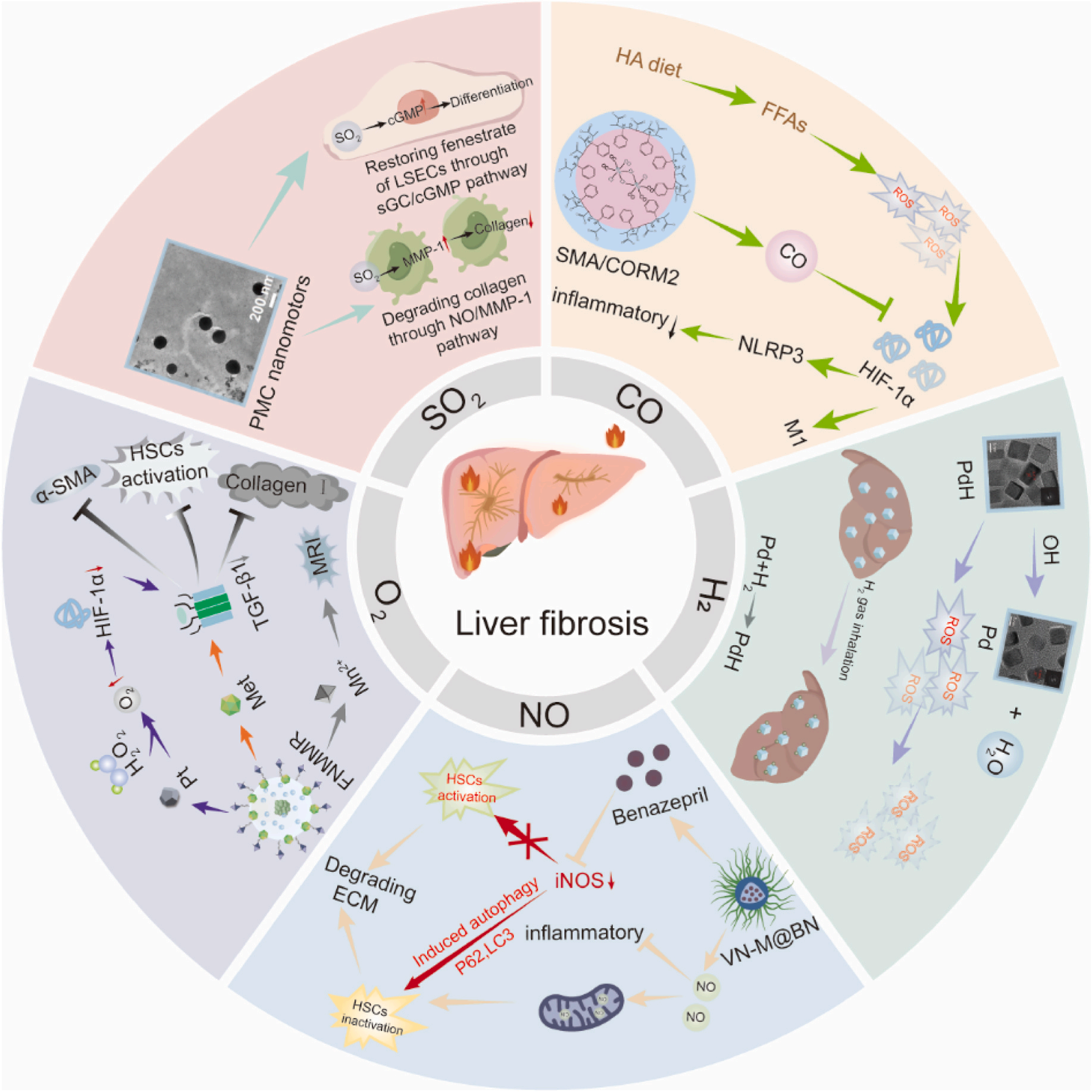
图1 医用气体疗法在肝纤维化中应用的示意图
1.2 肝纤维化现有治疗手段
目前临床对确诊肝纤维化患者采取多种干预措施。乙肝与丙肝患者首先进行病因治疗,针对乙肝使用替诺福韦等抗病毒药物,丙肝采用索磷布韦/维帕他韦等联合方案。抗病毒治疗通常需持续多年直至病毒载量检测不到,但纤维化改善效果存在个体差异,部分患者纤维化明显消退,部分仍持续进展。酒精性肝病患者的核心干预为戒酒,以尽可能改善肝功能与生存率,但目前尚无针对酒精性肝纤维化的特效药物。MASLD(尤其是非酒精性脂肪性肝炎NASH)相关肝纤维化已有获批药物Resmetirom,其为甲状腺激素受体β(THR-β)激动剂,可减少肝脏脂肪并改善纤维化。
临床已上市药物如SGLT2抑制剂、GLP‑1受体激动剂有望用于肝纤维化治疗,但多数仍处于临床试验阶段。总体而言,纤维化可进展为不可逆肝硬化,治疗选择极为有限。目前获批的抗纤维化药物仍十分稀缺,例如候选药物Selonsertib虽在体内实验效果显著,但Ⅲ期临床失败,无法有效缓解患者纤维化,可能与复杂纤维化微环境中的代偿机制有关。因此,扩充抗纤维化药物库、研发创新疗法至关重要。
1.3 医用气体疗法的兴起
医用气体疗法为肝纤维化靶向治疗提供了现代化方案,疗效前景良好。多项临床前与实验研究证实了气体的治疗特性。气体及其活性化合物可保护细胞、清除自由基、减轻炎症、抑制肝脏过度瘢痕形成。这些分子参与肝损伤修复机制与多条细胞信号通路。
低剂量一氧化碳(CO)可调控缺氧诱导因子‑1α(HIF‑1α)发挥保护作用,动物实验中CO释放胶束可靶向纤维化炎症肝脏,减轻炎症与纤维化且无全身毒性。
氢气(H₂)作为选择性抗氧化剂,可清除羟基自由基、过氧亚硝酸盐等强氧化应激物质,用于肝纤维化可降低肝脏炎症、改善代谢调控、减少活化HSC内的ROS,安全性显著优于常规治疗药物。
一氧化氮(NO)在肝脏中作用复杂,高浓度促炎,精准递送则可减轻纤维化;靶向HSC的NO载纳米粒可抑制TGF‑β信号,降低纤维化基因表达;光控释放NO可减轻肝脏炎症与胶原合成。
硫化氢(H₂S)作为内源性气体信号分子,通过抑制α‑SMA表达、阻止静息细胞向肌成纤维细胞转化,发挥强抗纤维化能力;肝损伤时H₂S代谢异常提示外源性H₂S供体具有治疗潜力。
二氧化硫(SO₂)虽被视为污染物,但也是内源性气体信号分子,可抑制HSC活化与胶原沉积。先进载体设计可显著提升这类气体的安全性与有效性,纳米载体可实现可控靶向释放,降低气体暴露。纳米医学与医用气体疗法结合,提升了稳定性、靶向性与给药精准度,向临床应用迈出重要一步。
1.4 纳米技术在提升医用气体疗法中的作用
纳米技术支撑医用气体疗法发展,尤其实现了时空可控递送。医用气体普遍存在扩散快、靶向性差的问题,还面临各自挑战:CO存在毒性暴露风险,H₂溶解度低。NO半衰期极短(毫秒级)、递送非特异性,促使研究者开发pH、谷胱甘肽(GSH)等刺激响应型NO供体,或酶响应等生理条件激活的前药。NO活性高,易产生ROS/RNS造成正常细胞氧化损伤,因此递送系统研发尤为重要。纳米技术进一步优化NO供体,例如包载于PEG化脂质体中,可实现在肿瘤部位蓄积长达48小时,精准靶向递送,避免在健康组织中无效转运与提前释放。NO供体的释放也可通过多种刺激响应方式调控。
硫化氢(H₂S)可通过GYY4137、N‑乙酰半胱氨酸等外源性供体发挥治疗作用,纳米创新技术提升了H₂S的靶向与递送效果。例如临床可用H₂S供体茴三硫被载入磁性纳米脂质体,在外磁场与超声辅助下实现递送与释放。一氧化碳(CO)释放分子(CORMs)可包载于核壳纳米结构中,实现光控释放与叶酸靶向。包载CORMs的纳米系统包括胶束、树枝状大分子、金属有机框架、无机核壳结构。高浓度CO不当释放会结合血红蛋白降低氧运输,导致中毒;精准纳米制剂可通过控释、刺激响应、被动靶向与生物相容性提升,降低CO使用风险。纳米技术还可实现多气体联合治疗,如CO与NO共释放,实现靶点协同效应。
综上,纳米技术是克服医用气体传统局限的关键:半衰期短、溶解度低、缺乏靶向性。它通过保护气体不被降解、实现靶向递送、表面修饰、刺激响应控释、支持多气体/多药联合治疗,为气体疗法提供全新解决方案。
本文综述医用气体治疗肝纤维化的研究,重点阐述其抗纤维化分子机制:减轻氧化应激、抑制炎症级联反应、阻止肝细胞凋亡、直接抑制HSC活化;同时探讨临床转化挑战,尤其是气体释放化合物、纳米载体等新型递送策略在提升靶向性与剂量精准性方面的潜力。通过梳理当前实验与临床前研究,夯实医用气体疗法的科学基础,并展望其临床应用前景。
---
2 医用气体精准递送纳米医药用于肝纤维化强化治疗
医用气体疗法正成为替代传统药物的革新性手段。其所用CO、H₂、NO、H₂S、SO₂等内源性气体是关键信号分子,可自由跨生物膜扩散。这类气体通过多模式机制起效,同时靶向多条病理通路,发挥强效抗氧化、抗炎、抗纤维化、抗凋亡效应。
机制上,气体信号分子调控关键信号通路影响细胞功能:激活Nrf2抗氧化通路减轻氧化损伤,同时抑制NF‑κB驱动的炎症反应。核心抗纤维化机制为直接抑制HSC活化与增殖,阻止过量ECM形成。气体的内源性特性使其可精准靶向氧化应激、慢性炎症与纤维化核心驱动因素,使气体疗法成为治疗肝纤维化这类复杂多因素疾病的通用方案,疗效优于单靶点药物。
2.1 CO在肝纤维化中的治疗潜力
CO为无色无味气体,因结合血红蛋白干扰氧运输而具有毒性,但低剂量外源性CO具有强抗纤维化作用。代谢功能障碍相关脂肪性肝病(MAFLD)可从脂肪性肝炎进展为肝硬化、肝细胞癌,HIF‑1α信号通路是MAFLD进展的关键上游调控因子。
Cui等设计将CO释放分子CORM2包载于苯乙烯‑马来酸共聚物(SMA)中,形成聚合物胶束。SMA/CORM2胶束水溶性良好,无需外界激活即可缓慢释放CO。纳米载体使CORM2半衰期延长35倍,水溶性提升(>50 mg/mL),通过EPR效应在肝脏被动蓄积,实现48–72小时长效控释,保护CORM2不被提前降解并降低血液毒性。MAFLD饮食小鼠模型中,SMA/CORM2主要通过强效抑制HIF‑1α表达,显著改善肝脏脂肪变性,延缓MAFLD进展。CO还可通过激活整合应激反应诱导应激颗粒形成;2023年研究表明,CO依赖型锌指蛋白Tristetraprolin激活可降低应激颗粒内纤溶酶原激活物抑制剂‑1水平,有助于改善年龄相关NAFLD。因此,探索CO与肝纤维化相关分子通路的相互作用,可为NAFLD/MAFLD带来新治疗方案。
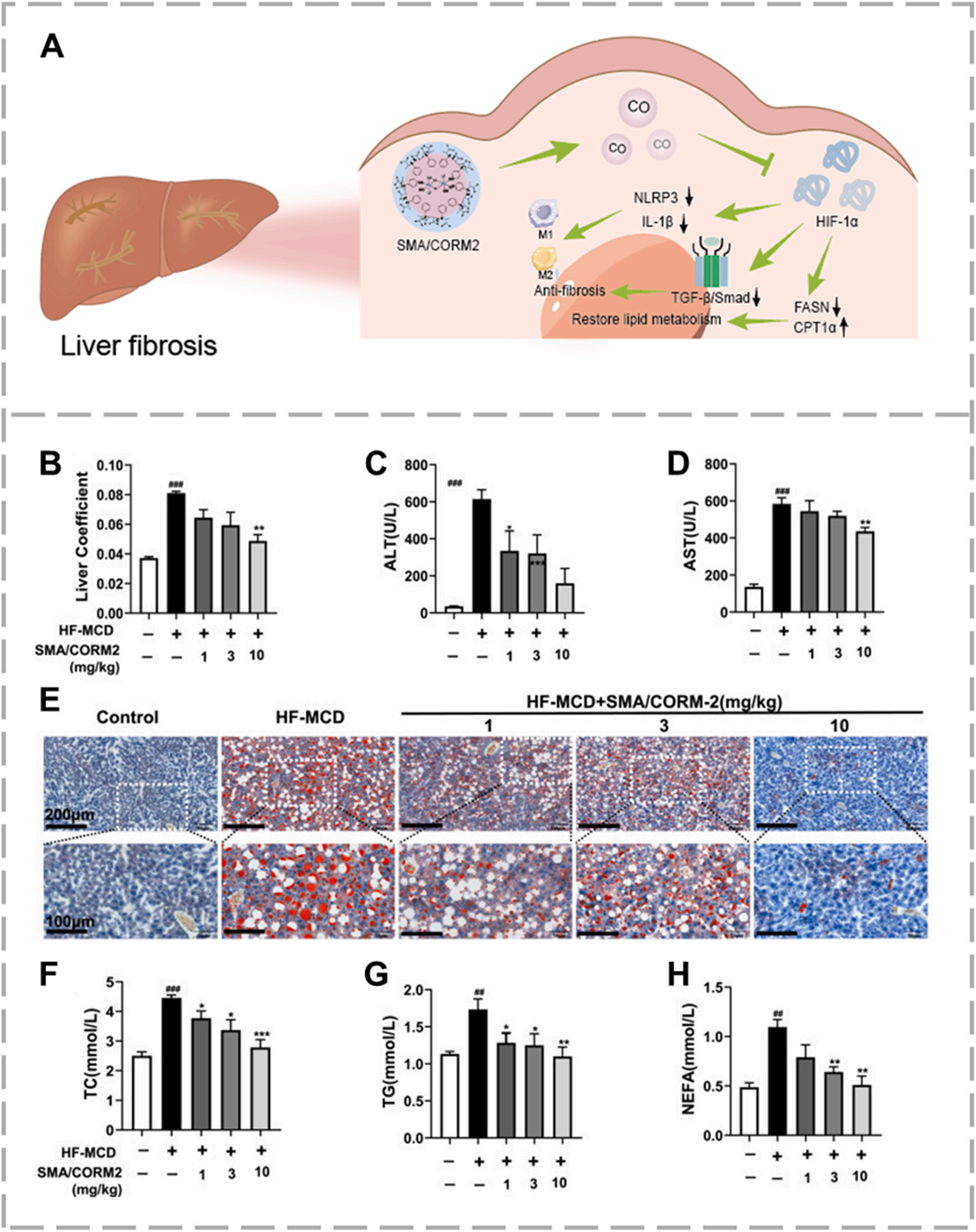
图2 SMA/CORM2胶束在MAFLD模型中的治疗效果评价
(A) 低剂量CO释放对肝纤维化发挥治疗作用;(B) 肝脏/体重比;(C、D) 肝损伤血清标志物;(E) 油红O染色肝脏组织切片(显示肝脂肪变性);(F‑H) 脂代谢相关指标。
2.2 氢气(H₂)在肝纤维化中的治疗潜力
氢气分子具有广谱抗炎与细胞保护作用,主要通过选择性清除毒性羟基自由基实现。其高生物安全性与治疗潜力已在肝炎等炎症相关疾病模型中得到证实。多项临床试验表明,饮用富氢水可改善慢性肝病患者的炎症与代谢紊乱。氢气吸入是另一种正在研究的慢性肝病给药途径。氢气的一大优势是,相比传统慢性肝病药物,它具有更高的安全性。
为提高治疗效果,靶向递送系统正在开发。Tao 等人提出一种策略:使用钯/氢化钯(PdH)纳米颗粒捕获吸入的氢气并以固态 PdH 形式储存,随后催化将毒性羟基自由基(•OH)还原为水。该钯系统不“携带”氢气,而是在吸入 4% 氢气时快速捕获流经肝脏的氢气,解决了氢气易扩散、溶解度极低(1.6 mg/L)的问题,避免了长时间、高浓度吸入的不可行性。钯系统通过形成 PdH 实现持续催化抗氧化,这是游离氢气难以做到的。
在非酒精性脂肪性肝炎(NASH)小鼠模型中,静脉注射钯纳米颗粒联合氢气吸入显著改善预后,对轻度和中度 NASH 均有预防和治疗效果。具体表现为:脂代谢改善(肝脏总胆固醇、甘油三酯降低)、肝酶(ALT、AST)下降、胶原沉积减少、血清炎症因子降低。该纳米平台在发挥作用后可被良好清除,注射谷胱甘肽可进一步加速清除(12 周后肝脏钯含量降至约 3%)。
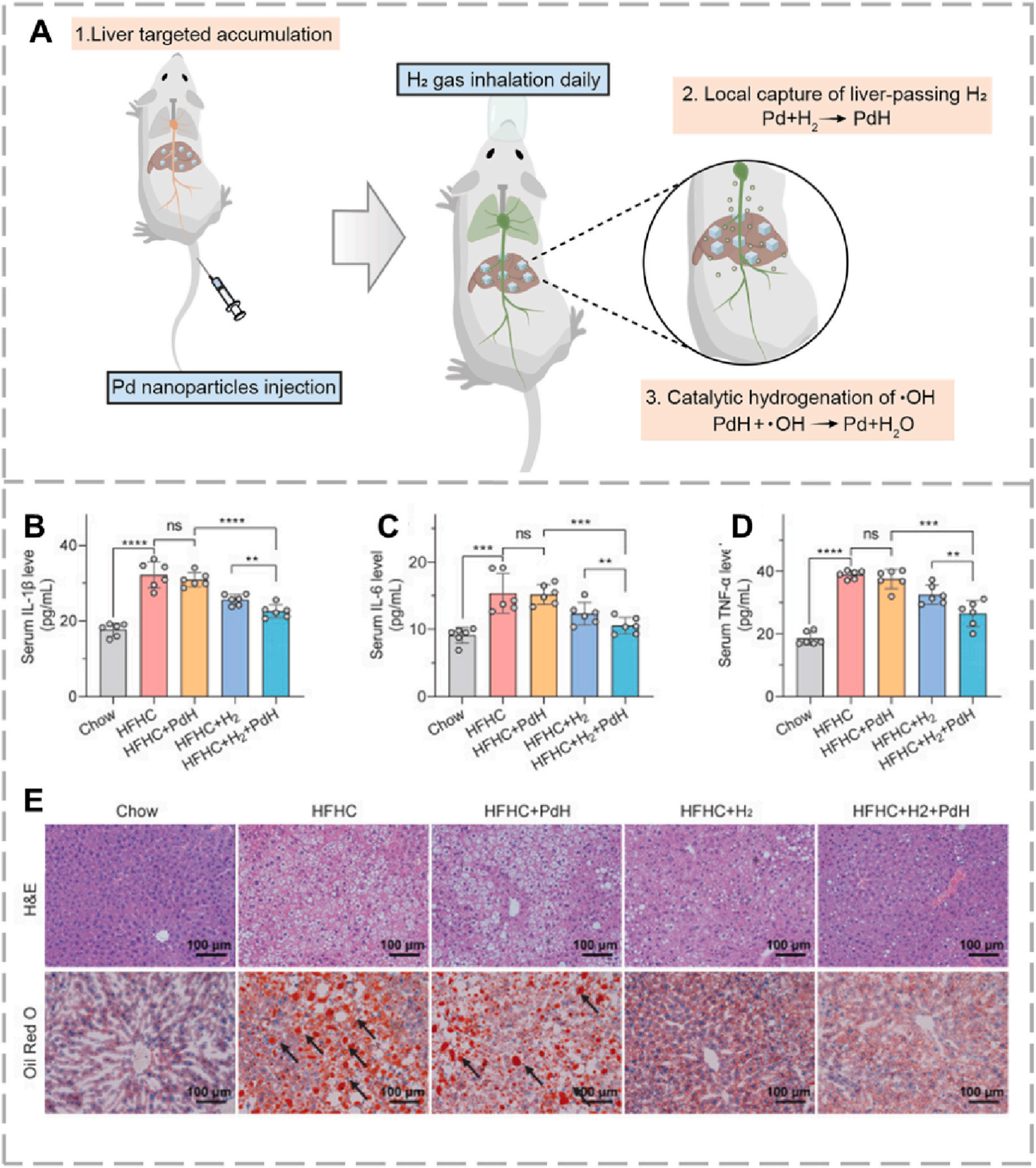
图 3. (A) 氧化应激、活性氧与促炎因子诱导纤维化,而氢气清除羟基自由基(•OH)恢复肝功能的示意图。(B–D) 血清 IL‑1β、IL‑6、TNF‑α 水平。(E) 肝脏 H&E 和油红 O 染色(标尺=100 μm)。氢气与 PdH+H₂ 处理减轻高脂高糖饮食诱导的脂肪变性与组织病理损伤。
此外,研究表明氢气可通过减轻氧化应激、上调肝脏 PPARα 和 PPARγ 改善非酒精性脂肪肝。富氢水还可通过不依赖 HO‑1/IL‑10 通路缓解细胞死亡、炎症和纤维化等核心肝病表型。这些发现说明氢气疗法的机制具有复杂性,为肝病治疗提供了新方向。
---
2.3 一氧化氮(NO)在肝纤维化中的治疗潜力
NO 是重要的气体信号分子,参与生理调控。其缺乏被认为是糖尿病、肝纤维化、心血管疾病、神经退行性疾病和部分肿瘤的诱因之一。内源性产生的 NO 可直接抑制肝星状细胞(HSC)活化,并降低其促存活自噬反应。
在健康肝细胞中,诱导型一氧化氮合酶(iNOS)以 L‑精氨酸为底物催化生成 NO,通过旁分泌减少内皮细胞诱导的 HSC 收缩,是重要的天然抗纤维化通路。由于 HSC 活化是肝纤维化的核心特征,NO 对活化 HSC 显著的促凋亡作用使其成为极具潜力的抗纤维化分子。
Liang 等人开发了靶向 HSC、近红外光控局部释放 NO 的纳米颗粒,在肝纤维化治疗中展现前景。2025 年,Yang 等人构建了维生素 A 修饰、载贝那普利(BN)的胶束(VN‑M@BN),由聚乙二醇‑聚碳酸硝酸酯共聚物自组装而成。维生素 A 配体可靶向 HSC 上的视黄醇结合蛋白受体;聚合物骨架中的聚碳酸硝酸酯结构可在谷胱甘肽(GSH)触发下靶向纤维化肝组织。该纳米胶束可在还原环境下48 小时长效可控释放 NO,而游离 NO 供体(硝酸酯)几分钟内就会过早释放。
在靶点部位,BN 阻断肾素‑血管紧张素‑醛固酮系统;释放的 NO 直接下调 α‑平滑肌肌动蛋白(α‑SMA),诱导活化 HSC 凋亡。结果显示 VN‑M@BN 在循环中稳定,可有效靶向纤维化肝组织,显著减少胶原沉积、延缓损伤肝脏的纤维化进程。这种精准递送至活化 HSC 的 NO 纳米疗法,在提高抗纤维化效果的同时降低了副作用。
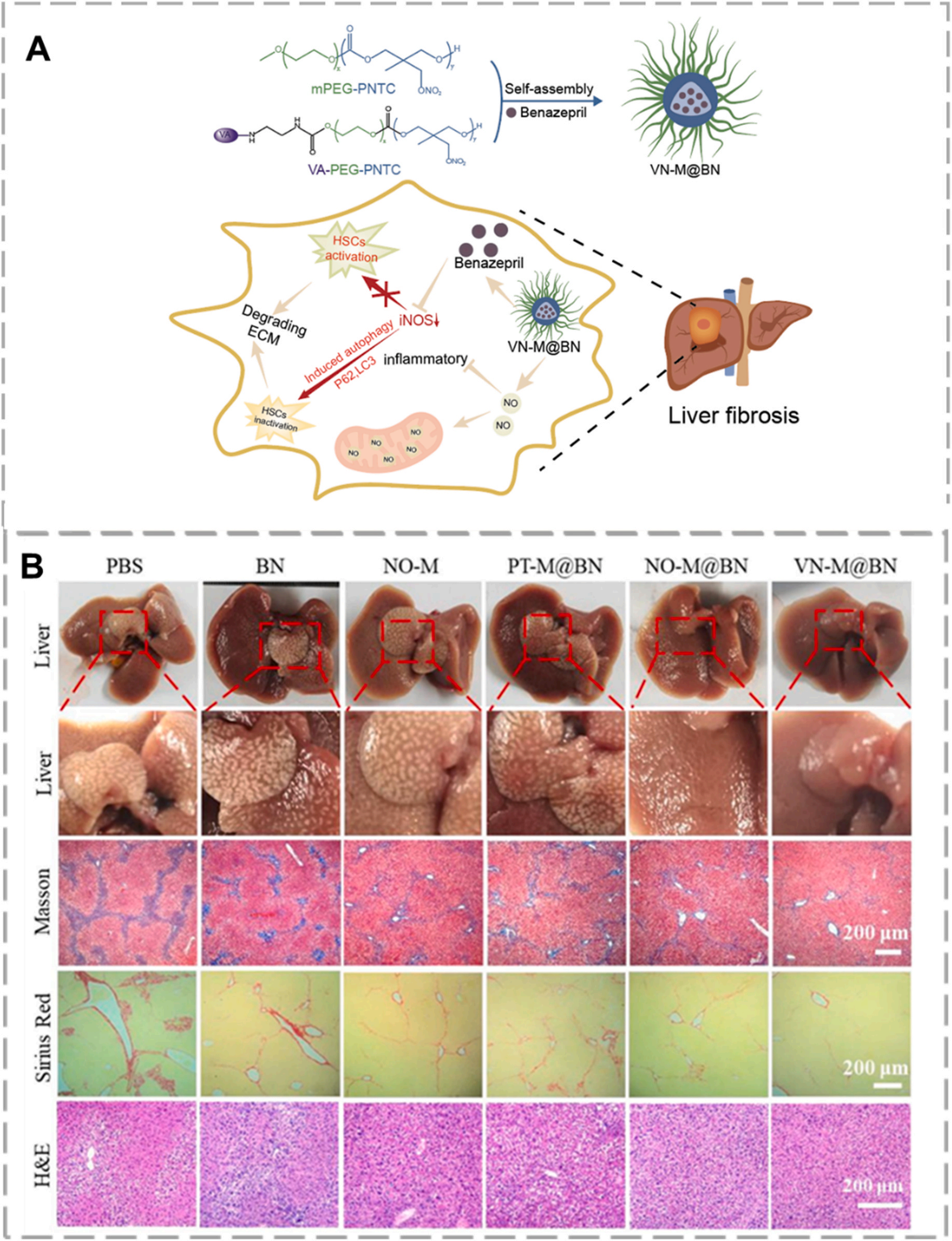
图 4. (A) NO 在肝纤维化中抗纤维化作用的示意图。(B) 肝脏组织照片及 Masson 三色、天狼星红、H&E 染色切片。
---
2.4 硫化氢(H₂S)在肝纤维化中的治疗潜力
H₂S 是内源性气体介质,其代谢紊乱参与纤维化疾病进程。研究证实,外源性补充 H₂S 供体具有抗纤维化作用,通过调控关键信号通路与离子通道抑制促纤维化过程。H₂S 在肝病中的重要性已得到广泛认可,但其确切细胞与分子机制尚未完全阐明。由于在多种生命活动中起关键作用,H₂S 被公认为基础气体信号分子。
烯丙基半胱氨酸(SAC)是大蒜提取物的主要成分,是一种明确的内源性 H₂S 供体。Gong 等人的研究显示,SAC(50 mg/kg/天)可显著缓解四氯化碳(CCl₄)诱导的大鼠肝纤维化,改善病理评分(H&E、油红 O、天狼星红)。机制上,SAC 降低肝脏 IL‑6、IFN‑γ、TNF‑α、TGF‑β 等炎症与纤维化关键因子的 mRNA 水平,同时提高超氧化物歧化酶、过氧化氢酶、谷胱甘肽过氧化物酶等抗氧化酶水平。
越来越多证据表明,人体内源性 H₂S 生成不足会促进纤维化;而补充 H₂S 可通过抗炎、抗氧化、抗纤维化作用,在多器官中抵抗纤维增殖性疾病。
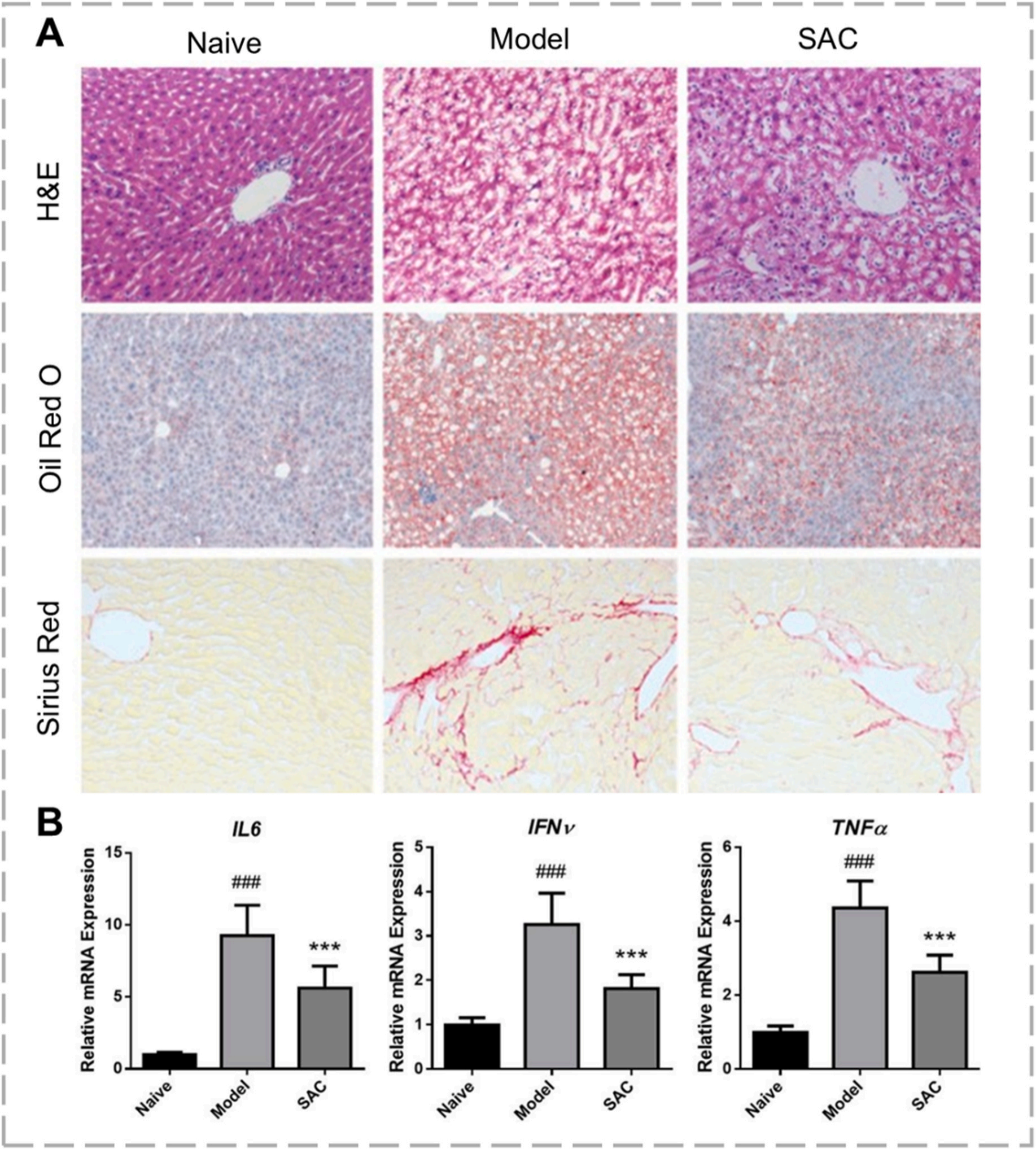
图 5. (A) SAC 处理缓解 CCl₄ 诱导的肝纤维化病理染色。(B) SAC 调控 IL‑6、IFN‑γ、TNF‑α 等炎症关键基因的表达。
---
2.5 二氧化硫(SO₂)在肝纤维化中的治疗潜力
SO₂ 是内源性气体信号分子,具有重要治疗潜力。在纤维化中,内源性 SO₂ 可抑制肝脏、肺等器官的纤维化重塑进程,减少 HSC 活化与胶原沉积。其保护机制包括:舒张血管、抑制 TGF‑β1/Smad 通路、减轻氧化应激与炎症,使其成为抗纤维化治疗的理想候选。
为提高 SO₂ 气体疗法效果,Chen 等人设计了肝损伤响应型 SO₂ 释放纳米马达。这些纳米马达带有 L‑半胱氨酸衍生物,可响应纤维化肝脏中半胱氨酸双加氧酶、天冬氨酸转氨酶的特异性酶浓度梯度,通过趋化作用增强药物在病灶的滞留。在纤维化区域经酶促催化释放 SO₂,进一步促进纳米马达滞留与肝损伤修复。
机制上,释放的 SO₂ 通过两条通路发挥作用:① 升高环磷酸鸟苷(cGMP),恢复肝窦内皮细胞(LSEC)正常形态;② 促进 NO 生成,激活基质金属蛋白酶‑1(MMP‑1)以降解胶原,穿透阻碍药物渗透的过度 ECM 屏障。体内实验证实纳米马达可有效滞留并显著逆转肝纤维化,纤维化区域从 5.1% 降至 0.9%。
目前内源性 SO₂ 与纤维化的研究较少,且多集中于心肌纤维化。阐明内源性 SO₂ 在纤维化中的生理作用与机制,将为心脏以外的器官带来重要治疗启示。后续研究有望揭示其在多器官系统中的抗纤维化潜力。
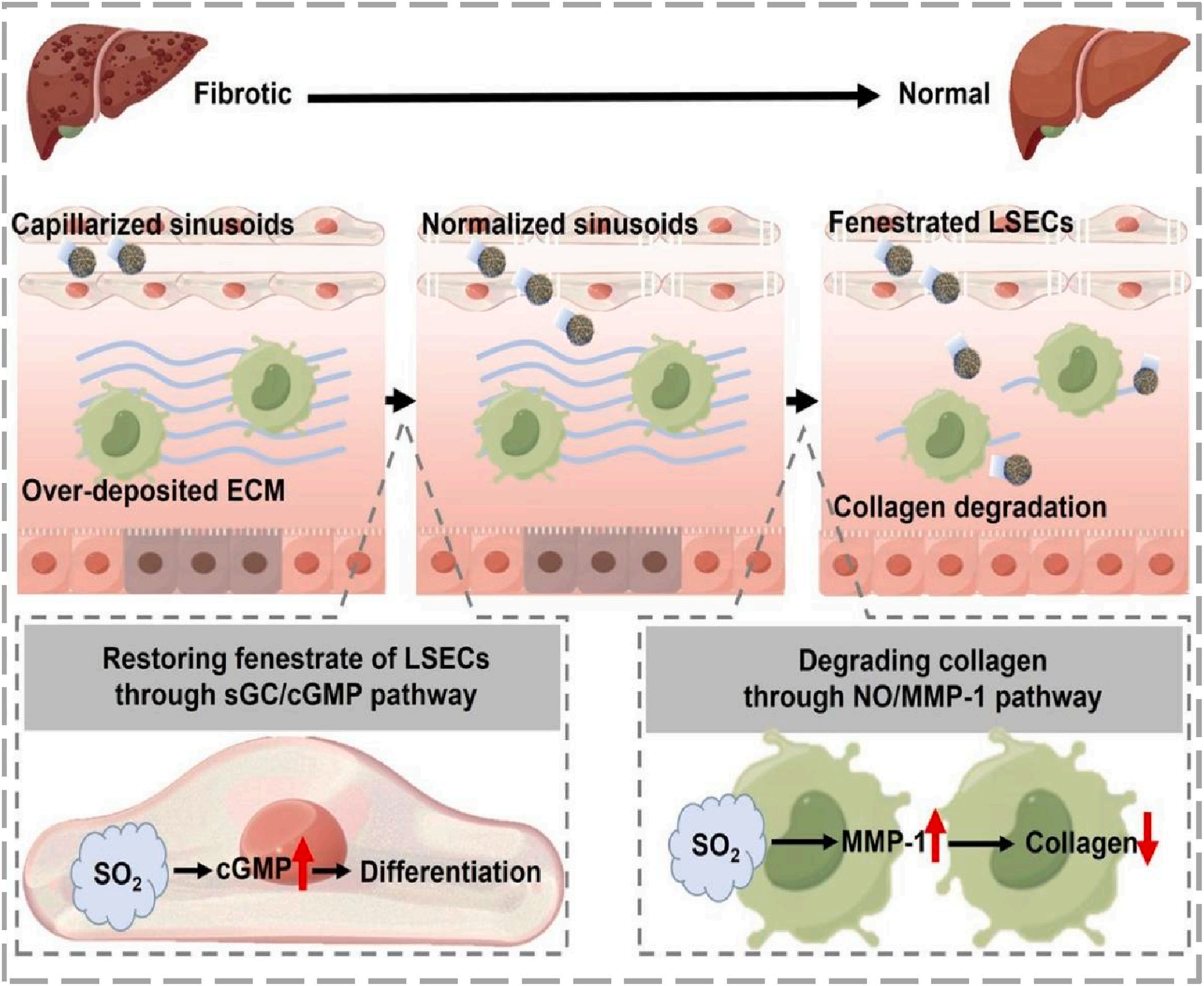
图 6. SO₂ 释放纳米马达的制备与抗纤维化治疗策略示意图。
---
2.6 氧气(O₂)在肝纤维化中的治疗潜力
氧气也通过创新策略用于肝纤维化治疗。研究利用靶向递送改善肝脏缺氧——缺氧是激活促瘢痕 HSC 的关键诱因,为阻断起始损伤、预防纤维化提供了新思路。
铁蛋白是内源性储铁蛋白,因其独特球形纳米笼结构与天然生物相容性,成为重要药物递送载体。Cui 等人构建了RGD 修饰、载二甲双胍的铁蛋白‑铂‑锰诊疗一体化纳米平台(FNMMR),用于肝纤维化的 MRI 成像与靶向治疗。该纳米笼具有类过氧化氢酶活性,可分解内源性过氧化氢(H₂O₂)产生氧气,改善缺氧微环境。
产氧可降低 HIF‑1α,进而抑制促纤维化 TGF‑β1/Smad 通路;共载的二甲双胍协同抑制同一通路,最终有效抑制 HSC 活化、显著减少胶原沉积。大量体内安全性评估(组织与血液分析)证实该平台生物相容性高、脱靶毒性低。
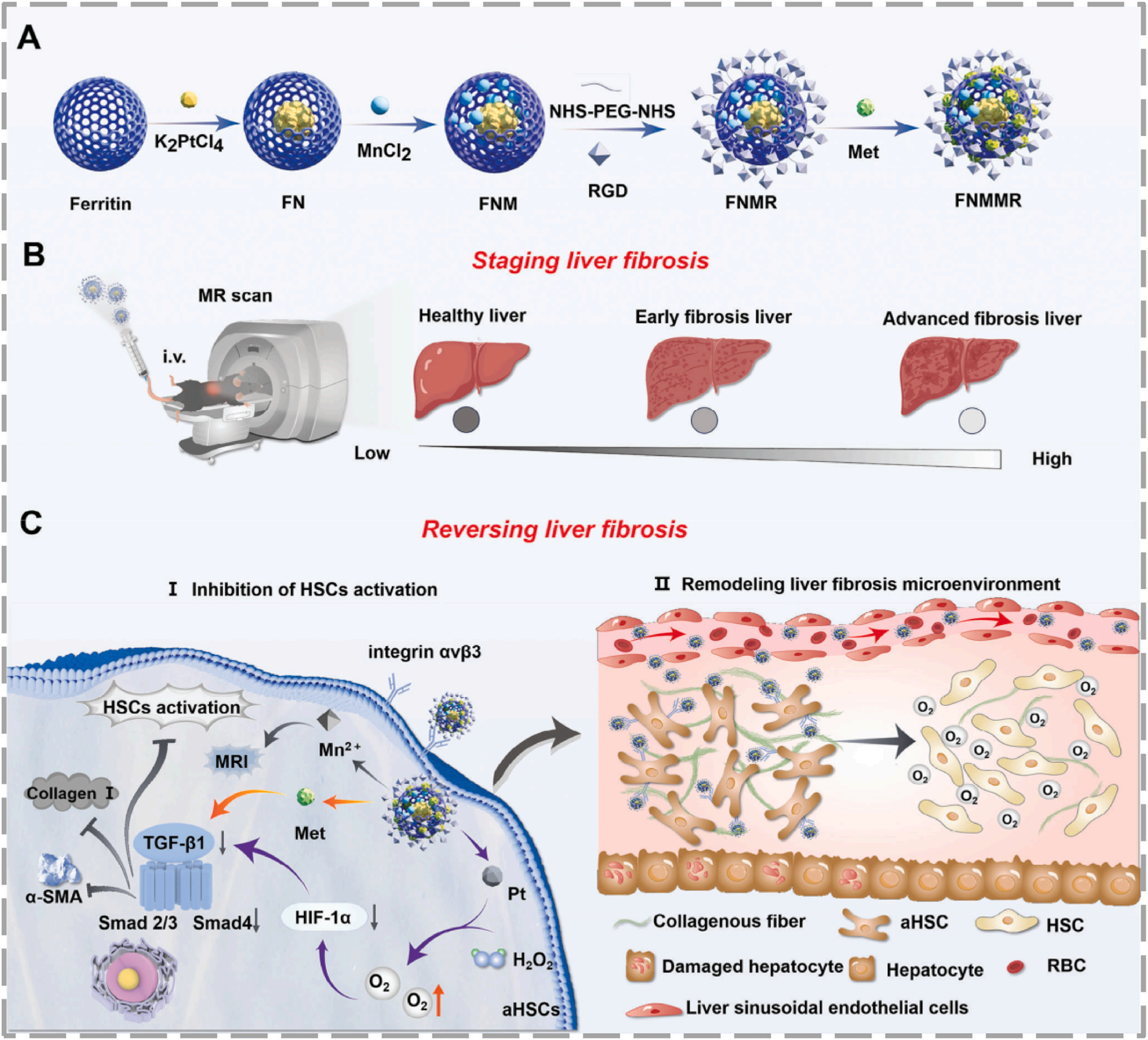
图 7. (A) FNMMR 的制备流程。(B) FNMMR 用于无创 MRI 同步评估肝纤维化分期与可视化的机制。(C) FNMMR 对纤维化组织的多靶点治疗作用示意图。
---
2.7 其他具有肝纤维化治疗潜力的气体
除 CO、NO、H₂、H₂S、SO₂、O₂ 外,更多气体的抗纤维化潜力正在被挖掘。研究较少的甲烷(CH₄)在实验模型中显示抗炎作用,特定条件下可延缓纤维化进展。尽管直接用于肝纤维化的研究不多,甲烷已在肝损伤中被广泛研究:富甲烷生理盐水可通过下调 TLR4/NF‑κB 通路与 NLRP3 活化,减轻小鼠肝脏炎症与纤维化;在脓毒症肝损伤中,同样通过该通路减轻炎症与氧化损伤;在 CCl₄ 肝损伤中也表现抗炎作用,提示无论损伤诱因如何,甲烷在损伤肝脏中均通过 NF‑κB 通路发挥作用。2026 年一篇肺纤维化研究使用甲烷前药 Fe(BPY)₂(CH₃)₂ 结合 PLGA‑PEG 共聚物,实现肺部可控释放甲烷,减轻炎症与纤维化。
与甲烷类似,氨(NH₃)在肝纤维化中作用复杂,但更多被视为疾病毒性产物,可用于靶向或清除。在非酒精性脂肪肝小鼠模型中,苯乙酸鸟氨酸用于清除氨,可显著预防纤维化进展。因此,除递送气体外,清除气体或抑制其生成,也是先进递送系统的重要研究方向。
---
3 讨论与未来展望
医用气体疗法有望从根本上革新肝纤维化治疗。CO、H₂、NO、H₂S、SO₂ 等气体作为内源性分子,可同时作用于疾病病理过程的多个环节。与大多数单靶点药物不同,这些气体信号分子可同步抗炎、抗氧化、直接灭活促瘢痕 HSC,对打破纤维化恶性循环至关重要。
该领域的重大突破是先进递送系统的出现:靶向纳米颗粒、自驱动纳米马达等。这些纳米载体解决了气体疗法长期存在的问题:半衰期太短、脱靶毒性、无法到达目标细胞。例如,可缓解肝脏缺氧的 CO 释放胶束、帮助修复受损血管的 SO₂ 释放纳米马达等,推动气体疗法走向真正的靶向治疗。
走向临床仍需克服关键挑战:
1. 开发更智能的多重刺激响应递送系统,仅在纤维化病灶释放气体(如同时响应高 H₂O₂ 与高 TGF‑β)。
2. 明确每种气体的最佳治疗剂量与全身脱靶效应。
3. 开展纳米气体系统的生物分布、长期命运、释放稳定性等安全性研究。
4. 与临床标准药物(Resmetirom、SGLT2/GLP‑1 激动剂)进行头对头比较。
5. 探索多气体协同递送,单颗粒搭载两种供体,多通路协同提高疗效、降低剂量。
将潜力转化为临床需要材料学、安全性评价与严格临床试验的跨学科合作。
---
4 结论
医用气体疗法联合先进纳米技术,为抗击肝纤维化提供了全新、高效策略。利用人体自身气体信号分子并结合病灶精准递送,肝纤维化治疗有望从单纯症状控制转向主动逆转瘢痕。尽管从基础研究到临床应用仍有距离,但动物实验的积极效果与技术的快速迭代,为这一常见疾病带来了新一代高效、靶向疗法的强烈希望。
https://blog.sciencenet.cn/blog-41174-1531084.html
上一篇:复合维生素矿物质或真能延缓生物衰老
下一篇:μ子磁测量与基因疗法突破分别斩获300万美元科学突破奖