博文
氢气疗法在呼吸系统疾病中的应用:作用机制、研究证据与技术考量
||
氢气疗法在呼吸系统疾病中的应用:作用机制、研究证据与技术考量
氢气(H₂)凭借其抗氧化、抗炎、抗凋亡及免疫调节作用,已成为呼吸病学领域极具前景的治疗性气体。随着急慢性呼吸系统疾病发病率不断攀升,氢气有望成为一种新型辅助治疗手段。本文系统整合了氢气的作用机制、临床前研究结果、临床数据及技术应用要点。
在机制层面,氢气可选择性清除羟自由基与过氧亚硝酸盐,保护线粒体功能,激活Nrf2介导的抗氧化应答,抑制炎症小体及NF-κB信号通路,并调控免疫细胞极化与凋亡通路。本综述遵循法拉利叙事综述框架,在MEDLINE、EMBASE、Google Scholar数据库中检索截至2025年6月的文献,并补充灰色文献。临床前研究一致证实,氢气在慢性阻塞性肺疾病、哮喘、肺纤维化、肺动脉高压、急性肺损伤、肺癌及新型冠状病毒肺炎(COVID-19)模型中均具有保护作用。早期临床试验与病例报告显示,氢气可改善氧合、运动耐量及炎症标志物水平,且安全性良好。
近年来工程技术进步实现了高浓度氢气的安全递送,但给药方案标准化、呼吸机兼容性等问题仍待解决。总体而言,氢气作为安全且多功能的治疗性气体,具备显著的临床转化潜力。未来研究需聚焦多中心随机对照试验、剂量‑效应研究及设备整合,以确立其在循证呼吸病诊疗中的地位。
Chuang, Ya-Ting, Wen-Chung Hung, and Tao-An Chen. "Molecular hydrogen therapy in respiratory diseases: mechanisms, evidence, and technical considerations hydrogen therapy in respiratory diseases." All Life 19.1 (2026): 2643533.
引言
氢气(H₂)凭借独特的抗氧化、抗炎、抗凋亡特性,已成为现代医学中极具潜力的治疗药物(Zajac等,2025)。自1783年安托万·拉瓦锡发现氢气以来,其长期被视为无生物学活性的惰性气体;20世纪末,氢气的治疗潜力首次被认识,21世纪初再度引发科研界广泛关注(Pilcher,1888;Dole等,1975;Gharib等,2001;Ohta,2015)。
作为小分子、无色、无味气体,H₂可快速弥散至组织,且在治疗浓度下几乎无毒性(Alwazeer等,2021;Lin等,2024;Salomez‑Ihl等,2024)。其可选择性中和羟自由基(•OH)与过氧亚硝酸盐(ONOO⁻),不干扰其他具有重要生理功能的活性氧(ROS),从而最大限度减少非靶向副作用(Ohsawa等,2007;Lin等,2024;Salomez‑Ihl等,2024;Xiao等,2024)。
越来越多研究表明,H₂可调控多条生物学通路(Ohsawa等,2007;Ma等,2023)。其可抑制巨噬细胞中NLRP3炎症小体激活,下调IL‑1β、IL‑6、TNF‑α等炎症因子,上调超氧化物歧化酶(SOD)、过氧化氢酶等关键抗氧化酶(Ohta,2023;Liu等,2024)。此外,氢气可激活核因子E2相关因子2(Nrf2),该因子是细胞抗氧化防御系统转录调控的核心分子(Ohta,2023)。
在肺部疾病中,临床前与临床研究不断证实氢气的保护作用(Long等,2024)。在动物模型与初步临床试验中,氢气吸入可通过硫氧还蛋白1(Trx1)‑动力相关蛋白1(Drp1)通路抑制线粒体分裂,减轻急性肺损伤(ALI)、氧化损伤,改善急性呼吸窘迫综合征(ARDS)的上皮屏障功能(Long等,2024)。COVID‑19疫情期间,氢气疗法因可减轻肺部炎症、改善氧合而备受关注(Salomez‑Ihl等,2024)。
综上,尽管前期研究结果积极,但仅有一篇综述系统探讨了氢气在多种肺部疾病中的治疗潜力(Zajac等,2025)。为弥补这一空白,本文全面综述氢气在哮喘、慢性阻塞性肺疾病(COPD)、COVID‑19、肺癌、肺损伤、肺纤维化、肺动脉高压等呼吸系统疾病中的应用,并通过图1 氢气在呼吸系统疾病中的潜在应用概览直观展示。结合最新研究证据与分子机制,本文为后续研究奠定基础。鉴于当前以临床前及早期临床研究为主,亟需开展严谨的大规模临床试验,进一步明确并验证氢气在呼吸病学中的治疗价值。
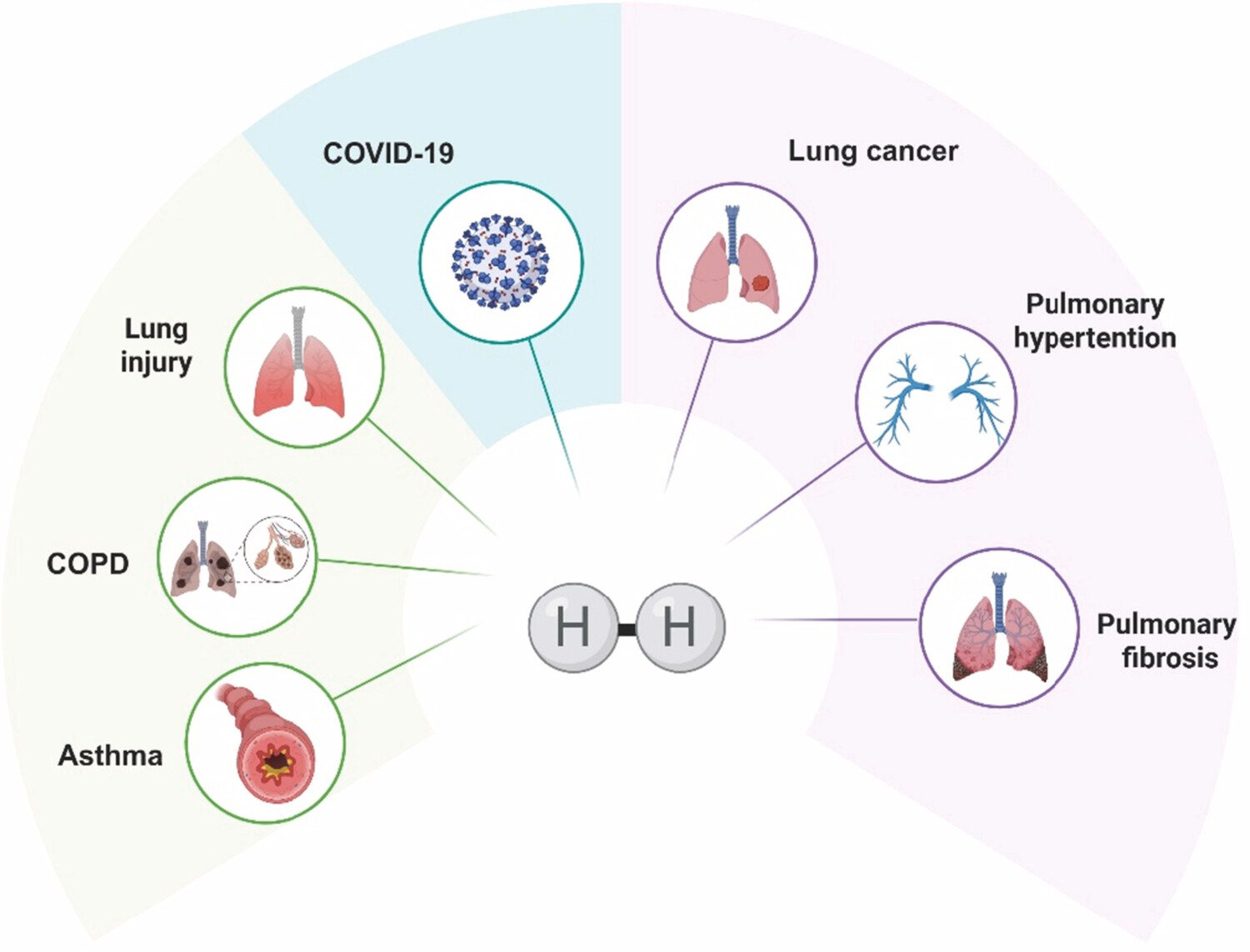
图1 氢气在呼吸系统疾病中的潜在应用概览(全文展示)
研究方法
本研究遵循法拉利叙事综述框架(Ferrari,2015)开展文献检索,纳入同行评议文献与灰色文献,系统梳理氢气疗法在呼吸系统疾病中的作用机制、临床前发现与临床应用。
在文献整合前,TAC、YTC、WCH完成并复核氢气疗法与呼吸疾病模型的预检索结果;随后在MEDLINE、EMBASE、Google Scholar进行系统检索,涵盖数据库建库至2025年6月的文献。不同数据库检索词略有差异,核心布尔检索策略为:(‘hydrogen’[标题] OR ‘molecular hydrogen’[标题/摘要] OR ‘H₂ therapy’[标题/摘要])
AND(‘Respiratory Tract Diseases’[主题词] OR respiratory diseases OR lung disease OR pulmonary disease OR COPD OR asthma OR ARDS OR pneumonia)。
本研究非系统综述,未提供PRISMA流程图。同时手工检索呼吸病学会、氢气疗法相关机构的灰色文献。全体作者共同审阅并整合纳入文献。
---
结果
一、氢气在呼吸系统疾病中的分子机制
氢气在呼吸系统疾病中的治疗分子机制见图2 氢气在呼吸系统疾病中的分子机制,按主题分类阐述如下:
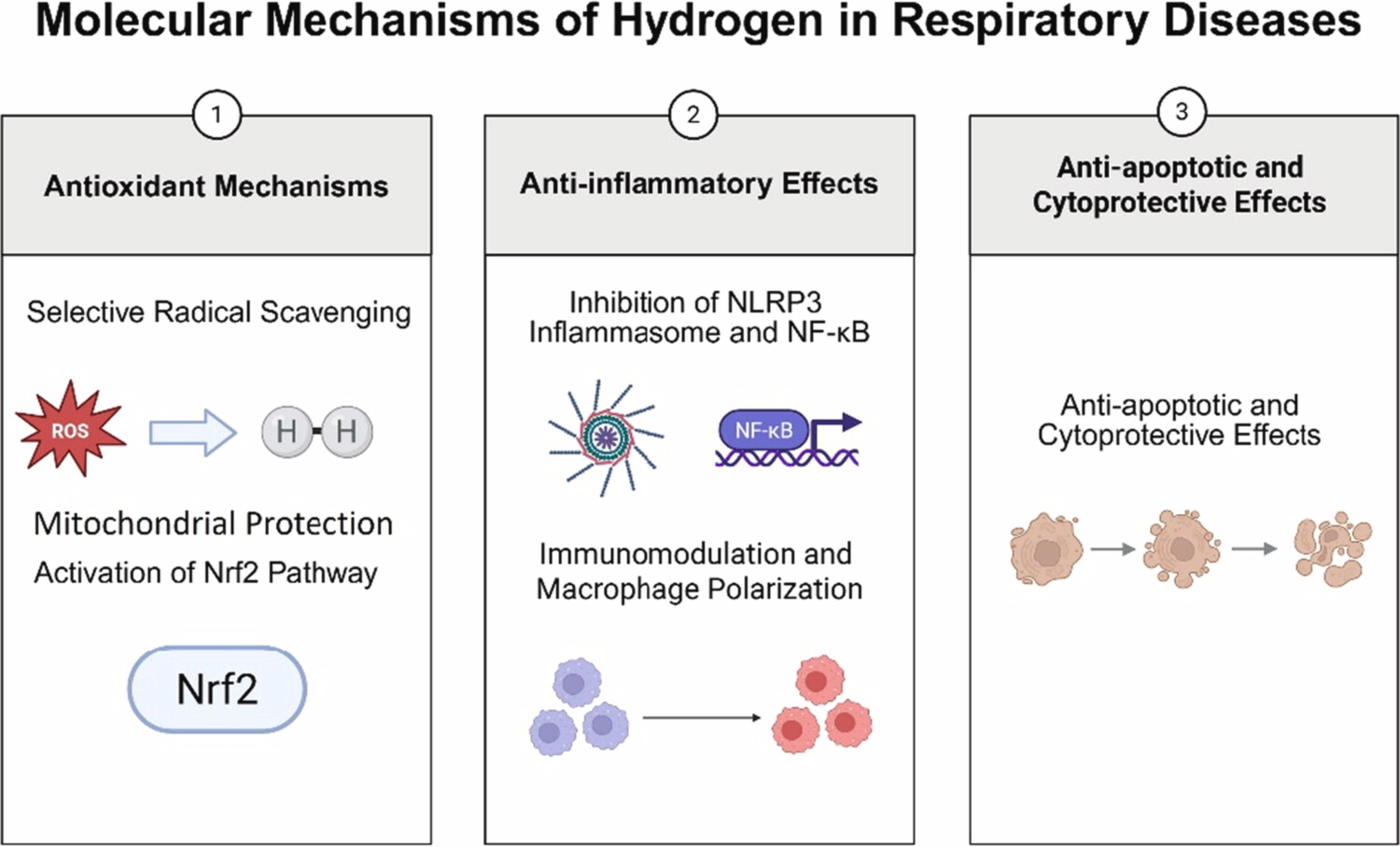
图2 氢气在呼吸系统疾病中的分子机制(全文展示)
(一)抗氧化机制
1. 选择性自由基清除
氢气特异性清除高活性氧氮自由基,尤其是羟自由基(•OH)与过氧亚硝酸盐(ONOO⁻),二者是氧化组织损伤的主要介质。与常规抗氧化剂不同,H₂不与超氧阴离子(O₂⁻)、过氧化氢(H₂O₂)反应,不干扰核心氧化还原信号(Ohsawa等,2007;Hirano等,2021;Kuo等,2023;Zajac等,2025)。羟自由基可氧化DNA产生丙二醛(MDA)、4‑羟基‑2‑壬烯醛(4HNE)、8‑羟基脱氧鸟苷(8‑OHdG)等标志物(Valavanidis等,2009;Niki,2014;Fu等,2022;Kuo等,2023;Zajac等,2025)。在脂多糖(LPS)诱导的小鼠ALI模型中,氢气吸入可显著降低肺组织与血清氧化标志物水平(Aokage等,2023)。
2. 线粒体保护
H₂通过调控线粒体动力学维持线粒体膜电位,下调Drp1蛋白抑制线粒体分裂,上调线粒体融合蛋白2(MFN2)促进融合(Dong等,2018;Zajac等,2025),维持三磷酸腺苷(ATP)合成,阻止细胞色素C释放,减少线粒体介导的凋亡(Cui等,2014;Liu等,2016)。同时减少线粒体电子传递链电子漏出,降低线粒体ROS生成,预防线粒体功能障碍(Gvozdjáková等,2020;Fu等,2022)。
3. Nrf2通路激活
Nrf2是抗氧化防御核心调控因子。氢气激活Nrf2并使其转位入核,上调血红素氧合酶‑1(HO‑1)、SOD、过氧化氢酶(CAT)、谷胱甘肽过氧化物酶(GSH‑Px)(Rangasamy等,2005;Wu等,2013;He等,2020;Quan等,2021;Fu等,2022;Kuo等,2023;Tsai等,2025;Zajac等,2025)。类风湿肺病、干燥综合征、间质性肺病(ILD)患者的临床研究显示,氢气吸入后抗氧化酶上调、氧化应激降低(Tsai等,2025),提示动物实验结果具有临床转化价值,需更大规模对照临床试验验证。
(二)抗炎效应
1. 抑制NLRP3炎症小体与NF‑κB
在多种小鼠及人肺部炎症模型中,H₂下调NLRP3炎症小体、NF‑κB等核心炎症通路,降低TNF‑α、IL‑1β、IL‑6、高迁移率族蛋白B1(HMGB1)水平(H. Chen等,2015;Kelley等,2019;Tao等,2019;Zou等,2019;Guan等,2020;Yang等,2020;Hirano等,2021;Quan等,2021;Fu & Zhang,2022;Fu等,2022;Zhang等,2022;Kuo等,2023)。老年小鼠LPS暴露实验中,2%氢气吸入24小时可显著抑制炎症因子与中性粒细胞浸润,在免疫衰老模型中仍有效(Aokage等,2023)。
2. 免疫调节与巨噬细胞极化
氢气促进巨噬细胞从促炎M1型向抗炎M2型极化,上调IL‑10、TGF‑β表达(Huang等,2019;Yao等,2019;Fu & Zhang,2022;Fu等,2022;Zhang等,2022;Kuo等,2023),减少中性粒细胞募集,减轻脓毒症、哮喘、纤维化模型中过度天然免疫反应的损伤(Chen等,2020;Wang等,2020;Zhuang等,2020;Fu & Zhang,2022;Fu等,2022;Zhang等,2022)。
3. 临床抗炎证据
干燥综合征合并ILD患者接受H₂治疗后,口干、失眠、呼吸困难、胸痛、头晕等症状显著改善(Tsai等,2025),伴随T/B细胞亚群优化、肺部影像学好转、全身炎症标志物降低。
(三)抗凋亡与细胞保护作用
H₂主要通过抗氧化调控凋亡,调节PI3K/Akt/GSK3β、JAK2/STAT3、Ask1/JNK、Ras/ERK1/2/MEK1/2等通路,平衡促凋亡与抗凋亡信号(Zajac等,2025)。具体表现为降低Bax、ROS‑p53等促凋亡因子,升高Bcl‑2、Bcl‑xl等抗凋亡因子,主要通过PI3K/Akt与JAK2/STAT3通路实现(Sun等,2017;Wu等,2018;Qiu等,2019;Yang等,2020;Fu等,2022)。
此外,H₂减少线粒体ROS生成,减轻氧化应激诱导凋亡(Sun等,2017;Wu等,2018;Qiu等,2019;Yang等,2020;Fu等,2022);通过调控PERK‑eIF2α‑ATF4、IRE1‑XBP1、ATF6通路缓解内质网应激,调节p‑mTOR/mTOR表达控制自噬,避免过度激活(Fu等,2020;Yang等,2020;Zhang等,2022)。
二、医用氢气吸入系统的安全性、技术考量与呼吸机兼容性
1969年研究证实人体可产生并排泄H₂,氢气自此被认定为无毒分子(Kurokawa等,2019)。大气中氧浓度约21%,吸入气氧浓度低于19.5%为缺氧气体(Kurokawa等,2019)。部分研究使用100%氢气,但纯氢气不可直接吸入,需与空气混合(Lin等,2020)。氢气在潜水医学应用历史悠久,高压高浓度下仍对人体无毒(Hayashida等,2008)。
既往因缺乏安全、耐用的高浓度氢气吸入装置,动物与临床研究多使用<4% H₂混合气或低浓度富氢水(Lin等,2020)。氢气在空气中浓度>4.1%易燃易爆,医用吸入混合气浓度多限制在2%~4%(Hirayama等,2011;Tan等,2018;Salomez‑Ihl等,2024)。日本东京消防厅消防技术安全部报告显示,即使考虑静电点火风险,环境空气中氢气浓度<0.3%仍安全(Chen等,2021)。
近年技术革新实现高浓度氢气安全递送,如约66% H₂+34% O₂的医用氢氧混合气(Lin等,2020),专用安全设计可有效降低爆炸风险,支持高浓度氢气吸入的临床应用(Lin等,2020)。近期动物研究使用73% H₂+23% O₂混合气,拓展了高浓度氢氧配方研究范围(Shih等,2024),但高浓度氢气临床应用仍有限,未广泛普及。
医用气体常通过机械通气递送,传统呼吸机设计用于21%~100%氮氧混合气,含氢气气体的安全递送可行性尚不明确。最新研究显示,未经改装的Servo‑i、Servo‑u、Evita V500呼吸机可精准递送2%氢气混合气,潮气量(VT)与吸入氧浓度(FiO₂)达标;但Babylog VN500等机型精度不足(Mancebo等,2025)。该研究未覆盖全部临床常用呼吸机,提示临床使用含氢气混合气时需严格评估与筛选呼吸机。
未来需扩大呼吸设备兼容性与性能研究,持续优化氢气吸入技术、改进呼吸机设计,对提升氢气吸入疗法的安全性与有效性、推动其临床普及至关重要。相关结论汇总见图3 呼吸系统疾病氢气疗法核心结论与未来方向整合总结。
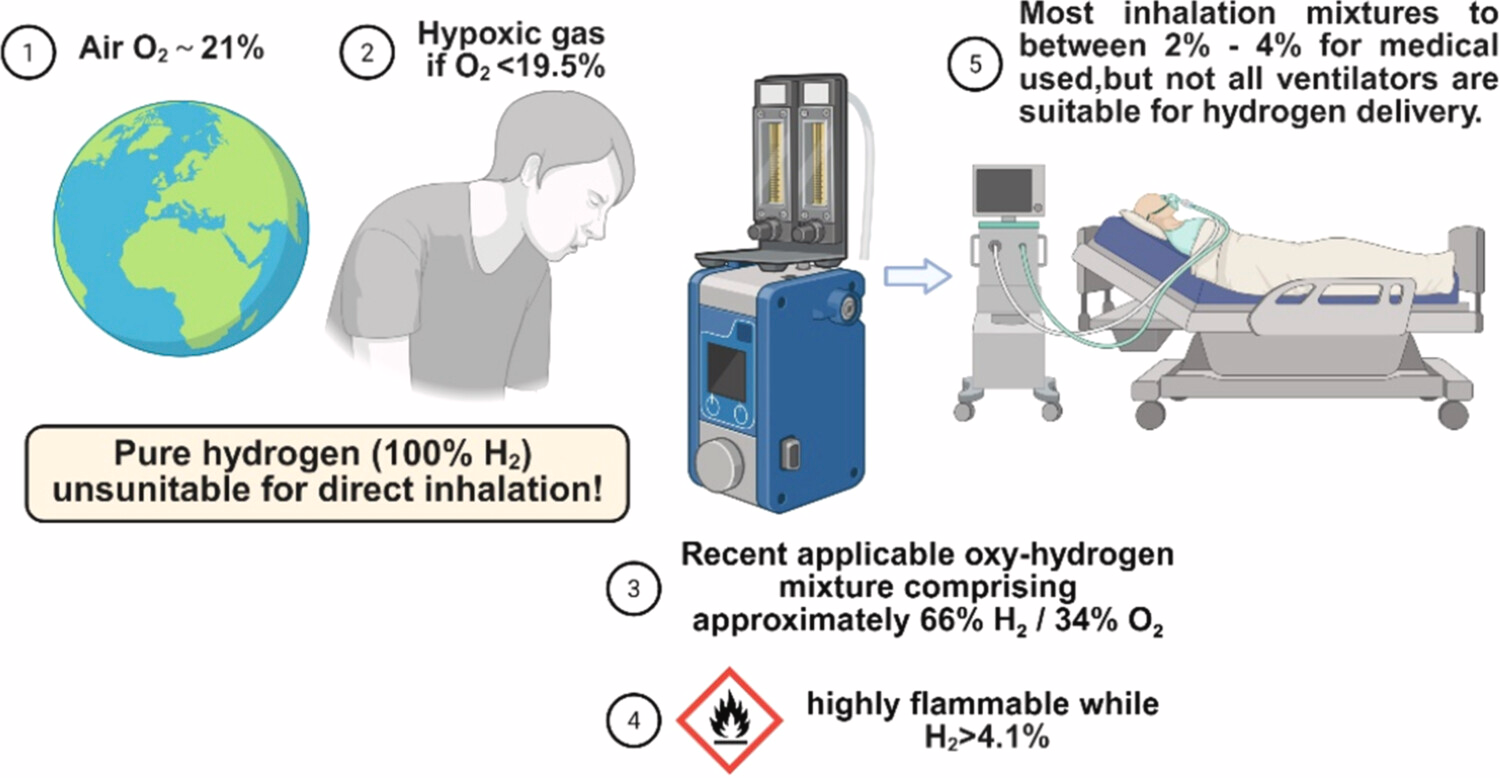
图3 临床含氢气混合气递送的安全阈值、技术考量与呼吸机兼容性示意图。
三、氢气在呼吸系统疾病中的临床前与临床证据
(一)慢性阻塞性肺疾病(COPD)
COPD是常见肺部疾病,以持续呼吸道症状、不可逆气流受限为特征,包括肺气肿、慢性支气管炎,表现为呼吸困难、运动耐量下降(Xu等,2024)。主要危险因素为吸烟、环境污染物、职业有害颗粒与化学物质长期暴露(Xu等,2024;Zajac等,2025),持续炎症与氧化应激是核心发病机制(Zajac等,2025)。
临床前研究显示,H₂吸入或富氢液可显著减轻香烟烟雾诱导的COPD大鼠肺损伤,改善肺顺应性,减少肺泡破坏,下调IL‑6、IL‑17、IL‑23、基质金属蛋白酶‑12(MMP‑12)等促炎因子(Ning等,2013;Liu等,2017;Lu等,2018)。机制上,H₂抑制EGFR磷酸化,阻断ERK1/2与NF‑κB通路(Ning等,2013;Lu等,2018;Fu & Zhang,2022)。
临床中,COPD患者饮用富氢液可提高血氧饱和度、降低氧化标志物、改善运动耐量(Singh等,2023);2.4%氢气吸入45分钟可快速减轻气道与全身炎症(Wang等,2020)。多中心随机试验证实,氢氧疗法可显著改善急性加重期症状,安全性与氧疗相当(Zheng等,2021)。
综上,H₂通过抗氧化、抗炎成为COPD极具潜力的辅助疗法。
(二)哮喘
哮喘是慢性炎症性疾病,以气道高反应、黏液高分泌、结构重塑为特征,氧化应激与2型炎症(Th2/ILC2轴)是核心机制(Zhang等,2021;Melén等,2024)。
卵清蛋白诱导的小鼠哮喘模型中,H₂吸入或富氢液可降低气道阻力、嗜酸性粒细胞炎症、Th2细胞因子(IL‑4、IL‑5、IL‑13),升高SOD、CAT等抗氧化酶活性,降低MDA、髓过氧化物酶(MPO)等氧化标志物(Xiao等,2013;Zhang等,2018;Huang等,2019;Zhang等,2021;Fu & Zhang,2022)。
氢气通过上调E‑钙黏蛋白、紧密连接蛋白‑1(ZO‑1)保护上皮屏障,抑制凋亡(Wang等,2020;Zhang等,2021);恢复巨噬细胞吞噬功能、激活Nrf2增强抗炎效应(Xiao等,2013;Huang等,2019;Wang等,2020;Fu & Zhang,2022);通过抑制NF‑κB降低MUC5AC、Ⅲ型胶原、血管内皮生长因子(VEGF)表达,减轻气道重塑(Xiao等,2013);还可正常化糖酵解代谢与线粒体功能,恢复哮喘细胞ATP合成(Niu等,2020)。
临床中,哮喘患者饮用富氢液可提高血氧饱和度,降低硫代巴比妥酸反应物(TBARS)、MDA等氧化标志物(Singh等,2023);2.4% H₂吸入45分钟可降低呼出气冷凝液与血液炎症标志物(Wang等,2020)。氢气还可减轻PM2.5、碳纳米颗粒等环境诱因导致的气道炎症,对污染相关性哮喘具有潜在价值(Choi等,2017;Feng等,2019)。
临床前与早期临床证据一致支持H₂作为哮喘辅助治疗,通过激活Nrf2、抑制NF‑κB发挥抗氧化、抗炎、上皮保护作用。
(三)肺癌
H₂通过降低氧化应激、促进凋亡、调节免疫、增强常规疗法疗效发挥抗癌作用。体外实验显示,H₂可抑制A549、H1975等肺癌细胞增殖并诱导凋亡(Saitoh等,2008;Wang等,2018;Zhang等,2022)。动物模型中,H₂可缩小结直肠癌与肺癌肿瘤体积,降低炎症标志物,延长生存期(Wang等,2018;Akagi & Baba,2019)。
机制上,H₂下调X连锁凋亡抑制蛋白(XIAP)、杆状病毒凋亡抑制蛋白重复序列3(BIRC3),促进胱天蛋白酶激活,抑制ROS/NLRP3/caspase‑1/GSDMD、Wnt/β‑catenin通路(Yang等,2020;Zhang等,2022);降低VEGF与染色体结构维持蛋白,抑制血管生成与肿瘤进展(Wang等,2018;Meng等,2020;Hirano等,2021)。
临床中,非小细胞肺癌(NSCLC)患者吸入H₂可实现肿瘤退缩、症状缓解,延长无进展生存期与总生存期,联合纳武利尤单抗或化疗效果更优(Akagi & Baba,2020;Chen等,2020)。H₂还可减轻放化疗毒性,降低ROS损伤、骨髓抑制、听力损失、疲劳等副作用,同时保留治疗疗效(Johnsen等,2023;Zajac等,2025)。
综上,H₂是安全且有前景的肿瘤辅助治疗手段,通过氧化、凋亡、免疫通路发挥直接抑瘤与全身保护作用。
(四)肺纤维化
肺纤维化(PF)是进展性间质性肺病,以慢性炎症、细胞外基质(ECM)过度沉积、肺组织不可逆瘢痕化为特征,核心机制为肺泡上皮反复损伤与异常修复(Osborn‑Heaford等,2015;Muri等,2024)。上皮‑间质转化(EMT)是关键环节,肺泡上皮细胞获得间质表型,激活肌成纤维细胞合成ECM(Zhang等,2015;Muri等,2024),EMT主要由氧化应激与TGF‑β信号驱动,H₂可在临床前模型中抑制二者(Tao等,2016;Hewlett等,2018;Fu & Zhang,2022)。
百草枯、LPS、博来霉素诱导的PF动物模型中,氢气吸入与富氢水均可降低肺硬度、保留肺顺应性、增加肺活量(Dong等,2017;Aokage等,2021),伴随IL‑4、IL‑6、IL‑13等炎症因子,ROS、MDA、羟脯氨酸等氧化标志物,纤连蛋白、胶原等纤维化蛋白水平降低(Zajac等,2025)。机制上,氢气抑制EMT,降低α‑平滑肌肌动蛋白(α‑SMA)、TGF‑β1表达(Tao等,2016;Hewlett等,2018;Fu & Zhang,2022;Li等,2024)。
矽肺模型中,氢气联合粉防己碱通过NF‑κB/NLRP3通路显著减轻PF,抑制炎症、氧化应激与EMT进程(Li等,2024),恢复E‑钙黏蛋白表达,时间依赖性抑制波形蛋白、α‑SMA上调(Gao等,2019;Li等,2024)。氢气对百草枯、类风湿关节炎相关间质性肺病(RA‑ILD)诱导的PF亦有效,提示其在不同病因中具有广谱潜力(Li等,2024)。
临床证据来自1例IgG4相关性PF‑ILD合并医院获得性肺炎患者,氢气辅助治疗后症状与影像学显著改善(Lui等,2024),免疫谱显示静息调节性T细胞(Treg)急剧升高,Fas⁺ Th、Tc亚群降低,提示氢气通过增强FOXP3 Treg功能发挥免疫调节作用(Yang等,2020;Zhu等,2020;Lui等,2024)。Treg功能异常、Fas‑FasL通路过度激活参与免疫介导纤维化,氢气的调控作用具有额外治疗价值(Kuwano等,1999)。
(五)肺动脉高压
肺动脉高压(PH)以肺动脉压升高、右心室肥厚、氧化应激增强为特征,均为H₂疗法靶点(Zajac等,2025)。临床前模型中,氢气吸入或富氢液可显著降低肺动脉压、减轻右心室重构、炎症细胞浸润与氧化硝化标志物,证实其抗氧化、抗炎作用(He等,2013;Kishimoto等,2015;Fu & Zhang,2022),还可改善血管功能、内皮完整性与线粒体保护(Zhang等,2011)。
临床中,H₂对自身免疫相关性PH具有辅助治疗潜力。结缔组织病相关性肺动脉高压患者口服H₂后,CD127⁺ Treg细胞升高,抗Ro抗体与B细胞亚群降低,临床状态稳定(Lin等,2024)。系统性红斑狼疮相关性PH合并右心衰竭患者中,H₂调控Tr1与Treg细胞,降低B细胞与浆细胞活性,减轻免疫介导血管损伤(Tu等,2025)。
临床观察与临床前结果一致,证实H₂可缓解PH的免疫紊乱与血管重塑,良好安全性支持其作为新型辅助策略(Lin等,2024;Tu等,2025;Zajac等,2025)。
(六)新型冠状病毒肺炎(COVID‑19)
严重急性呼吸综合征冠状病毒2(SARS‑CoV‑2)感染通过激活INF‑γ、NADPH氧化酶与NLRP3炎症小体,诱发过度炎症与氧化应激,导致细胞因子风暴、肺泡损伤、呼吸衰竭(Erlich等,2020;Ratajczak & Kucia,2020;Tay等,2020;Rodrigues等,2021),为氢气治疗提供理论依据。
氢气吸入(尤其66% H₂+33% O₂混合气)可快速缓解COVID‑19患者症状,改善呼吸困难、氧合与出院率(Alwazeer等,2021;Singh等,2021;Zeng等,2023)。其小分子高弥散性可降低气道阻力,提升气体交换效率(Luo等,2022;Zeng等,2023)。
Ⅰ期临床试验使用3.6% H₂(96.4% N₂),安全性良好,中度COVID‑19住院患者第3天即出现临床改善,提示非爆炸浓度下仍有效(Salomez‑Ihl等,2024)。中国回顾性分析证实,66% H₂+33% O₂疗法可降低中性粒细胞比例与C反应蛋白(CRP),发挥抗炎与器官保护作用(Luo等,2022)。
康复期患者接受14天氢气吸入,可显著改善用力肺活量(FVC)、1秒用力呼气容积(FEV₁)与6分钟步行试验(6‑MWT)等呼吸与运动功能,不受年龄性别影响(Botek等,2022)。
3.6%~66%不同浓度氢气在COVID‑19各阶段均安全有效,高浓度更利于急性症状缓解,低浓度为临床广泛应用提供安全可行方案(Botek等,2022;Luo等,2022;Salomez‑Ihl等,2024)。
(七)肺损伤
H₂在急性肺损伤(ALI)、急性呼吸窘迫综合征(ARDS)、缺血再灌注(I/R)、呼吸机相关性肺损伤(VILI)等多种肺损伤模型中具有多维度保护作用,核心机制为抗氧化、抗炎、抗凋亡、屏障稳定(Zajac等,2025)。
LPS诱导ALI模型中,氢气吸入或富氢盐水可改善氧合指数(PaO₂/FiO₂),降低IL‑1β、IL‑6、TNF‑α等炎症介质与MDA、硝基酪氨酸等氧化标志物(Chen等,2010;Qiu等,2011;Xie等,2012;He等,2013;Kishimoto等,2015;Liu等,2015;Zhang等,2015;Liu等,2016;Qiu等,2019;Wang等,2019;Du等,2022),减轻上皮与肺泡细胞损伤,上调Bcl‑2,下调caspase‑3/8(Qiu等,2011;Xie等,2012;Kishimoto等,2015;Liu等,2015;Qiu等,2019;Fu & Zhang,2022;Zajac等,2025),恢复水通道蛋白AQP‑1、AQP‑5表达与上皮屏障功能(Fu & Zhang,2022)。
I/R诱导肺损伤(尤其肺移植)中,氢气吸入降低IL‑1β、TNF‑α、ICAM‑1与脂质过氧化等氧化应激(Kawamura等,2010;Kawamura等,2011);腹主动脉阻断、肠系膜缺血等I/R模型中,氢气抑制NLRP3激活,降低MPO、MDA与凋亡相关基因表达(Mao等,2009;Zou等,2019)。
高氧诱导肺损伤中,H₂抑制炎症,减少TUNEL阳性凋亡细胞,激活PI3K/Akt/FoxO3a与SIRT1通路(Kawamura等,2013;Sun等,2017;Wu等,2018;Zhang等,2022)。
VILI模型中,氢气吸入双相减轻肺泡损伤、中性粒细胞浸润与NF‑κB结合活性,早期升高Bcl‑2,后期降低炎症信号(Fu & Zhang,2022)。
海水诱导ALI模型中,氢气降低肺MPO、IL‑1β/IL‑6/TNF‑α、caspase‑3,激活Nrf2/HO‑1通路(Chen等,2010;Diao等,2016;Kuo等,2023)。
ARDS模型中,氢气恢复紧密连接蛋白(闭合蛋白、ZO‑1),抑制Drp1 Ser616磷酸化减轻线粒体分裂,激活Trx1/ASK1/JNK轴(Long等,2024);还可降低组织因子、MMP‑9,升高Trx1,改善脓毒症诱导ALI(Xue等,2015;Tian等,2020;Li等,2021)。
---
讨论
H₂通过多维度抗氧化、抗炎、抗凋亡、免疫调节作用,成为多种呼吸系统疾病的潜力辅助疗法。临床前研究在COPD、哮喘、肺损伤、肺纤维化、肺动脉高压、肺癌、COVID‑19模型中均显示一致保护效应,早期临床试验与病例报告展现良好转化前景。
未来研究应优先开展大规模、多中心、随机对照试验,在不同人群中验证疗效、最优剂量与疗程;标准化临床与机制终点指标,确保研究间可比性。氢气浓度、暴露时间与疾病特异性结局的关系尚未明确,需系统剂量‑效应研究,尤其高浓度(>4%)递送虽急性症状缓解更优,但因易燃性需严格安全管控。
递送技术进步(呼吸机兼容系统、便携式吸入器)将拓展H₂疗法在急慢性疾病中的应用可行性。尽管66% H₂+34% O₂混合气已实现安全递送,但临床常规应用仍有限,需扩大机械呼吸机(尤其重症监护)设备兼容性评估,保障安全实施。
机制层面,Nrf2激活、线粒体动力学调控、炎症小体抑制等通路临床前证据充分,但直接临床验证不足,靶向生物标志物研究可明确人体机制、筛选应答者、指导精准医疗。此外,H₂保护正常组织同时诱导肿瘤细胞凋亡的双重作用,值得肿瘤领域深入探索。
综上,临床前与新兴临床证据显示,H₂在广谱呼吸系统疾病中具有一致治疗获益:动物模型中可减轻氧化应激、抑制促炎因子级联反应、稳定上皮内皮屏障、调节免疫细胞表型(增强Treg、抑制Th2)、阻断NF‑κB、NLRP3、TGF‑β/EMT、线粒体功能障碍等促纤维化与促凋亡通路,转化为肺顺应性改善、氧合指数提升、气道阻力降低、肺动脉压减轻、纤维化重塑缓解等生理获益。
临床中,尽管大规模试验有限,但早期随机试验、队列研究与病例报告一致显示症状缓解(呼吸困难减轻)、氧合改善、炎症标志物(CRP、中性粒细胞比例、TBARS、MDA)降低、功能指标(FVC、FEV₁、6‑MWT)好转。重要的是,2%~4%非爆炸浓度至高浓度氢氧混合气均显示良好安全性,无严重不良事件。其在氧化应激与免疫紊乱相关疾病(COPD急性加重、哮喘、COVID‑19、肺损伤、免疫相关性肺动脉高压)中效果尤为显著,提示氧化还原调控与免疫重平衡是核心治疗轴。
研究局限性
当前H₂疗法证据仍有限,多数临床研究样本量小、方案异质性高、依赖替代终点而非长期功能结局;大量研究为单中心观察性研究,外推性受限。吸入、富氢水、富氢盐水静脉输注等给药途径多样,增加结局解读与试验间比较难度。缺乏系统剂量‑效应数据,最优浓度、递送时长、频率尚未明确。上述方法学与技术局限提示,亟需设计严谨的多中心随机对照试验、标准化方案、给药途径头对头比较,强化临床证据,支持H₂疗法安全有效融入呼吸病诊疗。
结论
H₂作为新型、耐受性良好的治疗手段,兼具多维度抗氧化、抗炎、抗凋亡、免疫调节特性,在COPD、哮喘、肺损伤、肺纤维化、肺动脉高压、肺癌、COVID‑19等广谱呼吸系统疾病中均显示保护作用。临床前研究一致证实其可调控氧化应激、炎症、线粒体动力学与免疫应答,早期临床发现与病例报告展现积极转化潜力。
呼吸机兼容、高浓度递送系统等技术进步提升了给药可行性与安全性,但临床常规应用仍有限。为实现其全部临床价值,未来需开展大规模多中心随机对照试验,采用标准化终点指标明确最优剂量、疗程与给药途径;同时开展机制研究,验证Nrf2激活、炎症小体抑制等通路在人体中的作用。此外,阐明剂量‑效应关系(尤其高浓度吸入)、探索组织保护与肿瘤抑制双重作用,可拓展其治疗范围。克服当前方法学与技术局限,是将H₂纳入循证呼吸病诊疗、确立其在急慢性疾病中可靠辅助治疗地位的关键。
https://blog.sciencenet.cn/blog-41174-1527357.html
上一篇:红细胞作为主要葡萄糖汇,改善高海拔环境下的葡萄糖耐量
下一篇:老年人肌肉萎缩分子开关(PNAS)