ВЉЮФ
ЧтЦјМѕЧсАЂУЙЫиИЮЫ№ЩЫЛњжЦ
||
ЧтЦјМѕЧсАЂУЙЫиИЮЫ№ЩЫЛњжЦ
вЉЮяадИЮЫ№ЩЫЪЧвЉЮяЯрЙиМВВЁжаЕФвЛДѓживЊЮЪЬтЁЃАЂУЙЫиЃЈDOXЃЉгеЕМИЮЫ№ЩЫЕФШЗЧаЛњжЦЩаЮДЭъШЋВћУїЁЃЧтЦјвђЦфбЁдёадПЙбѕЛЏЬиадгыСМКУЕФАВШЋадЖјБИЪмЙизЂЃЌЕЋЦфЖдАЂУЙЫиЫљжТИЮЫ№ЩЫЕФБЃЛЄзїгУЩаЮДЭъШЋУїШЗЁЃБОбаОПЙЙНЈАЂУЙЫигеЕМИЮЫ№ЩЫФЃаЭЃЌЦРЙРИЮЙІФмМАВЁРэИФБфЃЌвдДЫЬНОПЧтЦјЕФжЮСЦаЇЙћЃЛВЂНјвЛВНМьВтбѕЛЏгІМЄгыбзжЂБъжОЮяЫЎЦНЃЌВћУїЦфЧБдкзїгУЛњжЦЁЃЧтЦјДІРэПЩЯджјМѕЧсАЂУЙЫиЫљжТИЮЫ№ЩЫЃЌвжжЦИЮЯИАћЯЫЮЌЛЏЁЃбаОПЗЂЯжЃЌЧтЦјПЩвжжЦАЂУЙЫиФЃаЭаЁЪѓИЮзщжЏЯИАћЕђЭіЁЂНЕЕЭбѕЛЏгІМЄЫЎЦНВЂИФЩЦбзжЂЗДгІЃЌЦфБЃЛЄзїгУжївЊЭЈЙ§ЕїПиNrf2/HO-1ЭЈТЗЪЕЯжЁЃживЊЕФЪЧЃЌдкHepG2ЯИАћжаИјгшNrf2вжжЦМСКѓЃЌЧтЦјЕФИЮБЃЛЄзїгУЯћЪЇЁЃЩЯЪіНсЙћБэУїЃЌЧтЦјПЩЭЈЙ§МЄЛюNrf2/HO-1аХКХЭЈТЗМѕЧсбѕЛЏгІМЄгыбзжЂЗДгІЃЌДгЖјЛКНтАЂУЙЫигеЕМЕФИЮЫ№ЩЫЁЃ
зїепРДздКгББжавНвЉДѓбЇ
1 в§бд
УПФъдМга7ЭђШЫЫРгкЖёаджзСі[1]ЁЃОЁЙмПЙжзСівЉЮяПЩЬсИпАЉжЂЛМепЩњДцТЪЃЌЕЋЦфСйДВгІгУГЃАщЫцбЯжиВЛСМЗДгІЃЌАќРЈИЮЖОадгыЩіЖОад[2,3]ЁЃИЮдрзїЮЊвЉЮяДњаЛгыНтЖОЕФжївЊЦїЙйЃЌМЋвзЪмЕНПЙжзСівЉЮяЖОадЫ№ЩЫ[4]ЁЃвђДЫЃЌЛКНтВЂИФЩЦПЙжзСіжЮСЦЯрЙиЕФИЮЖОаджСЙиживЊЁЃИУВпТдВЛНіПЩЬсЩ§жЮСЦАВШЋадЃЌЛЙФмдкВЛЫ№ЩЫИЮЙІФмЕФЧАЬсЯТБЃеЯгааЇПЙАЉЗНАИЕФЪЕЪЉЁЃ
АЂУЙЫиЃЈDOXЃЉЪєгкньЛЗРрвЉЮяЃЌЪЧФПЧАСйДВСЦаЇЯджјЁЂгІгУЙуЗКЕФПЙжзСівЉЮяжЎвЛ[5]ЁЃЕЋЦфСйДВгІгУГЃвђбЯжиЖОадЪмЯоЁЃАЂУЙЫизюГЃМћЕФВЛСМЗДгІАќРЈдьбЊЙІФмЫЅНпЁЂаФдрЖОадгыИЮЫ№ЩЫЃЌдМ40%НгЪмАЂУЙЫижЮСЦЕФЛМепЛсГіЯжИЮЫ№ЩЫ[6]ЁЃИУЖОадЕФжївЊЗжзгЛњжЦЮЊЃКАЂУЙЫидкИЮдрДњаЛЙ§ГЬжаВњЩњЛюадбѕЃЈROSЃЉЃЌв§ЗЂбѕЛЏгІМЄЁЂПЙбѕЛЏУИЫЎЦНЯТНЕЁЂЯИАћЕђЭіЁЂбзжЂЗДгІМАЯпСЃЬхЙІФмеЯА[7,8]ЁЃвђДЫЃЌАаЯђЕїПибѕЛЏгІМЄЪЧМѕЧсАЂУЙЫиЫљжТИЮЫ№ЩЫЕФЙиМќЁЃЬьШЛПЙбѕЛЏМСгыжВЮяЛЏбЇГЩЗжЃЈШчжВЮяЬсШЁЮяЃЉПЩЭЈЙ§ЧхГ§здгЩЛљЁЂдіЧППЙбѕЛЏЗРгљЁЂЕїПибзжЂЗДгІЗЂЛгБЃЛЄзїгУ[9]ЁЃР§ШчЃЌгабаОПБэУїЛЈЦьЫЩЫиЃЈTAXЃЉПЩЭЈЙ§вжжЦЬњЫРЭігыбѕЛЏЭЈТЗЛКНтЛЏСЦЫљжТИЮЖОадЃЌЭЙЯдСЫИЈжњСЦЗЈдкМѕЧсАЂУЙЫиЯрЙиИЮЫ№ЩЫЁЂЭЌЪББЃСєЦфПЙАЉСЦаЇЗНУцЕФЧБСІ[10]ЁЃвђДЫЃЌИФЩЦАЂУЙЫижЮСЦЗНАИЕФЖОадЗДгІЃЌЖдЬсЩ§ЛМепдЄКѓЁЂБЃеЯгУвЉАВШЋвтвхжиДѓЁЃ
ЧтЦјвђОпгабЁдёадПЙбѕЛЏЁЂЖдЯИАћЮоЖОЁЂЩњЮяЯрШнадгХвьЕШЬиЕуЃЌГЩЮЊМЋОпЧАОАЕФжЮСЦЗжзг[11]ЁЃЖрЯюбаОПжЄЪЕЃЌЧтЦјПЩЭЈЙ§вжжЦЕђЭіЁЂМѕЩйЬњЫРЭіЁЂдіЧПздЪЩЛКНтАЂУЙЫиЫљжТаФдрЖОад[12,13,14]ЁЃАЂУЙЫигеЕМИЮЖОадЕФЛњжЦАќРЈбѕЛЏгІМЄЁЂЯпСЃЬхЙІФмеЯАгыбзжЂЗДгІЃЌгыЫГВЌЕШЦфЫћЛЏСЦвЉЮяЕФЫ№ЩЫЛњжЦЯрЫЦ[15,16]ЁЃЕЋЧтЦјФмЗёМѕЧсАЂУЙЫиЫљжТИЮЖОадМАЦфОпЬхЛњжЦЩаВЛУїШЗЁЃЮЊДЫЃЌБОбаОПЙЙНЈАЂУЙЫигеЕМИЮЫ№ЩЫЕФЬхФкЭтФЃаЭЃЌЬНОПЧтЦјЕФБЃЛЄзїгУВЂВћУїЦфЧБдкЛњжЦЁЃ
2 НсЙћ
2.1 ЧтЦјЛКНтАЂУЙЫигеЕМЕФИЮЙІФмЫ№ЩЫ
ЪзЯШЦРЙРАЂУЙЫиДІРэаЁЪѓЕФЛљДЁзДЬЌЁЃШчЭМ1AЈCCЫљЪОЃЌгыЖдеезщЯрБШЃЌАЂУЙЫизщаЁЪѓЬхжиЯТНЕЃЌИЮдржИЪ§гыЦЂдржИЪ§Щ§ИпЃЛЖјАЂУЙЫиСЊКЯИЛЧтбЮЫЎЃЈHRSЃЉДІРэКѓЃЌЩЯЪіжИБъЯджјИФЩЦЃЈЭМ1AЈCCЃЉЁЃ
ЫцКѓМьВтИЮЙІФмЯрЙиЩњЛЏжИБъЁЃАЂУЙЫизщаЁЪѓбЊЧхЙШБћзЊАБУИЃЈALTЃЉЁЂЙШВнзЊАБУИЃЈASTЃЉЁЂМюадСзЫсУИЃЈALPЃЉЁЂзмЕЈКьЫиЃЈTBILЃЉгыІУ-ЙШАБѕЃзЊвЦУИЃЈІУ-GTЃЉЫЎЦНЯджјЩ§ИпЃЈЭМ1DЈCHЃЉЁЃЭЌЪБЃЌВЁРэШОЩЋЯдЪОАЂУЙЫизщаЁЪѓИЮаЁвЖНсЙЙЮЩТвЃЌУХТіЧјжмЮЇИЮЯИАћЙуЗКЛЕЫРЃЌАщЫцбзжЂвђзгНўШѓгыЯЫЮЌЛЏЃЈЭМ1JЈCLЃЉЃЌЬсЪОГіЯжИЮЙІФмЫ№ЩЫЁЃИјгшИЛЧтбЮЫЎКѓЃЌаЁЪѓбЊЧхALTЁЂASTЁЂALPЁЂTBILгыІУ-GTЫЎЦНЯТНЕЃЌИЮдрВЁРэНсЙЙвьГЃЕУЕНИФЩЦЃЈЭМ1DЈCLЃЉЁЃ

ЭМ1 ЧтЦјЛКНтАЂУЙЫигеЕМЕФИЮЙІФмЫ№ЩЫ
ЃЈAЃЉИїзщаЁЪѓЬхжиЃЛЃЈB,CЃЉИїзщаЁЪѓИЮдржИЪ§гыЦЂдржИЪ§ЃЈn=6ЃЉЃЛЃЈDЈCHЃЉИїзщаЁЪѓбЊЧхALTЁЂASTЁЂALPЁЂTBILЁЂІУ-GTКЌСПЃЈn=6ЃЉЃЛЃЈIЃЉИЮзщжЏHEШОЩЋЃЈБъГп=200 ІЬmЛђ50 ІЬmЃЌn=3ЃЌМ§ЭЗЪОЛЕЫРИЮЯИАћЃЉЃЛЃЈJЃЉИЮзщжЏMassonШОЩЋЃЈБъГп=200 ІЬmЃЌn=3ЃЉЃЛЃЈKЃЉИЮзщжЏЬьРЧаЧКьШОЩЋЃЈБъГп=200 ІЬmЃЌn=3ЃЉЃЛЃЈLЃЉИЮзщжЏЯЫЮЌЛЏУцЛ§ЖЈСПЁЃЪ§ОнвдОљжЕЁРБъзМЮѓЃЈSEMЃЉБэЪОЁЃ**p<0.01 vs. ЖдеезщЃЛp<0.05ЃЌp<0.01 vs. АЂУЙЫизщЁЃ
2.2 ЛљгкGEOЪ§ОнПтЗжЮіАЂУЙЫиИЮЫ№ЩЫАаЕу
ЭЈЙ§ЛљвђБэДязлКЯЪ§ОнПтЃЈGEOЃЉЛёШЁАЂУЙЫиДІРэHepG2ЯИАћЕФЛљвђБэДяЪ§ОнЃЌНјвЛВНЗжЮіЩИбЁГіАЂУЙЫиДІРэКѓБэДяЯджјИФБфЕФЛљвђЃЈЭМ2A,BЃЉЁЃИЛМЏЗжЮіЯдЪОЃЌетаЉЛљвђжївЊгыбѕЛЏгІМЄМАбзжЂЗДгІЯрЙиЃЈЭМ2CЃЉЁЃЯъЯИЗжЮіБэУїЃЌАЂУЙЫиДІРэКѓАзЯИАћНщЫи-6ЃЈIL-6ЃЉЁЂNODбљЪмЬхЕААз3ЃЈNLRP3ЃЉЁЂбЬѕЃАЗЯйрбпЪЖўКЫмеЫсСзЫсбѕЛЏУИ4ЃЈNOX4ЃЉЁЂУЬГЌбѕЛЏЮяЦчЛЏУИЃЈSOD2ЃЉгыКЫвђзгE2ЯрЙивђзг2ЃЈNFE2L2ЃЉЛљвђБэДяЩЯЕїЃЈЭМ2DЃЉЁЃ
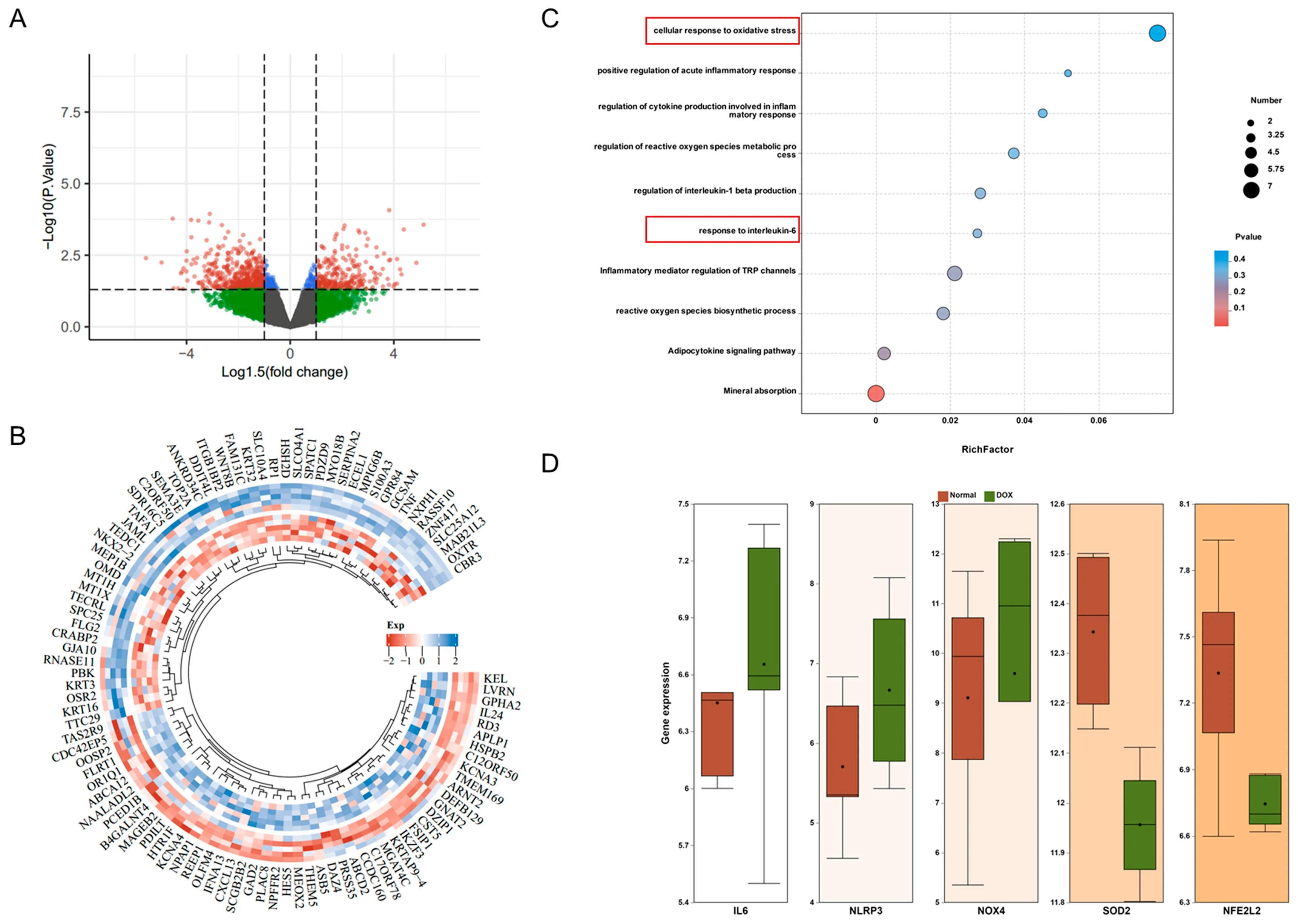
ЭМ2 GEOЗжЮіЩИбЁЧБдкАаЕу
ЃЈAЃЉЖдеезщгыАЂУЙЫизщВювьБэДяЛљвђЃЈDEGsЃЉЛ№ЩНЭМЃЈКьЩЋЃКЯджјЩЯЕїЛљвђЃЛТЬЩЋЃКЯджјЯТЕїЛљвђЃЛРЖЩЋЃКБЖЪ§БфЛЏЯджјЕЋPжЕЮоЭГМЦбЇвтвхЛљвђЃЛЛвЩЋЃКЮоЯджјВювьЛљвђЃЉЃЛЃЈBЃЉЛљвђБОЬхЃЈGOЃЉЗжЮіЛЗаЮЭМЃЌАќРЈЯИАћзщЗжЃЈCCЃЉЁЂЗжзгЙІФмЃЈMFЃЉгыЩњЮябЇЙ§ГЬЃЈBPЃЉЃЛЃЈCЃЉОЉЖМЛљвђгыЛљвђзщАйПЦШЋЪщЃЈKEGGЃЉИЛМЏЗжЮіЦјХнЭМЃЛЃЈDЃЉIL-6ЁЂNLRP3ЁЂNOX4ЁЂSOD2ЁЂNfe2l2ЛљвђЫЎЦНЯфЯпЭМЁЃ
2.3 ЧтЦјМѕЧсАЂУЙЫигеЕМаЁЪѓИЮзщжЏЯИАћЕђЭі
НјвЛВНМьВтАЂУЙЫиДІРэаЁЪѓИЮзщжЏЯИАћЕђЭіЧщПіЁЃЭИЩфЕчОЕЃЈTEMЃЉНсЙћЯдЪОЃЌгые§ГЃаЁЪѓЯрБШЃЌАЂУЙЫизщаЁЪѓИЮЯпСЃЬхсебЯжиЪмЫ№ЁЂНсЙЙВЛЭъећЃЈЭМ3AЃЉЁЃTunelШОЩЋЯдЪОЃЌгыЖдеезщЯрБШЃЌАЂУЙЫизщИЮЫ№ЩЫЧјгђЕђЭібєадЯИАћДѓСПОлМЏЃЛИЛЧтбЮЫЎДІРэПЩЛКНтАЂУЙЫигеЕМЕФИЮЯИАћЕђЭіЃЈЭМ3B,CЃЉЁЃ
ДЫЭтЃЌЕААзУтвпгЁМЃЃЈWestern blotЃЉНсЙћЯдЪОЃЌАЂУЙЫизщBax/Bcl-2БШжЕЩ§ИпЃЌАыызЬьЖЌУИ-3ЃЈcaspase-3ЃЉЫЎЦНЩЯЩ§ЃЛИјгшИЛЧтбЮЫЎКѓЃЌЩЯЪіЕААзЫЎЦНЯджјНЕЕЭЃЈЭМ3DЈCFЃЉЁЃзлЩЯЃЌИЛЧтбЮЫЎПЩгааЇМѕЧсАЂУЙЫиЫљжТИЮзщжЏЯпСЃЬхЫ№ЩЫгыЯИАћЕђЭіЁЃ

ЭМ3 ЧтЦјМѕЩйАЂУЙЫигеЕМаЁЪѓИЮзщжЏЯИАћЕђЭі
ЃЈAЃЉИЮзщжЏЯпСЃЬхЭИЩфЕчОЕЭМЃЈБъГп=2.0 ІЬmЛђ1.0 ІЬmЃЌn=3ЃЌКьЩЋМ§ЭЗЪОЯпСЃЬхсеЖЯСбЃЉЃЛЃЈB,CЃЉИЮзщжЏTunelШОЩЋЃЈБъГп=100 ІЬmЛђ50 ІЬmЃЌn=3ЃЉЃЛЃЈDЈCFЃЉИЮзщжЏBax/Bcl-2гыCaspase-3ЕААзБэДяМАЖЈСПЃЈn=4ЃЉЁЃЪ§ОнвдОљжЕЁРSEMБэЪОЁЃ*p<0.05ЃЌ**p<0.01 vs. ЖдеезщЃЛp<0.05 vs. АЂУЙЫизщЁЃ
2.4 ЧтЦјгааЇвжжЦАЂУЙЫигеЕМЕФИЮзщжЏбѕЛЏгІМЄ
ЭЌВНМьВтИЮзщжЏбѕЛЏгІМЄЫЎЦНЁЃНсЙћЯдЪОЃЌАЂУЙЫиДІРэаЁЪѓИЮзщжЏзмГЌбѕЛЏЮяЦчЛЏУИЃЈT-SODЃЉгыЙ§бѕЛЏЧтУИЃЈCATЃЉЛюадЯджјНЕЕЭЃЈЭМ4A,BЃЉЁЃЭЌЪБМьВтжЌжЪЙ§бѕЛЏВњЮяБћЖўШЉЃЈMDAЃЉгы4-єЧЛљШЩЯЉШЉЃЈ4-HNEЃЉЫЎЦНЃЌАЂУЙЫизщИЮзщжЏMDAКЌСПЩ§ИпЃЈЭМ4CЃЉЃЌMDAЕААзБэДяЩЯЕїЃЈЭМ4DЃЉЃЛУтвпзщЛЏЃЈIHCЃЉгыWestern blotНсЙћЯдЪО4-HNEЕААзЫЎЦНврЯджјЩ§ИпЃЈЭМ4EЈCGЃЉЁЃ
живЊЕФЪЧЃЌИЛЧтбЮЫЎДІРэПЩЯджјЬсЩ§ПЙбѕЛЏвђзгЃЈT-SODЁЂCATЃЉЫЎЦНЃЌНЕЕЭжЌжЪЙ§бѕЛЏВњЮяЃЈMDAЁЂ4-HNEЃЉКЌСПЁЃ
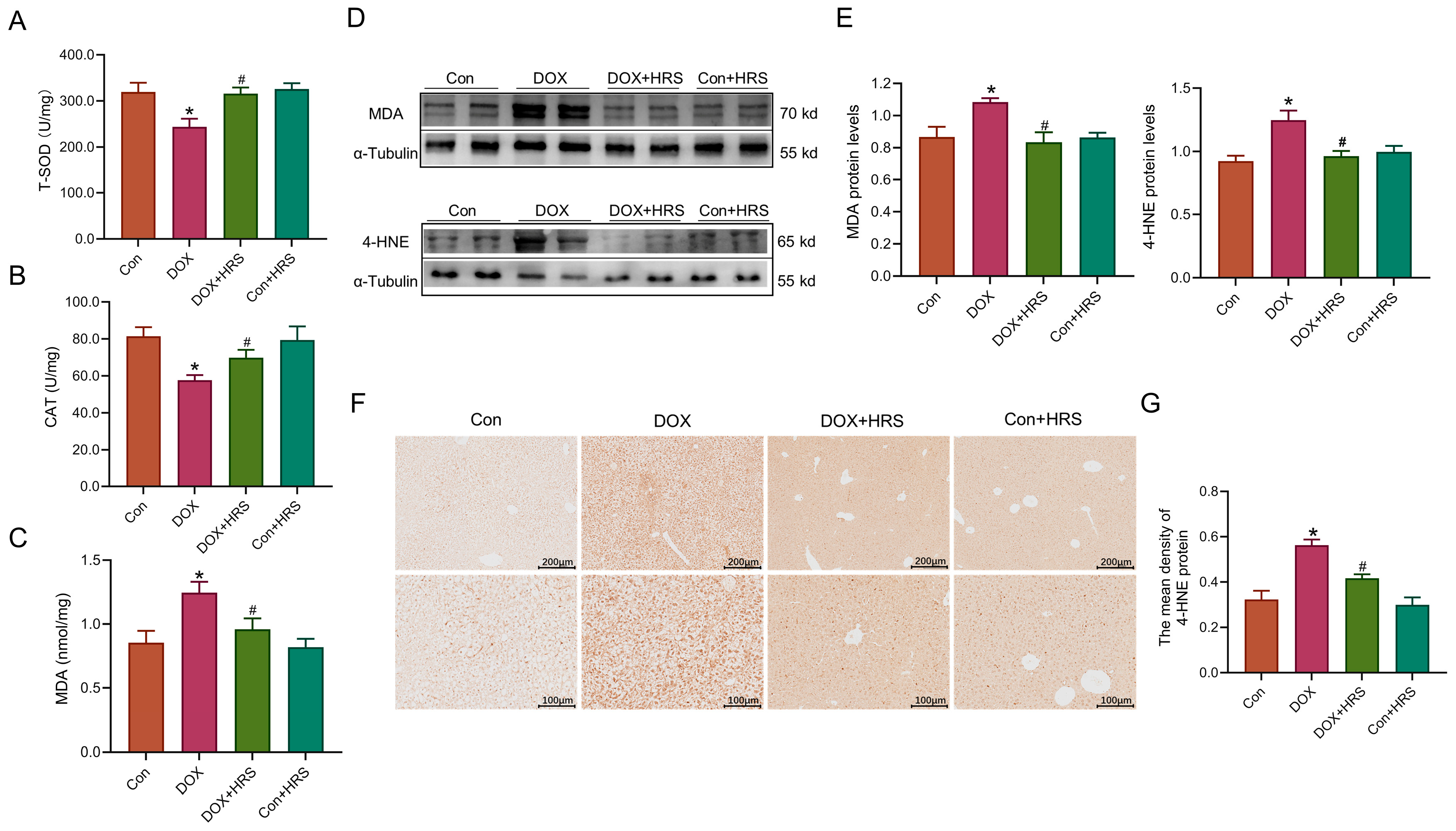
ЭМ4 ЧтЦјгааЇвжжЦАЂУЙЫигеЕМЕФИЮзщжЏбѕЛЏгІМЄ
ЃЈA,BЃЉИЮзщжЏT-SODгыCATЛюадЃЈn=6ЃЉЃЛЃЈCЃЉИЮзщжЏMDAКЌСПЃЈn=6ЃЉЃЛЃЈD,EЃЉWestern blotМьВтMDAгы4-HNEЕААзБэДяМАЖЈСПЃЈn=4ЃЉЃЛЃЈF,GЃЉУтвпзщЛЏМьВт4-HNEЕААзБэДяМАЖЈСПЃЈБъГп=200 ІЬmЛђ100 ІЬmЃЌn=3ЃЉЁЃЪ§ОнвдОљжЕЁРSEMБэЪОЁЃ*p<0.05 vs. ЖдеезщЃЛp<0.05 vs. АЂУЙЫизщЁЃ
2.5 ЧтЦјгааЇвжжЦАЂУЙЫигеЕМЕФИЮзщжЏбзжЂЗДгІ
ЗжЮіАЂУЙЫиДІРэаЁЪѓДйбзвђзгЫЎЦНЁЃУИСЊУтвпЮќИНЪдбщЃЈELISAЃЉНсЙћЯдЪОЃЌАЂУЙЫизщаЁЪѓбЊЧхДйбзвђзгIL-6ЁЂАзЯИАћНщЫи-1ІТЃЈIL-1ІТЃЉгыжзСіЛЕЫРвђзг-ІСЃЈTNF-ІСЃЉЫЎЦНЯджјЩ§ИпЃЈЭМ5AЈCCЃЉЃЛИЛЧтбЮЫЎДІРэКѓЃЌЩЯЪівђзгЫЎЦНЯджјЯТНЕЃЈЭМ5AЈCCЃЉЁЃ
ЭЌЪБЃЌАЂУЙЫизщаЁЪѓИЮзщжЏNLRP3бзжЂаЁЬхЕААзБэДяЯджјЩ§ИпЃЈЭМ5D,EЃЉЃЌИЛЧтбЮЫЎПЩЪЙЦфУїЯдНЕЕЭЁЃWestern blotгыУтвпзщЛЏНсЙћЯдЪОЃЌАЂУЙЫизщИЮзщжЏIL-6ЕААзЫЎЦНЩ§ИпЃЌОИЛЧтбЮЫЎДІРэКѓЯТНЕЃЈЭМ5DЈCGЃЉЁЃЩЯЪіНсЙћБэУїЃЌИЛЧтбЮЫЎПЩгааЇЛКНтАЂУЙЫигеЕМЕФДйбзвђзгМЄЛюЁЃ

ЭМ5 ЧтЦјЯджјЛКНтАЂУЙЫигеЕМЕФбзжЂЗДгІ
ЃЈAЈCCЃЉELISAМьВтбЊЧхIL-6ЁЂIL-1ІТЁЂTNF-ІСКЌСПЃЈn=6ЃЉЃЛЃЈD,EЃЉWestern blotМьВтNLRP3гыIL-6ЕААзБэДяМАЖЈСПЃЈn=4ЃЉЃЛЃЈF,GЃЉУтвпзщЛЏМьВтIL-6ЕААзБэДяМАЖЈСПЃЈБъГп=200 ІЬmЛђ100 ІЬmЃЌn=3ЃЉЁЃЪ§ОнвдОљжЕЁРSEMБэЪОЁЃ*p<0.05ЃЌ**p<0.01 vs. ЖдеезщЃЛp<0.05 vs. АЂУЙЫизщЁЃ
2.6 ЧтЦјМЄЛюNrf2/HO-1ЭЈТЗЛКНтАЂУЙЫиаЁЪѓИЮЫ№ЩЫ
НјвЛВНЬНОПАЂУЙЫиДІРэаЁЪѓИЮзщжЏNrf2/HO-1аХКХЭЈТЗЁЃЪЕЪБгЋЙтЖЈСПPCRЃЈQ-PCRЃЉНсЙћЯдЪОЃЌАЂУЙЫизщаЁЪѓИЮзщжЏNfe2l2ЃЈNrf2ЛљвђЃЉгыHmox1ЃЈбЊКьЫибѕКЯУИ-1ЃЌHO-1ЛљвђЃЉmRNAБэДяЯТНЕЃЈЭМ6A,BЃЉЁЃУтвпзщЛЏНсЙћЯдЪОЃЌАЂУЙЫизщИЮзщжЏNrf2гыHO-1ЕААзБэДяЯджјНЕЕЭЃЈЭМ6CЈCEЃЉЃЛWestern blotНсЙћНјвЛВНжЄЪЕЃЌKeap1ЁЂNrf2гыHO-1ЕААзЫЎЦНЯТНЕЃЈЭМ6FЈCIЃЉЁЃ
жЕЕУзЂвтЕФЪЧЃЌИЛЧтбЮЫЎДІРэКѓЃЌЩЯЪіНЕЕЭЕФNrf2гыHO-1ЛљвђМАЕААзЫЎЦНОљГіЯжВЛЭЌГЬЖШЛжИДЁЃ

ЭМ6 ЧтЦјМЄЛюNrf2/HO-1ЭЈТЗЛКНтАЂУЙЫиаЁЪѓИЮЫ№ЩЫ
ЃЈA,BЃЉИЮзщжЏNfe2l2гыHmox1ЛљвђБэДяЃЈn=3ЃЉЃЛЃЈCЈCEЃЉУтвпзщЛЏМьВтNrf2гыHO-1ЕААзМАЖЈСПЃЈБъГп=100 ІЬmЃЌn=3ЃЉЃЛЃЈFЈCIЃЉWestern blotМьВтKeap1ЁЂNrf2ЁЂHO-1ЕААзБэДяМАЖЈСПЃЈn=4ЃЉЁЃЪ§ОнвдОљжЕЁРSEMБэЪОЁЃ*p<0.05 vs. ЖдеезщЃЛp<0.05 vs. АЂУЙЫизщЁЃ
2.7 Nrf2/HO-1ЭЈТЗВЮгыЧтЦјЖдАЂУЙЫиДІРэHepG2ЯИАћЕФБЃЛЄзїгУ
ЮЊНјвЛВНУїШЗЧтЦјЛКНтАЂУЙЫигеЕМЯИАћЫ№ЩЫЕФзїгУЃЌВЩгУАЂУЙЫиЁЂNrf2МЄЖЏМСЃЈЫеФОЭЊAЃЌSAЃЉгыNrf2вжжЦМСЃЈML385ЃЉДІРэHepG2ЯИАћЁЃCCK8НсЙћЯдЪОЃЌАЂУЙЫизщЯИАћЛюСІЯджјНЕЕЭЃЈЭМ7AЃЉЃЛСїЪНЯИАћЪѕНсЙћЯдЪОАЂУЙЫизщЕђЭіЯИАћдіЖрЃЈЭМ7B,CЃЉЁЃЧтЦјгыSAДІРэПЩЯджјЬсЩ§ЯИАћЛюСІЁЂНЕЕЭЕђЭіТЪЃЌЖјML385ПЩФцзЊЧтЦјЕФБЃЛЄзїгУЃЈЭМ7AЈCCЃЉЁЃ
ДЫЭтЃЌАЂУЙЫизщжЌжЪROSЫЎЦНЩ§ИпЃЌЧтЦјгыSAДІРэПЩЪЙЦфЯджјНЕЕЭЃЈЭМ7DЃЉЁЃELISAНсЙћЯдЪОЃЌАЂУЙЫизщЯИАћХрбјвКжаIL-6ЁЂIL-1ІТЁЂTNF-ІСЕШДйбзвђзгЫЎЦНЯджјЩ§ИпЃЌЧтЦјгыSAДІРэПЩНЕЕЭЦфЫЎЦНЃЈЭМ7EЈCGЃЉЁЃQ-PCRгыWestern blotНсЙћЯдЪОЃЌАЂУЙЫизщNrf2гыHO-1ЛљвђМАЕААзБэДяЯджјНЕЕЭЃЈЭМ7HЈCLЃЉЃЛЧтЦјгыSAПЩЯджјЩЯЕїЦфБэДяЃЌЖјML385ПЩвжжЦЧтЦјЕФИУзїгУЁЃ

ЭМ7 ЧтЦјЭЈЙ§ЕїПиNrf2ЭЈТЗЛКНтHepG2ЯИАћЫ№ЩЫ
ЃЈAЃЉАЂУЙЫиЁЂЧтЦјЁЂML385ЁЂSAДІРэКѓHepG2ЯИАћЛюСІЃЈn=6ЃЉЃЛЃЈB,CЃЉСїЪНЯИАћЪѕМьВтИїзщЕђЭіЯИАћЃЈn=3ЃЉЃЛЃЈDЃЉСїЪНЯИАћЪѕМьВтBODIPY 581/591 C11гЋЙтЮќЪеЙтЦзЃЈn=3ЃЉЃЛЃЈEЈCGЃЉЯИАћХрбјвКIL-6ЁЂIL-1ІТЁЂTNF-ІСКЌСПЃЈn=3ЃЉЃЛЃЈH,IЃЉQ-PCRМьВтNfe2l2гыHmox1 mRNAЫЎЦНЃЈn=3ЃЉЃЛЃЈJЈCLЃЉWestern blotМьВтNrf2гыHO-1ЕААзЫЎЦНЃЈn=3ЃЉЁЃЪ§ОнвдОљжЕЁРSEMБэЪОЁЃ**p<0.01 vs. ЖдеезщЃЛp<0.05 vs. АЂУЙЫизщЃЛ&p<0.05 vs. АЂУЙЫи+ЧтЦјзщЁЃ
3 ЬжТл
АЉжЂШдЪЧЮЃКІШЫРрНЁПЕЕФИпЗЂМВВЁЃЌЗЂВЁТЪГЌ440/10ЭђШЫЃЌУПФъаТдіШЗеяВЁР§дМ1930Эђ[17]ЁЃАЂУЙЫизїЮЊньЛЗРрПЙЩњЫиЃЌЙуЗКгУгкЖржжЖёаджзСіЛЏСЦЁЃЕЋДѓМССПЛђГЄЦкЪЙгУАЂУЙЫиПЩв§ЗЂбЯжиИЮЖОадгыаФдрЖОадЃЌГЃЕМжТЛЏСЦжаЖЯЛђМССПЯТЕї[18]ЁЃвђДЫЃЌЙмПиАЂУЙЫиЖОИБзїгУЖдАЉжЂЛМепгааЇжЮСЦжСЙиживЊЁЃ
АЂУЙЫигеЕМИЮЖОадЕФЗжзгЛњжЦжївЊЮЊЃКвЉЮядкИЮдрДњаЛЙ§ГЬжаВњЩњROSЃЌЦЦЛЕбѕЛЏЛЙдЮШЬЌ[19]ЁЃАЂУЙЫиПЩЗЂЩњПЩФцадбѕЛЏЗДгІЃЌдкNADPHЛЙдУИДпЛЏЯТЩњГЩАыѕЋжаМфЬх[19]ЃЌНјЖјВњЩњГЌбѕвѕРызгЁЂЙ§бѕЛЏЧтЕШROSЃЌВЂПЩФмЩЯЕїNQO1БэДя[20]ЁЃЭЌЪБЃЌвЛбѕЛЏЕЊЃЈNOЃЉПЩгыO₂ЛђO₂⁻ЗДгІЩњГЩЛюадЕЊЃЈRNSЃЉЃЌв§ЗЂжЌжЪЙ§бѕЛЏгыDNAЫ№ЩЫ[21]ЁЃбаОПЗЂЯжАЂУЙЫижЮСЦЦкМфбѕЛЏгІМЄБъжОЮя8-єЧЛљЭббѕФёмеЃЈ8-OHdGЃЉЫЎЦНЩ§Ип[22]ЁЃДЫЭтЃЌбѕЛЏЫ№ЩЫПЩМЄЛюУтвпЯИАћЃЌгеЗЂбзжЂЗДгІЁЃгабаОПБэУїЃЌАЂУЙЫиПЩЭЈЙ§МЄЛюбзжЂЭЈТЗМгжиЖОадЫ№ЩЫЃЌШчгеЕМNLRP3НщЕМЕФаФМЁЯИАћНЙЭі[23]ЁЂЩЯЕїCD45гыЕЅКЫЯИАћЧїЛЏЕААз-1ЃЈMCP-1ЃЉБэДя[22]ЁЂДйНјИЮзщжЏДйбзвђзгЪЭЗХ[24]ЁЃвђДЫЃЌНЕЕЭбѕЛЏгІМЄЪЧЛКНтАЂУЙЫиИЮЖОадЕФгааЇВпТдЁЃ
ЧтЦјЪЧвЛРрОпгаживЊЩњЮябЇаЇгІЕФБЃЛЄадЦјЬхЃЌОпБИПЙбѕЛЏЁЂПЙбзЁЂПЙЕђЭіЁЂПЙЬњЫРЭіЕШзїгУЃЌБЛЪгЮЊбѕЛЏЛЙдЮШЬЌЕФживЊЕїПивђзг[25,26,27]ЁЃбаОПжЄЪЕЃЌЭтдДадВЙГфЧтЦјПЩЛКНтЖржжИЮЫ№ЩЫЁЂЕїПиЬЧжЌДњаЛЃЌЖдЮЌГжИЮдрЮШЬЌОпгаживЊзїгУ[26,28]ЁЃБОбаОПЗЂЯжЃЌЧтЦјПЩЯджјНЕЕЭАЂУЙЫиДІРэКѓALTЁЂASTЁЂALPЫЎЦНЃЌМѕЧсИЮзщжЏЫ№ЩЫЁЂвжжЦИЮЯИАћЕђЭіЃЈЭМ1ЃЉЁЃЧтЦјПЩбЁдёадЧхГ§єЧздгЩЛљЁЂЙ§бѕбЧЯѕЛљвѕРызгЕШROSгыздгЩЛљ[11,29]ЁЃЮвУЧЭЦВтЦфБЃЛЄзїгУгывжжЦбѕЛЏгІМЄЯрЙиЃЌНсЙћвржЄЪЕЧтЦјПЩФцзЊАЂУЙЫиЕМжТЕФИЮзщжЏбѕЛЏгІМЄЫЎЦНЩ§ИпЃЌдіЧППЙбѕЛЏФмСІЃЈЭМ4ЃЉЁЃ
баОПБэУїЃЌЧтЦјВЛНіПЩЭЈЙ§ПЙбѕЛЏМѕЧсИЮЫ№ЩЫЃЌЛЙФмвжжЦбзжЂЗДгІ[30]ЁЃРрЫЦбаОПжЄЪЕЃЌИЛЧтбЮЫЎЕФЩёОБЃЛЄзїгУгыШБбЊдйЙрзЂЙ§ГЬжаЕФбзжЂМАбѕЛЏгІМЄЕїПиЯрЙи[31]ЁЃЧтЦјПЩЭЈЙ§ЯТЕїIL-1ІТЁЂIL-6ЁЂTNF-ІСЕШДйбзвђзгМАИпЧЈвЦТЪзхЕААзB1ЃЈHMGB-1ЃЉЁЂNF-ІЪBЕШДйбззЊТМвђзгЃЌМѕЧсбѕЛЏгІМЄНщЕМЕФбзжЂадзщжЏЫ№ЩЫ[32,33]ЁЃБОбаОПНсЙћЯдЪОЃЌЧтЦјПЩЯджјвжжЦАЂУЙЫигеЕМЕФбзжЂЗДгІЃЌвжжЦбзжЂаЁЬхаЮГЩЁЂНЕЕЭбзжЂвђзгБэДяЃЈЭМ5ЃЉЁЃ
Nrf2ЪЧМцОпПЙбзгыПЙбѕЛЏзїгУЕФзЊТМвђзг[34]ЁЃбаОПБэУїЃЌЧтЦјПЩЕїПиNrf2аХКХЭЈТЗЃЌдкЖржжМВВЁФЃаЭжаЗЂЛгПЙбѕЛЏЁЂПЙбзЁЂПЙЬњЫРЭіЕШБЃЛЄзїгУ[25,27,35]ЁЃЬивьадЩЯЕїNrf2БэДяПЩЛКНтАЂУЙЫигеЕМЕФИЮЫ№ЩЫ[36]ЁЃNrf2/HO-1аХКХЭЈТЗЪЧДњаЛЯрЙижЌЗОадИЮВЁЕФЧБдкжЮСЦАаЕу[37]ЁЃЕЋЧтЦјФмЗёЭЈЙ§МЄЛюNrf2ИФЩЦАЂУЙЫиИЮЫ№ЩЫЩаВЛУїШЗЁЃЮЊДЫЃЌБОбаОППЊеЙЬхФкЭтЪЕбщЃЌНсЙћЯдЪОАЂУЙЫиФЃаЭжаNrf2БэДяНЕЕЭЃЌЖјЧтЦјПЩгааЇМЄЛюNrf2БэДяЁЃЯИАћЪЕбщжаЪЙгУNrf2вжжЦМСML385гыМЄЖЏМСSA[38,39]ЃЌНсЙћЯдЪОML385ПЩВПЗжвжжЦЧтЦјЖдЯИАћЙІФмЕФБЃЛЄзїгУЃЌгАЯьЦфПЙбзгыПЙбѕЛЏаЇгІЃЈЭМ8ЃЉЁЃживЊЕФЪЧЃЌNrf2МЄЖЏМСПЩФЃФтЧтЦјЕФБЃЛЄзїгУЃЌЬсЪОЧтЦјжСЩйВПЗжЭЈЙ§МЄЛюNrf2БэДяЗЂЛгИЮБЃЛЄаЇгІЁЃЩЯЪіНсЙћБэУїЃЌЧтЦјПЩЭЈЙ§ЕїПиNrf2/HO-1ЭЈТЗЗЂЛгПЙбзЁЂПЙбѕЛЏзїгУЃЌДгЖјМѕЧсАЂУЙЫигеЕМЕФИЮЖОадЁЃ
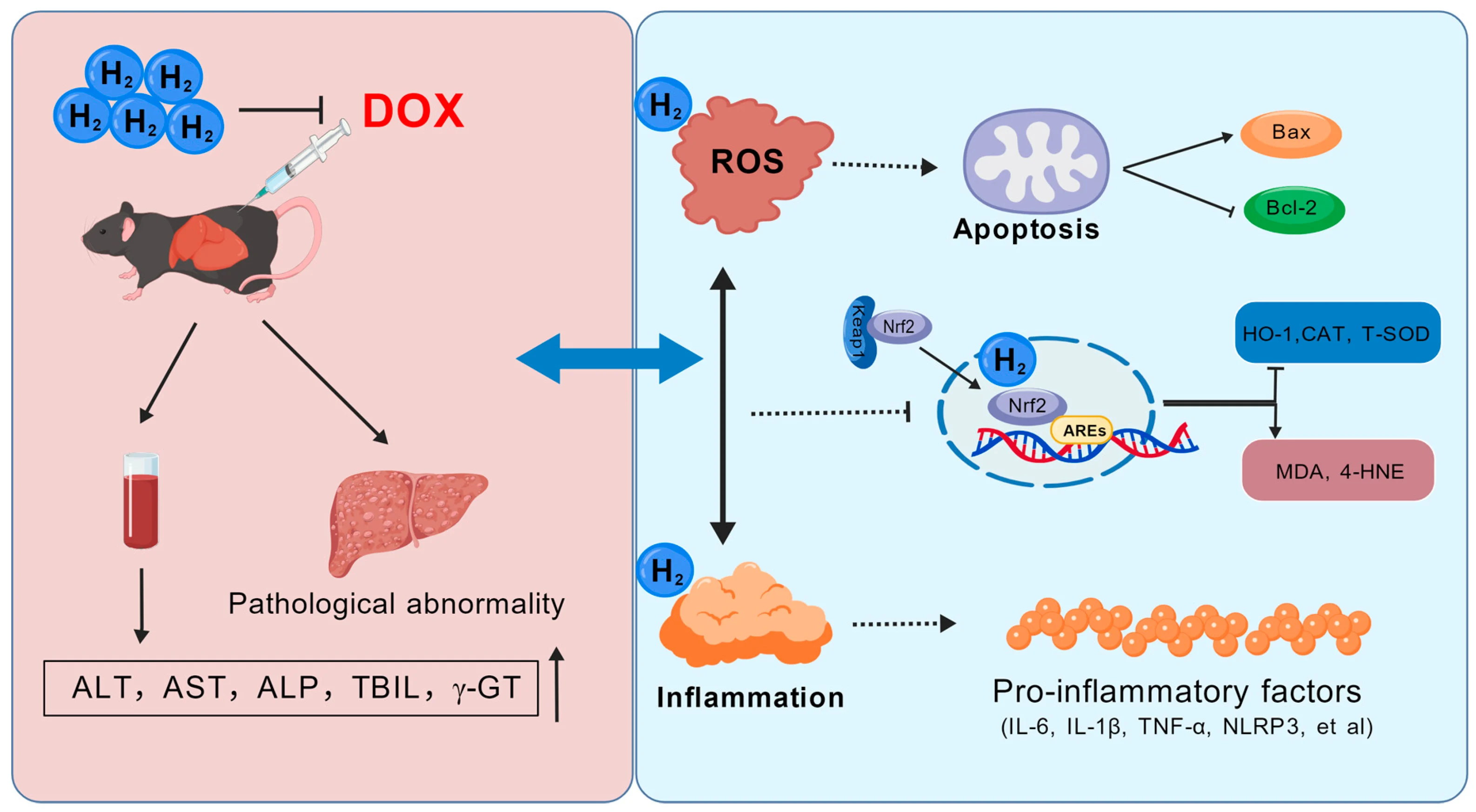
ЭМ8 ЧтЦјозПЙАЂУЙЫигеЕМИЮЫ№ЩЫЕФзїгУЛњжЦЪОвтЭМ
АЂУЙЫиПЩв§ЗЂИЮдрЩњЛЏгыВЁРэвьГЃЃЌДйНјROSЩњГЩЁЂгеЕМЯпСЃЬхвРРЕадЯИАћЕђЭіЃЛвжжЦKeap1гыNrf2БэДяЃЌНјЖјзшЖЯNrf2ЯТгЮHO-1ЁЂCATЁЂT-SODЕШПЙбѕЛЏаХКХЭЈТЗЃЛЭЌЪБЩ§ИпMDAЁЂ4-HNEЕШжЌжЪЙ§бѕЛЏВњЮяЃЌгеЗЂбзжЂЗДгІВЂДйНјДйбзвђзгЪЭЗХЁЃгыжЎЯрЗДЃЌЧтЦјПЩЭЈЙ§ЕїПиNrf2ЗЂЛгБЃЛЄзїгУЃЌМѕЧсАЂУЙЫигеЕМЕФИЮЙІФмвьГЃЃЌЛКНтбѕЛЏгІМЄгыбзжЂЗДгІЁЃ
БОбаОПШдДцдквЛЖЈОжЯоадЁЃжївЊЮЊНідкЬхЭтЫЎЦНЬНОПЧтЦјЖдNrf2ЕФЕїПизїгУЃЌКѓајашПЊеЙЬхФкЪЕбщНјвЛВНЭъЩЦЃЛДЫЭтЃЌЫфЙлВьЕНЧтЦјЖдNrf2ЕФЕїПиаЇгІЃЌЕЋЦфдкЩњЮяЬхФкЕФШЗЧаЕїПиЛњжЦШдашЩюШыбаОПЁЃ
4 ВФСЯгыЗНЗЈ
4.1 ЪЕбщЖЏЮя
SPFМЖC57BL/6NаладаЁЪѓЃЌЬхжи22~24 gЃЌЙКзджаЙњАВбєКгФЯЫЙПЦБДЫЙЩњЮяММЪѕгаЯоЙЋЫОЁЃаЁЪѓЫЧбјгкЪЕбщЖЏЮяжааФЃЌЮТЖШгыЪЊЖШПЩПиЁЃЫљгаЖЏЮяЪЕбщВйзїЗћКЯЁЖЪЕбщЖЏЮяЙмРэгыЪЙгУЙњМвжИФЯЁЗЃЌВЂОКгББжавНвЉДѓбЇЖЏЮяЪЕбщТзРэЮЏдБЛсХњзМЃЈТзРэХњзМКХЃКKJLL(D)20251026ЃЉЁЃ
40жЛC57BL/6NаЁЪѓЫцЛњЗжЮЊ4зщЃКЖдеезщЃЈConЃЉЁЂАЂУЙЫизщЃЈDOXЃЉЁЂАЂУЙЫи+ИЛЧтбЮЫЎзщЃЈDOX+HRSЃЉЁЂЖдее+ИЛЧтбЮЫЎзщЃЈCon+HRSЃЉЁЃАЂУЙЫизщгыАЂУЙЫи+ИЛЧтбЮЫЎзщаЁЪѓИЙЧЛзЂЩфАЂУЙЫиШмвКЃЌМССП4 mg/kgЃЌ4жмИјвЉ4ДЮЁЃИЛЧтбЮЫЎзщгыЖдее+ИЛЧтбЮЫЎзщУПШеИЙЧЛзЂЩфИЛЧтбЮЫЎЃЌМССП10 mL/kgЁЃЖдеезщИјгшЕШЬхЛ§ЩњРэбЮЫЎЁЃ
ЪЕбщНсЪјКѓГЦСПИїзщаЁЪѓЬхжиЃЌШ§фхввДМЃЈ200 mg/kgЃЉТщзэКѓВЩМЏИЮЁЂЦЂзщжЏЃЌМЦЫуИЮдржИЪ§гыЦЂдржИЪ§ЃЈдрЦїжЪСП/ЬхжЪСПЃЉЁЃ
4.2 ИЛЧтбЮЫЎжЦБИ
АДееЫЕУїЪщЃЈЩЯКЃЛнУРвНСЦПЦММЃЉжЦБИИЛЧтбЮЫЎЁЃВЩгУЧтЦјЗЂЩњзАжУЃЌдк0.4 MPaЬѕМўЯТНЋЧтЦјЭЈШыЩњРэбЮЫЎ6 hжСЙ§БЅКЭзДЬЌЁЃИЛЧтбЮЫЎЯжХфЯжгУЃЌЮЌГжХЈЖШ0.6 mmol/LЃЌЪЙгУеыаЭЧтЦјДЋИаЦїМрВтЧтЦјХЈЖШ[27,40]ЁЃ
4.3 ЪдМСгыПЙЬх
ЪдМСЃКNrf2вжжЦМСML385ЃЈHY-100523ЃЌMCEЃЉЁЂNrf2МЄЖЏМСЫеФОЭЊAЃЈSAЃЌHY-113556ЃЌMCEЃЉЁЂзмГЌбѕЛЏЮяЦчЛЏУИЃЈA001-1ЃЌФЯОЉНЈГЩЃЉЁЂБћЖўШЉЃЈA003-1ЃЌФЯОЉНЈГЩЃЉЁЂЙ§бѕЛЏЧтУИЃЈA007-1ЃЌФЯОЉНЈГЩЃЉЁЂаЁЪѓ/ШЫIL-6 ELISAЪдМСКаЃЈE-EL-M0044/E-EL-H6156ЃЌElabscienceЃЉЁЂаЁЪѓ/ШЫTNF-ІСЃЈEK0527/EK0525ЃЌBosterЃЉЁЂаЁЪѓIL-1ІТЃЈEK0394/EK0392ЃЌBosterЃЉЁЂRNAЬсШЁЪдМСКаЃЈDP419ЃЌЬьИљЃЉЁЂPrimeScript™ RTЪдМСКаЃЈRR047AЃЌTakaraЃЉЁЂSYBR-Green PCRЪдМСКаЃЈRR820AЃЌTakaraЃЉЁЂTunelЪдМСКаЃЈG1507ЃЌServicebioЃЉЁЃ
ПЙЬхЃКBcl-2ЃЈGB153375ЃЌServicebioЃЉЁЂBaxЃЈGB11007ЃЌServicebioЃЉЁЂCaspase 3ЃЈ14220ЃЌCSTЃЉЁЂMDAЃЈab243066ЃЌAbcamЃЉЁЂ4-HNEЃЈARG23717ЃЌArigoЃЉЁЂIL-6ЃЈDF6087ЃЌAffinityЃЉЁЂNLRP3ЃЈBA3677ЃЌBosterЃЉЁЂNrf2ЃЈGB115673ЃЌServicebioЃЉЁЂHO-1ЃЈGB12104ЃЌServicebioЃЉЁЂKeap1ЃЈbs-4900RЃЌBIOSSЃЉЁЂІС-TubulinЃЈGB11200ЃЌServicebioЃЉЁЃ
4.4 ЩњЛЏМьВт
ВЩгУБШЩЋЗЈМьВтбЊЧхИЮЙІФмЩњЛЏжИБъЃЌЪЙгУШЋздЖЏЩњЛЏЗжЮівЧЃЈBK-400ЃЌВЉПЦЃЉАДееЫЕУїЪщМьВтALTЁЂASTЁЂALPЁЂTBILЁЂІУ-GTЫЎЦНЁЃ
4.5 ВЁРэШОЩЋ
ЫеФОЫи-вСКьЃЈHEЃЉШОЩЋЙлВьИЮзщжЏЛљБОНсЙЙЁЃЪЏРЏАќТёИЮЧаЦЌЃЈ5 ІЬmЃЉОЖўМзБНЭбРЏЁЂЬнЖШОЦОЋЭбЫЎКѓЃЌЫеФОЫиШОЩЋЁЂбЮЫсОЦОЋЗжЛЏЁЂвСКьИДШОЃЌЬнЖШОЦОЋЭбЫЎЁЂЖўМзБНЭИУїЃЌжаадЪїНКЗтЦЌЁЃ
MassonШ§ЩЋШОЩЋЦРЙРИЮЯЫЮЌЛЏЁЃЭбРЏКѓЧаЦЌвРДЮОЫеФОЫиЁЂбЮЫсОЦОЋЁЂMassonРЖвКЁЂеєСѓЫЎЁЂРіДККьКьЁЂСзютЫсЁЂБНАЗРЖДІРэЃЌОЦОЋЭбЫЎЁЂЖўМзБНЭИУїЃЌжаадЪїНКЗтЦЌЁЃ
ЬьРЧаЧКьШОЩЋЦРЙРИЮЯЫЮЌЛЏЁЃЭбРЏИДЫЎКѓЬьРЧаЧКьШОЩЋЃЌОЦОЋЭбЫЎЁЂЖўМзБНЭИУїЃЌжаадЪїНКЗтЦЌЃЌЯдЮЂОЕЯТВЩМЏЭМЯёЁЃ
4.6 ЭИЩфЕчОЕ
ЭИЩфЕчОЕЙлВьЯпСЃЬхГЌЮЂНсЙЙЁЃаЁЪѓЩюЖШТщзэКѓПьЫйЗжРыИЮзщжЏЃЌЧаГЩЁм1 mm³аЁПщЃЌЙЬЖЈКѓЬнЖШОЦОЋЭбЫЎЁЂЛЗбѕЪїжЌАќТёЃЌГЌБЁЧаЦЌО4%ДзЫсгЫШОЩЋЃЌЭИЩфЕчОЕЃЈHT7800ЃЌШеСЂЃЉЯТЙлВьГЩЯёЁЃ
4.7 GEOЪ§ОнЗжЮі
ДгGEOЪ§ОнПтЛёШЁаОЦЌЪ§ОнМЏGSE11940ЃЈ2025Фъ9дТ1ШеЛёШЁЃЉЃЌЯТдиMINiMLИёЪНдЪМЪ§ОнВЂДІРэЁЃЪЙгУRШэМўЃЈ4.4.3АцЃЉНјааБГОАаЃе§гыЗжЮЛЪ§БъзМЛЏЃЌЬНеыЦЅХфЛљвђЗћКХЃЌЖрЬНеыЖдгІЭЌвЛЛљвђЪБШЁОљжЕЁЃВЩгУLimmaАќЃЈ3.60.3АцЃЉЩИбЁВювьБэДяЛљвђЃЌуажЕ|log₂FC|>1ЧваЃе§КѓP<0.05ЃЌЛцжЦЛ№ЩНЭМЁЃЪЙгУclusterProfilerАќЃЈ4.14.6АцЃЉНјааGOЃЈЯИАћзщЗжЁЂЗжзгЙІФмЁЂЩњЮябЇЙ§ГЬЃЉгыKEGGИЛМЏЗжЮіЃЌаЃе§КѓP<0.05ЮЊЯджјИЛМЏЃЌЗжБ№вдЛЗаЮЭМгыЦјХнЭМеЙЪОЁЃЬсШЁIL-6ЁЂNLRP3ЁЂNOX4ЁЂSOD2ЁЂNfe2l2БэДяЪ§ОнЃЌЯфЯпЭМБШНЯзщМфВювьЁЃ
4.8 УтвпзщЛЏШОЩЋ
УтвпзщЛЏМьВтИЮзщжЏЕААзБэДяЁЃЭбРЏЧаЦЌО3%Й§бѕЛЏЧтЗтБеФкдДадЙ§бѕЛЏЮяУИЃЌФћУЪЫсбЮПЙдаоИДвКИпЮТПЙдаоИДЃЌ10%бђбЊЧх37 ЁцЗтБе1 hЁЃМгШы4-HNEЁЂIL-6ЁЂNrf2ЁЂHO-1вЛПЙ4 ЁцЗѕг§Й§вЙЃЌДЮШеМгШыHRPБъМЧЖўПЙ37 ЁцЗѕг§1 hЃЌDABЯдЩЋЃЌжаадЪїжЌЗтЦЌЃЌЯдЮЂОЕВЩМЏЭМЯёЃЌImage-Pro PlusЃЈIPP 6.0ЃЉШэМўЖЈСПбєадЯИАћЦНОљУмЖШЁЃ
4.9 TunelШОЩЋ
TunelШОЩЋЦРЙРИЮЯИАћЕђЭіЁЃЭбРЏИДЫЎКѓPBSЯДЕгЃЌЕААзУИKЃЈ20 ІЬg/mLЃЉЪвЮТДІРэ20 minЃЌPBSЯДЕгКѓМгШыгЋЙтБъМЧвКгыжизщФЉЖЫЭббѕКЫмеЫсзЊвЦУИ37 ЁцЗѕг§60 minЃЌМгШыСДУЙЧзКЭЫи-HRP 37 ЁцЗѕг§60 minЃЌDABЯдЩЋЃЌжаадЪїжЌЗтЦЌЃЌIPP 6.0ШэМўЖЈСПбєадЯИАћЦНОљУмЖШЁЃ
4.10 ЪЕЪБгЋЙтЖЈСПPCR
Q-PCRМьВтNfe2l2ЃЈNrf2ЃЉгыHmox1ЃЈHO-1ЃЉmRNAБэДяЁЃЪЙгУRNAЬсШЁЪдМСКаЬсШЁИЮзщжЏзмRNAЃЌШЁ1 ІЬg RNAОЗДзЊТМЪдМСКаКЯГЩcDNAЃЌSYBR-GreenЪдМСКаНјааQ-PCRРЉдіЃЈCFX ConnectЃЌBio-RadЃЉЃЌВЩгУ2⁻^ІЄІЄ^CtЗЈМЦЫуЯрЖдБэДяСПЃЌв§ЮяађСаМћБэ1ЁЃ
Бэ1 ЛљвђБэДяМьВтв§ЮяађСа
4.11 ЕААзУтвпгЁМЃ
ИЮзщжЏЛђHepG2ЯИАћМгШыдЄРфRIPAСбНтвКЃЌдШНЌРыаФКѓBCAЗЈВтЖЈЕААзХЈЖШЁЃSDS-PAGEЕчгОКѓзЊгЁжСPVDFФЄЃЌ5%ЭбжЌХЃФЬЗтБеЃЌМгШыBaxЁЂBcl-2ЁЂCaspase 3ЁЂMDAЁЂ4-HNEЁЂNLRP3ЁЂIL-6ЁЂKeap1ЁЂNrf2ЁЂHO-1ЁЂІС-TubulinвЛПЙ4 ЁцЗѕг§Й§вЙЃЌДЮШеМгШыHRPБъМЧЖўПЙЪвЮТЗѕг§2 hЃЌECLЛЏбЇЗЂЙтЗЈЯдгАЃЌImage JЃЈ1.8.1АцЃЉЖЈСПЬѕДјЦНОљЛвЖШжЕЁЃ
4.12 ЯИАћХрбјгыЛюСІМьВт
HepG2ЯИАћХрбјгкКЌ10%ЬЅХЃбЊЧхЁЂЧрУЙЫи-СДУЙЫиЕФDMEMХрбјЛљЃЌ37 ЁцЁЂ5% CO₂ЬѕМўЯТХрбјЁЃЙЙНЈАЂУЙЫиЯИАћЫ№ЩЫФЃаЭЃЌХЈЖШ5 ІЬMЃЌДІРэ24 hЁЃЧтЦјзщЯИАћЪЙгУЭЌИЛЧтбЮЫЎХфжЦЕФИЛЧтХрбјЛљДІРэЁЃ
CCK-8ЪдМСКаМьВтЯИАћЛюСІЁЃHepG2ЯИАћвд1ЁС10⁴Иі/ПзНгжжгк96ПзАхЃЌОАЂУЙЫиЁЂЧтЦјЁЂML385ЃЈ2 ІЬMЃЉЁЂSAЃЈ20 ІЬMЃЉДІРэКѓЃЌМгШыCCK-8ЪдМС37 ЁцЗѕг§1 hЃЌЖрЙІФмУИБъвЧЃЈVarioskan LUXЃЌШќФЌЗЩЃЉ450 nmДІМьВтЮќЙтЖШЁЃ
4.13 ELISAМьВт
ELISAМьВтбЊЧхгыЯИАћХрбјвКбзжЂвђзгЁЃЪеМЏбЊЧхгыЯИАћЩЯЧхвКЃЌАДееЫЕУїЪщМьВтIL-6ЁЂIL-1ІТЁЂTNF-ІСХЈЖШЃЌЛцжЦБъзМЧњЯпЃЌ450 nmДІВтЖЈЮќЙтЖШВЂМЦЫуБэДяЫЎЦНЁЃ
4.14 ЭГМЦбЇЗжЮі
ЪЕбщЪ§ОнВЩгУSPSS 26.0ШэМўЗжЮіЁЃМЦСПЪ§ОнОShapiroЈCWilkе§ЬЌадМьбщгыLeveneЗНВюЦыадМьбщЃЌЗћКЯе§ЬЌЗжВМЧвЗНВюЦыЕФЪ§ОнвдОљжЕЁРSEMБэЪОЃЌЕЅвђЫиЗНВюЗжЮіЃЈANOVAЃЉКѓLSDЪТКѓМьбщЃЛВЛЗћКЯе§ЬЌЗжВМЛђЗНВюВЛЦыЕФЪ§ОнВЩгУKruskalЈCWallis HМьбщЁЃPЁм0.05ЮЊВювьОпгаЭГМЦбЇвтвхЁЃЪЙгУPrism 9.0ШэМўЛцжЦЭГМЦЭМБэЁЃ
5 НсТл
злЩЯЃЌБОбаОПБэУїАЂУЙЫиПЩЭЈЙ§діЧПбѕЛЏгІМЄгыбзжЂЗДгІгеЕМИЮЖОадЃЛЖјЧтЦјПЩЭЈЙ§ЩЯЕїNrf2БэДяЗЂЛгПЙбзЁЂПЙбѕЛЏзїгУЃЌДгЖјЛКНтАЂУЙЫиЫљжТИЮЫ№ЩЫЁЃИУНсЙћЮЊЧтЦјЕФСйДВгІгУЬсЙЉСЫРэТлвРОнЁЃ
https://blog.sciencenet.cn/blog-41174-1527004.html
ЩЯвЛЦЊЃККьЯИАћзїЮЊжївЊЦЯЬбЬЧЛуЃЌИФЩЦИпКЃАЮЛЗОГЯТЕФЦЯЬбЬЧФЭСП
ЯТвЛЦЊЃКЩњУќЪМзцВЛбсбѕ
ШЋВПзїепЕФОЋбЁВЉЮФ
ШЋВПзїепЕФЦфЫћзюаТВЉЮФ
ШЋВПОЋбЁВЉЮФЕМЖС
- • ДгСуПЊЪМбЇЃЁЪжАбЪжНЬФуЛЫЎФ§НКНсЙЙ
- • ПЦбЇЭј2026Фъ3дТЪЎМбВЉЮФАёЕЅЙЋВМЃЁ
- • ШчКЮДгПЦбааЁАзНјНзЮЊзЪЩюДѓПЇЃПаТаЫбЇепЬсЩ§МЦЛЎжЕЕУСЫНт
- • ЯуИлГЧДѓDuu-Jong LeeЭХЖгЃКУцЯђПЩГжајЙцФЃЛЏгаЛњЙтЗќЕФ Y ЯЕЪмЬхздзщзАЕїПи
- • КьЫПНЊЛЈЃКжВЮядАв§жжБГКѓЕФСНАйФъШЋЧђШыЧжЪЗ
- • ПЦбаШЫдБВЛдИЩѓИхЕФЩюВудвђЃКЦРМлЬхЯЕЪЇКтгыбЇЪѕЗўЮёМлжЕШБЮЛ