博文
氢气在脓毒症相关性脑病中的保护作用:研究现状
||
氢气在脓毒症相关性脑病中的保护作用:研究现状
The Protective Effects of molecular Hydrogen in Sepsis-associated Encephalopathy: current status
研究亮点
- 氢气(H₂)可通过靶向氧化应激与神经炎症减轻脓毒症相关性脑病(SAE)。
- 作用机制包括激活Nrf2、抑制NLRP3及保护血脑屏障。
- 临床前模型(盲肠结扎穿孔、脂多糖模型)已证实其疗效。
- 现有证据受动物模型与给药方案差异限制。
- 亟需开展临床试验并探索相关生物标志物。
摘要
脓毒症相关性脑病(SAE)是脓毒症患者出现的严重神经系统并发症,以认知障碍与神经功能异常为主要特征。其发病机制涉及氧化应激、炎症反应、线粒体功能障碍及血脑屏障破坏。
近年研究表明,氢气(H₂)因具有抗氧化与抗炎特性,对SAE具有治疗潜力。氢气可通过清除活性氧、抑制星形胶质细胞与小胶质细胞活化、改善线粒体功能,减轻SAE相关的氧化应激、神经炎症与神经元损伤。
但治疗方案(剂量、给药方式、给药途径)的差异限制了研究结论的外推性。尽管存在上述问题,氢气治疗安全性好、不良反应极少。本文综述了氢气治疗SAE的现有证据,并提出未来研究方向:方案标准化、治疗方案优化及长期效应评估。
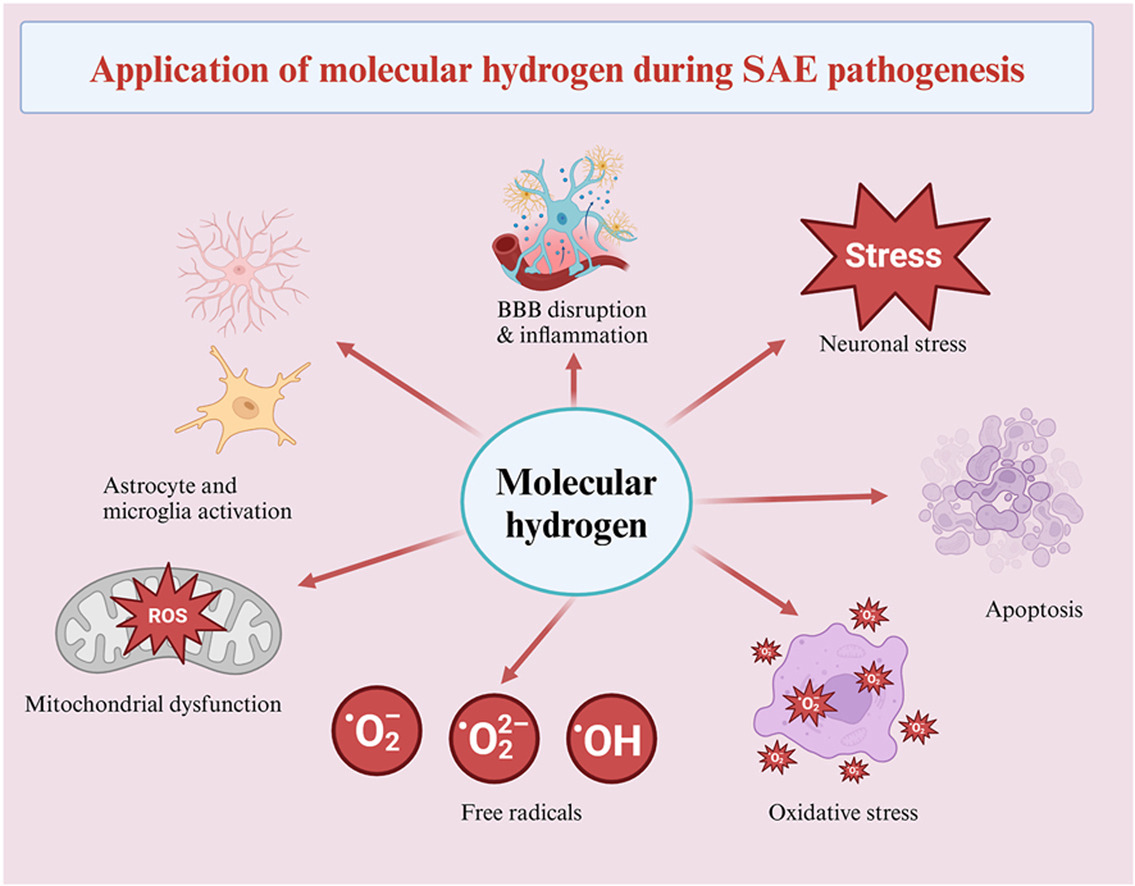
图文摘要
氢气(H₂)在脓毒症相关性脑病(SAE)中的保护作用:
氢气通过多种机制对SAE发挥神经保护效应:清除活性氧、减轻氧化应激、维持线粒体功能;抑制星形胶质细胞与小胶质细胞活化,从而减轻神经炎症;维持血脑屏障完整性、缓解神经元应激并发挥抗凋亡作用。上述作用共同提示氢气在改善SAE病程中具有治疗潜力。
注:O₂⁻:超氧阴离子;O₂²⁻:过氧化物;OH•:羟自由基;ROS:活性氧。
引言
脓毒症是感染引发的异常免疫反应所导致的危及生命的疾病,可引起全身炎症、多器官功能障碍与高病死率。在其并发症中,脓毒症相关性脑病(SAE)尤为突出,约累及70%脓毒症患者。
SAE表现为意识状态改变、认知功能障碍,病死率升高,给重症监护病房(ICU)带来巨大挑战,并导致长期病残与社会经济负担,对脑部仍处于发育阶段、疾病进程更复杂的儿童尤为显著。SAE的长期后遗症包括记忆丧失、认知障碍与行为改变,给患者、家庭及社会造成沉重压力。
SAE发病机制复杂且多因素参与,主要包括:氧化应激、神经炎症、线粒体功能障碍、神经元凋亡、血脑屏障(BBB)破坏。由活化小胶质细胞与星形胶质细胞驱动的神经炎症,可释放肿瘤坏死因子-α(TNF-α)、白细胞介素-1β(IL-1β)、白细胞介素-6(IL-6)等促炎因子,破坏血脑屏障并加重神经元损伤。
同时,活性氧(ROS)与抗氧化系统失衡引发的氧化应激,会加剧线粒体功能障碍,进一步损伤细胞能量代谢并促进神经退行性改变。线粒体损伤与ROS蓄积还可激活凋亡通路,最终导致神经元死亡与认知功能下降。上述病理过程在儿童与成人中均存在,但大脑发育阶段可显著影响疾病进程与临床表现,使儿科患者具有独特易感性。
目前,除控制原发感染外,SAE尚无特效治疗手段,因此亟需寻找有效干预药物以减轻其长期神经后遗症。
氢气(H₂)因其独特生物学特性成为极具前景的治疗手段:可选择性清除羟自由基(OH•)与过氧亚硝酸盐(ONOO⁻)、调控炎症通路、增强内源性抗氧化系统。前期研究显示,氢气治疗可改善SAE模型动物的神经认知功能、减轻神经元损伤、缓解炎症与线粒体功能障碍,其机制包括抑制神经炎症、调控线粒体质量、保护血脑屏障等。
此外,氢气治疗安全性高、不良反应轻微,并可调控多条氧化应激与炎症相关信号通路,上调内源性抗氧化酶表达、下调促炎因子水平。尽管氢气在多种疾病中已展现疗效,但在SAE模型中仍需深入研究以全面阐明其潜力。现有研究常受限于样本量小、给药方案不一、给药方式各异,亟需更系统的研究来验证并优化氢气的临床应用。
因此,本文就氢气对SAE的神经保护机制及现有证据进行综述,并提出未来研究方向。
https://blog.sciencenet.cn/blog-41174-1523530.html
上一篇:红细胞作为主要葡萄糖汇,改善高海拔环境下的葡萄糖耐量
下一篇:重新评估瘦素的潜在价值:治疗1型糖尿病