博文
重组层粘连蛋白为帕金森病干细胞疗法铺平道路  精选
精选
|
重组层粘连蛋白为帕金森病干细胞疗法铺平道路
通过降低变异性和解决生产问题,重组层粘连蛋白正帮助研究人员推进针对帕金森病及其他神经退行性疾病的细胞疗法研发。
多巴胺能神经元退化或功能异常与帕金森病及其他神经和精神疾病相关。图片来源:BioLamina
干细胞替代疗法:帕金森病治疗的前沿策略
帕金森病(PD)是一种神经退行性疾病,其特征是多巴胺能神经元进行性丢失,并伴随震颤、肌肉僵硬、运动迟缓等典型运动症状。干细胞替代疗法是该疾病治疗领域中发展迅速的策略——研究人员通过将健康神经元移植到大脑病变区域,旨在重建多巴胺信号通路、缓解症状,有望实现当前药物治疗无法达到的长期疗效。
“从理论上讲,帕金森病的细胞替代疗法非常简单,”瑞典隆德大学发育与再生神经生物学教授马林·帕尔马(Malin Parmar)解释道,“我们植入新的健康神经元,以替代因疾病丢失的神经元。尽管疾病可能仍在进展,但患者不会感受到其影响,因为新细胞会起到代偿作用。”
然而,该疗法的实际实施远非易事。十多年来,帕尔马团队一直在研发**STEM-PD**——一种基于人胚胎干细胞(hESC)定向分化为多巴胺能神经元的细胞疗法。团队已收集到具有前景的临床前数据,证实该疗法的安全性和有效性,使其成为帕金森病患者传统药物治疗的潜在替代方案(传统药物治疗往往会随时间推移失效,并常引发不良副作用)。
2023年,STEM-PD的临床前开发和临床试验设计取得成功并发表相关成果,目前该疗法正处于早期临床试验阶段[1]。但在达成这一里程碑之前,帕尔马团队必须克服一个重大监管障碍:确保疗法的生产符合**药品生产质量管理规范(GMP)** 标准。
为满足GMP标准,帕尔马团队与BioLamina公司展开密切合作。BioLamina在重组层粘连蛋白领域的专业知识及合规经验,为临床用底物的选择提供了关键指导。
人胚胎干细胞的GMP合规之路
GMP法规明确了质量标准,以确保生产过程的可扩展性和可重复性。要将实验室级别的人胚胎干细胞分化方案转化为符合GMP标准的临床级生产流程,帕尔马团队必须替换关键试剂,选用同时满足生产目标和监管要求的替代材料。
“在我们最初的实验室级方案中,细胞分化使用的底物是一种组织提取物——来源于小鼠肉瘤的细胞外基质提取物,”帕尔马表示。尽管这种提取物适用于实验室研究,但存在三大问题使其无法用于临床转化:**异源来源**(非人类来源)、**成分不确定**、**批次间变异性大**。因此,它不能用于先进治疗 medicinal products(ATMPs,先进疗法药品)的临床或GMP生产。
“我们知道必须替换方案中的蛋白质混合物,但始终找不到能让细胞附着并生长的其他底物,”帕尔马回忆道。而对细胞外基质(ECM)核心成分的深入研究,成为了突破这一困境的转折点。
更优的细胞培养:聚焦层粘连蛋白的关键作用
“如果将细胞外基质视为一个器官,它将是人体最大的器官,”帕尔马的前同事特蕾泽·卡卢尔(Therése Kallur)表示。卡卢尔现任BioLamina公司首席科学官兼业务发展总监——该公司是瑞典一家生物技术企业,专注生产全长重组人层粘连蛋白(层粘连蛋白是一个蛋白质家族,也是细胞培养和临床转化中使用的细胞外基质的主要成分)。
“当研究人员培养干细胞并将其分化为神经祖细胞和神经元时,他们会将时间、精力和资金集中在培养基和生长因子上,”卡卢尔指出,“但他们很少关注细胞维持的另一个关键部分:细胞外基质的各类成分,以及细胞生长所依赖的底物纯度和质量。”
在卡卢尔看来,重组层粘连蛋白不仅是研究工具,更是推动细胞疗法生产进入新时代的“催化剂”。她解释道,使用成分明确的**Biolaminin系列底物**,既能提升细胞质量,也能改善细胞整体健康状态。“由于这些底物兼容临床转化,它们正助力重新定义细胞疗法生产的标准。”
层粘连蛋白的生物学特性与功能
层粘连蛋白对于基底膜(所有上皮组织和内皮组织的支撑结构)的组装至关重要,其缺失或错误折叠会导致严重的发育缺陷。“哺乳动物中至少存在16种层粘连蛋白亚型,”卡卢尔介绍,“每种亚型都有特定功能,且在不同组织(甚至不同细胞类型)中特异性表达。”无论是单独作用还是协同作用,这些亚型都与不同器官的“微环境(niche)”和功能紧密相关。
层粘连蛋白是由α、β、γ三条链组成的大型异源三聚体,含有丰富的结合位点。“层粘连蛋白通过与整合素(integrin)及其他受体相互作用,支持细胞功能,”卡卢尔解释,“其富含糖链的‘臂状结构’能结合生长因子和促分裂原,精准调控这些分子的释放与呈现——这使得层粘连蛋白成为模拟天然微环境、生成治疗用靶细胞的关键物质。”
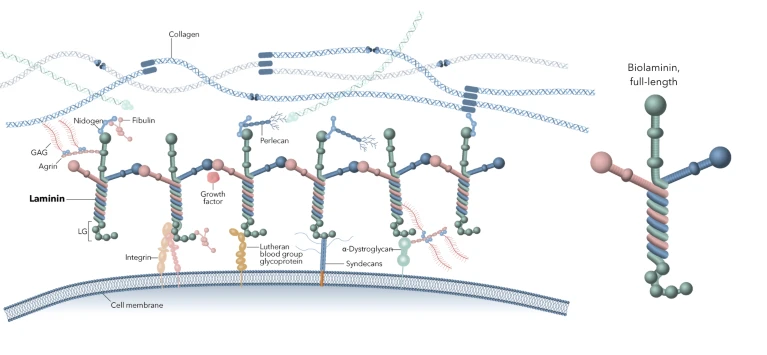
> 全长层粘连蛋白是基底膜的核心组织者。它们通过与多种细胞表面受体(包括整合素、 Syndecan蛋白、路德教血型糖蛋白)以及其他基质成分(如巢蛋白、集聚蛋白)结合,将细胞与周围的细胞外基质连接起来。通过这些相互作用,层粘连蛋白帮助构建细胞生长环境,并调控细胞附着、信号传导、存活及功能。图片来源:Mikko Sallinen(为BioLamina提供)
只有**完整的全长层粘连蛋白**,才能提供调控细胞附着、信号传导、存活和功能所需的复杂结合位点网络。这类蛋白质高度整合于细胞微环境中,无法从组织中提取出纯净且完整的形式,因此**重组生产**成为获取该物质的必要途径。
重组层粘连蛋白在STEM-PD生产中的应用
在符合GMP标准的研究方案中,帕尔马团队使用了重组生产的Biolaminin底物。“在我们的生产流程中,层粘连蛋白用于两个关键阶段:干细胞维持和多巴胺能神经元分化,”帕尔马表示。这一选择以及最终达到GMP标准的能力,均得益于与BioLamina的密切合作。
“BioLamina帮助我们筛选候选底物,并调整辅助材料以满足临床用GMP法规要求,”帕尔马说,“这是一次互动性强且成果显著的合作。”
“由于我们的产品通过重组技术生产,我们能对其研发、生产和纯化过程进行极高水平的控制,”卡卢尔补充道,“这使我们能够克隆、表达并纯化出科学家所需的特定全长层粘连蛋白。使用全长蛋白的优势在于,它能完整保留蛋白质的生物功能。”
全长层粘连蛋白:释放临床治疗的全部潜力
通过利用层粘连蛋白的生物学精准性,BioLamina帮助研究人员重建细胞微环境——这一突破显著加速了治疗方法的研发进程。帕尔马团队的实践充分体现了这一影响:通过使用特定的层粘连蛋白亚型,多巴胺能祖细胞的产量提升了43倍。“产量的提高意味着他们能更快推进至临床阶段,并为患者治疗提供更充足的临床用细胞供应,”卡卢尔表示。
该研究方案显示,细胞纯度达98.7%、存活率达83%,且非靶细胞比例低于0.5%[1]。在大鼠模型中,STEM-PD成功恢复了动物的运动功能,生成了有功能的多巴胺能神经元,且未观察到不良反应——这些结果为该疗法进入临床测试提供了有力支持。
展望:关注细胞外基质,推动更多神经疾病疗法研发
卡卢尔呼吁研究人员重视层粘连蛋白(具体而言)和细胞外基质(整体而言)的复杂性与重要性。
“在数据分析中,细胞外基质常常被忽视,但研究层粘连蛋白和整合素的表达,能揭示细胞或组织真正需要的亚型,”卡卢尔说,“过去,研究人员难以获取多种层粘连蛋白亚型;但如今,借助我们全新的Biolaminin底物,是时候重新聚焦细胞外基质了。”
STEM-PD的成功,为帕尔马团队研发更优的帕金森病治疗方案(乃至其他疾病疗法)奠定了基础。
“我们从STEM-PD研发中获得的经验,可应用于其他神经退行性疾病,”帕尔马表示,“通过与亨廷顿病和中风领域的专家合作,我们正将细胞分化、生产和移植方面的经验转化为新一代疗法。”
https://blog.sciencenet.cn/blog-41174-1514244.html
上一篇:分子氢:被忽视的土壤生物地球化学过程关键驱动因子
下一篇:研究表明:老年女性过量饮用咖啡不利于骨健康
