博文
间歇性缺氧对内皮功能的影响及富氢水的作用【加论文3】
||
第一部分:富氢水减轻睡眠呼吸暂停模型鼠血管损伤1
第二部分:氢气预防间歇呼停血管损伤研究细节 2
第3章:间歇性缺氧对内皮功能的影响及富氢水的作用
3.1 引言
IH是睡眠呼吸暂停综合症(OSA)的主要病理特征,而OSA是最常见的与睡眠相关的呼吸障碍。已经明确,缺氧既是心血管疾病(CVDs)的触发因素也是伴随因素。然而,持续气道正压通气(CPAP)在减少OSA患者的CVDs发病率方面几乎没有显示出益处。内皮功能障碍是CVDs的初始阶段,定义为一氧化氮(NO)的生物可用性受限。在健康志愿者中,通过摄入富氢水(HRW)30分钟后,肱动脉的血流介导扩张得到改善,表明HRW可能改善人类的内皮功能。然而,该研究只调查了一次剂量HRW的急性效应。对于OSA患者多次给药的效果尚不清楚。
本章的研究旨在检验这样一个假设:IH导致内皮功能障碍,而HRW可能是除了CPAP之外的一个有前景的治疗方法,可以改善内皮功能。炎症细胞因子、氧化应激标志物、抗氧化酶表达以及衰老标志物的评估,是为了弄清楚HRW作用的机制。
3.2 结果
3.2.1 动物特征
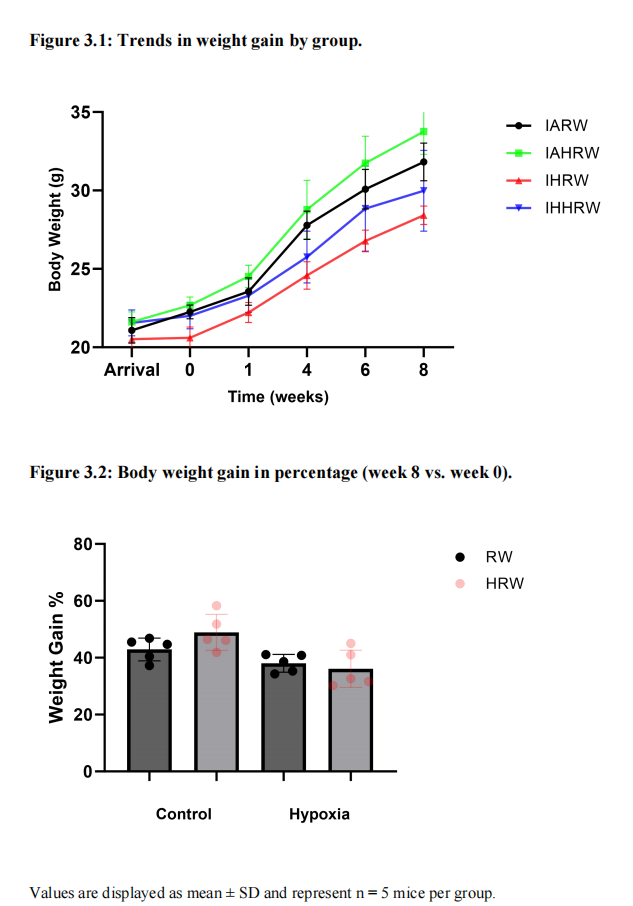
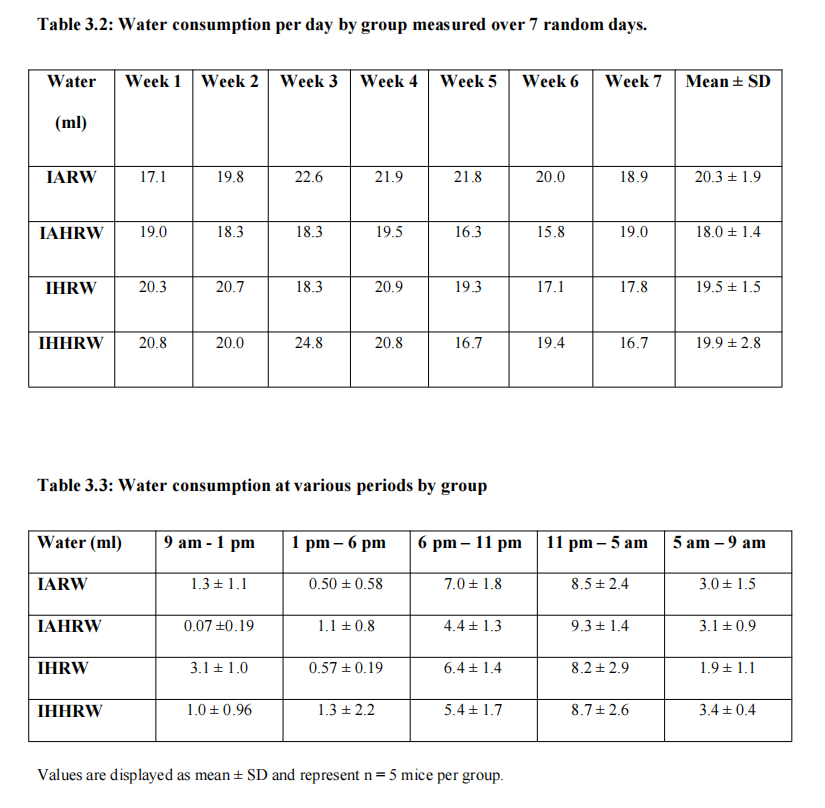
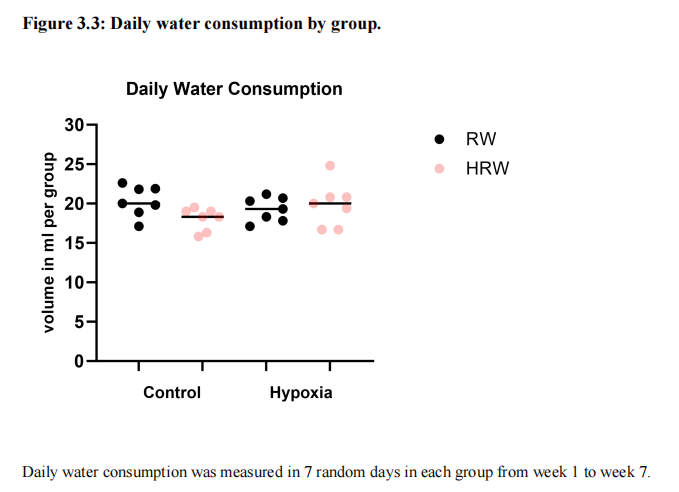
一些动物在暴露于IH的初期表现出轻微的不适迹象(啃咬笼子和铺垫),然而,在整个研究期间没有观察到任何动物出现疾病迹象。表3.1显示了8周内动物体重的变化,图3.1展示了各组的体重增加情况。四组间的体重增加百分比无差异(图3.2)。表3.2和表3.3显示了每天和不同时间段各组消耗的水量。四组间日常水消耗量(RW和HRW)无差异(图3.3)。
表3.1:研究阶段小鼠的体重

3.2.2 缺氧增加了小鼠肾脏中HIF-1α的表达
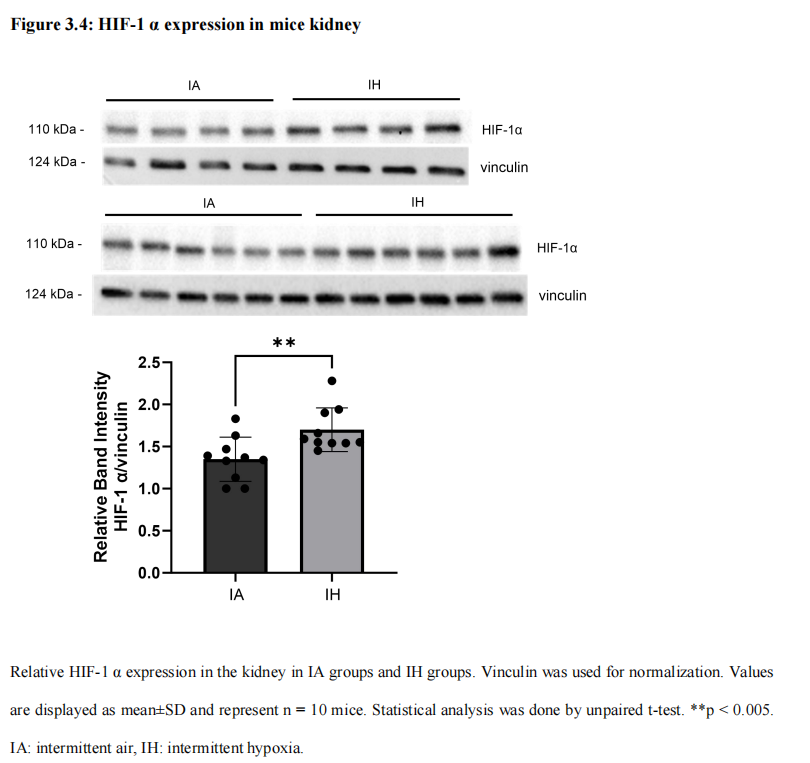
低氧诱导因子1(HIF-1)是由HIF-1α和HIF-1β组成的异二聚体蛋白复合物,在身体对低氧浓度的反应中起着关键作用。HIF-1α是一种普遍存在的蛋白质,包含一个氧依赖性降解域,该域在正常氧条件下调节其持续降解。当低氧稳定HIF-1α时,它会转位到细胞核内,在那里与HIF-1β二聚化形成活性转录因子,并调控目标基因的表达。与暴露于间歇性空气(IA)的小鼠相比(HIF-1α/vinculin: 1.30 ± 0.21),暴露于间歇性缺氧(IH)的小鼠肾脏中的HIF-1α表达水平显著增加(HIF-1α/vinculin: 1.70 ± 0.26)(p < 0.05)(图3.4)。在IARW和IAHRW之间(P=NS),以及IHRW和IHHRW之间(P=NS)没有差异。
3.2.3 缺氧增加了暴露于IH的小鼠炎症标志物的水平
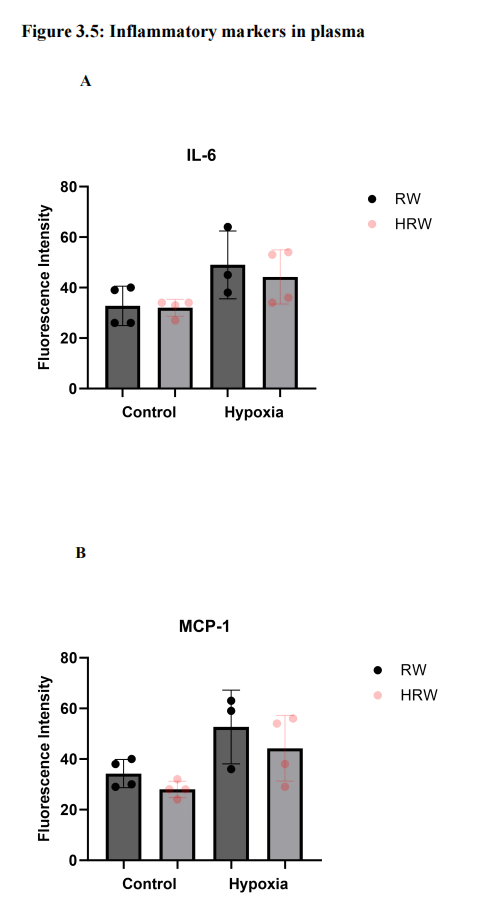
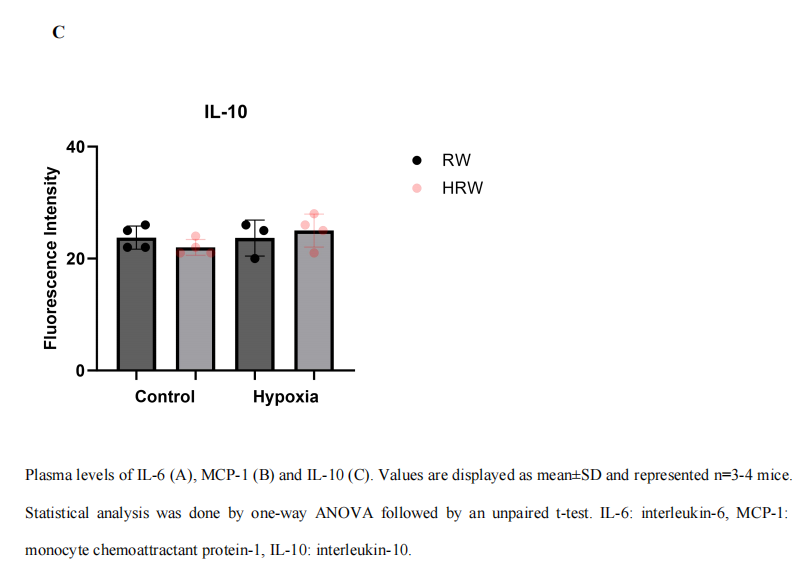
与对照组相比,暴露于间歇性缺氧(IH)的小鼠血浆中的白细胞介素6(IL-6)水平增加(FI: 49 ± 13.45 vs. 32.75 ± 7.80, p < 0.1)(图3.5 A)。此外,与对照组相比,暴露于IH的小鼠血浆中的单核细胞趋化蛋白-1(MCP-1)水平也增加(FI: 52.67 ± 14.57 vs. 34.25 ± 5.56, p < 0.1)(图3.5 B)。缺氧和富氢水(HRW)对白细胞介素10(IL-10)水平没有影响(p > 0.1)(图3.5 C)。
3.2.4 氢气改善了暴露于IH的小鼠内皮功能障碍
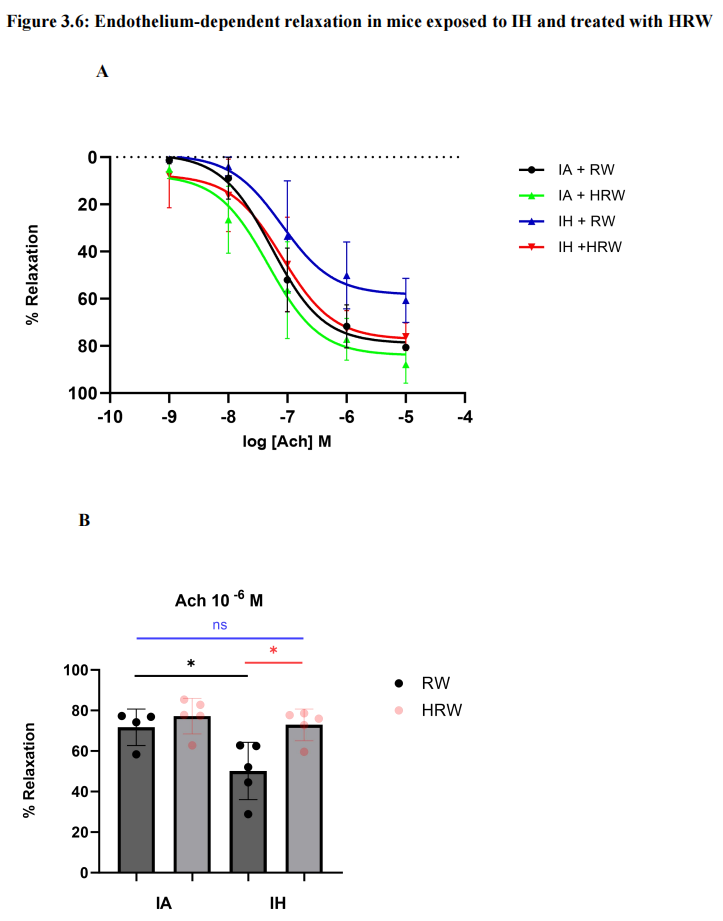
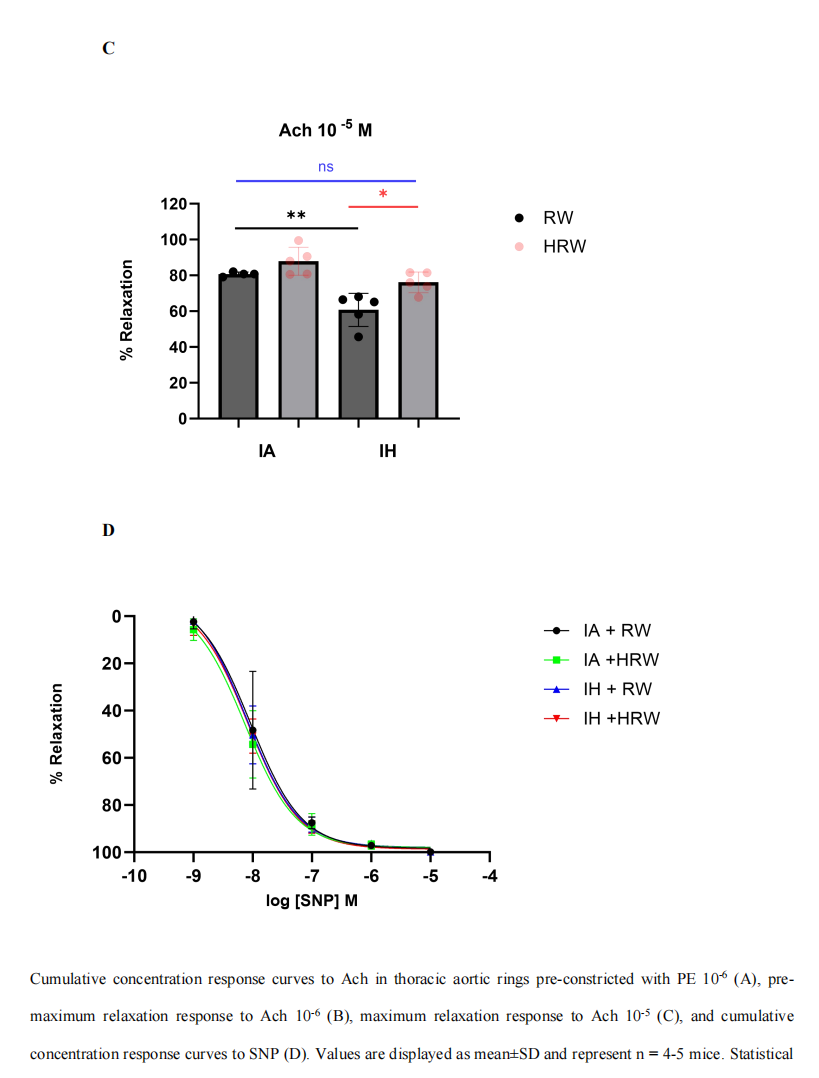
通过累加乙酰胆碱(Ach)刺激预先用PE收缩的主动脉段,以引发一氧化氮(NO)依赖性血管舒张。四组中不同浓度Ach引起的血管舒张情况如图3.6 A所示。与IARW组相比,IHRW组在Ach (10^-6)时的血管舒张功能降低(p < 0.05),而HRW具有保护作用(IHHRW vs. IHRW, p < 0.05)。最大浓度Ach (10^-5)诱导的最大松弛在IHRW组显著减弱,与其他组相比差异显著(Emax(%): 60.70 ± 9.22%, p < 0.005)(图3.6 C)。HRW治疗改善了IH组的Emax至对照组水平(Emax(%): 76.12 ± 5.75%比Emax(%): 80.65 ± 1.23%,p = 0.1704)(图3.6 C)。所有组之间Ach的EC50没有显著变化(p=NS)。使用硝普钠(SNP)测量非内皮依赖性松弛,以确认松弛变化是内皮依赖性的。在四组之间未观察到SNP诱导的血管舒张有差异(p=NS)(图3.6 D)。
3.2.5 氢气减少了暴露于IH的小鼠的血管收缩
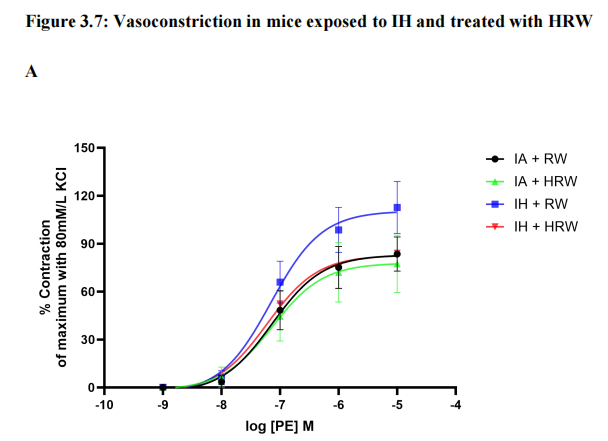
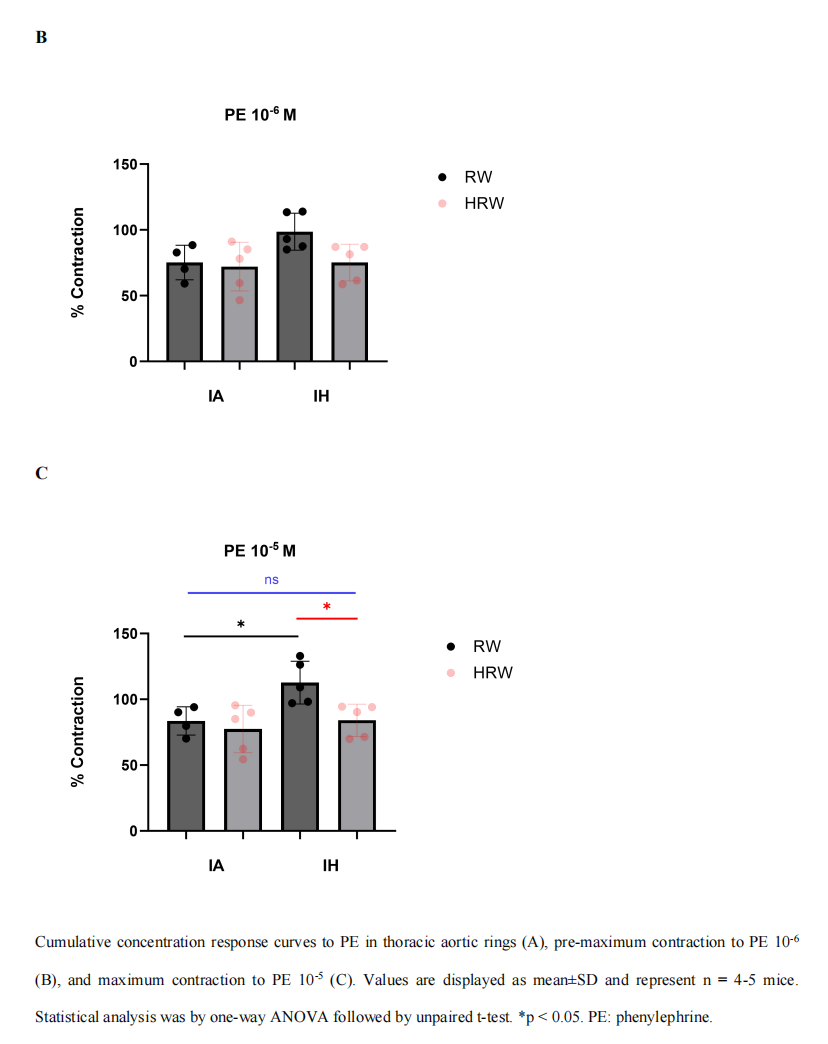
通过累加苯肾上腺素(PE)来刺激血管收缩(图3.7 A)。与IARW组相比,IHRW组在最大PE (10^-5)诱导的收缩显著增加(p < 0.05)(图3.7 C)。HRW治疗显著减弱了IH组的收缩(p < 0.05),并将其降至对照组水平(p=NS)(图3.7 C)。所有组之间PE的EC50没有显著变化(p=NS)。
3.2.6 氢气恢复了暴露于IH的小鼠的基础NO产生
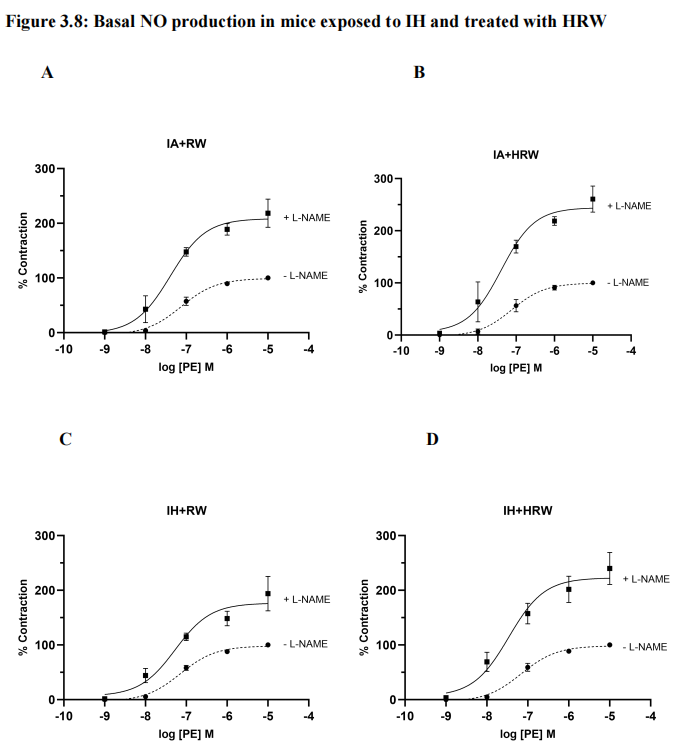
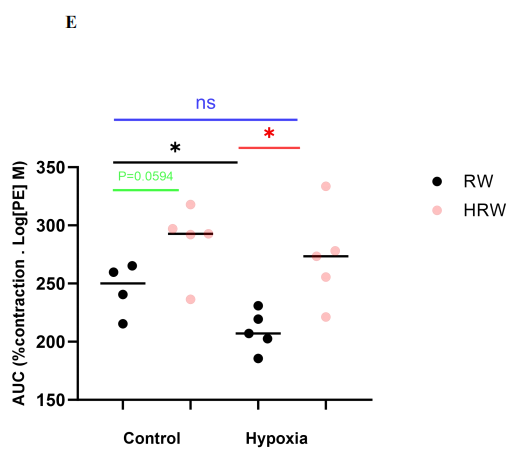
基础NO产生在血管静止时维持血管舒张张力,该张力的丧失会增加静息时的血管收缩和内皮功能障碍。在四组中,分别在有无N-硝基-L-精氨酸甲酯(L-NAME)的情况下获得对PE的浓度反应曲线(图3.8 A-D)。计算存在L-NAME时的曲线下面积(AUC),并将其除以不存在L-NAME时的AUC。加入L-NAME后,IARW组与IHRW组相比,PE引起的收缩反应增强(Emax(%):218.45±25.86%比193.94±31.59%)(图3.8 A & C)。与IHRW组相比,IARW组的基础NO产生显著更高(AUC=245.23±22.51比209.15±17.18, p<0.05)(图3.8 E)。HRW治疗显著改善了IH组的基础一氧化氮产生(AUC=272.37±40.83, p<0.05)(图3.8 E)。给予HRW后,IHHRW组与IARW组之间无差异(p=0.2754)(图3.8 E)。
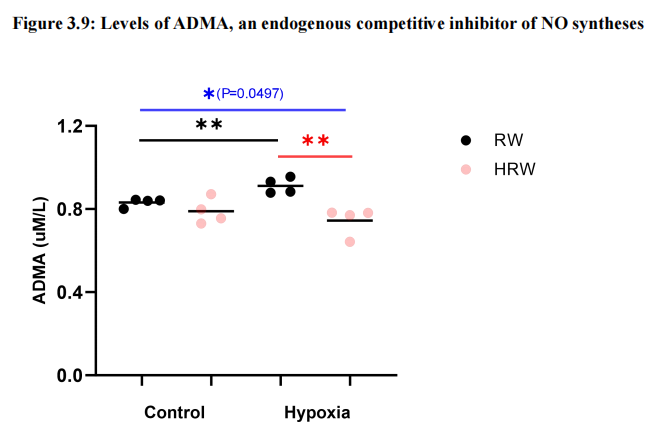
3.2.7 氢气降低了暴露于IH的小鼠中ADMA的水平
非对称二甲基精氨酸(ADMA)是内皮一氧化氮合酶(eNOS)的内源性抑制剂,通过与L-精氨酸竞争来损害NO的产生,从而导致内皮功能障碍,进而引发动脉粥样硬化。与对照组相比,暴露于IH的小鼠的血浆ADMA水平显著升高(0.91 ± 0.04μM/L比0.83 ± 0.02μM/L, p < 0.001)(图3.9),而HRW治疗有效降低了ADMA水平(0.74 ± 0.07μM/L, p < 0.001)(图3.9)。
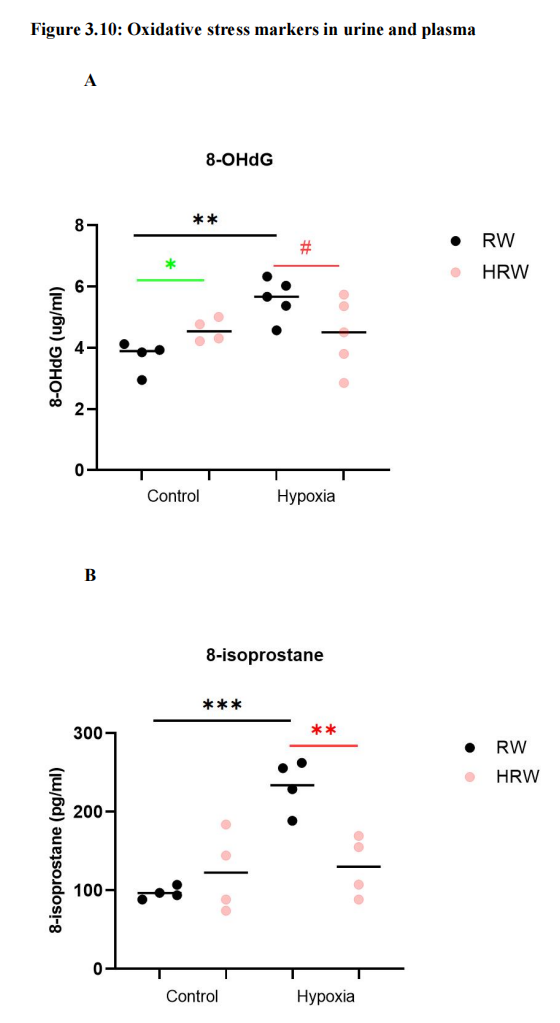
3.2.8 氢气降低了暴露于间歇性缺氧的小鼠的全身氧化应激
与对照组相比,暴露于IH的小鼠尿液中8-羟基-2′-脱氧鸟苷(8-OHdG)的水平显著升高,这是一种DNA损伤的氧化应激标志物(5.59 ± 0.68比3.58 ± 0.54 μg/ml, p < 0.01)(图3.10 A)。HRW降低了暴露于IH的小鼠的8-OHdG水平(4.45 ± 1.17 μg/ml, p < 0.1)(图3.10 A)。生活在常氧条件下的小鼠饮用HRW后,尿液中的8-OHdG水平也有所增加(4.70 ± 0.36 μg/ml, p < 0.05)(图3.10 A)。此外,与对照组相比,暴露于IH的小鼠血浆中的8-异前列腺素水平显著升高,这是脂质过氧化的氧化标志物(214.65 ± 38.42比96.53 ± 78.5 pg/ml, p< 0.001)(图3.10 B)。HRW有效地降低了暴露于IH的小鼠的8-异前列腺素水平(130.06 ± 38.42 pg/ml, p < 0.01)(图3.10 B)。
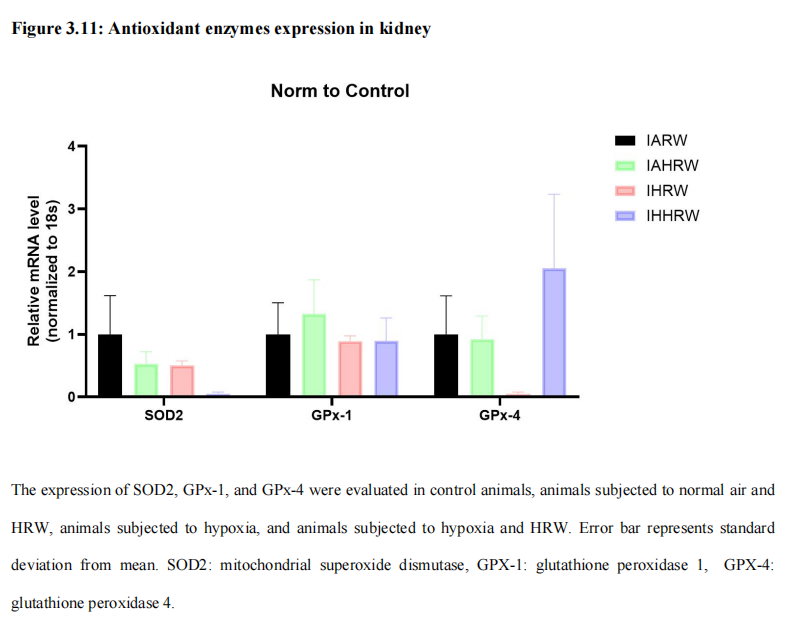
3.2.9 IH和HRW处理动物中抗氧化酶的表达
超氧化物歧化酶(SOD)催化超氧化物(O2 -)转化为氧气和过氧化氢(H2O2),在对抗氧化应激的抗氧化防御中发挥重要作用。哺乳动物中存在三种形式的SOD:胞质超氧化物歧化酶(SOD1)、线粒体超氧化物歧化酶(SOD2)和细胞外超氧化物歧化酶(SOD3)。我们观察到IH组中的SOD2水平下降(图3.11)。有趣的是,我们发现HRW处理组中的SOD2水平进一步下降(图3.11)。谷胱甘肽过氧化物酶1(GPX-1)和谷胱甘肽过氧化物酶4(GPX-4)是谷胱甘肽过氧化物酶家族的成员,参与脂质过氧化物的解毒。GPX-1降解过氧化氢、烷基过氧化物和脂肪酸氢过氧化物,而Gpx4能降解脂蛋白和复合脂质中的氢过氧化物。暴露于IH的动物中GPX-4的表达降低,并在HRW处理后得到改善(图3.11)。四组之间未观察到GPX-1的差异(图3.11)。
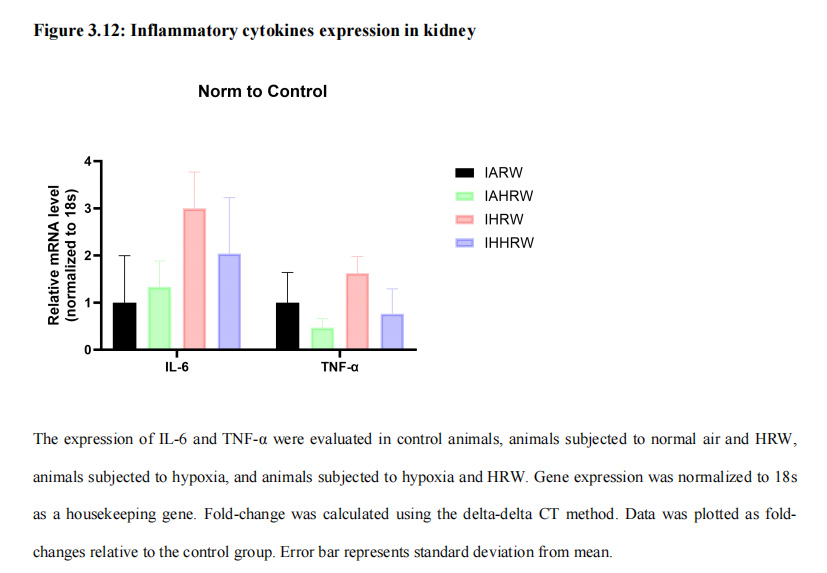
3.2.10 IH和HRW处理动物中炎症因子的表达
在IHRW组中,我们记录到IL-6的表达增加,而在IHHRW组中IL-6的表达略有下降(图3.12),这与血浆中炎症因子的测量结果相似(图3.5A)。动物和人类研究已经确定了OSA与肿瘤坏死因子α(TNF-α)水平升高之间的显著关联。与IARW组相比,IHRW组中的TNF-α水平升高(图3.12)。HRW降低了IA和IH组中与RW处理组相比的TNF-α水平,但没有观察到统计学意义(图3.12)。
3.2.11 IH和HRW处理动物中的衰老标志物
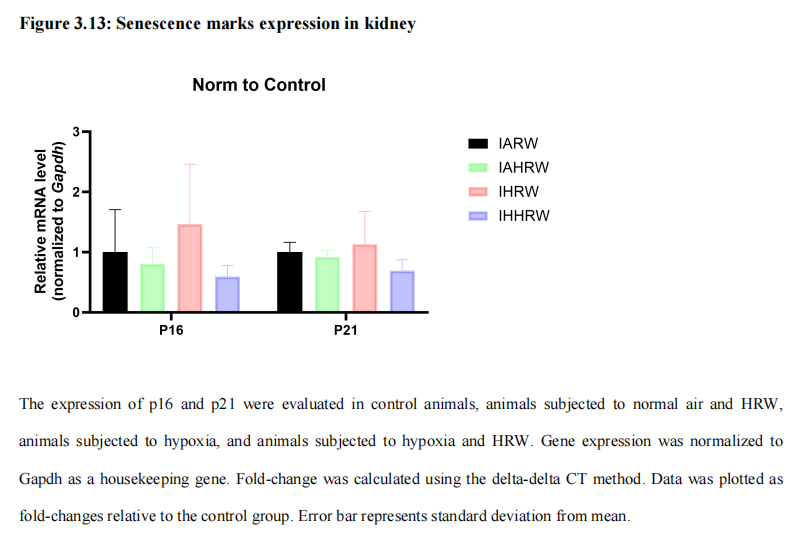
细胞衰老的两个主要特征途径是p16-pRB和p53-p21。在四组中测量了肾脏中的p16和p21的表达。与IARW相比,IHRW中的p16表达增加,而与IHRW相比,IHHRW中的p16表达减少(图3.13)。四组中的p21水平没有差异(图3.13)。
第3章 总结
实验组动物中HIF-α水平的升高证实了它们确实暴露于缺氧环境中,表明IH模型建立成功。IH动物血液中的炎症因子和氧化应激标志物增加。IH还导致内皮功能障碍,表现为乙酰胆碱诱导的血管舒张受损、PE引起的血管收缩增加、基础NO产生减少以及ADMA水平升高。HRW在改善氧化应激和内皮功能障碍方面显示出益处。此外,HRW影响抗氧化酶的表达,并减轻了由缺氧引起的加速衰老过程。
https://blog.sciencenet.cn/blog-41174-1458658.html
上一篇:干燥综合征患者氢疗案例【台湾】
下一篇:减肥药将如何改变世界,许多想不到!《自然》