博文
巨噬细胞的脂质循环促进脑癌生长  精选
精选
|
在脑肿瘤中,被称为巨噬细胞的免疫细胞从神经元的髓鞘中清除脂质碎片。这些富含脂质的巨噬细胞导致免疫抑制,它们将脂质转移到肿瘤上,从而助长了癌症的生长。
一种起源于大脑的恶性肿瘤,称为胶质母细胞瘤,与高度免疫抑制的微环境相关1。来自癌细胞及其在肿瘤微环境中的邻居的各种信号导致了T细胞的排斥和功能抑制——这些免疫细胞有潜力杀死胶质母细胞瘤细胞2,3。广泛的研究增加了科学家们对肿瘤相关免疫细胞的了解,例如小胶质细胞(大脑驻留型巨噬细胞)和单核细胞衍生的巨噬细胞(在胶质母细胞瘤中与癌症促进和免疫抑制相关)4–6。Kloosterman等人在《细胞》杂志上发表文章7,研究了胶质母细胞瘤小鼠模型中小胶质细胞和单核细胞衍生的巨噬细胞群体的广泛谱系,并为胶质母细胞瘤细胞与肿瘤浸润性免疫细胞之间的复杂相互作用提供了机制性见解。
作者对胶质母细胞瘤细胞进行了分子分析,并确定了与疾病不同阶段相关的几个主要的巨噬细胞和小胶质细胞亚群。其中一个亚群引起了作者的关注,因为其存在与日益激进的癌症有关,并且在一种叫做间充质胶质母细胞瘤的亚型中最丰富,该亚型与高水平的免疫细胞浸润和特别差的预后相关。这个称为脂质负载巨噬细胞(LLMs)的亚群特征是脂质积累和脂质代谢的变化。LLMs主要在源自骨髓的单核细胞的巨噬细胞群体中检测到,但也由大脑驻留的小胶质细胞产生。
LLMs最初在肥胖的背景下被报道8,随后发现与包括糖尿病、肝病、动脉粥样硬化9和癌症10在内的一系列疾病有关。在许多免疫细胞群体中观察到了脂质代谢的改变。这种重编程帮助细胞适应代谢需求高的条件,并与细胞功能的变化有关。在包括巨噬细胞和单核细胞在内的髓系免疫细胞中,观察到与LLM形成相关的强烈免疫抑制能力在各种疾病中的诱导,包括一些影响中枢神经系统的疾病11。
通过一系列实验方法,Kloosterman及其同事深入了解了LLMs与间充质胶质母细胞瘤细胞之间复杂的关系,这种关系促进了癌症的侵袭性和降低了免疫系统的抗癌反应。作者展示了LLMs在缺氧(低氧)生态位——恶性间充质胶质母细胞瘤细胞居住的区域——中积累,并且在治疗后再发的胶质母细胞瘤病例中水平最高。为了调查可能的核内效应,作者检查了称为染色质的蛋白质-DNA复合体的特征。这种“表观遗传”分析包括测量染色质对核大分子(如影响转录的蛋白质)的物理可及性。
作者揭示炎症基因的染色质可及性降低,表明这些基因在LLMs中的表达水平低于非脂质负载的巨噬细胞。这些染色质可及性的改变与增强的免疫抑制功能相关,并且也损害了抗原呈递——一个过程中,T细胞被蛋白质片段称为抗原的片段激活,使它们能够识别并针对具有匹配抗原的癌细胞(图1)。
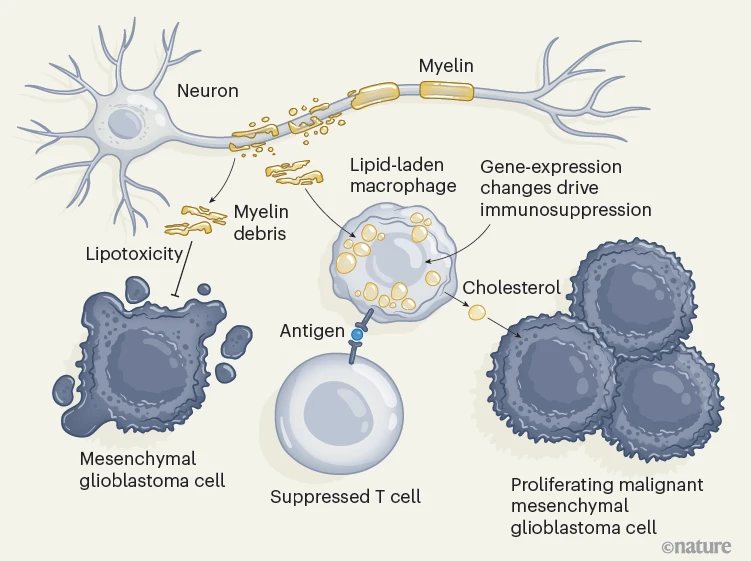
图1 | 脑肿瘤细胞指示巨噬细胞回收和循环利用脂质。Kloosterman等人7研究了称为胶质母细胞瘤的脑肿瘤微环境中细胞间的复杂相互作用。间充质胶质母细胞瘤是这种癌症的一种特别激进的亚型。当神经元脱落包裹它们的髓鞘碎片时,间充质胶质母细胞瘤细胞向称为巨噬细胞的免疫细胞发出信号,指示它们从这些碎片中回收和循环利用胆固醇。积累胆固醇的这种巨噬细胞被称为富含脂质的巨噬细胞(LLMs)。LLMs在吞噬髓鞘的过程中被重新编程,并表现出脂代谢的改变和促炎基因表达的降低。它们具有免疫抑制作用,并且减少了将抗原(肽片段)呈递给免疫系统T细胞的能力。来自LLMs的胆固醇转移到间充质胶质母细胞瘤细胞,这有助于推动肿瘤细胞的增殖。通过代谢髓鞘碎片,LLMs保护癌细胞免受髓鞘的脂毒性影响,并为肿瘤的生存和进展提供燃料。
一个关键的问题是如何使巨噬细胞进入富含脂质的状态以及累积的脂质来源于何处。脂质分析显示,这些脂质是从肿瘤微环境中的外部来源摄取的,而不是新合成的。脂质的组成表明,巨噬细胞吸收了包裹神经元的髓鞘碎片。髓鞘的摄取导致胆固醇的积累,这触发了一个负反馈循环,减少了胆固醇的产生并增加了其从LLMs中的释放。在体外,当巨噬细胞暴露于髓鞘碎片和间充质胶质母细胞瘤细胞释放的因素时,LLMs的形成增加了,这表明胶质母细胞瘤细胞指示巨噬细胞摄取髓鞘碎片。
这就提出了一个问题,即间充质胶质母细胞瘤细胞如何从LLMs中获益。作者展示了间充质胶质母细胞瘤细胞展现出低水平的脂质生物合成;因此,它们依赖于巨噬细胞来回收和循环利用产生脂质的髓鞘碎片,如胆固醇,然后将其转移给癌细胞。这种互惠相互作用促进了肿瘤细胞的增殖,并减少了髓鞘对胶质母细胞瘤细胞的脂毒性影响(图1)。
鉴于巨噬细胞积累与肿瘤进展之间的关联,针对巨噬细胞的治疗方法正在浮现。然而,这些策略常常因为抗性机制或不良反应而失败。需要详细了解疾病相关巨噬细胞亚群的特征,以开发能够精确且局部限制性靶向的策略,并阻断促进癌症的功能。Kloosterman及其同事的工作展示了一种系统的方法,用于定义促进疾病的巨噬细胞群体的身份,并剖析胶质母细胞瘤细胞指导巨噬细胞回收髓鞘碎片的底层机制。这种功能共选择使肿瘤细胞能够利用大脑中原本无法获得的脂质资源。此外,这是一种有效的免疫逃避方法,因为它引发了一种强烈的免疫抑制状态。
为了测试操纵LLMs作为治疗策略的潜力,Kloosterman等人使用几种方法来针对它们。用磺基琥珀酰亚胺油酸酯(SSO)抑制蛋白CD36阻止了髓鞘碎片的摄取,而阻断脂质输出蛋白ABCA1则阻止了脂质从LLMs转移到胶质母细胞瘤细胞,抑制蛋白LXR减少了胆固醇的积累。用SSO结合放疗治疗携带胶质母细胞瘤的小鼠,与对照小鼠相比,明显提高了生存率。在体外实验中,用SSO或ABCA1或LXR的抑制剂处理小鼠胶质母细胞瘤细胞,阻断了LLMs的促增殖效应。
尽管作者的结果很有希望,但以LLM为靶标的策略可能最适合作为组合疗法的一部分,旨在缓解巨噬细胞介导的免疫抑制同时重新激活受抑制的T细胞。Kloosterman及其同事的工作为这一更广泛的概念提供了证据。作者检查了已发布数据集中的人类临床信息,并证明LLMs的存在可以用来预测胶质母细胞瘤患者的生存时间和对免疫治疗的反应——尽管仅针对LLM的治疗并未强烈影响T细胞的数量。
未来的工作可能会探讨在高度免疫抑制的肿瘤类型中,将针对LLM的治疗与其他免疫疗法(例如,免疫检查点阻断或其他T细胞定向疗法)结合使用的适用性。随后评估LLM针对性治疗(有或无额外免疫疗法)对肿瘤浸润免疫细胞的影响将提供关键见解,可能使设计成功、定制化的组合疗法成为可能。
https://blog.sciencenet.cn/blog-41174-1450860.html
上一篇:氢气预防细胞冻存损伤的研究【赞】
下一篇:开放获取正在塑造科学传播