博文
Cells 抑制p38MAPK/NF-κB通路:缓解内皮细胞氧化应激性早衰的新策略
||
氧化应激介导的微血管内皮细胞衰老及相关炎症因子的释放,与血脑屏障完整性的破坏和功能丧失紧密相关。p38MAPK/NF-κB作为氧化应激中的核心信号通路,其在内皮细胞衰老和血脑屏障功能障碍中的致病机制及治疗潜力尚不明确。来自诺丁汉大学医学院的Ulvi Bayraktutan副教授及其研究团队发现,靶向抑制p38MAPK/NF-κB通路或直接清除衰老细胞,能有效减轻内皮细胞衰老、恢复紧密连接完整性,并抑制炎症反应,从而保护血脑屏障功能。这一发现为治疗血脑屏障功能障碍开辟了新的治疗途径。
研究过程和结果
1. H₂O₂通过激活p38MAPK-NF-κB信号通路介导内皮细胞衰老
作者通过H₂O₂处理人脑微血管内皮细胞,发现氧化应激后的内皮细胞出现了典型的衰老表型:细胞形态增大、衰老相关β-半乳糖苷酶活性升高、DNA损伤标志物γH2AX增加 (图1)。同时研究发现,氧化应激在极短时间内迅速激活了p38MAPK和NF-κB的磷酸化,并且证实NF-κB是p38MAPK的下游效应器 (图2)。抑制p38MAPK-NF-κB信号通路能够有效减轻内皮细胞衰老相关变化。
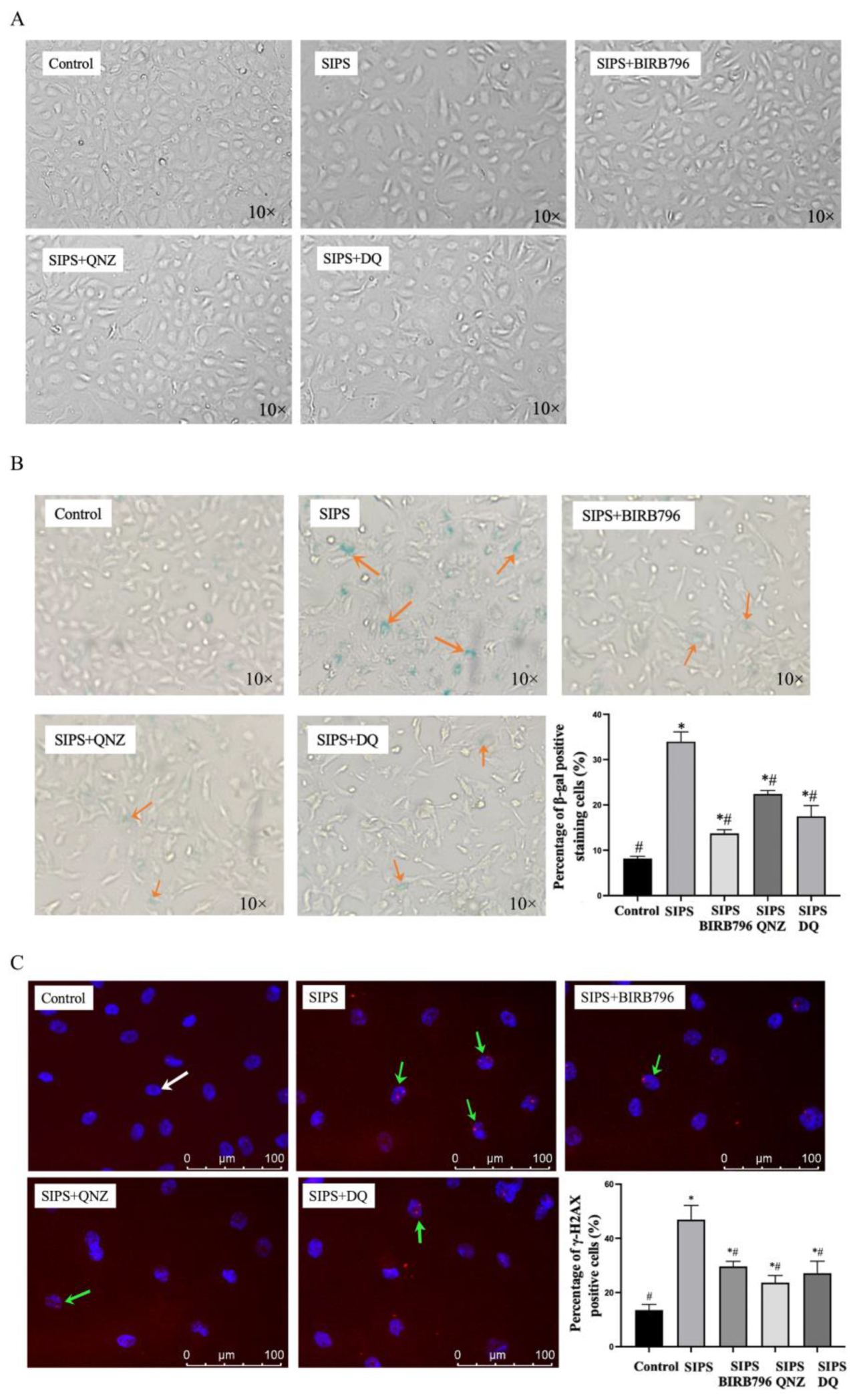
图1. H₂O₂诱导的衰老细胞形态变化和核损伤
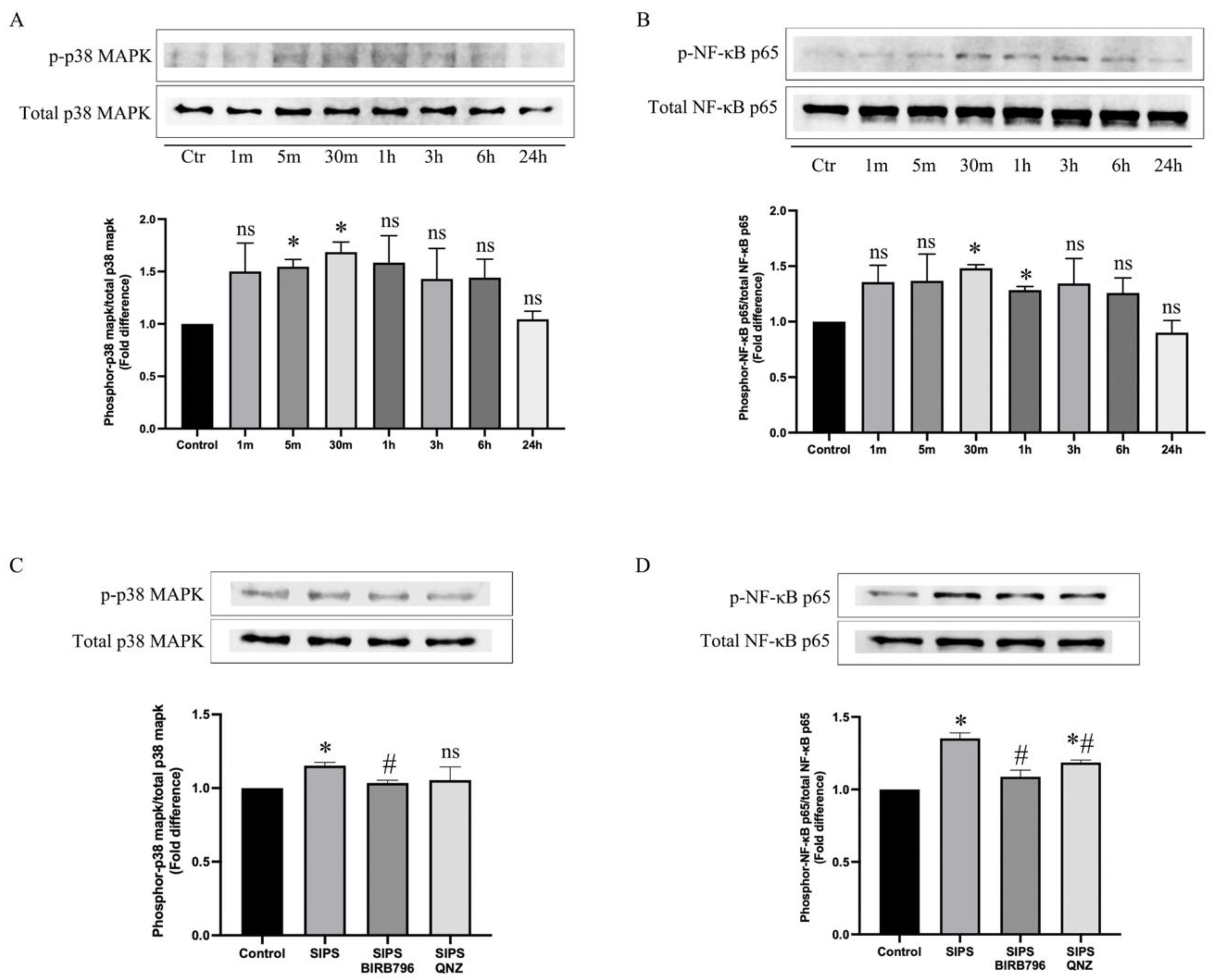
图2. H₂O₂对 p38MAPK 和 NF-κB 磷酸化的影响
2.内皮细胞衰老可诱导血脑屏障功能障碍,抑制血管生成并促进炎症发生
氧化应激下的衰老内皮细胞显示出跨内皮电阻抗降低和通透性增加,同时,衰老内皮细胞的成管能力显著下降。机制研究表明,衰老引起了细胞间连接蛋白ZO-1的错误定位 (图3),从而破坏屏障结构。此外,内皮细胞衰老特异性的激活了基质金属蛋白酶-2,可能通过降解基底膜破坏屏障的物理支撑。衰老内皮细胞获得了促炎表型,通过分泌炎症因子营造促炎微环境。
该研究创新性地联合使用通路特异性抑制剂 (BIRB796和QNZ) 与衰老细胞清除药物 (达沙替尼+槲皮素)。结果显示,抑制p38MAPK-NF-κB信号通路或清除衰老细胞,均可抑制促炎细胞因子的释放,恢复紧密连接结构的完整性,并改善血脑屏障功能。这些保护效果在包含多种细胞的人源化体外血脑屏障模型中得到了验证。
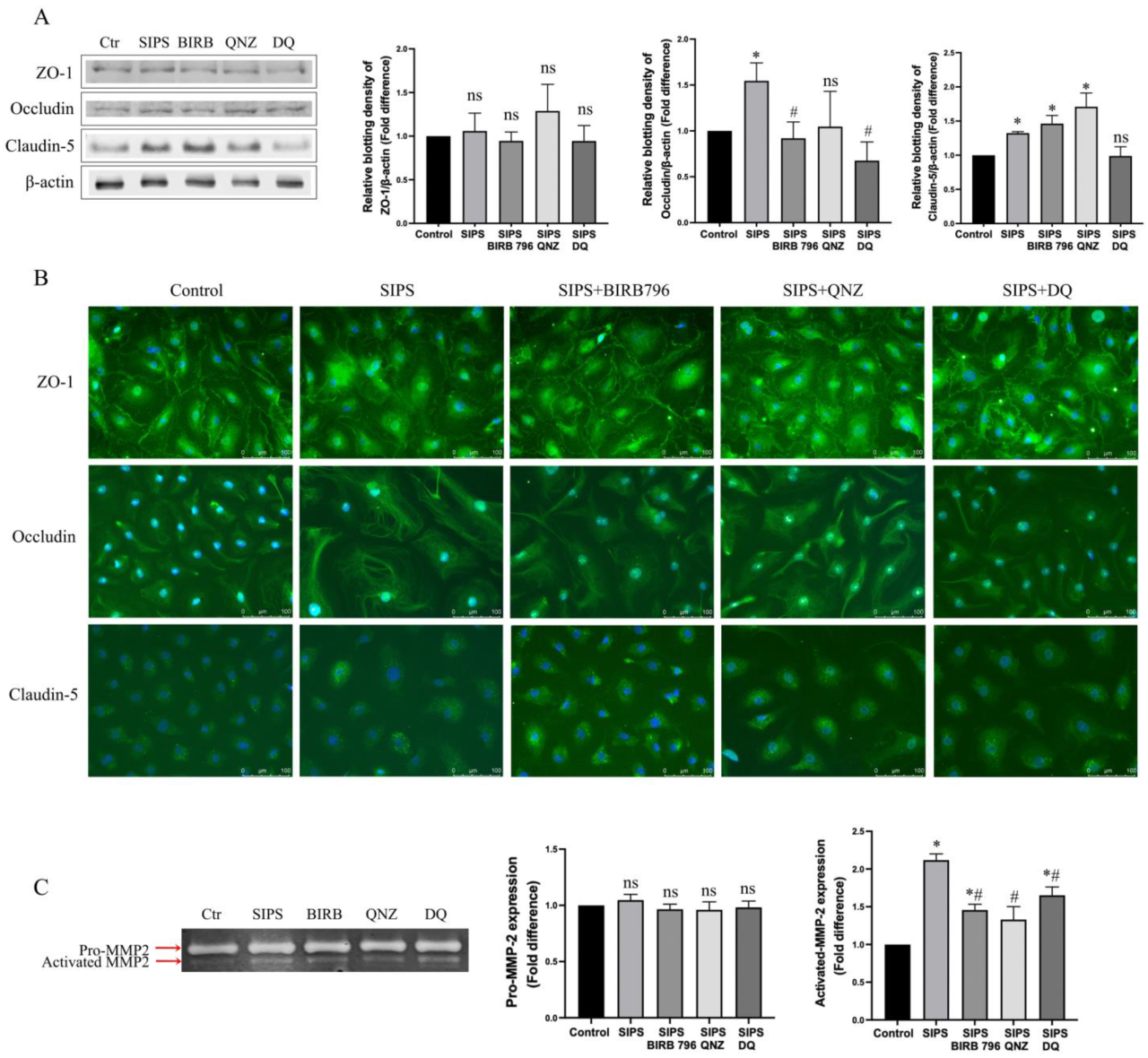
图3. 应激诱导的过早衰老显著影响紧密连接蛋白的表达和定位,并激活基质金属蛋白酶-2
研究总结
内皮细胞衰老过程中氧化应激升高,会通过时间依赖性方式激活p38MAPK/NF-κB通路,导致ZO-1紧密连接蛋白错误定位、基质金属蛋白酶-2异常激活并释放促炎细胞因子,进而破坏血脑屏障的完整性与功能,同时损害其血管生成能力。药物抑制p38MAPK/NF-κB信号通路或使用衰老细胞清除剂清除衰老内皮细胞,是保护血脑屏障免受氧化应激损伤、维持神经血管健康的潜在有效策略。但这些发现目前仅限于体外模型,需要在体研究进一步验证。
阅读英文原文:https://www.mdpi.com/2073-4409/13/15/1292
Cells 期刊介绍
主编:Cord Brakebusch, The University of Copenhagen, Denmark; Alexander E. Kalyuzhny, University of Minnesota, USA
期刊涵盖细胞生物学、分子生物学和生物物理学等方面的研究。目前已被SCIE (Web of Science)、PubMed、MEDLINE、PMC等数据库收录。
2024 Impact Factor:5.2
2024 CiteScore:10.5
Time to First Decision:15.5 Days
Acceptance to Publication:2.8 Days
期刊主页:https://www.mdpi.com/journal/cells

https://blog.sciencenet.cn/blog-3516770-1529665.html
上一篇:Lubricants 中国矿业大学朱少禹博士和合肥工业大学孙军教授主持特刊:轴承润滑的多物理场建模
下一篇:Molecules 天津大学丁辉副教授与展思辉教授主持特刊“中国绿色化学:推进可持续科学,共创美好世界 (第二卷)”