博文
Microorganisms MASLD的肠-肝轴机制:从宿主-微生物组交互到精准治疗
||
研究背景
代谢功能障碍相关脂肪性肝病 (MASLD) 已成为全球最常见的慢性肝病,其病程可从单纯性肝脂肪变性进展为脂肪性肝炎,甚至发展为肝硬化和肝细胞癌。然而,当前临床诊疗面临两大瓶颈:诊断上依赖有创的肝穿刺活检;治疗上则因患者依从性差而效果有限,且获批药物极少。在这一困境下,位于肠道与肝脏之间的“肠-肝轴”成为了研究焦点。肠道微生物群作为连接宿主代谢与免疫的桥梁,被认为是调控MASLD病程的关键“推手”。
基于此,南京大学医学院王婷婷/赵越团队在 Microorganisms 发表综述论文,系统梳理了宿主因素如何塑造MASLD易感性微生物组,揭示了菌群失调促进肝病进展的核心机制,并展望了基于机制的精准治疗策略。
主要内容
谁在塑造“促病”的肠道微生态?
肠道微生物组的组成和功能持续受宿主遗传和多种生活方式因素影响 (图1)。性别对肠道菌群构成和MASLD易感性有深远影响,男性患病率更高,且肠道菌群多样性降低,这与雌激素的保护作用及性别特异的菌群分布密切相关。遗传因素同样参与调控,PNPLA3风险基因型与特定细菌和真菌类群的改变相关,而肠道TM6SF2的扰动可通过肠-肝轴加重MASLD表型。饮食是重要的可调节因素,西式高脂低纤维饮食会减少短链脂肪酸 (SCFA) 的产生,破坏肠道屏障;而地中海饮食则能促进有益菌增殖,改善代谢。此外,昼夜节律紊乱、吸烟和药物 (如质子泵抑制剂、二甲双胍) 均可通过影响肠道菌群参与MASLD发病。这些因素共同作用,最终形成一个“代谢性菌群失调”的状态,为MASLD的发生埋下伏笔。
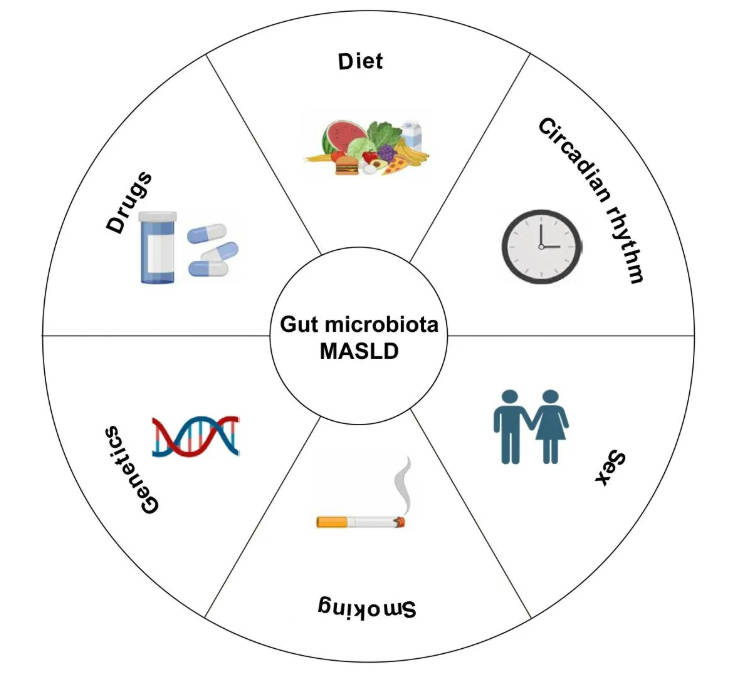
图1. 影响MASLD肠-肝轴的宿主与行为因素
肠道菌群如何“攻击”肝脏?
MASLD相关的菌群失调不仅是组成变化,更是功能改变,主要通过两个相互关联的机制轴损害肝脏 (图2)。
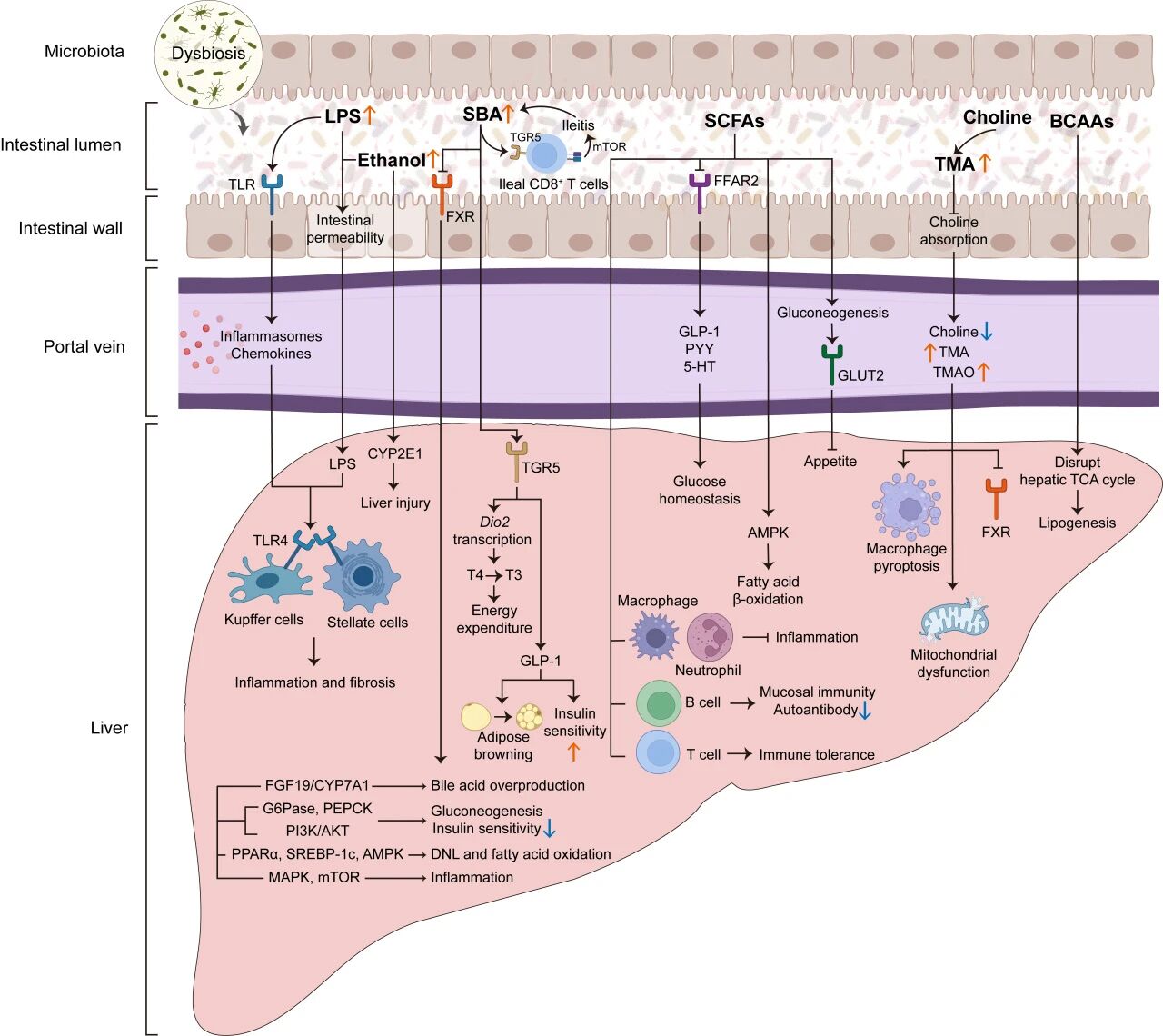
图2. 肠道菌群失调通过肠-肝轴促进MASLD进展的机制
肠屏障-免疫轴:菌群失衡可破坏肠道紧密连接完整性,增加肠黏膜通透性,促使脂多糖 (LPS) 等病原体相关分子模式 (PAMP) 通过门静脉易位至肝脏。LPS靶向Kupffer细胞和肝星状细胞表面的Toll样受体,激活炎症反应和纤维化信号通路,进一步破坏肠黏膜完整性,形成恶性循环 (图3)。
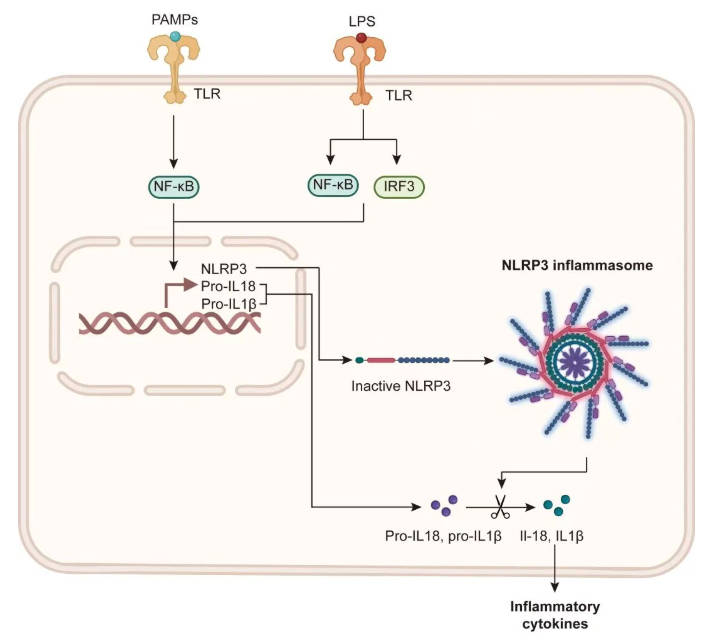
图3. 肠道来源的病原体相关分子模式诱导肝脏炎症的分子机制
代谢轴:菌群代谢产物是肝脏功能的重要调节分子。胆汁酸代谢紊乱是MASLD进展的核心机制之一,通过FXR和TGR5受体扰乱糖脂代谢和炎症反应。SCFA具有多面性作用,既可作为肠上皮能量来源,也能激活游离脂肪酸受体,调节胃肠激素分泌、肠道糖异生和免疫细胞分化。胆碱代谢方面,特定细菌可将膳食胆碱转化为TMA,进而在肝脏氧化为促炎物质TMAO,加剧肝脏脂肪变性和纤维化。此外,菌群产生的内源性乙醇、支链短链脂肪酸等代谢物也可加重肝脏脂肪变性和炎症。
治疗策略:从“广谱调节”走向“精准打击”
基于上述机制,综述评估了当前的微生物靶向疗法 (图4)。益生菌、益生元和合生元等第一代微生物靶向疗法可通过抗炎、增强屏障和抗菌机制改善脂质代谢;粪菌移植 (FMT) 短期内可改善胰岛素敏感性和肝脏脂肪。后生元通过靶向微生物代谢途径 (如胆汁酸受体激动剂) 或通过增加共生菌产生的有益代谢物 (如SCFA) 的水平改善MASLD。特定微生物及其代谢物还可通过免疫调节减轻炎症。此外,地中海饮食和限时进食 (TRE) 等饮食策略也可调整肠道菌群的组成和功能,从而改善炎症和脂质积累。
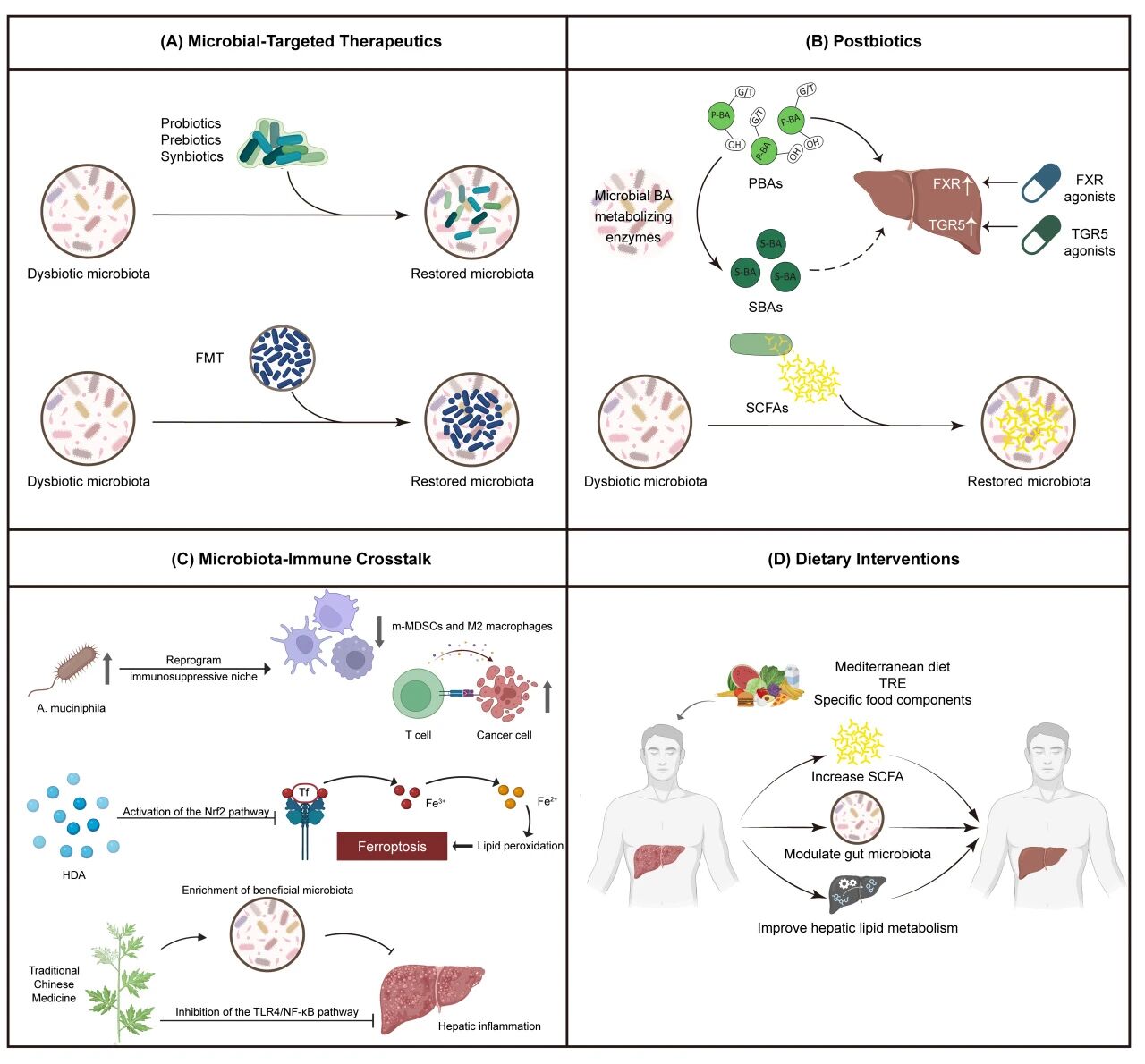
图4. 针对MASLD的微生物靶向干预措施
研究总结
综上所述,MASLD绝非简单的肝脏孤立性疾病,而是由宿主因素、环境与肠道微生态系统共同作用下的多系统代谢紊乱。本综述通过整合现有证据,将我们对MASLD的认识从“相关”提升到了“机制”层面,并构建了一个清晰的“环境因素 → 菌群失调 → 核心机制轴 → 肝脏病理”的逻辑链条。
展望未来,MASLD的管理必须从“一刀切”的补充剂模式,转向基于多组学患者分层的因果驱动型精准治疗。利用噬菌体精准清除致病菌、利用工程菌递送特定药物、利用真菌代谢物调节宿主代谢,这些新兴技术将重塑MASLD的治疗格局。正如文中所言,下一个突破点在于:将“肠-肝轴”的基础机制洞察,切实转化为能够延缓、阻止甚至逆转肝病进展的个性化治疗方案。
阅读英文原文:https://www.mdpi.com/2076-2607/14/2/471
Microorganisms 期刊介绍
主编:Nico Jehmlich, UFZ-Helmholtz Centre for Environmental Research, Germany
期刊主题涵盖微生物学的各个研究领域,主要发表环境、植物、食品、肠道、医药、技术等微生物相关领域的学术文章。现已被 SCIE (Web of Science)、PubMed (NLM)、Scopus 等重要数据库收录。
2024 Impact Factor:4.2
2024 CiteScore:7.7
Time to First Decision:20 Days
Acceptance to Publication:2.9 Days
期刊主页:https://www.mdpi.com/journal/microorganisms

https://blog.sciencenet.cn/blog-3516770-1528221.html
上一篇:能源类期刊4月2日华中科技大学专场 | MDPI 作者培训会
下一篇:Agronomy:迈向循环、健康与智能的农业新生态