博文
Medical Sciences:氧化应激——糖尿病血管并发症的核心驱动与治疗新方向
||
研究背景
糖尿病及其血管并发症已成为全球重大健康威胁。2019 年全球糖尿病患病率达 9.3%,预计 2045 年将增至 10.9%,影响 7 亿人。糖尿病引发的大血管 (冠心病、脑血管疾病等) 和微血管 (糖尿病肾病、视网膜病变等) 并发症,是导致患者致残致死的主要原因。Wayne State University 的 Bipradas Roy 博士在 Medical Sciences 发表的综述,系统揭示了氧化应激在糖尿病血管并发症中的核心作用及分子机制,为临床治疗提供了全新靶点。
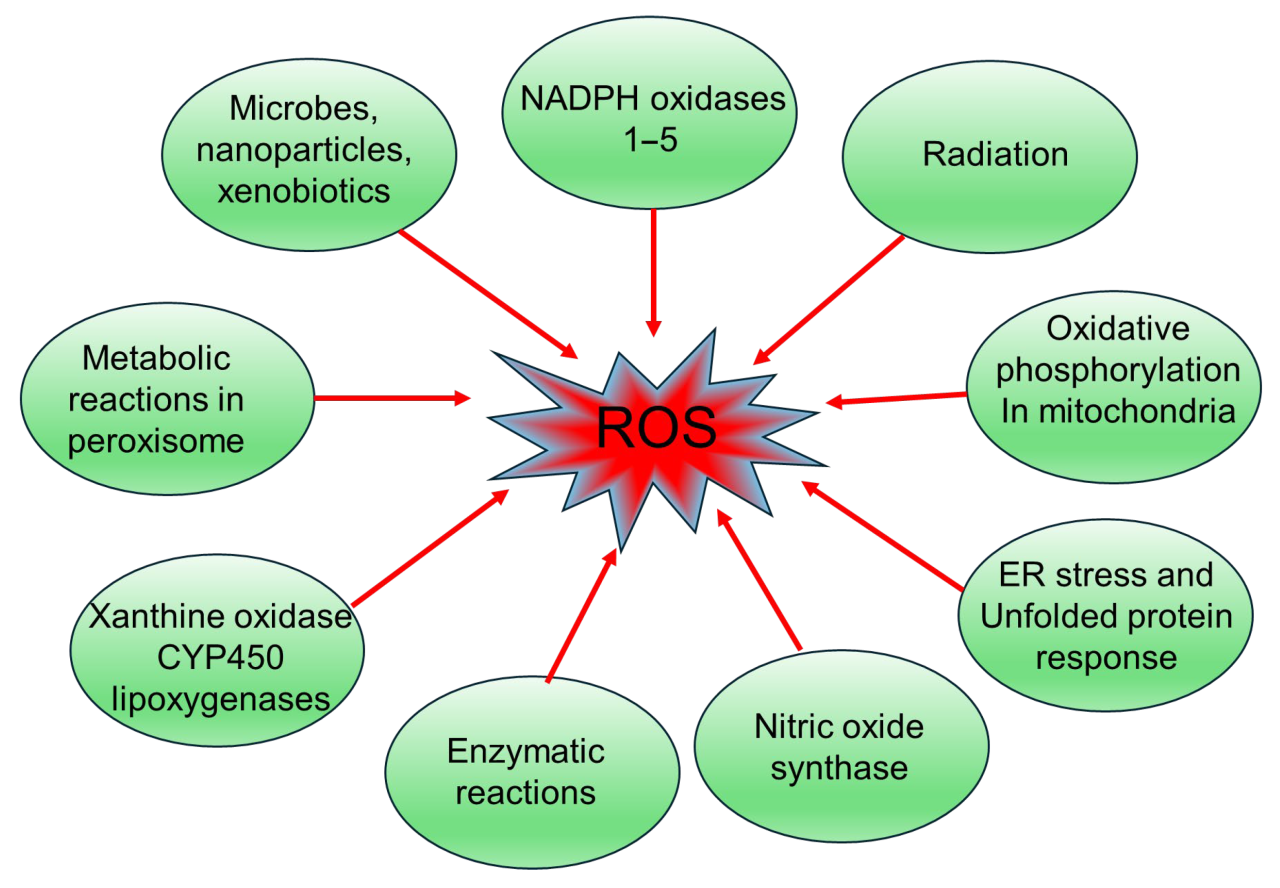
注:ROS 产生途径包括 NADPH 氧化酶 (1-5 亚型)、线粒体氧化磷酸化、内质网应激、黄嘌呤氧化酶、一氧化氮合酶等,多途径共同加剧糖尿病状态下的氧化应激损伤。
氧化应激:糖尿病血管损伤的重要危险因素
氧化应激源于活性氧 (ROS) 的过量产生与抗氧化系统失衡。在糖尿病慢性高血糖状态下,线粒体电子传递链泄漏、NADPH 氧化酶激活等多重机制导致 ROS 大量累积,攻击蛋白质、脂质和 DNA 等生物分子,引发血管细胞功能紊乱。
ROS 不仅直接损伤血管内皮细胞,导致一氧化氮 (NO) 生物利用度下降、血管舒张功能障碍,还会激活 AGE/RAGE、PKC 等信号通路,进一步放大炎症反应和血管重构。研究发现,糖尿病患者体内抗氧化酶 (如超氧化物歧化酶、过氧化氢酶) 活性显著降低,使得血管组织对氧化损伤的抵抗力减弱,加速动脉粥样硬化、肾纤维化等并发症进展。
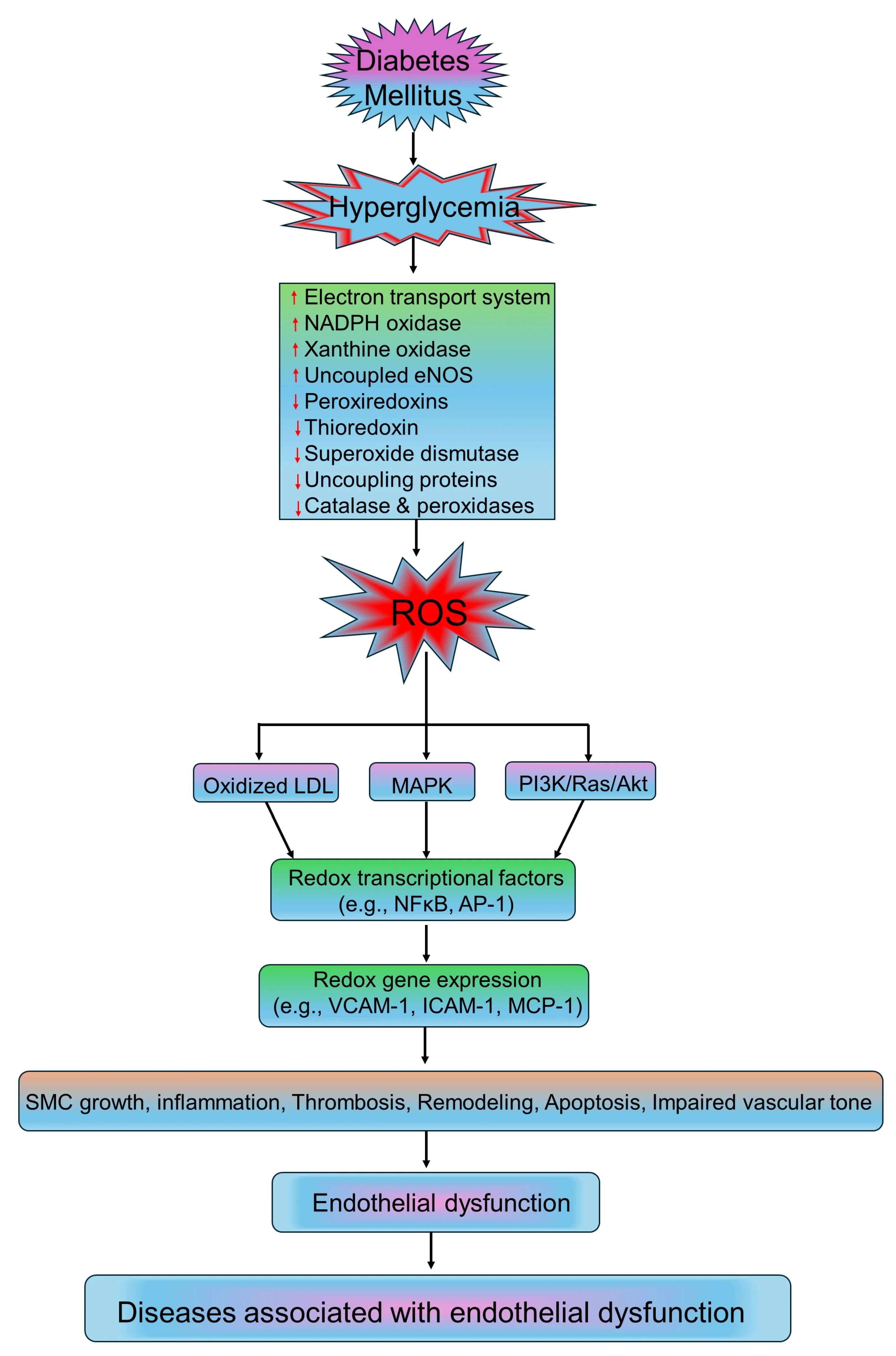
注:高血糖通过上调电子传递链、NADPH 氧化酶等途径增加 ROS 产生,同时抑制抗氧化防御系统,最终通过激活 NFκB、AP-1 等转录因子,引发血管平滑肌细胞增殖、炎症反应和血栓形成。
多维度治疗策略:靶向氧化应激的突破
针对氧化应激的核心作用,研究提出了多层次治疗方案。在血糖管理药物中,SGLT2 抑制剂 (如达格列净) 和 GLP-1 受体激动剂 (如利拉鲁肽) 已被证实具有独立于降糖作用的抗氧化效应,通过抑制线粒体 ROS 生成、激活 AMPK/SIRT1 通路保护血管功能。
靶向 ROS 生成源头的药物研发取得进展,NOX 抑制剂 (如 GKT137831) 可选择性抑制 NADPH 氧化酶 1 和 4 亚型,减少血管 ROS 产生;线粒体靶向抗氧化剂 (如 MitoQ、SS-31) 能精准清除线粒体来源的 ROS,修复线粒体功能。此外,Nrf2 激活剂 (如萝卜硫素) 可增强机体自身抗氧化能力,通过上调 HO-1、NQO1 等抗氧化基因表达,减轻血管炎症和纤维化。
值得关注的是,ferroptosis 抑制剂 (如铁抑素 - 1) 和纳米药物递送系统的发展,为精准干预氧化应激提供了新工具。联合生活方式干预 (如地中海饮食、规律运动) 可进一步激活体内抗氧化通路,与药物治疗形成协同效应。
研究展望:从机制到临床的转化
尽管传统抗氧化剂 (如维生素 E、C) 在大型临床试验中未显示明确获益,但精准靶向氧化应激通路的新一代疗法展现出巨大潜力。未来研究需聚焦生物标志物指导下的个体化治疗,通过检测氧化 LDL、8-iso-PGF2α 等指标,筛选适合抗氧化治疗的患者群体。
同时,多靶点联合治疗策略 (如 SGLT2 抑制剂 + NOX 抑制剂) 已在动物实验中显示协同保护效应,有望成为临床研究的新方向。随着对氧化应激分子机制的深入解析, redox 生物学指导的精准医疗将为糖尿病血管并发症的防治带来革命性突破,为全球数百万患者带来新希望。
阅读英文原文:https://www.mdpi.com/2076-3271/13/3/87
Medical Sciences 期刊介绍
主编:Prof. Dr. Antoni Torres, Universidad de Barcelona; Instituto de Salud Carlos III, Spain
期刊旨在发表基础、转化和临床医学各方向的研究,主要刊发疾病发病机理、转化研究、实验室和动物研究、药理学、临床医学、流行病学和健康改善策略等领域的最新研究成果。目前已被 PubMed、PMC、MEDLINE、DOAJ 等重要数据库收录。
2024 Impact Factor:4.4
2024 CiteScore:8.7
Time to First Decision:18.7 Days
Acceptance to Publication:2.8 Days
期刊主页:https://www.mdpi.com/journal/medsci

https://blog.sciencenet.cn/blog-3516770-1526167.html
上一篇:Hearts:心脏病学中的大型语言模型
下一篇:Social Sciences 陪产假:不止是假期,更是责任