博文
UCLA化学家首先合成了可对抗帕金森氏症的海洋分子
||
UCLA化学家首先合成了可对抗帕金森氏症的海洋分子
诸平
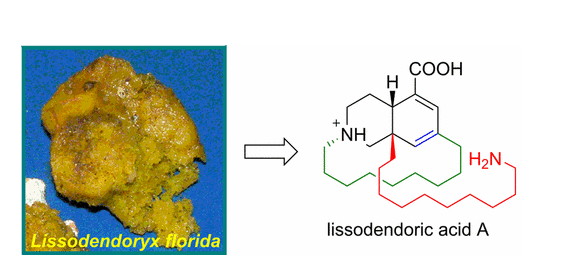

Fig. 2 Neil Garg
据美国加州大学洛杉矶分校(University of California Los Angeles简称UCLA)2023年1月19日报道,该校的化学家首先合成了可以对抗帕金森氏症的海洋分子(UCLA chemists are first to synthesize ocean-based molecule that could fight Parkinson’s)。在生产 lissodendoric acid A 时,该团队使用了一种他们认为可能有助于加速药物发现过程的方法。
要点(Key takeaways):
l 在实验室中重建天然分子作为寻找潜在的疾病新药的一部分可能是困难、昂贵且缓慢的。
l 问题是许多化学过程往往不仅会产生自然界中发现的分子版本,还会产生可能无用甚至危险的分子镜像版本。
l 加州大学洛杉矶分校的化学家在合成一种在海海绵(sea sponge)中发现的新的、具有潜在治疗作用的分子时使用了一种反应性化合物,这种化合物可以帮助他们只生成所需的分子版本,从而使合成效率更高、成本更低。
加州大学洛杉矶分校的有机化学家创造了在海海绵中发现的一种分子的第一个合成版本,这种分子可能对帕金森病(Parkinson’s disease)和类似疾病有治疗作用。这种被称为 lissodendoric acid A 的分子似乎可以抵消其他可能破坏DNA、RNA和蛋白质甚至破坏整个细胞的分子。
在一个有趣的转折中,研究团队使用了一种不寻常的、长期被忽视的化合物,称为环状丙二烯(cyclic allene),以控制在实验室中产生可用分子版本所需的化学反应链中的关键步骤——他们说这一进步可能证明在开发用于药物研究的其他复杂分子方面具有优势。相关研究结果于 2023年1月19日已经在《科学》(Science)杂志网站发表——Francesca M. Ippoliti, Nathan J. Adamson, Laura G. Wonilowicz, Daniel J. Nasrallah, Evan R. Darzi, Joyann S. Donaldson, Neil K. Garg. Total synthesis of lissodendoric acid A via stereospecific trapping of a strained cyclic allene. Science, 19 Jan 2023, 379(6629): 261-265. DOI: 10.1126/science.ade0032. https://www.science.org/doi/10.1126/science.ade0032
加州大学洛杉矶分校的肯尼斯·特鲁布拉德(Kenneth N. Trueblood)化学与生物化学教授(UCLA’s Kenneth N. Trueblood Professor of Chemistry and Biochemistry)、该研究的通讯作者尼尔·加格(Neil Garg)说:“当今绝大多数药物都是通过合成有机化学制造的,我们在学术界的作用之一是建立新的化学反应,这些反应可用于快速开发具有复杂化学结构的药物和分子,从而造福世界。”
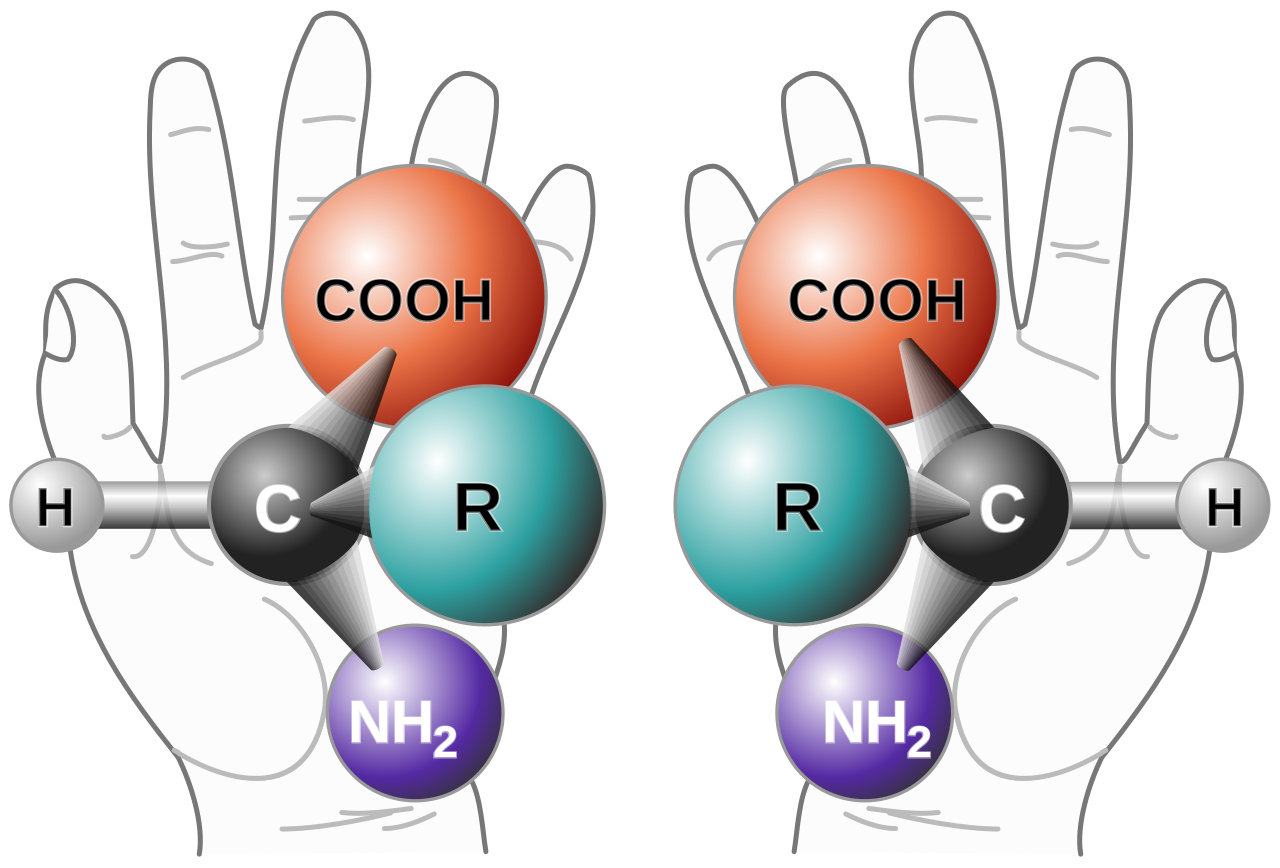
尼尔·加格说,使这些合成有机分子的开发复杂化的一个关键因素就是手性(chirality or “handedness”)。许多分子——包括 lissodendoric acid A——可以以两种不同的形式存在,这两种形式在化学上是相同的,但却是彼此的3D镜像,就像人的左右手一样,它们被称为对映异构体或对映体(enantiomer)。
当用于药物时,分子的一种对映异构体可能具有有益的治疗效果,而另一种可能根本不起作用——甚至被证明是危险的。不幸的是,在实验室中创建有机分子通常会产生两种对映异构体的混合物,并且化学去除或逆转不需要的对映异构体会增加困难、成本和延迟过程。 图2(Fig. 2)说明了自然界中的分子——在这种情况下,是一种普通氨基酸——如何有两种对映体,或镜像版本。
为了应对这一挑战并快速有效地只生产几乎只存在于自然界中的lissodendoric acid A对映体,尼尔·加格和他的团队在他们的12步反应过程(12-step reaction process)中使用环丙二烯作为中间体。这些高反应性化合物于20世纪60年代首次被发现,此前从未被用于制造如此复杂的分子。
尼尔·加格说:“环状丙二烯,自从半个多世纪前被发现以来,它们在很大程度上已被遗忘。这是因为它们具有独特的化学结构,并且在生成时只存在几分之一秒。”
研究小组发现,他们可以利用这些化合物的独特性质来生成一种特殊的手性形式的环状丙二烯,这反过来又会导致化学反应,最终几乎完全产生所需的 lissodendoric acid A 分子的对映异构体。
化学家们说,尽管能够合成出一种lissodendoric acid A的类似物是测试该分子是否具有适合未来治疗的性质的第一步,但合成该分子的方法可以立即使其他参与药物研究的科学家受益。
尼尔·加格说:“通过挑战传统思维,我们现在已经学会了如何制造环状丙二烯并使用它们来制造复杂的分子,如 lissodendoric acid A。我们希望其他人也能够使用环丙二烯来制造新药。”
该研究的共同作者是加州大学洛杉矶分校的博士生弗朗西斯卡·伊波利蒂(Francesca Ippoliti),现为美国威斯康星大学(University of Wisconsin)的博士后学者;加州大学洛杉矶分校的博士生Laura Wonilowicz和Joyann Donaldson(现为辉瑞肿瘤药物化学研究者);加州大学洛杉矶分校博士后研究员南森·亚当森(Nathan Adamson)和埃文·达兹(Evan Darzi);和加州大学洛杉矶分校化学与生物化学助理兼职教授丹尼尔·纳斯鲁拉(Daniel Nasrallah)。埃文·达兹现任初创公司ElectraTect的首席执行官,该公司是尼尔·加格实验室的衍生品。
上述介绍,仅供参考。欲了解更多信息,敬请注意浏览原文或者相关报道。
Chemists often rely on strained intermediates to drive reactions that relieve the strain. In this context, however, cyclic allenes that cram adjacent double bonds into tight carbon rings have been underexploited. Ippoliti et al. now report a synthetic route to lissodendoric acid A, a marine natural product that relies on transient generation of a cyclic allene to prepare the fused ring core (see the Perspective by Jankovic and West). They accessed a single mirror-image form of the allene from a chiral precursor by fluoride attack on a silicon substituent and displacement of an adjacent bromide, setting up a stereospecific Diels-Alder cycloaddition with a pyrone reagent. —JSY
Small rings that contain allenes are unconventional transient compounds that have been known since the 1960s. Despite being discovered around the same time as benzyne and offering a number of synthetically advantageous features, strained cyclic allenes have seen relatively little use in chemical synthesis. We report a concise total synthesis of the manzamine alkaloid lissodendoric acid A, which hinges on the development of a regioselective, diastereoselective, and stereospecific trapping of a fleeting cyclic allene intermediate. This key step swiftly assembles the azadecalin framework of the natural product, allows for a succinct synthetic endgame, and enables a 12-step total synthesis (longest linear sequence; 0.8% overall yield). These studies demonstrate that strained cyclic allenes are versatile building blocks in chemical synthesis.
https://blog.sciencenet.cn/blog-212210-1372934.html
上一篇:更好地了解癌症和心脏病
下一篇:结肠癌试验的“显著”结果