博文
【深读文献】当激酶活性可以用光控制后会发生什么?
 精选
精选
|||
2017年2月24日,science杂志发表了斯坦福大学MichaelZ. Lin组蛋白改造方面的文章,题目为“Optical controlof cell signaling by single- chain photoswitchable kinases”。文章主要内容是设计了受光调控的激酶蛋白,可以对细胞内的信号通路进行人为控制。
引言:
此前,大家已经发现了许多自然界存在的光敏蛋白结构域,主要通过改变细胞内定位、异构调节、扣留或者片段补偿等方式实现利用光照改变蛋白的活性,但是没有真正意义上的不受细胞内定位影响的光控激酶被报道。
正文:
作者首先寻找合适的受光调控的可二聚化的结构域,因为自然界不存在,所以作者从此前已经被报道的可以被可见光照射解聚的四聚体绿色荧光蛋白Dronpa145N,通过引入突变打破了原先反向平行的二聚体表面,使横向的二聚体表面亲和力加强,并且为了提高二聚化的能力,作者设计了可受光解离的Dronpa二聚体结构域,并取名为pdDronpa1(图1)。这种结构域在500nm的青色光照射下会发生解聚而使自身荧光消失,但是在400nm的紫色光下自身荧光又会恢复。并且通过一系列生化实验证明这个结构域适合形成分子内的二聚化。
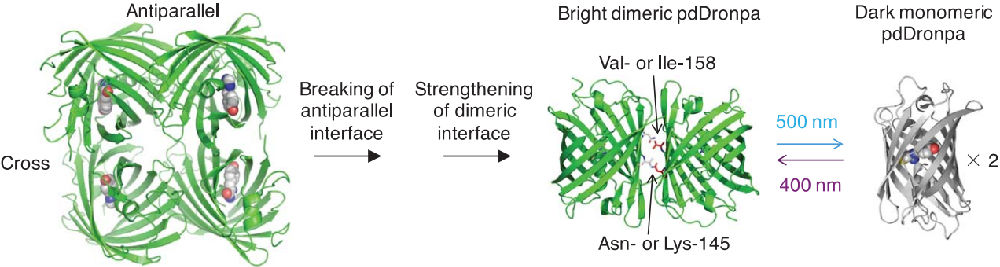
图1 pdDronpa1结构域的改造示意图
接下来就是应用了。
作者首先选择了影响细胞增殖、分化、迁移和凋亡过程的Raf-MEK-ERK信号通路。通过将pdDronpa1结构域与MEK1的激酶结构域连接起来(如图2A所示),称为psMEK1。然后将质粒转入细胞,发现500nm的青色光照射后细胞内的磷酸化ERK水平明显增加,其中未转染质粒的细胞用血清刺激后磷酸化ERK水平增加是作为阳性对照,因为血清中存在生长因子,可以刺激细胞内这条信号通路激活(如图2B所示)。另外,PsMEK1tight质粒是通过对结构域进行改造降低了细胞内的本底磷酸化ERK水平。通过这个实验可以看出psMEK1活性确实可以被青色光控制。
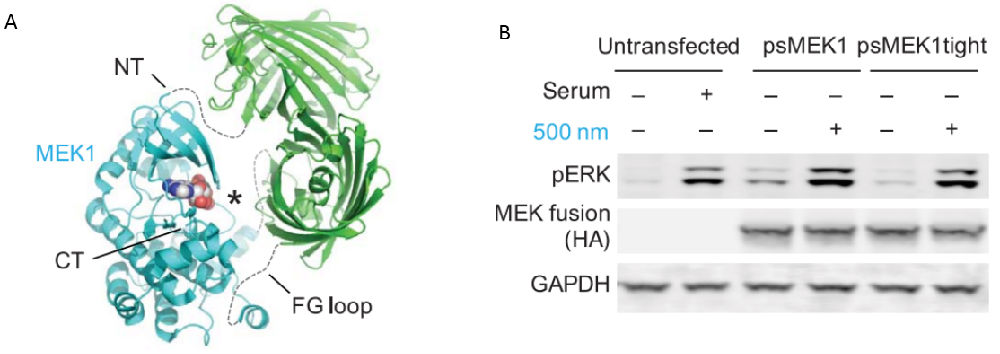
图2 psMEK1在青色光照射下显著增加pERK水平
既然设计的psMEK1酶活可以被人为控制,那么这个蛋白可以作为工具进行抑制剂筛选。具体的策略是过表达psMEK1融合磷酸化ERK移位的报告基因(未磷酸化ERK在细胞核,磷酸化ERK在细胞质)质粒(psMEK1-P2A-ERKKTR-mRuby)的细胞在药物处理后再用500nm青色光照射,如果抑制剂有作用,磷酸化ERK主要在细胞核;如果抑制剂没有作用,磷酸化ERK转移到细胞质(图3A和B)。从图3C可以看出MEK和ERK的抑制剂是有作用的,而EGFR和Raf的抑制剂并不起作用。

图3 利用 psMEK1蛋白筛选RAS-Raf-MEK-ERK信号通路抑制剂
另外,作者还鉴定到了RAS-Raf-MEK-ERK信号通路中的一个负反馈机制,即磷酸化的ERK可以促进磷酸化的MEK发生去磷酸化,从而避免ERK过度磷酸化激活(图4)。
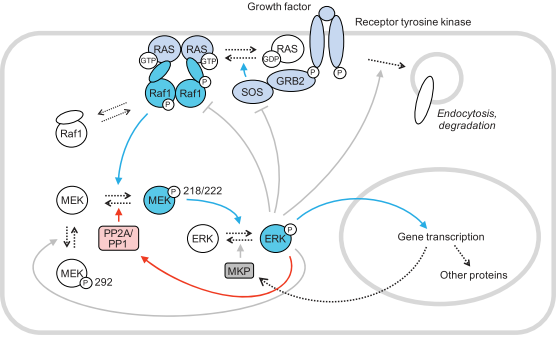
图4 pERK 负反馈抑制促进MEK去磷酸化
最后,作者还想通过在活体动物体内检测构建的psRaf1和psMEK1是否具有生理作用。他们采用线虫作为研究模型,因为线虫的尾部会因细菌感染而激活Raf-MEK-ERK通路发生保护性的肿胀反应。在wildtype组虽然用500nm青色光照射,但是并没有发现肿胀现象,用激活的MEK1和Raf1-CAAX载体转入线虫细胞后发现出现明显的变化,和文献报道一致,作为阳性对照。接着,可以发现psRaf1和psMEK1质粒转入后在500nm青色光照射下可以诱导明显的尾部肿胀表型(图5)。

图5 psRaf1和psMEK1过表达导致线虫发生尾部肿胀反应
整篇文章显示了作者们强大的蛋白改造能力,有兴趣的同学可以看全文。pdf mp4
最后介绍一下通讯作者Michael Z. Lin博士和实验室

Michael Z. Lin博士
Michael Z. Lin博士本科在哈佛取得文科学士学位,在UCLA取得医学博士学位,然后又在哈佛师从生化和神经生物学系Michael Greenberg教授并取得哲学博士学位。获得博士学位后去了诺贝尔奖获得者钱永健实验室从事博士后训练。2009年获得斯坦福大学儿科和生物工程系助理教授职位并建立自己的实验室。在斯坦福主要研究荧光蛋白的改造,创造出神经活性和可塑性的新感应器蛋白,并可以用光控制蛋白的活性。Lin博士获得众多奖项,包括:Burroughs Wellcome Career Award forMedical Scientists, a Rita AllenScholar Award, 和Damon Runyon-Rachleff Innovation Award等。
https://blog.sciencenet.cn/blog-294011-1039674.html
上一篇:【实验方法】我是如何做分子克隆的
下一篇:诱导多能干细胞技术的十年回顾以及展望