博文
两个老靶点,一点新突破:RAS和MYC的降解剂
||
2026年2月下旬,Nature Communications上发表了一篇题为Heterobifunctional proteomimetic polymers for targeted degradation of MYC and KRAS的文章,由美国西北大学(Northwestern U)的Nathan C. Gianneschi和Sarki A. Abdulkadir两个实验室合作完成,其重要贡献在于采用一种的HYbrid DegRAding Copolymer (HYDRAC)的靶向蛋白降解技术平台,实现了两种著名的癌基因编码的蛋白KRAS和MYC,并且体外强效的降解可以转化为不错的体内抗肿瘤效果。
直接RAS为靶的抗癌药研究,我在以前已经发表过文章介绍(科学网的两篇博文,以及本公众号2019年的文章),源于我在组内的文献分享/演讲,以及后续的文献追踪。该领域最初的突破来源于实验室的RAS G12C突变体的靶向分子的成功,在2013年由美国加大旧金山分校(UCSF)的Kevin Shokat实验室于Nature刊发论文,并在后续成立Mirati公司,将MRTX849(即Adagrasib,阿达格拉西布)开发上市。与此同时,工业界也不甘人后,Amgen公司研发的AMG-510(即Sotorasib,索托拉西布),最终于2021年成为首先上市的RAS靶向抗癌药。
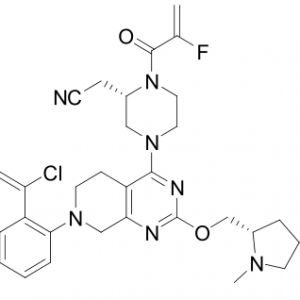
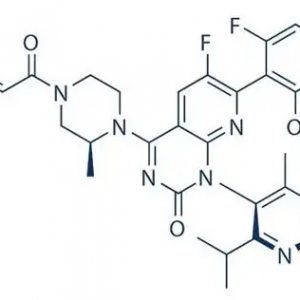
这二家公司从药化角度上说思路是类似的:均是基于switch Ⅱ变构口袋的共价结合抑制剂。二者的结构也有不少类似之处,从结构上直观地可以看到(如下图)。
不过,Sotorasib含有阻转异构体,要获得正确构象的分子,对于合成化学家来说还是挺有挑战性的。从生物学/疾病治疗角度看,Adagrasib的作用与Sotorasib在多个指标上略强或不相上下,但毒性稍强、不良反应率高。此外,Adagrasib入脑能力强,因此对癌症的脑转移有效,这是Sotorasib不具备的特点。
在RAS的不同突变体中,R12C靶向药先获得突破,是因为其处于靶向部位的半胱氨酸的巯基可用共价结合方式获得高亲和力,但该突变所占肿瘤比例其实并不算很高。此后的技术发展,则开始针对R12D等高发生率的肿瘤RAS基因突变,乃至多种突变体同时起效(pan-RAS抑制剂)。有的候选药物如Revolution Medicines的daraxonrasib在今年4月份AACR 2026年会上报告了对胰腺癌获得不错的3期临床试验效果,显著延长中位总生存期(OS),有望获批上市。
以MYC为靶的抗癌药研究开始更早一些,同样也是困难重重,但难点与RAS不同。RAS是GTPase但缺乏足够深的腔穴供小分子强力结合,而直接竞争结合GTP结合位点又面临与激酶抑制剂类似的体内高GTP浓度的阻碍,因此直到发现switch II可被共价抑制剂靶向这一变构位点才获得成功。C-MYC则是转录因子(TF),此前这类蛋白以无法成药即undruggable target而闻名,只有其中能结合小分子内源配体的一类TF,也称作核受体(NR),能被正常或者说经典药化手段所靶向。因此,与RAS靶向类似,前期药化学者对C-MYC也有通过其上下游调控的替代靶向方式,而直接靶向MYC且被成功推上临床的例子据我所知仅有omo-MYC,是一种由91个残基组成的小蛋白(mini-protein,因为如此大的多肽分子,已经不好意思用“肽”称呼了),序列源自MYC bHLH-LZ结构域并进行了数个位点的残基替换。MYC直接靶向之所以能成功,我认为很大程度源于其helix-helix的有序结构可以被靶向。尽管如此,MYC被非肽有机小分子靶向仍是非常困难。顺便说一句,近年来随着司美格鲁肽的巨大成功,肽的成药困难也原来越受关注,对此本文不多做讨论。另外的思路则是利用核酸类分子(RNAi,反义寡核苷酸ASO等),而非传统的通过靶向蛋白质调控其功能。
随着PROTAC为代表的新型蛋白降解剂的大热,人们发现不具备可被传统方式靶向条件的蛋白亦可通过降解方式加以调控,起到比非共价结合的抑制作用更强和更持久的抑制作用(尽管抑制过强和非特异性导致的不良反应是一种隐患),因此各种XXTAC技术不断涌现。
我这里提及的这篇Nat Comm文章,正是通过一种HYDRAC技术(平台),降解KRAS和c-MYC这两个“臭名昭著”的癌蛋白。具体而言,是将与靶点蛋白的结合片段(例如RAS的结合分子,MYC的bHLH-LZ结构域的衍生肽H1),连接上可诱导降解的肽段(例如源自VHL、KEAP 1、CRBN的片段),最终获得不同结合片段-降解片段组合的偶联物,实现对KRAS或c-MYC的降解,并在小鼠体内产生抗肿瘤作用,且无明显全身毒性。
鉴于RAS和MYC在肿瘤发生发展过程中具有协同作用,因此如果能够同时降解两个癌基因将是更有价值的事情。不知HYDRAC同时引入RAS和MYC的结合片段后,是否在与相应的癌蛋白结合时不互相干扰,以及降解作用是否正常。出于某种可以理解的原因(也许是不能等那么久再发大论文,或者是同时降解RAS和MYC的HYDRAC做出来了但效果不佳,需要进一步结构优化),就先发出这篇Nat Comm了吧。
总之,该文的主要目的应该是宣传推广他们的HYDRAC技术,理论上它有同时降解二者的潜力,这也是我最感兴趣的内容。如果论单独降解这两个蛋白,我国科学家已经做出了不错的蛋白降解剂:如厦大的XMU-MP-9降解RAS,深圳实验室的C1降解MYC。文献中也有WBC100这类可诱导原有降解机制实现MYC降解的分子。
注:本文首发于2026.4.23微信公众号“分子间的斗争”
https://blog.sciencenet.cn/blog-99934-1531838.html
上一篇:从C&EN近期的一篇报道谈科研进步与竞争
下一篇:耳顺之年的话(四)科研基金与产出的回顾与思考