博文
氢气注射预防内毒素肝损伤【广中医】
||
氢气注射预防内毒素肝损伤【广中医】
背景:脓毒症时肝脏极易受到内毒素诱导的损伤。氢气(H₂)是一种无色无味气体分子,具有抗氧化与抗炎作用。然而,腹腔注射氢气对脓毒症所致急性肝损伤的作用及其潜在机制尚不明确。
方法:采用生化检测、H&E染色、免疫印迹、免疫荧光及TUNEL染色,探究腹腔注射氢气对脂多糖(LPS)诱导小鼠急性肝损伤的作用与机制;利用AML12细胞及药理学挽救实验验证氢气的作用靶点。
结果:腹腔注射氢气预处理可改善LPS诱导的小鼠急性肝损伤,表现为肝脏炎性细胞浸润减少、血清丙氨酸氨基转移酶(ALT)与天冬氨酸氨基转移酶(AST)水平下调、肝脏3-硝基酪氨酸(3-NT)、丙二醛(MDA)、髓过氧化物酶(MPO)水平降低,还原型谷胱甘肽(GSH)水平上调。机制上,氢气抑制TLR4下游IKK-NF-κB及MAPK(ERK、p38、JNK)信号通路,进而降低LPS小鼠肝脏促炎因子TNF-α、IL-1β、IL-18水平。此外,氢气处理可逆转LPS小鼠肝脏焦亡相关信号:NLRP3炎症小体(NLRP3、ASC、Caspase-1)-GSDMD、Caspase-8/11-GSDMD、Caspase-3-GSDME通路及TUNEL阳性信号。体外通过NLRP3激动剂尼日利亚菌素(nigericin)与抑制剂MCC950的药理学挽救实验,进一步证实氢气靶向NLRP3。
结论:腹腔注射氢气预处理通过调控氧化还原稳态、TLR4介导的固有免疫信号、NLRP3炎症小体激活及焦亡信号,减轻LPS诱导的小鼠急性肝损伤。
Hydrogen gas (H2) pretreatment improves lipopolysaccharide-induced acute liver injury in mice by inhibiting NLRP3 inflammasome activation and pyroptosis signaling
1 引言
脓毒症是宿主对感染反应失调所致的危及生命的多器官功能障碍(1)。脓毒症中,病原体入侵启动的免疫反应无法恢复稳态,最终形成以持续过度炎症与免疫抑制为特征的病理综合征(2)。肝脏参与调控解毒、代谢、免疫等多种生理与病理过程,使其在脓毒症中极易遭受内毒素损伤(3–5)。脓毒症的炎症反应依赖肝脏病原体识别受体(Toll样受体TLRs)的激活,其在脓毒症及脓毒症相关肝损伤发病中至关重要(6)。脂多糖(LPS)是革兰氏阴性菌的组分之一,通过结合靶器官受体TLR4诱导急性炎症并产生促炎因子(7)。LPS诱导的急性肝损伤小鼠模型广泛用于脓毒症及相关器官损伤的发病机制研究、新靶点发现与药物研发。尽管1985–2019年多数国家脓毒症相关死亡率有所下降(8),但脓毒症与感染性休克仍是重大医疗难题,每年累及全球数百万人,致死率达1/3~1/6(9)。因此,亟需为脓毒症患者探寻有效治疗手段与潜力候选药物。
氢气是强效抗氧化剂,兼具抗炎作用。但哺乳动物内源性氢气主要由含氢化酶的微生物产生,因哺乳动物细胞无功能性氢化酶基因。通过吸入氢氧混合气、饮用富氢水、注射富氢生理盐水等方式补充外源性氢气,可对代谢相关脂肪性肝病(MASLD)及缺血再灌注(I/R)肝损伤发挥肝脏保护作用(10)。然而,腹腔注射氢气是否对上述疾病具有治疗作用尚不明确。本团队前期发现,腹腔注射氢气可改善LPS诱导的心功能障碍(11)、减轻急性乙醇暴饮暴食所致急性肝损伤(12)及蛋氨酸胆碱缺乏饮食诱导的小鼠MASLD(13)。本研究采用LPS诱导急性肝损伤小鼠模型模拟脓毒症肝损伤,探究腹腔注射氢气预处理对急性肝损伤的作用;若有效,将进一步解析其潜在的固有免疫分子机制。
2 材料与方法
2.1 脂多糖诱导急性肝损伤动物模型及给药方案
本研究选用雄性C57BL/6小鼠(21–23 g),购自广州中医药大学动物实验中心。所有动物饲养于温度可控、12 h光暗循环的动物房,自由摄食饮水。所有动物均接受人道照料,动物实验方案经广州中医药大学实验动物伦理与使用委员会批准。动物研究遵循ARRIVE 2.0(动物研究:体内实验报告)指南(14,15)。
简要而言,LPS诱导急性肝损伤模型通过单次腹腔注射溶于生理盐水(1 mg/mL)的LPS(5 mg/1000 g,L2880,Sigma-Aldrich;Merck KGaA,德国达姆施塔特)构建。LPS+H₂低剂量组(L)与高剂量组(H)小鼠分别以0.5 mL/100 g、1.0 mL/100 g剂量腹腔注射氢气(99.999%,广州燃气集团有限公司),连续4 d,每日1次。第4天注射氢气30 min后,LPS+H₂(L)、LPS+H₂(H)及LPS组小鼠腹腔注射LPS;对照组给予等体积生理盐水。LPS给药6 h后,小鼠深度麻醉,眼眶静脉丛采血至离心管,室温分离血清,颈椎脱臼处死(16)(图1)。采集肝脏样本,-80 ℃冻存或置于4%多聚甲醛固定液(G1101,Servicebio,武汉)备用。
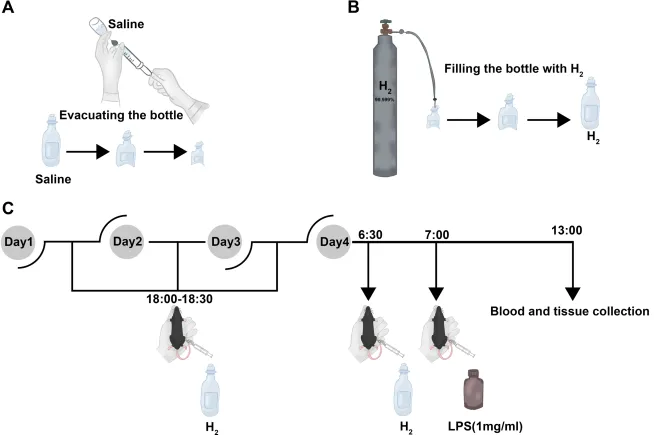
图1
A图:用注射器从瓶中抽取液体制备真空瓶;B图:从气瓶向瓶内充入氢气;C图:为期4天的实验时间线,显示指定时间注射生理盐水或氢气、给予LPS溶液,第4天采血与取材。
氢气腹腔注射方法及实验流程。(A)用50 mL无菌注射器将100 mL无菌生理盐水输液瓶抽真空。(B)打开铝制高压气瓶减压阀,小流量排气,吹扫管路与针头残留空气;随后调大减压阀,向输液瓶充入氢气至无死体积。(C)氢气处理组小鼠前3 d每日18:00–18:30腹腔注射氢气(低剂量0.5 mL/100 g,高剂量1.0 mL/100 g)。第4天末次注射氢气30 min后,LPS组与处理组小鼠腹腔注射LPS(5 mg/1000 g)。LPS给药6 h后,小鼠深度麻醉,眼眶静脉丛采血分离血清,颈椎脱臼处死。具体操作:注射器与针头间连接二通阀,打开阀门,将针头插入氢气瓶,抽取所需体积氢气,立即关闭阀门并拔出针头;快速将针头刺入小鼠腹腔,打开二通阀完成氢气腹腔注射。
2.2 生化检测
采集血样3500 rpm离心15 min。血清ALT、AST检测参照本团队既往方法(17)。肝脏MDA、MPO、GSH按南京建成生物工程研究所试剂盒说明书检测(A003-1-2、A044-1-1、A006-2-1)。
2.3 H&E染色
组织病理学分析采用石蜡切片与苏木精-伊红(H&E)染色,标准流程:(1)肝脏组织4%多聚甲醛固定;(2)置于包埋盒,脱水机(Excelsior AS,Leica,德国)脱水;(3)石蜡包埋,-20 ℃快速冷冻过夜;(4)石蜡切片机(RM2245,Leica,德国)切取约4 μm切片;(5)H&E染色,中性树脂封片,图像采集系统观察。
2.4 免疫印迹
肝脏组织用裂解液提取总蛋白(18),BCA蛋白定量试剂盒(Thermo Fisher Scientific,23225)定量。SDS-PAGE电泳分离蛋白,转印至PVDF膜(Millipore,IPVH00010),按标准流程孵育一抗与二抗(表1)(18)。增强化学发光液(NCM Biotech,P10300)显色,全自动化学发光仪(Tanno 5200,上海天能)成像。Image J软件定量蛋白灰度值,条带右侧分子量按抗体说明书标注(表1)。
表1 抗体信息
2.5 免疫荧光染色
肝脏组织4%多聚甲醛固定24 h,依次经15%、30%蔗糖溶液各脱水24 h。样本包埋于冰冻切片包埋剂(BL557A,Biosharp,合肥),-20 ℃冰冻切片机切片。切片依次用1×PBS洗30 min、1×TBS洗10 min、1×TBST洗10 min;室温羊血清封闭2 h,一抗3-NT孵育过夜。1×TBS洗10 min、1×TBST洗20 min,避光室温二抗孵育2 h。1×TBS洗3次(每次10 min),抗荧光淬灭封片剂(Solarbio,S2110,北京)封片,Zeiss倒置荧光显微镜观察3-NT。GSDMD免疫荧光步骤同3-NT,仅一抗换为GSDMD,二抗换为Alexa Fluor 488标记山羊抗兔IgG。
2.6 肝脏样本TUNEL染色
采用TUNEL试剂盒(E-CK-A320,Elabscience,武汉),流程:石蜡切片二甲苯脱蜡2次(每次10 min),无水乙醇2次(每次5 min),90%、80%、70%乙醇各3 min;PBS洗3次(每次5 min),滤纸吸干周边液体。每样本加100 μL 1×蛋白酶K工作液(蛋白酶K:PBS=1:99),37 ℃孵育20 min;PBS洗3次(每次5 min),加100 μL TdT平衡液,37 ℃孵育20 min,吸水纸吸干。加50 μL标记工作液(TdT平衡液:标记液:TdT酶=35:10:5),室温避光孵育60 min;PBS洗3次(每次5 min)。含DAPI抗淬灭封片剂(Solarbio,S2110,北京)封片,荧光显微镜观察。
2.7 细胞培养与药理学挽救实验
AML12细胞源于转人TGFα基因的CD1小鼠肝细胞,购自武汉普诺赛生命科技有限公司(CL-0602)。肝细胞在AML12专用培养基(CM-0602,普诺赛)中培养,培养基含DMEM/F12+10%胎牛血清+0.5% ITS-G(100×)+40 ng/mL地塞米松+1%双抗,培养条件37 ℃、5% CO₂。肝细胞悬液(100 μL/孔)接种96孔板,至密度约80%。每板设3孔仅含培养基的空白孔。含1%胎牛血清的培养基饥饿24 h,富氢培养基预处理30 min;加入1 μg/mL LPS孵育4 h,再加入5 μM NLRP3激动剂尼日利亚菌素孵育2 h(19);或1 μg/mL LPS孵育5 h,再加入5 μM NLRP3抑制剂MCC950孵育1 h(20)。处理结束后避光加10 μL CCK-8溶液,铝箔包裹孵育1 h。酶标仪450 nm测吸光度(A),细胞存活率(%)=[(A给药组−A空白)/(A对照组−A空白)]×100%。
2.8 统计学分析
符合正态分布(Shapiro-Wilk检验)与方差齐性(Brown-Forsythe检验)的数据采用单因素方差分析(ANOVA),Bonferroni事后检验;正态分布但方差不齐的数据采用Brown-Forsythe与Welch ANOVA,Dunnett T3事后检验。数据以均数±标准差表示,P<0.05为差异有统计学意义。柱状图采用GraphPad Prism 9.3.0(GraphPad Software,美国加州)绘制。
3 结果
3.1 腹腔注射氢气预处理减轻LPS诱导的小鼠急性肝损伤
肝脏是脓毒症主要受累器官之一。本研究首先探究腹腔注射氢气预处理对LPS诱导小鼠急性肝损伤的作用。与对照组相比,LPS诱导肝细胞嗜酸性变性坏死,中央静脉及肝窦内炎性细胞浸润增加(图2A);氢气预处理可改善上述病理改变,高剂量效果优于低剂量(图2A)。此外,氢气预处理较LPS组降低血清ALT、AST水平(图2B、C);但两处理组ALT及LPS+H₂(L)组AST仍高于对照组,LPS+H₂(H)组ALT、AST低于LPS+H₂(L)组,且LPS+H₂(H)组AST与对照组无差异。各组实验前后体重无统计学差异(图2D)。表明腹腔注射氢气预处理对LPS诱导的小鼠急性肝损伤具有预防作用。
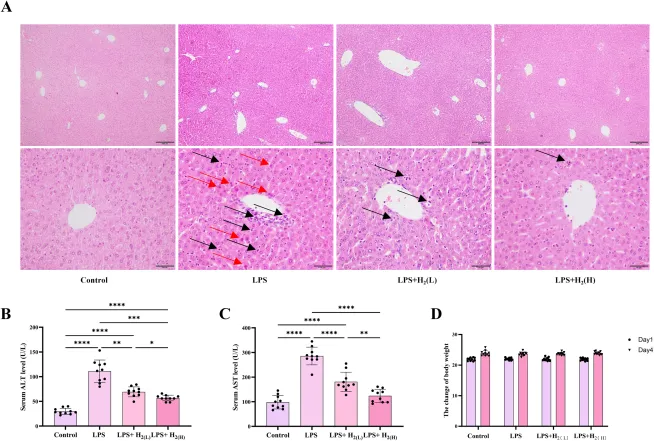
图2
A图:对照组、LPS组、LPS+低剂量H₂、LPS+高剂量H₂肝脏染色显微图,箭头示细胞损伤,呈轻至重度组织学改变;B、C图:血清ALT、AST柱状图,LPS显著升高,氢气处理部分降低;D图:各组第1、4天体重变化,组间差异极小。
氢气预处理减轻LPS诱导的小鼠急性肝损伤。(A)肝脏H&E染色,上图标尺200 μm,下图50 μm;红箭头示变性坏死肝细胞,黑箭头示浸润炎性细胞。(B)血清ALT水平。(C)血清AST水平。(D)实验前后体重。每组n=10,*P<0.05,P<0.01,*P<0.001,P<0.0001;横线示左侧组与右侧组比较。
3.2 氢气预处理抑制LPS小鼠肝脏氧化应激
LPS可增加活性氧(ROS)生成,加剧肝脏氧化应激(21)。3-NT是反映氧化应激的标志物之一(22)。免疫荧光与免疫印迹均显示,LPS升高肝脏3-NT水平,氢气预处理可降低,高剂量效果更优(图3A–C)。ROS可直接损伤脂质,MDA是反映脂质过氧化的常用标志物(23)。结果显示,LPS组肝脏MDA较对照组升高,高剂量氢气预处理可逆转(图3D)。MPO为免疫细胞血红素过氧化物酶家族成员,可生成次氯酸(HOCl)等强氧化物(24),反映组织炎症与氧化应激程度。与对照组相比,LPS升高肝脏MPO水平,LPS+H₂(H)组降低(图3E)。与氧化损伤物质相反,GSH可将H₂O₂还原为H₂O,反映抗氧化能力(25)。LPS组肝脏GSH较对照组降低,高剂量氢气可逆转该下调(图3F)。表明腹腔注射氢气预处理可维持LPS小鼠肝脏氧化还原稳态。
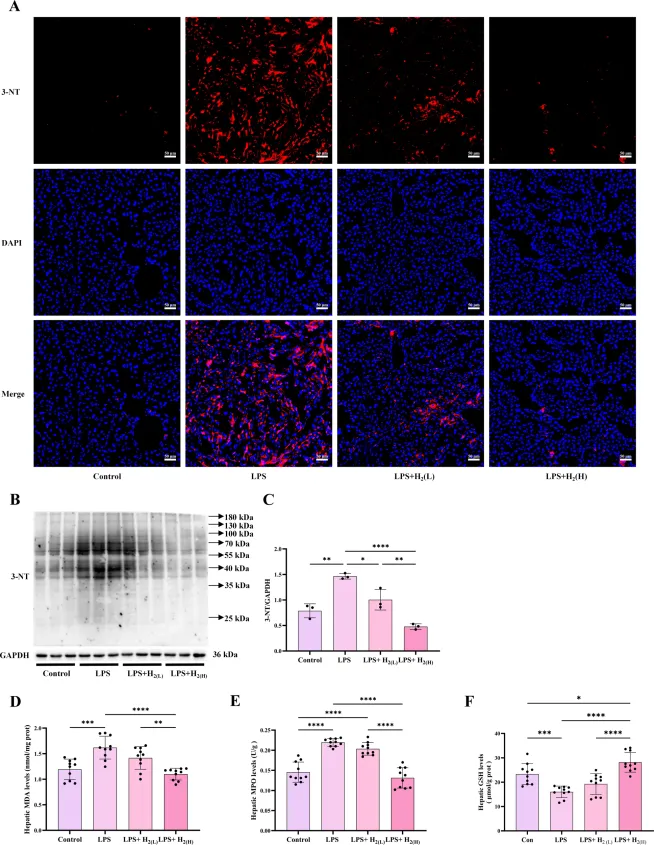
图3
A图:4组肝脏3-NT免疫荧光(红)、DAPI核染(蓝)及融合图,LPS组3-NT信号增强,氢气干预减弱;B图:肝脏3-NT与GAPDH免疫印迹;C图:3-NT/GAPDH定量柱状图;D–F图:肝脏MDA、MPO、GSH定量,LPS升高氧化应激,氢气改善。每组n=3(免疫印迹)、n=10(生化),*P<0.05,P<0.01,*P<0.001,P<0.0001。
3.3 氢气预处理抑制LPS小鼠肝脏TLR4介导的固有免疫信号过度激活
LPS(内毒素)为革兰氏阴性菌外膜关键组分,通过细胞膜TLR4识别,TLR4信号过度激活在脓毒症发病中起关键作用(26)。为探究腹腔注射氢气对LPS小鼠肝脏TLR4信号的影响,免疫印迹检测TLR4及其下游IKK、NF-κB p65、ERK1/2、p38 MAPK、JNK的表达或活化。LPS上调TLR4表达(图4A),增强IKK(图4B)、NF-κB(图4C)磷酸化,氢气可抑制上述上调,高剂量优于低剂量。LPS升高ERK1/2、p38 MAPK、JNK磷酸化,低、高剂量氢气均可抑制MAPK磷酸化,高剂量更优(图5)。表明腹腔注射氢气预处理抑制LPS小鼠肝脏TLR4介导信号过度激活。
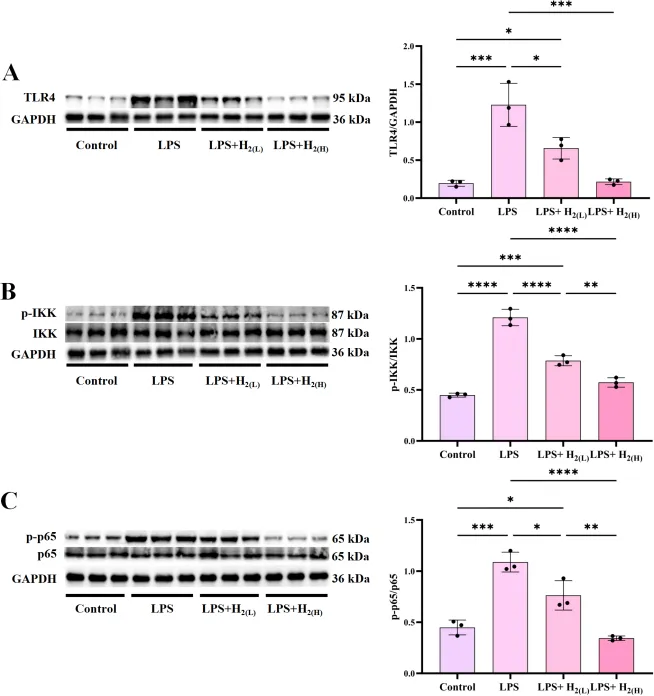
图4
三图分别为TLR4、p-IKK/IKK、p-p65/p65免疫印迹及定量柱状图,LPS升高,氢气处理降低,差异显著。
氢气预处理抑制LPS小鼠肝脏TLR4-IKK-NF-κB固有免疫信号。每组n=3,*P<0.05,P<0.01,*P<0.001,P<0.0001。
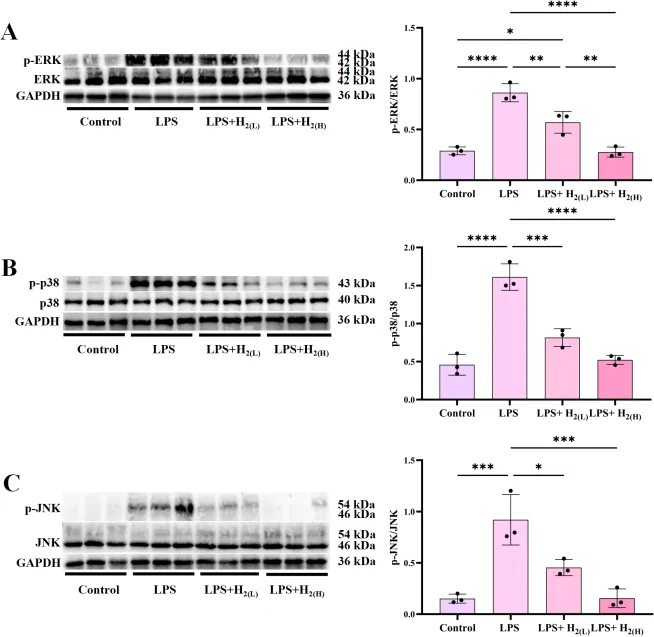
图5
A–C分别为p-ERK1/2、p-p38、p-JNK免疫印迹及定量,LPS升高磷酸化,氢气降低,差异显著。
氢气预处理抑制LPS小鼠肝脏MAPK信号。每组n=3,*P<0.05,P<0.01,*P<0.001,P<0.0001。
3.4 氢气预处理抑制LPS小鼠肝脏促炎因子表达与剪切
TLR4介导固有免疫信号过度激活可导致TNF-α、IL-1β、IL-18过量产生,放大炎症与氧化损伤(27,28)。LPS升高肝脏TNF-α、pro-IL-1β、cleaved-IL-1β、pro-IL-18、cleaved-IL-18水平;氢气预处理可降低上述促炎因子的表达与剪切(cleaved-IL-18无统计学差异)(图6)。表明腹腔注射氢气预处理抑制LPS小鼠肝脏促炎因子表达与剪切。
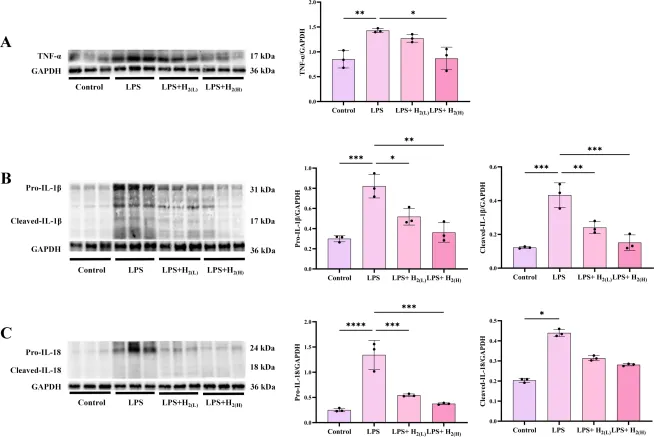
图6
TNF-α、IL-1β、IL-18免疫印迹及定量,LPS升高表达,氢气减弱,差异显著。
氢气预处理抑制LPS小鼠肝脏促炎因子表达与剪切。每组n=3,*P<0.05,P<0.01,*P<0.001,P<0.0001。
3.5 氢气预处理抑制LPS小鼠肝脏NLRP3炎症小体激活与焦亡
TLR4信号除诱导促炎因子表达外,还可通过NF-κB促进NLRP3转录翻译(29)。结果显示,氢气预处理降低LPS诱导的肝脏NLRP3表达,低剂量效果更优(图7A)。多种刺激下,NLRP3与接头蛋白ASC、Caspase-1形成复合物,即NLRP3炎症小体(30,31)。炎症小体的生化功能为激活Caspase-1,促使IL-1β、IL-18成熟及GSDMD剪切,诱导焦亡(炎性程序性死亡)(32)。进一步探究氢气对IL-1β、IL-18剪切的作用是否与调控NLRP3炎症小体相关。免疫印迹显示,LPS上调ASC(图7B)、全长及剪切型Caspase-1(图7C),氢气预处理可降低(图7B、C)。体外NLRP3激动剂尼日利亚菌素与抑制剂MCC950的药理学挽救实验进一步证实氢气作用于NLRP3(图7D、E),提示NLRP3是氢气关键靶点。LPS升高肝脏GSDMD蛋白水平与免疫荧光强度,氢气预处理可降低,低剂量更优(图8A、B)。此外,Caspase-11(人Caspase-4/5同源物)、Caspase-8可剪切GSDMD,Caspase-3可剪切GSDME,诱导非经典焦亡(33,34)。结果显示,LPS升高肝脏全长及剪切型Caspase-8、-11、-3、GSDME水平及TUNEL阳性信号;两种剂量氢气均可抑制Caspase与GSDME的表达、剪切及TUNEL信号,高剂量更优(图8C–G)。表明腹腔注射氢气预处理抑制LPS诱导的小鼠肝脏NLRP3炎症小体激活与焦亡。
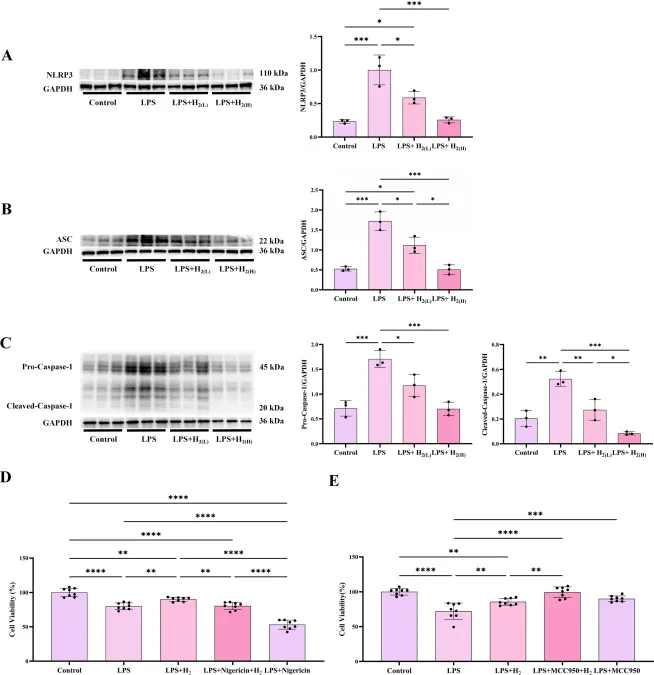
图7
A–C:NLRP3、ASC、Caspase-1免疫印迹及定量;D–E:体外NLRP3激动剂/抑制剂挽救实验细胞存活率。体内n=3,体外n=8,*P<0.05,P<0.01,*P<0.001,P<0.0001。
氢气预处理在LPS小鼠与肝细胞中均抑制NLRP3炎症小体激活。
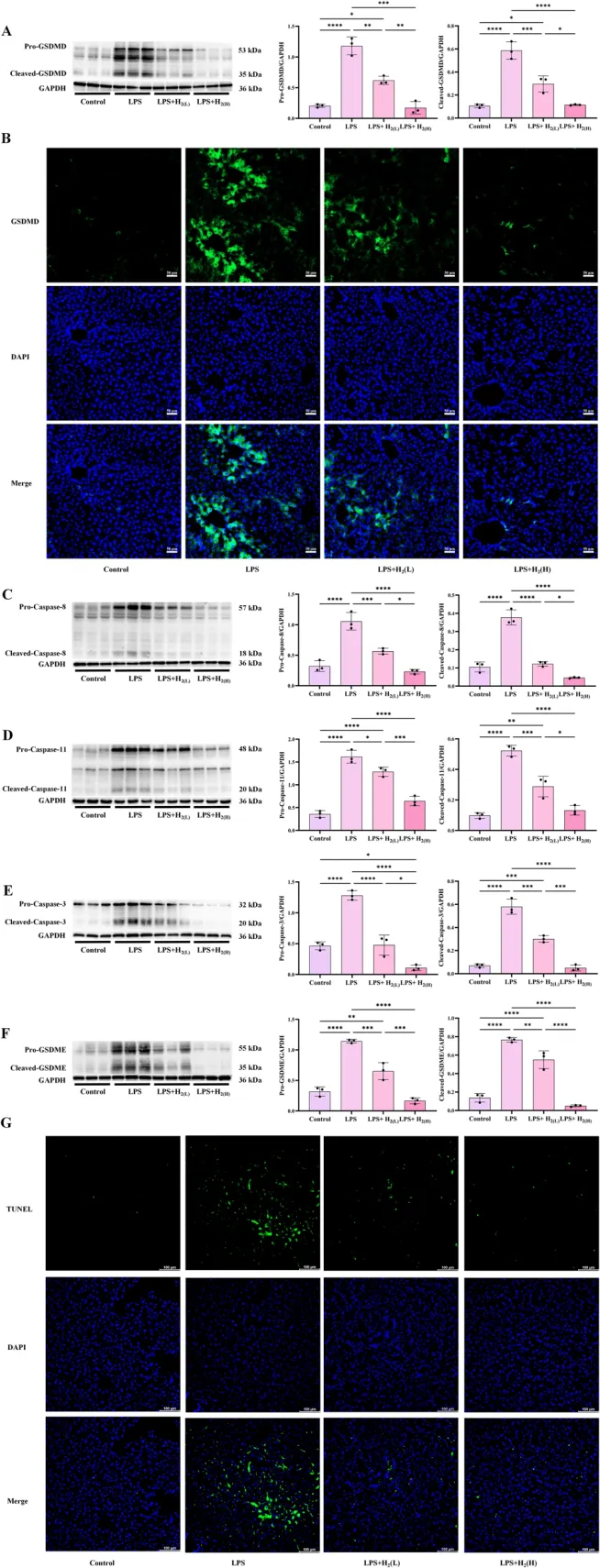
图8
A、C–F:GSDMD、Caspase-8、-11、-3、GSDME免疫印迹及定量;B、G:GSDMD、TUNEL免疫荧光。LPS升高,氢气降低,差异显著。
氢气预处理抑制LPS小鼠肝脏焦亡信号。每组n=3,*P<0.05,P<0.01,*P<0.001,P<0.0001。
4 讨论
氢气是无色、无味、最轻且高弥散性气体分子。2007年,大泽郁朗等报道外源性氢气可选择性清除细胞毒性氧自由基,发挥治疗性抗氧化作用。此后多项研究表明,外源性氢气可保护肝、胆、胃、肠、胰、脑、心、肺、肾、睾丸、卵巢、乳腺、眼、耳、骨骼、皮肤等器官免受急慢性损伤(10)。外源性氢气补充方式主要包括吸入氢氧混合气、饮用富氢水、腹腔注射富氢生理盐水(10)。本研究发现,腹腔注射氢气预处理对LPS诱导急性肝损伤具有预防作用。需注意,本研究采用LPS单次打击模型,表现为全身性内毒素血症与无菌性炎症肝损伤,但无法完全模拟多重细菌脓毒症。脓毒症临床前研究动物模型主要分为三类:(1)外源性毒素(LPS、酵母多糖)给药;(2)强毒细菌/病毒攻击;(3)宿主屏障破坏(盲肠结扎穿孔CLP、结肠支架腹膜炎CASP)(35)。脓毒症病理生理小鼠模型中,CLP兼具组织坏死、自体粪便泄漏所致多重细菌脓毒症,及与临床脓毒症相似的血流动力学与生化反应(35)。因此,腹腔注射氢气对细菌性脓毒症的作用需在CLP等更复杂模型中进一步验证。
本团队及其他研究者前期报道,腹腔注射氢气可改善LPS诱导的心功能障碍(11)、小鼠急性酒精性肝损伤(36),减轻兔心搏骤停模型脑缺血再灌注损伤并改善心肺脑复苏预后(37)。上述研究证实腹腔注射氢气对重要器官的保护作用。氢气吸入需专用设备,存在燃烧爆炸风险;富氢水、富氢生理盐水载氢量有限。相比之下,腹腔注射氢气可弥补上述不足,且可降低血清TNF-α、IL-1β、IL-18水平(11),但腹腔注射氢气对器官指数等全身效应的系统性研究仍缺乏。内源性氢气亦可保护肝脏:饲喂含20%高直链玉米淀粉饲料增强肠道氢气生成,可减轻大鼠肝脏I/R损伤(38);肠道菌群来源氢气改善刀豆蛋白A(Con A)诱导肝炎,抗生素抑制菌群则加重(39)。由此提出:不同个体抗感染免疫水平是否与内源性氢气相关?若相关,能否通过升高内源性氢气改善脓毒症?
LPS诱导细胞内ROS生成,为TLR4介导固有免疫所必需(40)。脓毒症急性肝损伤时,受损肝细胞线粒体(41)与驻留免疫细胞(42)产生过量ROS。氢气可选择性清除细胞毒性氧自由基,发挥治疗性抗氧化作用(43)。因此本研究探究氢气对LPS肝脏氧化应激的作用。哺乳动物组织生理与病理状态下,分子氧、一氧化氮源性活性物质对蛋白质的氧化翻译后修饰普遍存在,可发挥调控或细胞毒性作用(44)。过氧亚硝酸盐(ONOO⁻,一氧化氮与超氧阴离子反应产物)、硝酰氯(NO₂Cl)、二氧化氮(•NO₂)等活性氮与酪氨酸活化芳环反应生成3-NT,可发生于游离氨基酸及肽链、蛋白结合酪氨酸(45)。免疫印迹与免疫荧光均显示,LPS升高肝脏3-NT,氢气预处理可抑制,与大泽郁朗报道一致——氢气选择性清除毒性最强的羟自由基(43)。高水平ROS直接损伤脂质形成MDA等过氧化物(23),LPS升高肝脏MDA,氢气可逆转。GSH直接清除羟自由基、过氧亚硝酸盐、H₂O₂等氧化物,或在谷胱甘肽过氧化物酶(GPX)催化下将H₂O₂(脂质过氧化物)还原为水(相应脂质醇),同时GSH氧化为谷胱甘肽二硫化物(GSSG)(46)。本研究显示氢气升高LPS降低的肝脏GSH,提示抗氧化能力增强。MPO为白细胞来源血红素过氧化物酶,催化ROS(如次氯酸)生成(47,48);其源性ROS在中性粒细胞抗菌与宿主防御中关键,但升高亦与炎症及氧化应激相关(49)。肝脏MPO升高提示免疫细胞过度激活,H&E染色亦证实,氢气预处理可降低MPO。表明腹腔注射氢气可减轻LPS诱导的肝脏氧化应激。
LPS诱导的经典信号转导为TLR4介导的固有免疫信号,TLR4是LPS经典受体(27)。除TLR3外,所有TLR均以MyD88为接头蛋白(27)。MyD88依赖型TLR4信号中,E3泛素连接酶TRAF6对TAB-TAK1激活及后续NEMO-IKKα/β-NF-κB激活至关重要,胞质游离TRAF6复合物则激活MAPK-AP-1(27)。本研究显示,LPS升高肝脏TLR4表达及IKK、NF-κB p65、ERK1/2、p38 MAPK、JNK磷酸化,氢气均可降低。氢气似乎可抑制本研究中TLR4信号多数检测分子的激活。但固有免疫信号为复杂级联反应,氢气是直接抑制上述分子,还是通过调控固有免疫信号负调控因子间接抑制(50),或主要通过选择性抗氧化(43)间接减弱氧化还原敏感信号节点(如TLR4或炎症小体),仍有待后续探究。
NF-κB等转录因子激活导致TNF-α、IL-1β、IL-18等促炎因子上调(27)。氢气抑制TLR4上游,必然降低TNF-α、pro-IL-1β、pro-IL-18水平。本团队前期报道氢气可降低LPS小鼠促炎因子mRNA水平(11)。更重要的是,氢气可抑制肝脏IL-1β、IL-18的成熟。剪切型Caspase-1负责剪切pro-IL-1β、pro-IL-18使其成熟(30)。活化Caspase-1是NLRP3等炎症小体的经典组分,NLRP3炎症小体由NLRP3、ASC、Caspase-1组成(30,31)。本研究中,LPS升高NLRP3、ASC、全长及剪切型Caspase-1,氢气可抑制,提示氢气抑制NLRP3炎症小体激活。活化Caspase-1还可剪切激活GSDMD,诱导炎性程序性死亡——焦亡(51)。本研究显示氢气降低全长及剪切型GSDMD,免疫荧光进一步证实。与Yang团队结果相似:氢气吸入通过抑制NLRP3炎症小体介导焦亡改善心脏重构与纤维化(52–54)。人Caspase-4、小鼠同源Caspase-11及人Caspase-5可高特异性、高亲和力结合LPS与脂质A(33)。除Caspase-1外,剪切型Caspase-8、-11亦可激活GSDMD诱导非经典焦亡(33),Caspase-3可剪切GSDME诱导另一类非经典焦亡(34)。LPS增强肝脏上述非经典焦亡信号,氢气可逆转其表达与激活;TUNEL染色进一步证实氢气抑制肝脏细胞死亡。表明腹腔注射氢气同时抑制LPS小鼠肝脏NLRP3炎症小体-GSDMD经典焦亡信号,及Caspase-8/11-GSDMD、Caspase-3-GSDME非经典焦亡信号。
综上,腹腔注射氢气预处理通过抑制肝脏氧化应激、TLR4-IKK-NF-κB与MAPKs固有免疫信号、NLRP3炎症小体激活及GSDMD/GSDME介导的焦亡信号,减轻LPS诱导的小鼠急性肝损伤。上述信号间存在相互作用,氢气可抑制这些信号(尤其NLRP3),该抑制在改善肝细胞活力中起关键作用。但氢气对各信号的作用是独立的,还是通过调控关键信号分子实现?未来仍需加强氢气关键靶点研究。
https://blog.sciencenet.cn/blog-41174-1527139.html
上一篇:氢气吸入对脑血流的影响大【新进展】
下一篇:氢气疗法在呼吸系统疾病中的应用:作用机制、研究证据与技术考量