博文
双效肥胖药重塑食欲脑回路  精选
精选
||
大脑负责调节每天摄入的食物量和燃烧的卡路里数量,但在肥胖症中,这种平衡被打破,导致体重增加。直到几年前,持续减重的最有效的策略还是手术。现在,流行的抗肥胖药物semaglutide(以Ozempic和Wegovy的名字销售)和tirzepatide(以Mounjaro的名字销售)在引发体重减轻方面几乎与手术一样有效。这些药物基于一种在肠道中产生的名为GLP-1的肽,并且它们作用于大脑中的GLP-1受体以抑制进食。然而,这些药物价格昂贵,需求量大,并产生不同的效果——这推动了对更多肥胖治疗选择的需求。在《自然》杂志上发表文章的Petersen等人描述了如何将GLP-1受体激活剂与另一种作用于大脑的药物结合使用,可能是治疗肥胖的有效方法。
GLP-1受体的激动剂已被证明可以刺激在大脑中暴露于血液循环的区域表达该受体的神经元——即脑干和下丘脑。这导致在更高大脑中心调节进食、食欲和奖励的神经回路的激活。
Petersen及其同事设计了一种药物,由GLP-1受体激动剂与另一种在大脑中广泛发现的受体的抑制剂(拮抗剂)连接而成,这种受体被称为NMDA受体。这个受体与神经递质分子谷氨酸结合,并在调节突触可塑性方面发挥重要作用——这个过程允许神经元之间的通信通过加强或减弱神经元连接来适应活动模式。人类基因组研究也将NMDA受体和谷氨酸信号传导与肥胖联系起来,加强了这种药物策略的合理性。尽管针对NMDA受体减重并不是一个新想法,但之前的尝试因为当大脑中的NMDA受体被不加区分地抑制时会出现高温症和过度运动(过多移动)等副作用而失败。作者的双模式化合物克服了这个问题:NMDA受体拮抗剂(MK-801,也称为dizocilpine)只有在药物与GLP-1受体结合并被细胞内化后才被激活。然后MK-801可以减弱神经元的兴奋性,并且因为它与GLP-1受体激动剂结合,这一作用仅限于表达GLP-1受体的神经元(图1)。
(博主:抑制NMDA受体,具有神经保护作用,但这个受体的作用太重要,这种药物容易产生副作用。按照类似的逻辑,如果将MK801和其他分子偶联起来,例如某些能被巨噬细胞或小胶质细胞吞噬的分子,而这种细胞激活往往和神经元损伤有关系,从而实现在炎症或损伤局部释放MK801,这样一方面减少了药物副作用,另一方面实现细胞局部给药的目的。妙哉)
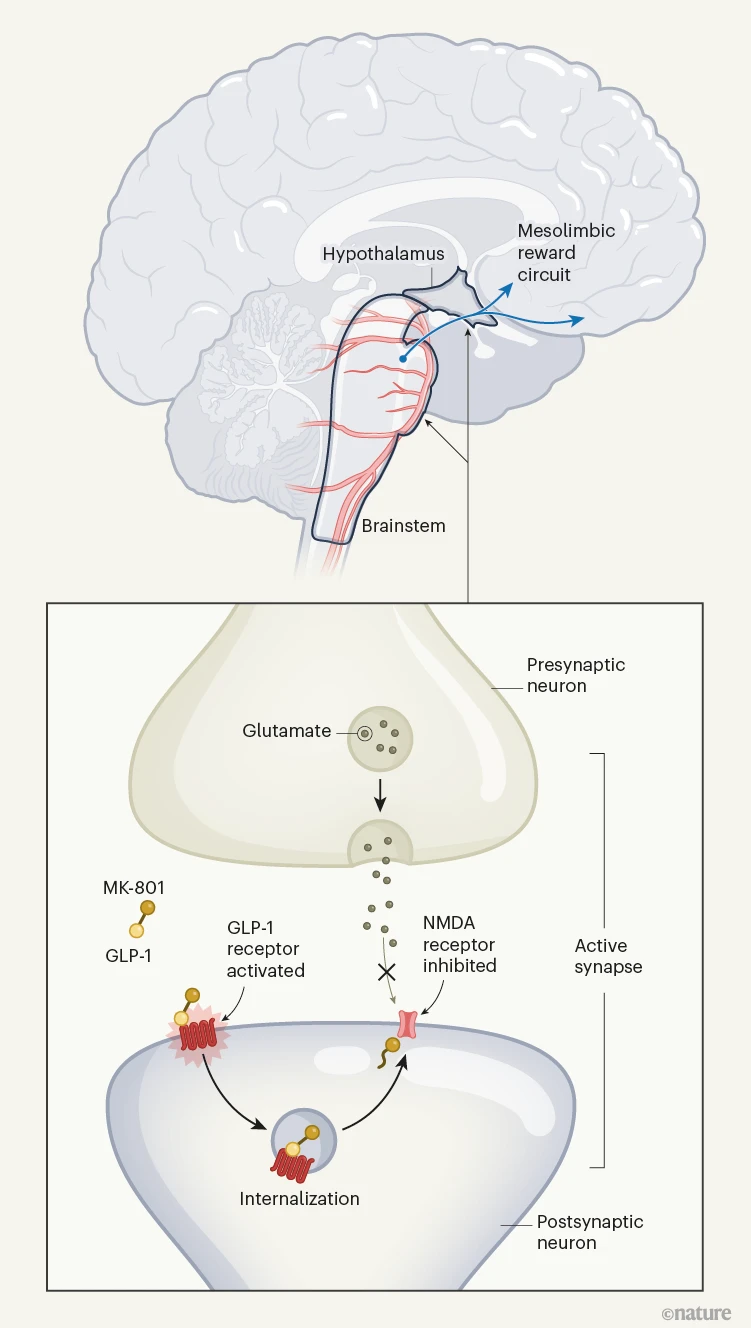
图1 | 一种二合一减肥药物重塑大脑回路。GLP-1是一种在肠道中产生并作用于大脑以控制饮食和食欲的肽。Petersen等人设计了一种双模式药物,由GLP-1受体的激活剂与大脑中发现的另一种名为NMDA受体的抑制剂结合而成,该受体在突触可塑性(神经元适应其连接强度的能力)中发挥作用。这种药物(GLP-1–MK-801)通过血液传播,并特别针对脑干和下丘脑中表达GLP-1受体的神经元。GLP-1受体被激活后被神经元内化,释放MK-801,后者抑制NMDA受体。这阻止了神经递质分子谷氨酸与之结合,降低了神经元的兴奋性。通过这两条途径的协同信号调节突触可塑性,激活控制奖励的神经通路,如中脑边缘奖励回路。在啮齿类动物中,这减少了食物摄入并增加了卡路里消耗,导致显著且持续的体重减轻。
作者发现,与单独使用GLP-1类似物和其他GLP-1受体激动剂(包括semaglutide)相比,GLP-1–MK-801在大鼠和小鼠体内的处理方式相似,但在减轻体重方面更有效。Petersen等人表明,将NMDA受体抑制作用特定地集中在表达GLP-1受体的神经元上是产生这种效果的必要条件,而将MK-801与其他被认为能抑制进食的肠肽连接起来,并不比单独使用MK-801或GLP-1类似物在减轻体重方面更有效。除了显示出心血管代谢健康改善和无肝脏损伤迹象外,用GLP-1–MK-801治疗的动物还表现出与GLP-1激动剂(恶心)和NMDA受体抑制剂(高温症和过度运动)相关的常见副作用的相对温和指标。
有趣的是,用GLP-1–MK-801治疗的动物减掉的体重甚至超过了限食动物,后者被喂食与治疗动物相同数量的食物。这表明该药物影响能量平衡超出了减少食物摄入。为了进一步探索这一点,动物们在测量它们的代谢率的笼子中被研究。尽管用GLP-1–MK-801治疗的小鼠体型明显更小,食物摄入量也少于肥胖对照小鼠,但它们燃烧的卡路里数相同。因此,这种药物可能克服了节食和运动带来的一个问题,即大脑通过降低代谢率来抵消减重,这使得随时间维持较低的体重变得困难。
Petersen等人还发现,GLP-1–MK-801改变了与GLP-1和MK-801都相关的信号通路中的基因表达,这表明两个受体系统之间存在协同作用。在某种程度上,GLP-1–MK-801与其他针对GLP-1受体的疗法作用相似,因为它激活了涉及饮食、食欲和奖励的神经回路——但与semaglutide相比,它更强烈地激活了大脑中调节奖励的区域,如中脑边缘系统。这一点值得注意,因为人们认为食用高度美味、能量密集的食物会劫持大脑的奖励系统,这可能会促进过度消费并导致肥胖。未来的研究可以测试GLP-1–MK-801是否特别减少了对不健康食物的消费驱动。
响应GLP-1–MK-801治疗的突触可塑性相关基因也上调。此外,直接注射到大脑中的GLP-1–MK-801的急性剂量在减少食物摄入方面比semaglutide有更持久的效果,这表明其对突触可塑性的影响可能是长期的。这一点很有趣,因为药物介导的减肥的另一个大缺点是个体在停药后会重新增加体重。这意味着,与其它心血管代谢治疗方法类似,如果人们希望保持体重减轻,他们不能停止服药。鉴于目前GLP-1受体激动剂的费用,一些人可能无法获得长期治疗肥胖的机会。如果Petersen及其同事的双模式分子改变了神经元的可塑性,它可能比必须定期服用的当前抗肥胖药物更具成本效益。然而,Petersen等人并没有让动物接触GLP-1–MK-801超过两周,因此其长期有效性和安全性需要进一步验证。
最后,GLP-1受体激动剂的一个相当大的问题是它们可能会导致瘦体质量(无脂肪体质)的损失。不幸的是,GLP-1–MK-801也导致了显著的瘦体质损失,但是一组限制食物的动物,使它们失去了与治疗动物相同的体重量,相比之下甚至失去了更多的瘦体质。因此,与单独限制热量相比,GLP-1–MK-801治疗可能对瘦体质稍微有更多的保护作用。
尽管这些数据展示了针对GLP-1受体表达神经元的靶向重塑在治疗肥胖方面的潜在希望,但这些临床前研究结果必须在人类中进行评估。确定优化脂肪减少、保持肌肉质量并限制成本的药物给药时间表是关键的下一步。鉴于GLP-1–MK-801仍然导致了瘦体质的损失和食物厌恶(而不仅仅是饱腹感),看起来药物可能有一些不希望的方面。然而,这种创新的药物策略以及该药物调节了突触可塑性的事实是在用药物干预对抗肥胖的努力中的关键进展。
https://blog.sciencenet.cn/blog-41174-1434559.html
上一篇:梭菌产氢气涉及的代谢网络
下一篇:皮下植入镁片释放氢气减少心肌梗塞损伤【哈医大】