博文
氢气对辐射心脏病的防治作用【八章】  精选
精选
|
氢气对辐射心脏病的防治作用
辐射损伤是最经典的氧化损伤,所谓经典,一是这种损伤明确存在自由基增加的证据,因为生物组织和水经辐射会必然产生自由基,二是这种自由基损伤是自由基生物学最早研究和确认的自由基损伤。因此对抗辐射损伤的基本策略就是对抗自由基和抗氧化损伤。氢气对辐射损伤的作用,也从一个角度证明氢气具有明确抗氧化作用。虽然这种作用是否可以达到临床应用的价值尚不得而知,但从基础和临床研究的初步证据看,氢气对抗辐射损伤的作用是比较明确的。本文作者是长期从事心脏疾病和辐射损伤研究的学者,从抗辐射角度进行比较全面总结了氢气对辐射损伤作用的研究。需要特别指出的是,中国学者特别是海军军医大学对氢气抗辐射损伤进行了大量研究,为这一领域做出了突出贡献。
辐射诱发的心脏病(RIHD)是纵隔放射治疗的常见并发症。RIHD包括心包、冠状血管、心肌、瓣膜和传导系统的结构与功能异常。其潜在的病理机制复杂,主要与内皮细胞损伤、氧化应激和炎症有关。辐射能导致心肌细胞死亡、组织纤维化,最终可能以心力衰竭告终。为了克服这些并发症,需要寻找特定的治疗干预措施,而这仍是一个缺失的领域。氢分子被认为是一种在不同疾病环境中具有抗氧化、抗炎和抗凋亡保护作用的分子。体外以及体内研究表明,氢气对辐射引起的损伤,包括RIHD,都具有预防或治疗效果。氢气可以通过多种机制减轻RIHD,例如选择性中和羟基自由基、防护炎症和凋亡损伤、抗纤维化和抗肥大效果等。需要更多的研究来进一步阐明氢气的作用机制,并在临床试验中验证氢气疗法的有效性。
前言
放射治疗在许多肿瘤疾病的治疗中仍然被广泛使用。放疗的目的是杀死肿瘤细胞;然而,它可能对周围健康组织产生有害的副作用。如果应用于纵隔区域(例如治疗乳腺癌、肺癌、食管癌或霍奇金淋巴瘤),由于心脏与其解剖位置接近,可能会发生不必要的心脏辐射。纵隔辐射的不良心血管副作用综合征称为辐射诱发的心脏病(RIHD)[1]。许多大型临床研究已证实,放射治疗增加了心脏病相关死亡率的风险[2, 3]。尽管通过使用新的放射技术已经减少了RIHD的发病率,但研究表明现代技术并未完全消除RIHD的风险[4]。
RIHD的病理谱包括传导异常、瓣膜病、冠状动脉疾病、心包疾病、心肌病和心肌纤维化[5]。这些是由多种机制通过多个复杂途径相互作用的结果。辐射增加氧化应激,随后引发包括核因子-kappa B(NF-κB)激活在内的炎症反应[6]。炎症级联由血管损伤和内皮功能障碍启动。受损细胞诱导促炎细胞因子和生长因子的分泌,包括与组织纤维化发展密切相关的转化生长因子-beta(TGF-β)。心肌纤维化被认为是RIHD的最后阶段,其特征是在受损心脏组织中过量沉积胶原蛋白,最终导致心力衰竭[7]。
由于炎症反应和氧化应激在RIHD的发展中起着重要作用,抗炎和抗氧化化合物可以显示出放射保护效果。氢分子通过选择性减少羟基自由基()和过氧亚硝酸盐(ONOO−)以及通过调节转录因子而起到抗氧化作用。抗炎和细胞保护效果也已被很好地描述[8]。氢气可以减轻与辐射损伤相关的不同病理生理过程,如纤维化、肥大或缺氧。动物实验和临床试验已证明氢气在不同的器官中表现出放射保护效果[9]。
氢气是一个非常小的分子,这使它能够轻松穿过细胞膜并扩散到细胞质中。在短时间内,氢气能够穿透到亚细胞器,如线粒体和细胞核。氢气也能够轻松穿越血脑屏障[10]。其他优点包括氢气给药方法的广泛范围,包括吸入氢气、口服富氢水(HRW)和注射富氢盐水(HRS)[11]。
本文将回顾RIHD的病理生理学和分子氢减轻放疗这一负面副作用的潜在用途。手稿的重点将放在氢气作用的假定机制上,并对未来的前景提供一些见解。
RIHD的病理生理学
了解RIHD的发病机制对于评估可行的治疗靶点和可能的治疗选择非常重要。放射治疗同时对大血管、微血管和心肌造成损伤[12]。大量证据表明,辐射诱导的大分子(包括DNA、蛋白质和脂质)的即时氧化损伤是RIHD的起始事件。增加的氧化应激触发了其他生物过程,包括内皮细胞损伤、急性炎症和各种形式的细胞死亡[13]。几种代偿机制,包括内皮细胞增殖和心脏肥大,在亚致死损伤的幸存细胞中发展[14]。如果这些代偿机制耗尽,慢性炎症过程和纤维化在疾病进展中发挥核心作用,最终导致心力衰竭(见图8.1)[15]。
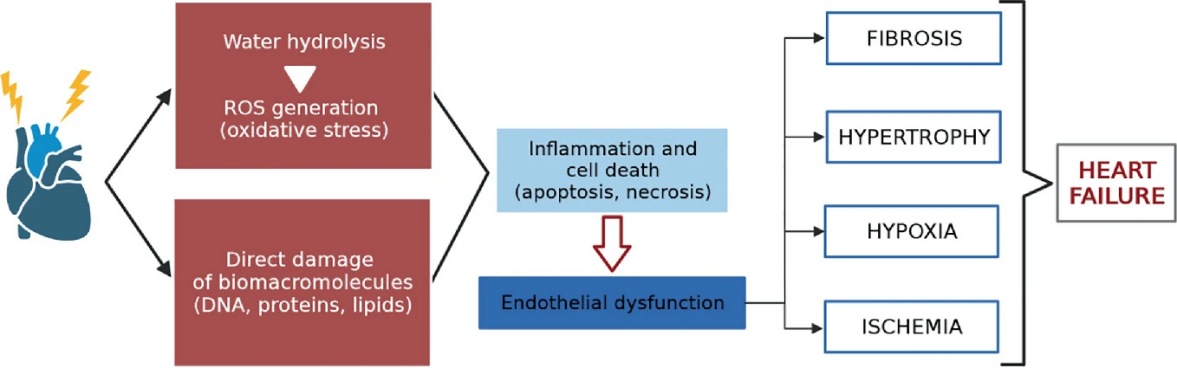
图. 8.1 辐射引起的心脏病(RIHD)的病理生理机制。辐射后,心脏中的DNA和其他大分子要么直接受到损伤,要么是通过水解作用形成的活性氧(ROS)造成损伤。这两种机制都会导致炎症过程或细胞死亡,主要损害内皮细胞。此外,这还会引起心脏和血管的多种病理状况,最终导致心力衰竭。
氧化应激
与其他心脏疾病一样,氧化应激在RIHD中也扮演着重要角色[16]。大约80%的组织和细胞由水分组成。因此,辐射引起的初始细胞损伤主要是由水辐射分解产生的活性氧物种(ROS)导致的间接效应。水辐射分解产生的主要反应性物种包括羟基自由基(⋅OH)、超氧阴离子(O2−)和过氧化氢(H2O2)[17]。电离辐射可能上调诱导型一氧化氮合酶(iNOS),从而产生大量一氧化氮(⋅NO),它可以与O2−反应形成过氧亚硝酸盐(ONOO−)和其他次级的活性氮物种(RNS)[18]。
累积的ROS/RNS可能导致大分子损伤。除了DNA损伤外,ROS/RNS还可能导致脂质和蛋白质的过氧化,并激活多个信号通路[19]。氧化应激对线粒体和核DNA都造成损害。8-羟基-2′-脱氧鸟苷(8-OHdG)被认为是氧化DNA损伤的标志。脂质过氧化的结果主要是形成活性脂质衍生物,主要是反式-4-羟基-2-壬烯醛(4-HNE)或丙二醛(MDA),它们被用作脂质过氧化的标志。蛋白质的氧化修饰主要导致蛋白质羰基衍生物的形成[19]。在不同的动物模型中,辐射后已发现氧化应激标志物水平升高[20, 21]。
辐射可以直接破坏线粒体的呼吸链,导致呼吸链功能障碍,从而减少ATP的产生,增加ROS的产生,降低抗氧化能力,并诱导凋亡[22]。辐射产生的自由基可以上调几种酶,包括烟酰胺腺嘌呤二核苷酸磷酸氧化酶(NADPH氧化酶)、脂氧合酶(LOXs)和环加氧酶(COXs),这些是持续产生ROS的其他来源[23]。ROS通过与NF-κB的相互作用促进炎症。在人类颈部小血管中,辐射后4至500周检测到NF-κB上调[24]。
氧化和硝化变化可能在最初的辐射暴露后数月甚至数年持续存在,这可能是由于通过不同机制不断增加的ROS/RNS的产生,例如线粒体损伤、炎症和细胞死亡过程、心脏组织中ROS生成酶的过度表达,以及抗氧化机制不足[16]。
内皮细胞损伤和炎症
心脏肌细胞对辐射损伤相对抵抗力较强。然而,内皮细胞对辐射依然敏感,RIHD的病理生理学似乎主要与内皮细胞的损伤有关[6]。过量的ROS产生是内皮功能障碍的初始原因。首先观察到内皮激活,其特征是内皮细胞异常的促炎和促血栓形成作用。这最终导致一氧化氮(NO)生物利用度降低,血管张力受损以及其他内皮变化[25]。
受损的内皮细胞分泌粘附分子和生长因子,促使急性炎症反应的激活。NF-κB是这一过程的介质[26]。粘附分子促进炎症细胞招募到受损的内皮,主要表现为急性期的中性粒细胞。炎症细胞释放促炎和促纤维化细胞因子,包括肿瘤坏死因子-α(TNF-α)、白细胞介素-6(IL-6)、IL-8、TGF-β、血小板源生长因子(PDGF)、成纤维细胞生长因子(FGF)等[15]。
除了炎症变化外,心脏辐射后在血管中观察到由于内皮细胞中von Willebrand因子(vWF)增加释放而引起的凝血和血小板功能变化。微血管和动脉中的血小板粘附以及血栓形成增加[27]。辐射通过TGF-β的抑制作用降低了抗凝剂血栓调节素的水平,这损害了内源性纤维蛋白溶解并促进了凝血[28]。
内皮功能障碍的关键后果之一是由于血管舒张剂特别是NO的生物利用度降低而导致的内皮依赖性血管舒张受损[29]。内皮细胞暴露于电离辐射后,NO被超氧自由基迅速失活,导致过氧亚硝酸盐的形成[30]。辐射诱导的氧化应激还会导致内皮NO合酶(eNOS)解耦,导致NO释放减少[31]。即使在较长时间后,内皮依赖性血管舒张似乎也受到损害,如在乳腺癌放疗患者中,在放疗后3年以上检测到[29]。
对纵隔结构的辐射可能会影响心脏毛细血管内皮细胞,导致它们的增殖、损伤、肿胀和变性,并显著减少毛细血管的数量。尽管内皮细胞可以再生,但毛细血管网络的损伤是不可逆的[32]。心脏是人体主要的耗氧器官,因此血液供应减少可能导致心肌缺氧,这将加剧心肌损伤。心肌缺血和缺氧、炎症反应、胶原沉积以及内皮细胞和成纤维细胞的增殖导致组织重塑、心脏纤维化和动脉粥样硬化[33]。
细胞死亡
辐射可以在心脏组织的不同细胞类型中诱导细胞死亡,包括心肌细胞、内皮细胞、成纤维细胞以及传导系统的细胞[14]。根据目前的知识,RIHD中细胞死亡途径的关键方面是细胞器室和分子结构的不可逆损伤、线粒体功能障碍和内质网(ER)应激[34]。
电离辐射直接诱导一系列DNA损伤,包括碱基损伤、单链断裂和双链断裂,但也通过ROS的形成间接诱导。如果受损的DNA没有得到适当修复,细胞可能会进入凋亡[35]。
线粒体功能障碍与ER应激密切相关。在心肌细胞辐射后,受刺激的ER将钙离子释放到细胞质中,导致线粒体钙过载和线粒体肿胀[22]。已经显示,辐射暴露导致促凋亡蛋白Bax的表达和激活增加,这导致其易位并插入线粒体外膜。这增强了线粒体膜的通透性,并降低了线粒体膜电位,这与线粒体通透性转换孔(mPTP)的开放密切相关[36]。可渗透的线粒体膜释放促凋亡因子,如细胞色素c,这启动了凋亡的内在途径[22]。
辐射引起的线粒体膜通透性增加也导致级联反应,产生大量ROS。ROS进一步促进内质网释放钙离子,导致肌原纤维过度收缩和线粒体钙过载,从而增加了ROS的产生。这可能导致由辐射引起的长期毒性,最终导致细胞周期停滞[37]。
纤维化和肥大
辐射诱导的心肌纤维化被认为是RIHD的最终阶段,其特征是受损心脏组织中过量的胶原沉积[7]。这是炎症、氧化应激和基因表达慢性变化的多条汇聚途径的结果。炎症途径可能是纤维化的主要介质[38]。
纤维生成的起始阶段是由辐射诱导的初级血管内皮细胞损伤驱动的。TGF-β被认为是照射后触发纤维化过程的关键因素。其在受辐射组织中的表达是持续的[39]。TGF-β作为成纤维细胞的介质,可以诱导成纤维细胞分化为肌成纤维细胞,这加剧了胶原的分泌。在受辐射的心脏中,与未受辐射的心脏相比,总组织胶原浓度显著增加。I型和III型胶原都有所增加;然而,I型胶原的数量增加不成比例[40]。
辐射诱导的TGF-ß表达可以通过不同机制刺激。ROS上调TGF-β,刺激I型胶原的产生,并支持辐射诱导的纤维化。辐射后诱导的DNA损伤可以导致细胞死亡。凋亡和衰老负责诱导巨噬细胞释放TGF-β[41]。微血管损伤引起的慢性缺氧导致缺氧诱导因子α(HIF1-α)上调,这是TGF-β的另一个刺激因素[38]。
辐射导致心脏不同层次的纤维化,包括心肌、心内膜和心外膜[7]。辐射诱导的纤维化损伤也在瓣膜中报道。瓣膜的纤维化损伤不太可能与微血管损伤有关,因为心脏瓣膜是无血管的。接受至少35 Gy心脏剂量的患者尸检调查显示,瓣膜心内膜因弹性纤维而局部增厚[42]。
渐进性和弥漫性间质纤维化导致组织弹性和收缩力降低,以及通过分离和取代心肌细胞导致的慢性缺氧[16]。影响心脏传导系统的纤维化或心肌细胞传导可能干扰电生理信号的传输,引起心律失常[43]。
在辐射诱导的急性细胞损伤和死亡之后,为了补偿由于心肌细胞损失导致的心脏功能下降,存活的心肌细胞中会启动代偿性肥大。心肌细胞肥大也可能由于纤维化瓣膜功能不足而发展。慢性缺氧和反复缺血可能在代偿性肥大的发展中发挥作用[44]。
氢气预防RIHD的作用
氢气是最轻和最丰富的化学元素。氢气的分子质量相对较小,这有助于其穿透细胞膜并分散到细胞质、线粒体、细胞核和其他细胞器中以发挥生物活性。此外,氢气能够通过血脑屏障[45]。氢气的给药方法有很多种。氢气主要通过吸入、饮用富含氢的水或注射含氢生理盐水来给药。近年来,也已经开发了纳米材料传递系统[8]。
许多研究已经探讨了氢气在不同疾病情况下的保护作用或有益效果,包括缺血/再灌注(I/R)损伤[46, 47]、器官移植[48, 49]、代谢综合征[50]、炎症[51, 52],以及辐射损伤[20, 53]。氢气的辐射防护效应被认为与清除辐射诱导的自由基有关,但也暗示与抗炎和抗凋亡特性以及基因表达的调节间接相关(见图8.2)[9]。
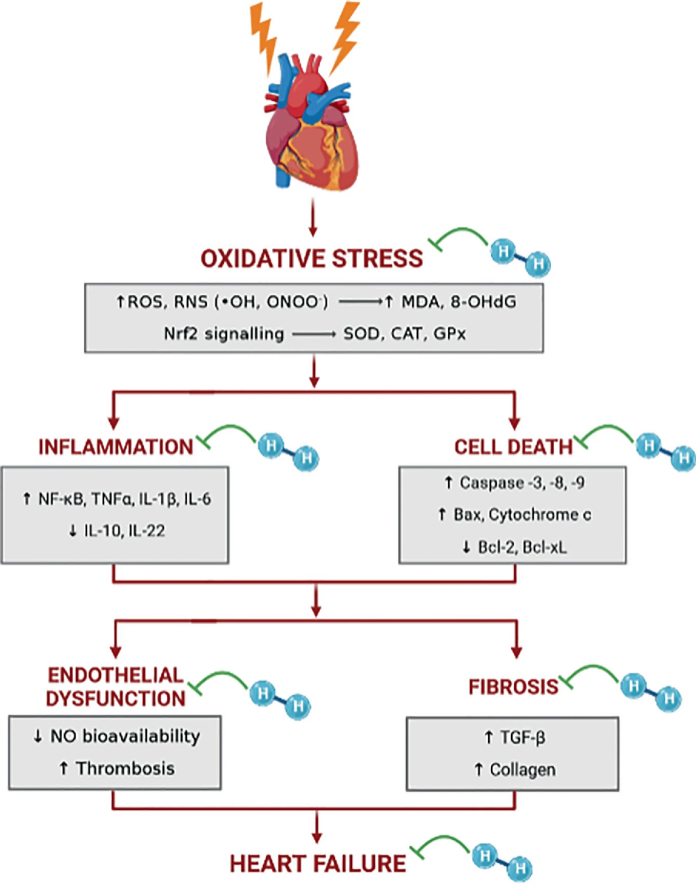
图 8.2氢气保护辐射性心脏病中可能生物学效应。氢气的放射保护作用通过其清除自由基、抗炎、抗凋亡或抗纤维化作用与多种途径有关。
氢气抗氧化作用
氢气的抗氧化效果在于其与自由基结合的特殊能力,尤其是羟基自由基,这种自由基在辐射期间会大量产生。Ohsawa等人[10]表明,氢气是一种选择性减少高反应性ROS和RNS(如⋅OH和ONOO−)的抗氧化剂,但不与其他具有生理功能的ROS(如超氧阴离子O2−和过氧化氢H2O2)反应。在体外模型中,氢气已被证明可以保护透明质酸分子不被羟基自由基诱导降解[54]。Terasaki等人[55]证明,氢气可以减少活体肺上皮细胞中辐射产生的细胞内ROS(⋅OH和ONOO−)。另一项研究报告称,氢气通过清除ROS作为有效的放射防护剂对免疫系统有保护作用[56]。
辐射诱导的反应性物质可能会对生物分子造成氧化损伤。根据Chuai等人[57]的研究,用氢气预处理生殖细胞可以显著抑制羟基自由基与细胞大分子的反应,从而减少脂质过氧化、蛋白质羰基化和氧化性DNA损伤。研究评估了不同的氧化应激标志物,主要是8-OHdG作为DNA氧化的指标,以及MDA作为脂质氧化的指标。Kura等人[58]显示,大鼠心肌中的MDA水平在辐射后增加。用HRW处理将这些值降低到非辐射对照组的水平。在另一项研究中,HRW的管理降低了辐射大鼠大脑中的MDA和8-OHdG水平[53]。其他作者也描述了氢气的类似保护效果[20, 59]。
氢气还能通过刺激内源性抗氧化剂提供抗氧化保护。许多研究表明,氢气促进核因子红细胞2相关因子2 (Nrf2) 的表达,该因子调节先天抗氧化和细胞保护酶的表达[60, 61]。Mei等人[62]检验了氢气对人类角质形成细胞HaCaT细胞的放射防护效果。氢气通过增加超氧化物歧化酶(SOD)和谷胱甘肽(GSH)活性等方式保护细胞免受辐射伤害。Gharib等人[63]发现,氢气在肝脏炎症模型中增加SOD活性并降低MDA水平。在大鼠模型中,吸入氢气通过减少氧化应激和刺激内源性抗氧化剂SOD和过氧化氢酶(CAT)的酶活性来减轻脑损伤[64]。氢气吸入减少了活性氧积累,并在皮肤缺血/再灌注损伤后上调了抗氧化酶活性[SOD, CAT, 谷胱甘肽过氧化物酶(GPx)] [65]。
氢气抗炎症作用
氢气的抗炎特性首次由Gharib等人在一项研究[63]中证明。在慢性肝脏炎症的小鼠模型中,他们发现经过两周的氢气吸入后,循环肿瘤坏死因子α (TNF-α) 水平下降。其他研究的结果也证实,分子氢能减少包括TNF-α、NF-κB和一些白细胞介素在内的各种促炎细胞因子的表达[66, 67]。由于炎症被认为是辐射诱导损伤的主要介质之一,氢气的抗炎作用构成了其可能的放射防护机制之一。在Kura等人的工作[58]中,氢气显著降低了受辐射损伤心肌中的MDA和TNF-α水平。周等人[59]检验了氢气对大鼠皮肤模型的放射防护效果。他们展示了氢气显著降低了受损皮肤中的MDA和IL-6水平。HRS通过减少促炎细胞因子TNF-α、IL-1β和IL-6的产生,保护大鼠皮肤组织免受UVB辐射损伤[68]。
氢气的抗炎作用还通过增加抗炎细胞因子的水平来执行。研究发现,吸入氢气可以通过上调抗炎细胞因子IL-10来减轻运动诱导的海马炎症[69]。HRW处理防止了小鼠乙醇诱导的脂肪肝。摄入HRW降低了促炎细胞因子TNF-α和IL-6的水平,但增加了抗炎分子IL-10和IL-22的水平[70]。
氢分子已被证明能有效恢复内皮细胞的功能,这些细胞可能会受到辐射的损害。用HRS治疗通过减少氧化应激、抑制炎症、保护线粒体功能以及增强一氧化氮生物利用度来缓解血管功能障碍[71]。Sakai等人[72]已经表明,每天摄入含有氢气的水可能通过中和有害的ROS来保护血管系统,以保持NO的生物利用度以及抑制炎症反应。王等人[73]报告说,氢气可能抑制血小板激活并防止血栓形成。
氢气细胞保护作用
氢气的放射防护效果不仅与增强细胞的抗氧化和抗炎保护有关,还与调节细胞死亡途径有关。洪等人[74]确定了氢气在大鼠脑细胞中的抗凋亡作用。在他们的研究中,氢气增加了抗凋亡蛋白Bcl-2的表达,并减少了促凋亡蛋白Bax和半胱天冬酶3。在大鼠心脏缺血/再灌注损伤模型中,氢气处理后也抑制了半胱天冬酶-3的活性,从而减少了细胞凋亡[46]。在使用肠隐窝上皮细胞系IEC-6的实验中,作者们展示了氢气抑制线粒体去极化、细胞色素c释放以及半胱天冬酶-3和半胱天冬酶-9的活性。他们进一步证明了氢气处理后Bcl-xl和Bcl-2表达增加,Bax蛋白表达减少[75]。HRS通过减少促凋亡蛋白Bcl-2、半胱天冬酶-3、半胱天冬酶-9、半胱天冬酶-8的表达,并增加抗凋亡Bax的水平,促进了肾功能在缺血/再灌注(I/R)损伤后的恢复[76]。
Terasaki等人[55]发现,氢气保护了体外培养的肺上皮细胞A549免受辐射诱导的氧化应激损伤,这一点通过减少凋亡反应和提高细胞活力得到了证明。氢气显著降低了辐射细胞中作为凋亡标志的Bax和活性半胱天冬酶3的水平。在另一项研究中,用氢气预处理细胞显著抑制了辐射诱导的人淋巴细胞(AHH-1)的凋亡[20]。
氢气抗纤维化抗增生作用
辐射引起的氧化应激和随后的炎症过程导致组织纤维化的发展,其特征是胶原沉积增加。TGF-β作为这一反应中的主要介质[77]。在不同研究中,发现分子氢能抑制促纤维化细胞因子TGF-β。氢气处理被证明能够减轻辐射小鼠肺部的氧化应激和随后的长期纤维化损伤,这一点通过减少TGF-β和III型胶原的水平得到了证实[55]。在另一个肺损伤模型中,吸氢减少了肺泡纤维化,减弱了促炎白细胞介素的上调,并抑制了TGF-β的表达[78]。高等人[79]证明,吸氢通过抑制氧化应激、TGF-β和抑制胶原I的生成来减轻肺纤维化。氢气还在肾损伤模型中被发现有效抑制纤维化。用HRW处理通过调节TGF-β诱导的其下游分子沉默信息调节因子1(Sirtuin 1)的表达来缓解肾纤维化[80]。在自发性高血压大鼠中,HRS通过抑制TGF-β信号通路来减少氧化应激和纤维化[81]。
于和郑[82]探讨了HRS处理对自发性高血压大鼠左心室肥厚的影响。HRS处理通过减轻氧化应激、抑制炎症过程和保护线粒体功能来减轻左心室肥厚。张等人[83]发现氢气通过抗氧化途径抑制异丙肾上腺素诱导的心脏肥厚。在另一项研究中,发现HRS能够减轻压力超负荷引起的大鼠心脏肥厚,并减少心房纤维化和纤维性颤动,可能是通过抑制JAK-STAT信号通路实现的[84]。
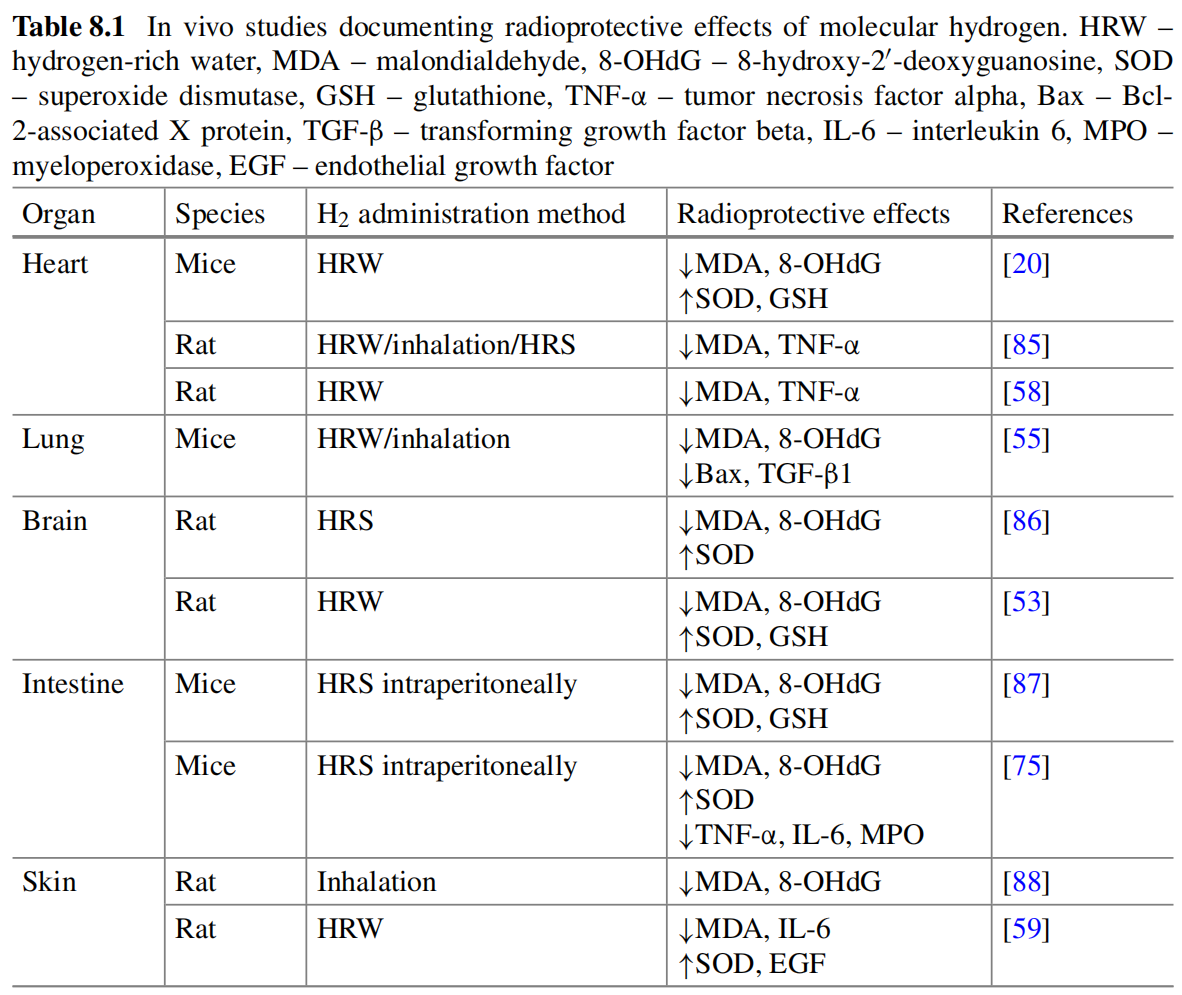
氢气减轻辐射诱导损伤的证据
氢气展现出广泛的生物活性,包括抗氧化、抗炎、细胞保护和抗纤维化作用,这些都可能有助于缓解辐射引起的损伤。氢气在缓解辐射引起的伤害方面的潜在应用已经在包括心脏、肺、脑、肠和皮肤等不同器官中进行了研究[9]。这些研究总结在表8.1中。
钱等人[20]测试了氢气在辐射小鼠中的心脏保护效果。在这项研究中,氢气预处理保护了心肌免受辐射引起的损伤,降低了心肌MDA、8-OHdG的水平,并增加了心肌内源性抗氧化剂SOD和GSH。与对照组相比,接受氢气治疗的小鼠存活率提高。斯莱扎克等人[85]证明,在受辐射损伤的大鼠心脏中,氢气给药显著降低了MDA和TNF-α水平。在另一项研究中,库拉等人[58]对大鼠的纵隔区域进行辐射。连续45天使用氢气减轻了辐射后心肌的氧化和炎症损伤,如MDA和TNF-α水平降低所示。氢气处理后,作者还证明了与纤维化和肥大相关的特定miRNAs(miRNA-1、-15b、-21)在辐射后的大鼠心肌中正常化。
氢气的放射防护效果也在全身胸部辐射后的小鼠肺部得到了证明。氢气处理在辐射后1周内减少了氧化应激和细胞凋亡。在氢气治疗后,辐射小鼠肺组织中的MDA、8-OHdG、促纤维化细胞因子TGF-β1和Bax线粒体转移显著减少。氢气处理的放射防护效果在暴露于辐射后5个月仍持续存在,在损伤的晚期阶段,表现为抑制肺纤维化[55]。
一些研究调查了氢气处理对受辐射损伤大脑的保护效果。在霍等人[86]的一项研究中,氢气被证明可以缓解辐射引起的急性脑损伤。氢气降低了氧化应激标志物MDA和8-OHdG,并增加了脑匀浆中内源性抗氧化剂SOD的含量。他们还发现,氢气组海马神经细胞的损伤程度较轻。另一项研究表明,HRW对辐射引起的认知功能障碍具有保护作用,可能的机制主要涉及氢气的抗氧化和抗炎作用。作者记录了用HRW治疗后辐射组大脑皮层中GSH浓度和SOD活性的增强以及MDA和8-OHdG浓度的降低[53]。
氢气已被证明能有效减轻辐射引起的肠道损伤。在钱等人[87]的一项工作中,辐射损伤了小鼠的肠道,证据包括粘膜中性粒细胞浸润、绒毛上皮丧失和绒毛缩短。腹腔注射HRS改善了所有这些组织学发现。研究还揭示了血浆MDA和肠8-OHdG水平的降低以及内源性抗氧化剂GSH和SOD血浆水平的增加。邱等人[75]证明,HRS显著减少了辐射引起的肠道粘膜损伤,改善了肠道功能,并提高了辐射小鼠的存活率。氢气处理通过降低MDA、8-OHdG并刺激SOD活性来减轻辐射引起的氧化应激。此外,氢气显著降低了炎症分子TNF-α和IL-6的血浆水平以及髓过氧化物酶的活性,这表明辐射引起的炎症反应得到了缓解。
在辐射引起的皮肤损伤模型中,渡边等人[88]检测到了氢气吸入对辐射性皮炎的保护效果。作者确定了非吸入组和吸入后组与吸入前组相比血清中MDA和8-OHdG浓度的增加,但这些差异并不具有统计学意义。周等人[59]研究了HRW对放疗引起的皮肤损伤的愈合效果。氢气处理后,他们观察到受损皮肤的愈合时间缩短和愈合率增加。这可能与其抗氧化和抗炎作用有关,因为氢气降低了MDA、IL-6的水平,并增加了SOD的活性。内皮生长因子(EGF)水平也显著增加。
未来展望
到目前为止,已经测试了几种物质来保护肿瘤周围正常组织在放疗期间免受辐射损伤。其中,氨磷汀是唯一获批用于临床的放射防护剂。然而,其使用伴随着低血压、恶心和呕吐等副作用[89]。
氢气是一种对包括辐射引起的疾病在内的各种疾病都有预防和治疗作用的分子[54]。它具有许多优点,如能快速穿过生物膜和屏障,或多种给药方式。此外,氢气通常被认为是一种安全的试剂。大多数临床试验显示,给予氢气后没有副作用[90]。
研究表明,氢气在不损害抗肿瘤效果的情况下发挥其放射防护作用。康等人[91]报告说,HRW改善了接受放疗的肝癌患者的生活质量。治疗组和非治疗组在对放疗的肿瘤反应上没有差异。平野等人[92]已经表明,吸入氢气缓解了放疗引起的骨髓损伤,同时不影响抗肿瘤效果。
基于这些信息,氢气在临床上用于减轻辐射引起的正常组织损伤具有很好的潜力。然而,需要进一步的研究来在更大规模的临床研究中确认这些结果。
结论
在纵隔区域接受放疗的患者患辐射引起的心脏病(RIHD)的风险增加。尽管现代放疗技术已降低了RIHD的发生率,但它仍然是癌症幸存者发病和死亡的主要原因。RIHD的发展涉及几条途径,包括微血管损伤、炎症和纤维化,尽管其他途径也可能有所贡献。了解RIHD进展中的确切分子机制对于开发预防和治疗策略是必要的,而不会减弱放疗对癌细胞的效果。
氢气是一种有效的活性氧和氮物种的清除剂。有益的效果也通过抑制炎症、细胞死亡和其他途径间接表现出来。管理炎症和氧化损伤是减轻辐射引起的毒性的可能策略之一。因此,氢气可能具有作为放射防护剂的潜在临床应用。氢气应用的优势在于其能轻松穿过细胞膜到达作用部位。另一个好处是氢气的给药方法范围广。根据到目前为止进行的研究表明,氢气应用似乎没有或只有轻微的副作用,并且对放疗结果没有负面影响。还需要更多的研究来阐明详细机制,并验证氢气治疗效果的有效性程度。
其他章节
科学网—祝贺新书《氢分子与健康疾病》出版 - 孙学军的博文 (sciencenet.cn)
一章科学网—从宇宙起源到医学应用的氢 - 孙学军的博文 (sciencenet.cn)
二章科学网—氢气生物学效应的目标分子 - 孙学军的博文 (sciencenet.cn)
三章科学网—氢气对线粒体保护的研究 - 孙学军的博文 (sciencenet.cn)
四章科学网—氢气是纠正线粒体异常的新工具 - 孙学军的博文 (sciencenet.cn)
五章科学网—喝氢水对运动员自主神经系统的影响 - 孙学军的博文 (sciencenet.cn)
六章科学网—氢气的临床应用【第六章】 - 孙学军的博文 (sciencenet.cn)
七章科学网—氢气和稳态【七章】 - 孙学军的博文 (sciencenet.cn)
https://blog.sciencenet.cn/blog-41174-1423975.html
上一篇:炎症性衰老如何克服?
下一篇:氢气是一种新型辐射防护剂【十章】