博文
从宇宙起源到医学应用的氢
||
科学网—祝贺新书《氢分子与健康疾病》出版 - 孙学军的博文 (sciencenet.cn)
第一章 氢从宇宙起源到医学应用
近年来,氢气因其卓越的抗氧化和抗炎特性而受到广泛关注。然而,对氢气在能源领域的应用的广泛研究往往掩盖了它作为医学和生物活性气体的潜力。令人惊讶的是,对氢生物医学方面的调查最早可以追溯到1793年。氢气表现出非凡的药代动力学,可迅速穿过细胞生物膜,包括血脑和睾丸屏障,进入亚细胞器。摄入后,氢气沿着阻力最小的路径通过循环系统,主要通过呼气排出。尽管复杂的分子机制和精确的靶标仍然难以捉摸,但氢的抗氧化作用涉及通过激活 Nrf2/keap1 途径上调内源性抗氧化剂。最近的研究强调了Fe-卟啉作为氧化还原相关生物传感器的潜在作用,促进氢与羟基自由基的反应并触发额外的信号转导过程。此外,本文还深入研究了氢的物理化学性质,特别强调了氢的摩尔溶解度、对术语饱和度的考虑以及氢的其他独特特性进行了讨论。围绕氢历史的知识和研究不断扩大强调其在生物医学应用中的变革潜力,并为未来利用其治疗特性的进展铺平道路。
介绍
氢元素是宇宙的先驱,有一个引人入胜的故事,在浩瀚的宇宙时空里展开,可以追溯到大约 138 亿年前宇宙的黎明。作为现存最轻、最丰富的元素,氢拥有我们宇宙起源的秘密,与宇宙的结构交织在一起。从原始阶段到今天,氢的旅程简直是非同寻常。氢气的发现可以追溯到18世纪末,当时英国科学家亨利·卡文迪许(Henry Cavendish)发现了一种具有独特特性的新气体。他将氢气命名为“易燃空气”,因为它具有高度易燃的性质[1]。1783年,氢气在雅克·查尔斯(Jacques Charles)和罗伯特兄弟(Robert brothers)进行的首次载人氢气球飞行中发挥了至关重要的作用,开创了人类航空时代[2]。
在整个 19 世纪和 20 世纪,氢气在工业中得到了各种应用。氢气被广泛用于填充飞艇,并作为煤气灯和焊接工艺的燃料[3]。然而,1937年臭名昭著的兴登堡灾难,当时一艘充满氢气的飞艇着火,使与氢相关的重大安全问题成为人们关注的焦点[4]。
在二十世纪下半叶,研究人员开始探索氢作为清洁和可持续能源的潜力。氢燃料电池通过氢气和氧气之间的电化学反应发电,成为一种很有前途的技术[5]。在同样质量的比较中,氢气释放的能量大约是汽油的三倍。由于氢气的能量密度高,航天工业也采用氢气作为火箭燃料[6]。近几十年来,氢作为向低碳经济转型的关键参与者,再次受到极大关注。因此,氢气作为一种多功能能源载体具有巨大的潜力,可以通过电解从各种可再生能源(如太阳能和风能)中生产。氢燃料电池越来越多地用于运输,包括汽车、公共汽车甚至火车,为传统的化石燃料车辆提供了零排放替代品[6]。
此外,氢气正在探索其在能源之外的应用。在生物医学研究中,氢气因其抗氧化和抗炎特性而显示出治疗潜力[7]。生物医学领域正在积极研究氢气在缓解各种健康状况和促进整体健康方面的潜在价值[7]。氢的生物医学史也是本章的主要关注点之一。
氢研究的历史概述
在过去的二十年中,氢气研究的爆炸式增长使氢气成为几个不同领域的前沿。最广泛认可的研究领域涉及将其用作清洁和适应性强的能源载体[6]。图 1.1 说明了在过去 22 年内发表的关于氢气的文章数量惊人 。现在有超过2000篇关于氢的生物医学效应的文章发表。
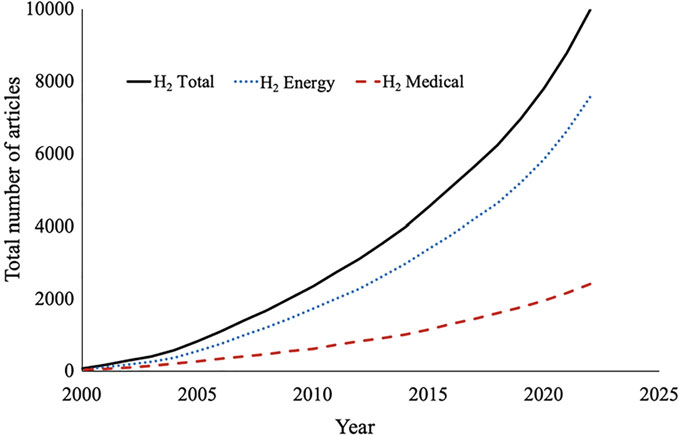
图1.1与氢气、氢能源和氢气医疗用途相关的文章
然而,这个令人印象深刻的数字可能被发表的关于使用氢气作为能源的文章的近四倍所掩盖。不过,毕竟有超过 2000 篇与氢分子氢的生物医学效应相关的出版物规模。氢气已被证明在170多种疾病模型中具有治疗作用,基本上涵盖了人体的每个器官[8]。这类研究的大部分是在2007年Oshawa等人在Nature Medicine上发表开创性论文后发表的[9]。作者报告说,在大鼠卒中模型中,氢气可以大大减轻大脑中动脉闭塞引起的缺血/再灌注相关的脑损伤[9]。2%氢是提供这些显着效果的必要条件,这低于在空气中可燃性的浓度水平。事实上,人们历史上对氢气的生物医学效应特别是非药用途的兴趣已经持续了很久[10]。
氢气在人体中的非药用应用
有趣的是,氢气在各种人类实践中的利用已经研究了100多年[10],但意涵的是没有认识到其作为医学或生物活性气体的潜力[11]。这些实践包括可生物降解的植入物、身体伤口检测、潜水应用、血流测量、吸收不良诊断和检测胃酸缺乏。
可生物降解植入物
自1878年以来,金属镁作为可生物降解植入物的有前途的材料,在骨科和生物医学工程中备受关注[12]。这些植入物在体内逐渐溶解,同时不断释放出氢气和镁离子(Mg + 2H2O →Mg(OH)2+ H2)。毫不奇怪,最近的研究表明,镁基植入物释放的氢气可能为患者提供了有益的益处[13-15]。
肠道穿孔诊断
1888年,氢分子被美国医学界用于定位胃肠道中的穿透伤,如枪伤和刀伤[16,17]。 该技术涉及直肠吹入氢气,进入肠道内的氢气会在伤口周围积聚为气泡。气泡被点燃以确认它们的存在,证明了氢气的诊断和无菌特性。直肠吹入氢气被证明是一种可靠的试验,对敏感组织无毒性或刺激性作用[16,17]。
潜水气体
1941年,人们发现在高压下潜水员呼吸97%氢气和3%氧气的混合物具有良好的耐受性和安全性[18]。这一发现导致在深海潜水中使用氢气来预防减压病。尽管氢气具有可燃性,但其重量轻且麻醉作用降低,使其成为传统潜水气体氦气的可行替代品[19,20]。 根据氢气医学效应的研究,推测在潜水中使用氢气也可能带来额外的好处,例如减少潜水员的氧化应激[21]。
血流测定标志物
1963年,氢气与准确测量局部血流相关的医疗应用有关[22]。该技术已被用于研究各种器官和组织的血流[23-28]。由于氢气的潜在血管活性作用,研究氢气对血流的影响可能存在意想不到的抗损伤作用。
消化吸收障碍的诊断
肠道细菌在不可消化的碳水化合物发酵过程中产生氢气[29]。在碳水化合物吸收不良的情况下,氢气产量增加[29]。至少从1969年开始,呼气氢分析就被用作检测碳水化合物吸收不良的诊断工具[30-36]和小肠细菌过度生长[37,38]。值得注意的是,虽然呼吸氢气增加与不利条件(即SIBO或消化不良)有关,但来自肠道细菌的氢气也具有多种益处[39]。
胃酸缺乏的检测
胃酸缺乏的特征是消化系统中盐酸含量低或不存在,可导致各种疾病。1985 年,通过测量元素镁和盐酸 (Mg + 2HCl→MgCl2+ H2) 反应产生的呼气氢气,用于评估胃酸缺乏 [40-43]。
氢气的上述非治疗用途突出了其与人类的独特历史关系,当这个时间线与 18 世纪后期氢气发现后不久发生的医学研究并列时。氢的历史时间表主要与其生物效应有关,如图1.2.所示。
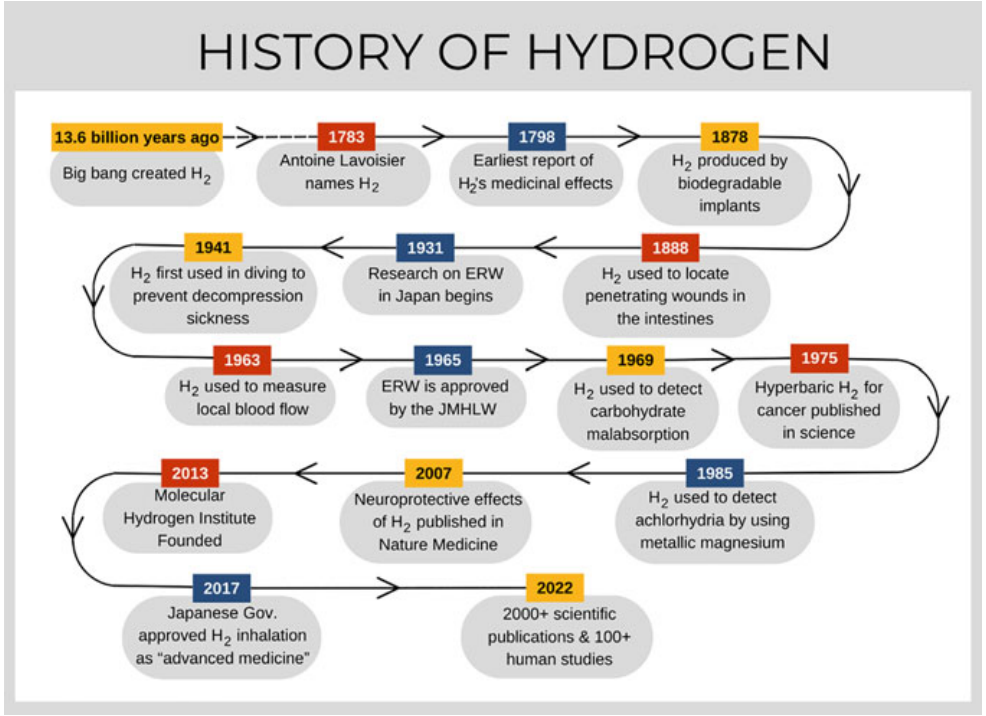
图1.2氢气生物医学研究时间线
氢气治疗疾病的历史研究
1793年,托马斯·贝多斯(Thomas Beddos)在英国布里斯托尔的医学气动研究所(Medical Pneumatic Institute)对氢的药用特性进行了有限的研究[10]。然而,正是在 1798 年,居住在伦敦的意大利物理学家提比略·卡瓦洛 (Tiberius Cavallo) 发表了一篇题为“关于人造空气的药用特性的论文”的论文。在附录中,关于血液的性质,他全面讨论了氢气的治疗用途[44]。Cavallo观察到,吸入硫酸和铁反应产生的氢气可以缓解肺部炎症,咳嗽和其他炎症性疾病。他报告说,在以“肺部区域紧绷和剧烈咳嗽”为特征的病例中,通过吸入“4夸脱氢气和20夸脱普通空气的混合物”,几乎可以立即缓解[44]。
汉弗莱·戴维(Humphry Davy)在布里斯托尔的贝多斯(Beddoes)的指导下进行了平行研究[10]。在他1800年的论文,题为“研究、化学和哲学;主要涉及一氧化二氮或脱氢亚硝酸空气及其呼吸作用”,戴维广泛研究了包括氢气在内的各种气体与一氧化二氮,戴维进行了涉及各种生物的实验,如哺乳动物、昆虫、两栖动物、鱼、蜗牛和蠕虫,尽管按照今天的标准,其中一些实验在道德上被认为是不合适的。他还进行了自我实验,并向朋友和患者(包括知名人士)施用气体[10]。贝多斯、卡瓦洛和戴维的这些早期工作为探索氢气的治疗潜力奠定了基础,为该领域的进一步研究铺平了道路。
1931年,人们报道了一种称为电解还原水(ERW)的氢水在农业中应用时具有益处[45]。电解还原水由水电解产生,电解将水分解成氢气和氧气(2H2O → 2H2+ O2) [46]。电解还原水是在“还原”的阴极收集的水。电解还原水的特点是具有碱性pH值和负氧化还原电位(ORP)。尽管现在人们认识到电解还原水含有不同水平的溶解氢[47],但自使用后数十年里,这种特性很少被提及。1965年,日本厚生劳动省根据《药事法》批准电解水装置安全有效地用于治疗各种胃肠道症状[45]。随着电解还原水的普及,轶事性健康声明的激增导致了1990年代调查研究的加强[47-51]。许多细胞和动物研究报告了电解还原水的健康有利特性,包括抗氧化和抗炎作用。然而,直到2007年后,氢分子在电解还原水中的作用才得到仔细研究[47]。在电解还原水的大部分历史中,氢分子的参与实质一直被忽视,因为氢气仅仅被认为是水被电解出生物惰性副产物[47]。由于缺乏对电解还原水生物效益的机制本质解释,导致许多伪科学猜想试图解释其观察到的效益。这些主张包括用于中和毒素的弱碱性pH值,可增加细胞能量的氧气,改变水分子结构(例如,小分子团簇)的水合增强作用,以及负氧化还原电位(ORP),表明归因于水中的“自由电子”,活性氢原子,负氢离子,矿物氢化物和氢氧根离子等各种想法的抗氧化作用[47,52]。
随着电解还原水研究的进展,每一种说法都经过了严格的审查和调查,最终导致它们一一被驳斥[47]。现在已经确凿地确定,氢气才是导致ORP阴性和ERW治疗效果的唯一因素[47]。例如,大量研究表明,从电解还原水中去除氢气会消除其治疗益处[47]。值得注意的是,尽管早在1931年就认识到电解还原水的好处,但半个多世纪以来,氢气的作用仍然不为人知。事实上,大多数早期的电解还原水文章都没有报告氢气的浓度,而氢气现在已经成为电解水效应的标准解释。不幸的是,许多电解还原水的支持者仍然没有认识到氢分子的重要性,坚持推广科学上不可信和被驳斥的概念来解释电解还原水,而不是关注氢分子本身的简单性[47]。这是有问题的,因为电解还原水也可能带来一些与氢分子无关的潜在健康风险,正如最近所评价的那样[53]。
1975年,当美国研究人员研究高压氢气治疗小鼠皮肤癌的作用时,对氢气在医疗应用中的潜力的探索有了显着的复苏[54]。来自贝勒大学和德克萨斯农工大学的Dole及其同事进行的开创性研究证明了高压氢治疗对小鼠皮肤癌的积极生物学效应[54]。然而,Roberts随后在1978年使用小鼠实体移植肿瘤进行的研究未能重现这些显著结果[55]。
1988年,Neale提出一个假说,认为肠道细菌产生的氢气可以作为一种有效的抗氧化剂,因为它具有标准的还原电位[56]。2009年,哈佛大学福赛斯研究所和佛罗里达大学进行的一项研究证实了肠道微生物群产生氢气的保护作用[57]。他们发现,用产氢大肠杆菌(而不是缺氢突变体大肠杆菌)重建肠道微生物群可预防刀豆球菌蛋白A诱导的肝炎[57]。抗糖尿病药物如α-葡萄糖苷酶抑制剂等化合物也被发现会增加人类的呼吸氢浓度[58,59]。 其中一些化合物,如阿卡波糖,对预防心血管疾病和高血压有额外的未知作用[59]。这些化合物的作用可能归因于细菌产生氢气。此外,摄入膳食纤维果胶或高直链淀粉玉米可增强盲肠氢的产生,有望缓解大鼠缺血再灌注损伤[60]。
有趣的是,1996年,大卫·琼斯(David Jones)在《自然》杂志上写了一篇名为“代达罗斯”的讽刺短文,讲述了氢气的好处[61]。他幽默地建议,氢气是一种对抗羟基自由基的极好抗氧化剂,并且可以减少炎症。在当时,这只是琼斯专栏中的一个幽默表述。他甚至开玩笑地谈到了虚构的DREADCO化学家,他们创造了氢气浸泡饮料[61]。虽然琼斯的讽刺专栏包括当时没有现实基础的富有想象力的想法,但有趣的是,他的短文中提到的一些概念在后来的几年里巧合地成为真正的科学研究的主题[7]。
事实上,也许有点讽刺的是,在2001年,来自法国的研究人员受到了琼斯专栏的启发。他们研究了氢气对血吸虫病相关慢性肝脏炎症小鼠模型的影响[62]。他们的研究结果表明,小鼠的血流动力学得到改善,抗氧化酶活性增加,一氧化氮合酶II活性增强,纤维化和肿瘤坏死因子α水平降低[62]。
尽管有这些令人鼓舞的发现,但氢气的生物医学应用几乎没有引起人们的兴趣,这主要是由于担心其与氧气结合时的可燃性。然而,随着 Ohsawa 及其同事在 Nature Medicine 上发表的一份报告,该研究在 2007 年获得了显着的动力 [9]。他们的研究表明,即使在2-4%的低浓度下,氢气也能显着减少缺血再灌注损伤大鼠模型中的脑梗塞体积。作者进一步强调,氢选择性地还原了有毒的羟基自由基(•OH)在生物学上可行的浓度下,同时保持其他生理上重要的活性氧/氮物质不受影响[9]。在过去的十几年里,对氢气的研究呈爆炸式增长,导致 2000 多篇出版物探索其潜在的医学应用。超过 100 项人体研究已经证明了从动物模型到人类在各种疾病中的转化潜力。这些临床疾病包括代谢综合征[63,64]、糖尿病[65]、高脂血症[66]、帕金森病[67]、认知障碍[68]、类风湿性关节炎[69]、慢性乙型肝炎[70]、血管功能[71]、运动成绩表现[72,73]、脑梗死[74]等疾病[8,75]。2017年,一项使用吸入氢气的临床试验被日本厚生劳动省批准为治疗心脏骤停后综合征的先进药物[76]。
氢分子令人鼓舞的治疗效果表明,除了用于绿色能源外,氢气在生物医学领域还有光明的未来。然而,还需要对氢分子疗法的药代动力学和药效学进行更多的研究。在简要讨论这些领域之前,首先讨论氢的一些物理化学性质,包括其水中溶解度。
氢的理化性质和溶解度
氢气(H2)由双原子分子组成,具有独特的物理和化学性质,有助于其在科学研究中的重要性。氢气的摩尔质量约为每摩尔 2.016 g,是自然界最轻的分子,由两个共享共价键的氢原子组成 [3]。氢分子的电子结构由两个电子和两个质子组成,使分子具有电中性。氢气也是非极性的,因为两个氢原子之间的电子分布相等。
由于氢气的高扩散率和独特的化学性质,氢气的储存和密封带来了挑战。例如,它可以扩散到各种金属的晶格结构中,并通过称为氢脆的过程破坏结构完整性[77]。它还可以很容易地渗透到大多数材料中,例如塑料,这限制了其长期储存选择[78]。因此,富氢水不能像普通碳酸饮料那样储存在塑料瓶中。这需要在生产过程中使用富氢水,或储存在铝制容器(例如罐子和小袋)中,这些容器可以长期储存氢水[79]。
它体积小,分子量低,具有显著的扩散性,能够以极快的速度渗透到各种介质中,包括固体、液体和气体[78]。氢原子的范德华半径为120 pm[80]。因此,氢分子的硬球直径估计为287 pm[81]。氢渗出率约为氧气的4倍根据格雷厄姆定律,根据菲克扩散定律和基于布朗运动原理的斯托克斯-爱因斯坦方程,氢在水中扩散速度比氧气快约2.39倍[82]。因此,氢在气体中具有最高的扩散率之一,使其能够迅速扩散和分散到周围环境中。这有助于氢分子生物医学的吸引力,因为它可以轻松快速地渗透到细胞屏障并到达所需的亚细胞位置[9],这将在药代动力学部分讨论。
氢分子非极性有助于其通过细胞生物膜的扩散能力。然而,这一特性也会降低其水溶性。尽管是非极性的,氢气在标准环境压力(1atm)和温度(25°C)条件下的溶解度为0.78mM[52]。文献中经常提到氢在水中的溶解度使用各种不同的表示单位,表1.1对此进行了总结。在最后一列中添加了注释,以指示表示氢浓度/溶解度的推荐单位在生物医学领域或根据IUPAC的建议[83]。
在讨论氢气的溶解度时,需要考虑的要点有饱和度、溶解浓度和单位等三个,现在将讨论这些。
气体饱和度
不幸的是,当氢的饱和度/溶解度在讨论时,通常以暗示浓度不能更高的方式进行(例如,“氢气可能达到最大浓度......1.8 ppm [STP 条件]...并且不能进一步提高“[85])。然而,需要注意的是,术语饱和度与压力和温度有着内在的联系。如果不定义具体条件,饱和度是没有意义的,具体条件主要涉及气体的分压、温度和溶剂的详细信息(例如,溶剂是什么、离子强度/活性等)。[86]氢的浓度气体与其分压成正比,如亨利定律所示:C = P/KH;C是浓度(摩尔浓度),P是压力(大气压),KH是特定气体在给定温度下的亨利溶解度常数(单位为 L·atm/mol)。由于氢气约占 5.50×10−5大气压的百分比,暴露在开放大气中的纯水将含有大约 8.65×10−7mg/L氢气。在这种情况下,8.65×10−7mg/L 也可以认为是饱和点,因为这是氢气体达到平衡后的最终浓度(即 同样时间氢在水中溶解分子数和离开水的分子数量相等),其分压为 5.50×10−7ATM[52]。
为了比较不同化学品/药物(在本例中为气体)的溶解度,我们必须标准化压力和温度变量。因此,根据 IUPAC 标准 [83]氢的饱和标准环境压力和温度 (SATP)为1.55 mg/L。 SATP 是指压力为 100.000 kPa (≈0.9868 atm) 和 25 °C 的温度。在这些条件下,氢气体会溶解到水中,直到其分压达到平衡。该平衡浓度为1.55 mg/L,或在1个大气压下为1.57 mg/L。一旦压力发生变化,增加或减少,氢的浓度在水中不再处于平衡状态,因此要么不饱和,要么过饱和[52]。
例如,如果立即将氢水从具有1个大气压氢气体分压的腔室中取出,到总压力为 1个大气压但氢的分压仅为 5.50×10−7ATM的开放气氛,那么该水将被视为“过饱和”。因此,浓度将迅速开始降低,直到达到与分压(即新饱和点)的新平衡,即 8.65 × 10−7毫克/升。即使总压力仍为1 个大气压,也会发生这种情况。那是因为只有 氢分压才会影响氢气体的溶解浓度[86]。
如果立即将水置于10个大气压的纯氢气中,那么最初 1.57 mg/L氢水将被视为“不饱和”。这是因为增加的氢压力 (10 atm) 将导致 15.7 mg/L 的新饱和点,一旦氢入水和离开水建立新平衡,就会达到该饱和点。如果你把这种氢水放回只有 1 个大气压的氢压力,浓度将被视为“过饱和”并立即开始下降,直到达到 1.57 mg/L。它将无限期地保持在这个浓度,直到氢的分压发生改变。例如,如果将其放入开放大气中,则会发生相同的现象。即使总压力仍为 1 个大气压,因为此时氢的分压少得多(5.50 × 10−7ATM)。因此,氢气浓度会逐渐降低,直到达到新的平衡。
因此,饱和度是气体分压的固有特性[86]。传统上,当讨论气体的术语“饱和度”时,它直接指的是一组特定的条件(例如,STP或SATP)。因此,不应将其误解为不能高于SATP饱和点,因为需要做的就是增加压力或降低温度。还应该理解,如果增加氢浓度高于平衡饱和度,“过量”气体不会立即从水中消散并恢复到 SATP 饱和度,因为平衡需要时间才能实现。平衡条件的变化将导致气体开始从水中消散,但不会立即达到平衡。虽然氢水浓度越高,一旦暴露在环境大气中的释放速度越快,但并不是立竿见影达到平衡。因此,氢的初始浓度是否为1.66毫克/升,一旦暴露在开阔的大气中,都被认为是氢“过饱和”的.因此,它们都将开始逐渐降低,直到它们与大气氢气分压达到平衡对应的终浓度约为8.65×10−7毫克/升[52]。
氢气溶解浓度
通常当一个人了解到氢浓度在标准条件下,溶解度和剂量仅为 1.6 mg/L,溶解度和剂量往往成为问题。在药物中,溶解度是剂量和生物利用度的主要预测因素[87]。各种阈值已被用于描述物质的溶解度(例如,极溶性、可溶性、微溶性、不溶性等)。根据药典,气体溶解度给出一个单位溶质质量(Msv)溶解的溶剂质量单位(Msv)、氢的气体溶解度为 641,000 Msv/Msu,这被认为是几乎不溶的。然而,氢的分子量低于普通药物(2 g/mol vs. 300 g/mol)。如果我们假设氢具有相同的摩尔溶解度为 0.78 mM,则这将把溶解度的类别从几乎不溶(或不溶)修改为微溶。
有趣的是,在药理学中,当最高剂量强度可溶于250mL或更少的水性介质时,可以认为药物是高度可溶的[87]。虽然氢的最高剂量强度尚未确定(如果存在),根据已发表的临床研究,0.5mg剂量被认为是较低有效的剂量。浓度为2 mg/L 将产生 0.5 mg氢的剂量在250 毫升中。几项临床研究使用了 250 mL 体积的氢水,其中含有超过 6 mg/L 的氢从而提供超过 1.5 mg氢的剂量 [64、88、89]。
此外,由于氢作为最轻和最小的分子,用摩尔而不是质量来比较它的溶解度更合适。在这种情况下,摄入 1 L 的氢饱和水比100 毫克剂量的维生素 C能提供更多的还原性分子(氢气为0.79 毫摩尔,100毫克维生素C只有0.57mmol)[75]。
浓度单位
通常使用百万分之一 (ppm) 或十亿分之一 (ppb) 的单位来表示氢的溶解度,而无需指定含义。如表1所示,术语ppm有三种实质性的不同用途来表示氢在水中的浓度。由于氢同位素(即氘和氚)的浓度通常使用摩尔/摩尔比率以 ppm 为单位报告,因此使用 ppm (wt/wt)表示氢浓度可能会造成混淆。例如,海水中的氘浓度约为156 ppm[90]。这听起来比含有氢气体饱和浓度1.57 ppm要多得多,但前者为 mol/mol,后者为 wt/wt。将单位调换,我们发现氘的浓度在wt/wt时为0.035 ppm(或0.33 ppm作为HDO),对于氢溶解在水中的气体使用 mol/mol 它是 14.04 ppm。此外,在物理学领域,ppm 在描述比例现象、测量不确定度和光谱学中的化学位移方面具有多种应用。例如,它可以表示每摄氏度长度的变化 (α = 1.2 ppm/°C),表示测量的准确性 (1 ppm),或表示光谱分析中的化学偏移 (2 ppm)。此外,ppb 上下文中的“十亿”一词在不同国家/地区的值可能不同,代表 10–9或 10–12.此外,值得一提的是,根据国际标准化组织(International Organization for Standardization, ISO)的建议,ppm并未得到国际单位制(SI)的正式认可,也不被视为符合SI标准的表达式[91]。因此,根据国际氢标准协会(IHSA)的标准和认证,建议以摩尔/摩尔浓度和毫克/毫克每升(mg/L)为单位作为表示氢剂量和浓度的首选措施。

氢气的药代动力学
如前所述,分子氢的较小尺寸和非极性使其能够快速穿透细胞生物膜并到达亚细胞器,包括线粒体和细胞核[92]。此外,氢可轻易穿透血脑屏障和睾丸屏障,并扩散至灌注受限的部位,如关节和肌腱[93]。然而,尽管具有优异的渗透性能,但氢不会简单地均匀地扩散到全身。相反,一旦摄入氢气,就会沿着阻力最小的路径前进,这意味着氢气会通过循环系统携带[94,95]。 对于氢水,氢气体主要在肠道中吸收并进入静脉血。然后将其从心脏泵送到肺部。近90%的氢在呼出的呼吸中消失,只有10%继续进入动脉血[96]。这就解释了为什么摄入低浓度氢水(0.08mg/L)不会增加大鼠大脑中的氢浓度[97]。吸入氢气体导致更高的动脉浓度,可以更好地到达更远端的器官[94]。作为氢溶解在血液中,它按照正常布朗运动的原理,根据其浓度梯度渗透细胞。虽然氢不像血红蛋白上的氧气那样由蛋白质载体运输,它比氧气更快地扩散到各个器官并到达亚细胞基质。氢气的扩散在整个微循环过程中,可能通过扩增效应促进其药理活性[98]。停止氢气给药时,无论如何给药,大约60分钟内氢气均可从体内清除并恢复到基线水平[94,95,96,99]。
氢气的药理作用
氢气的药理作用表现出广泛的多样性,包括各种生理条件[7]。氢气通过调节信号转导通路、miRNA表达、蛋白磷酸化级联反应和线粒体活性来发挥其作用[100]。然而,负责介导这些多方面生物学效应的具体分子机制和主要靶点尚未完全了解[101]。虽然人们认为氢气清除羟基自由基的能力有助于其产生一些作用[92],但仅凭这种机制不太可能解释所有观察到的作用[75]。反对氢生物学意义的主要论点是清除羟基自由基的反应速率常数显着低于其他二级反应,其速度相差三个数量级[75]。然而,最近研究表明,主要存在于线粒体和红细胞中的Fe-卟啉的存在可能作为氢气的氧化还原相关生物传感器[102]。据报道,这种Fe-卟啉生物传感器可催化氢气与•OH并规避较低的反应速率常数。此外,据报道,在吸附/配位氢的存在下,Fe-卟啉可以催化二氧化碳分子还原到一氧化碳,一氧化碳是一种以其治疗作用而闻名的气体递质[102,103]。
氢的主要抗氧化机制被认为通过内源性抗氧化剂的上调来减少氧化应激[75]。具体而言,氢气已被证明可诱导转录因子核因子红细胞2相关因子2(Nrf-2)易位到细胞核中[104]。Nrf2/keap1通路的激活和随后诱导血红素-1加氧酶在氢分子的抗氧化活性中起着至关重要的作用[101]。然而,氢气诱导Nrf2 激活的确切机制尚未确定。最近提出的基于Fe-卟啉分子的机理,其中由氢催化形成的氢原子可作为亲电试剂氧化KelcH样ECH相关蛋白 1(Keap1),导致激活Nrf2。然而,需要进一步的实验研究来验证和支持氢气的这些作用。氢药理作用的图形说明如图1.3.所示。
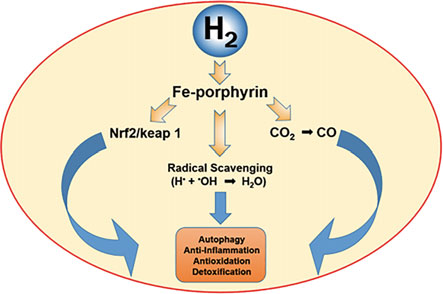
图1.3 氢气生物作用的可能机制
氢气的使用方法
氢气使用方法多种多样,包括不同的摄取途径和技术。这些包括吸入氢气体[105],通过管饲输送氢[106],静脉注射富氢盐水[107],氢用于血液透析的丰富透析液[108],高压氢腔室 [54],富氢水沐浴[109],增加肠道细菌氢的产生[110]、局部应用[111]、口服产氢片[112]和简单饮用富氢水(HRW)[63]。HRW可以通过多种方式制备,例如用氢气体加压水、电解水(2H2O → 2H2+ O2),或与金属镁反应的水(Mg+2H2O → H2+ 镁(OH)2)或其他金属[75]。市场上提供有一系列迎合消费者的产品,包括铝袋/罐装即饮饮料[79]、电解装置、氢-生产片剂和吸入机。但值得注意的是,并非所有产品都可能产生或含与人体研究中使用的浓度相当的氢浓度,相同水平也不能保证其稳定性[53]。
结论
氢的历史证明了其适应性和对其多样化应用的理解不断发展。从发现一种神秘的气体到目前作为有前途的能源载体和生物医学剂的作用,氢继续吸引着科学家和创新者,为可持续和氢驱动的未来铺平了道路。它在医学领域有着悠久的历史,早期的实验可以追溯到18世纪后期[10]。尽管最初对其感兴趣,但直到最近几年,它的治疗潜力在很大程度上被忽视了[11]。直到2007年,研究人员才开始密切关注[9]。从那时起,氢气在世界范围内得到了广泛的研究,甚至在新冠病毒大流行期间得到了利用[113]。今天,越来越多的科学文献证明了氢气的积极医疗效果。它在神经退行性疾病、糖尿病、运动表现和运动诱发损伤等多个领域都显示出前景[73]。尽管过去存在怀疑和兴趣波动,但氢气有望在二十一世纪的医学中发挥更重要的作用[10]。现在是时候让这种被忽视的分子得到认可并考虑用于更广泛的医学应用,希望氢气的医疗潜力不会像过去那样消退。
LeBaron T W, Sharpe R, Pyatakovich F A, et al. Hydrogen: From Stars to Fuel to Medicine[M]//Molecular Hydrogen in Health and Disease. Cham: Springer Nature Switzerland, 2024: 1-20.
44. Cavallo T (1798) An essay on the medicinal properties of factitious airs: with an appendix on the nature of blood. 1798: Printed for the author, and sold by C. Dilly [and 2 others]
https://blog.sciencenet.cn/blog-41174-1422508.html
上一篇:受限水能显著提高氢气的溶解度【2024】
下一篇:脑机接口对研究脑功能提供了新方法