ВЉЮФ
ИЮгВЛЏбЊвКОоЪЩЯИАћДњГЅЯжЯѓ
|
ИЮдрФкОоЪЩЯИАћДиДњГЅЯжЯѓ
ИЮдрЮЛгкГІЕРКЭЬхбЛЗжЎМфЕФНчУцПЩЗРжЙбЊдДадИаШОЃЈ1,2ЃЉЁЃ ЮЊДЫЃЌИЮдрЪЙгУУмМЏЕФЯСеЕФИЮёМбЊЙмЭјТчЃЌдЪаэЪмЮлШОЕФбЊвКЛКТ§СїЙ§зщжЏЁЃетаЉбЊЙмжаГфГтзХПтЦеИЅЯИАћЃЌетЪЧвЛжжИЮдрЕФГЃзЄОоЪЩЯИАћЃЌзЈУХДгбЛЗжаВЖЛёВЁдЬхЃЌетаЉЯИАћдкбЊвКжиаТНјШыЬхбЛЗжЎЧАЧхНрбЊвКЃЈ3ЃЉЁЃШЛЖјЃЌдкТ§адИЮВЁКЭЯрЙиЯЫЮЌЛЏжаЃЌетжжЯИАћЦСеЯЯЕЭГЪмЕНИЩШХЃЌЙЙГЩВЁдЬхШЋЩэДЋВЅЕФбЯжиЗчЯеЃЈ4ЃЉЁЃPeiselerЕШШЫзюНќдкЁЖПЦбЇЁЗдгжОЃЈ5ЃЉБЈИцСЫЯЫЮЌЛЏИЮдрЕФвЛИіЯдзХЬиеїЃЌМДИЮЭтЕФбЊвКбЛЗОоЪЩЯИАћБЛеаФМЕНЦїЙйжаВЂаЮГЩГЌШ§АћЬЅвдЧхГ§бЊдДадВЁдЬхЁЃдкетбљзіЕФЙ§ГЬжаЃЌетаЉГЌМЏШКБЃСєСЫИЮдрзїЮЊЙ§ТЫЦїЕФзїгУЃЌМДЪЙдкЛМИЮгВЛЏЪБвВЪЧШчДЫЁЃ
НЁПЕИЮдржаЃЌПтЦеИЅЯИАћЧЖШыаЧзДЯИАћЁЂИЮЯИАћКЭИЮёМФкЦЄЯИАћжаЃЌЭГГЦЮЊПтЦеИЅЯИАћЩњЬЌЮЛЁЃетаЉЩњЬЌЮЛЯИАћЙВЭЌдкПтЦеИЅЯИАћЩЯгЁМЧИЮдрЬивьадЙІФмЃЈ6ЃЉЃЌАќРЈЭЈЙ§ЩцМАЯИАћБэУцЪмЬхЕФЙ§ГЬдке§ёМЩЯРЉеЙЫПзДЮБзуВЂЭЬЪЩбЊдДадВЁдЬхЕФФмСІЃЌР§ШчВЙЬхУтвпЧђЕААзЪмЬх[ЃЈCRIgЃЉвВГЦЮЊВЙЬхЪмЬхV-setКЭУтвпЧђЕААзНсЙЙгђКЌЕААз4ЃЈVSIG4ЃЉЃЈ3)].CRIgдкШЫКЭаЁЪѓПтЦеИЅЯИАћЩЯБэДяЃЌБэУїCRIgНщЕМЕФЯИОњВЖЛёЪЧетаЉЯИАћЕФНјЛЏБЃЪиЙІФмЃЈ7ЃЉЁЃдкЮШЖЈзДЬЌЯТЃЌПтЦеИЅЯИАћЧјЪвБЃГжздЩэЃЌЖРСЂгкбЛЗЕЅКЫЯИАћЃЈ8ЃЉЃЌЕЋдкПтЦеИЅЯИАћЖЊЪЇЪБЃЌР§ШчдкТ§адИЮЫ№ЩЫЦкМфЃЌеаФМЕФЕЅКЫЯИАћжиаТЬюГфПтЦеИЅЯИАћГиЃЈ6,9ЃЉЁЃ гЩгкЕЅКЫЯИАћЕФзщжЏЬиЛЏЮЊГЃзЄОоЪЩЯИАћашвЊЪ§дТЪБМфЃЌВЂЧввЛЕЉЭъГЩЃЌЫЦКѕЖдБфЛЏгаЕжПЙСІЃЈ10ЃЉЃЌвђДЫзщжЏОоЪЩЯИАћЩэЗнЕФгЁМЧБЛШЯЮЊЪЧВЛПЩФцЕФЁЃ
PeiselerЕШШЫБЈИцЫЕЃЌдкЯЫЮЌЛЏаЁЪѓИЮдржаЃЌГЃзЄПтЦеИЅЯИАћШЅЗжЛЏВЂЪЇШЅСЫаэЖрЮШЬЌЪєадЃЌАќРЈCRIgЕФБэДяЁЃвђДЫЃЌЫќУЧгааЇЕиЪЇШЅСЫИЮдрЬивьадКЭзЈУХЕФВЁдЬхВЖЛёФмСІЁЃМјгкАќРЈаЧзДЯИАћдкФкЕФаЁПщЯИАћдкПтЦеИЅЯИАћЩэЗнгЁМЧжаЕФживЊзїгУЃЌзїепЬсГіЃЌЯЫЮЌЛЏИЮдржаПтЦеИЅЯИАћКЭаЧзДЯИАћжЎМфНгДЅУцЛ§ЕФЩЅЪЇЪЧетжжЩэЗнЩЅЪЇЕФЛљДЁЁЃPeiselerЕШШЫБэУїЃЌПтЦеИЅЯИАћдкЯЫЮЌЛЏаЁЪѓИЮдржаЪЇШЅСЫПтЦеИЅЯИАћЩэЗнжїзЊТМвђзгИЮдрXКЫЪмЬхІСЃЈNr1h3ЃЉЃЈ6,11ЃЉЕФБэДяЁЃПтЦеИЅЯИАћжаNr1h3ЕФБэДяЪЧгЩРДзде§ЯвФкЦЄЯИАћЕФNotchаХКХКЭРДздаЧзДЯИАћЕФЙЧаЮЬЌЗЂЩњЕААз9ЃЈBMP9ЃЉ[вВГЦЮЊЩњГЄЗжЛЏвђзг2ЃЈGDF2ЃЉ]аХКХДЋЕМЕФзщКЯгеЕМЕФЃЈ6ЃЉЁЃетБэУїПтЦеИЅЯИАћжаЕФNotch-BMP9аХКХдкЯЫЮЌЛЏИЮдржаЗЂЩњСЫИФБфЁЃ
ФПЧАЩаВЛЧхГўПтЦеИЅЯИАћжа Nr1h3 ЕФЯТЕїБэДяМАЦфЫцКѓИЮдрЬивьадЩэЗнЕФЩЅЪЇЪЧЗёЪЧЯЫЮЌЛЏЕФгАЯьЃЌжБНгЯожЦСЫаЧзДЯИАћКЭ ПтЦеИЅЯИАћжЎМфЕФНгДЅЃЌДгЖјЯожЦСЫЫќУЧЖд BMP9 ЕФЗУЮЪЃЌЛђепаЧзДЯИАћКЭ/Лђе§ЯвФкЦЄЯИАћЪЧЗёИФБфСЫЫќУЧЕФЛљвђБэДяЦзВЂЭЃжЙВњЩњгЁМЧПтЦеИЅЯИАћЩэЗнЕФвђзгЁЃжЕЕУзЂвтЕФЪЧЃЌPeiselerЕШШЫЗЂЯждкЯЫЮЌЛЏИЮдржаЗЂг§ЕФЕЅКЫЯИАћРДдДЕФПтЦеИЅЯИАћШБЗІCRIgЃЌетБэУїПтЦеИЅЯИАћЩњЬЌЮЛдкЯЫЮЌЛЏжаБЛЦЦЛЕЁЃ
ЮоТлШЗЧаЕФЗжзгЛњжЦШчКЮЃЌPeiselerЕШШЫБЈИцЫЕЃЌаЁЪѓЯЫЮЌЛЏИЮдргЩПтЦеИЅЯИАћЬюГф - ГЃзЄПтЦеИЅЯИАћКЭЕЅКЫЯИАћРДдДЕФПтЦеИЅЯИАћ - ШБЗІCRIgЕФБэДяКЭЯрЙиЕФЬиЪтВЁдЬхВЖЛёФмСІЁЃетЭЙЯдСЫИЮдрНсЙЙдкЪмЩЫЪБЮЌГжВЁдЬхВЖЛёЙІФмЕФОжЯоадЁЃШЛЖјЃЌИЮдрВЖЛёбЊдДадВЁдЬхЕФећЬхФмСІНіТдгаМѕШѕЁЃ
ЮЊСЫРэНтетжжВювьЃЌPeiselerЕШШЫбаОПСЫОоЪЩЯИАћдкаЁЪѓИЮдржаЕФЮЛжУЁЃдкНЁПЕЕФИЮдржаЃЌПтЦеИЅЯИАћНіЮЛгкИЮёМИННќЃЌгыЯШЧАЕФЙлВьНсЙћвЛжТЃЈ6ЃЉЁЃШЛЖјЃЌдкЯЫЮЌЛЏИЮдржаЃЌОоЪЩЯИАћвВдкНЯДѓЕФаЁОВТіКЭВржЇбЊЙмФкаЮГЩДѓЕФЖрЯИАћОлМЏЬхЁЃетаЉОлМЏЬхЛђКЯАћЬхМИКѕЭъШЋгЩЕЅКЫЯИАћбмЩњЕФОоЪЩЯИАћзщГЩЁЃКЯАћОоЪЩЯИАћЫЦКѕВЩгУСЫИЮдрЬивьадВЁдЬхВЖЛёЛњжЦЃЌCRIgЕФИпБэДяжЄУїСЫетвЛЕуЃЌВЂДгбЛЗжаВЖЛёСЫбЊдДадВЁдЬхЁЃДЫЭтЃЌдкНЁПЕИЮдржаЯрСкЕФаЧзДЯИАћППНќЯЫЮЌЛЏИЮдржаЕФаЁОВТіКЭВржЇбЊЙмЃЈМћЭМЃЉЁЃ
PeiselerЕШШЫЬсГіЕФвЛИіМйЩшЪЧаЧзДЯИАћЧЈвЦвдНЋВЁдЬхВЖЛёЙІФмгЁМЧдкКЯАћОоЪЩЯИАћЩЯЁЃШЛЖјЃЌвЛжжЯрЗДЕФЛњжЦЃЌМДаЧзДЯИАћЕФЧЈвЦЯШгкКЯАћЬхаЮГЩЃЌвВПЩвдНтЪЭетаЉЗЂЯжЁЃШчЙћЪЧетбљЃЌМВВЁдчЦкЕФаЧзДЯИАћЧЈвЦПЩФмЕМжТе§ЯвСкНќЕФПтЦеИЅЯИАћЕФЙІФмЩЅЪЇЁЃЮоТлШчКЮЃЌетаЉЗЂЯжЬсГіСЫвЛИіЮЪЬтЃЌМДИЮдрЩњЬЌЮЛЪЧЗёвдаЕїЕФЗНЪНЖдЫ№ЩЫзіГіЗДгІЃЌЛђепдкЫ№ЩЫЪБЃЌИїжжЩњЬЌЮЛЯИАћЪЧЗёвдЭбНкЕФЗНЪНзіГіЗДгІКЭЧЈвЦЃЌДгЖјДђЦЦЮШЬЌЩњЬЌЮЛВЂПЩФмНЈСЂаТЕФбзжЂЩњЬЌЮЛЁЃ
PeiselerЕШШЫЛЙШЗЖЈСЫКЯАћОоЪЩЯИАћЩЯДцдкЕФСНжжеГИНЗжзг - CD44КЭбЊаЁАхЬЧЕААз4ЃЈCD36ЃЉ - зїЮЊГЌЭХДиаЮГЩЕФЙиМќВЮгыепЁЃHyalyronanЪЧCD44ЕФХфЬхЃЌдкЯЫЮЌЛЏИЮаЁОВТіКЭВрБкЩЯИпЖШБэДяЃЌвђДЫдЪаэБэДяCD44ЕФЕЅКЫЯИАћеГИНЃЌЗжЛЏГЩЧАКЯЬхОоЪЩЯИАћЁЃCD36ЖдгкетжждчЦкеГИНЪЧПЩгаПЩЮоЕФЃЌЕЋЕЅКЫЯИАћКЭЫцКѓЕФОоЪЩЯИАћашвЊШкКЯГЩКЯАћЬхЁЃжЕЕУзЂвтЕФЪЧЃЌОЁЙмCRIgБэДядіМгЃЌЕЋШБЗІCD36ЕФФММЏОоЪЩЯИАћЮДФмаЮГЩКЯАћЬхЛђВЖЛёбЊдДадВЁдЬхЁЃвђДЫЃЌКЯАћЬхЖдВЁдЬхЕФгааЇЩуШЁЫЦКѕЪЧе§ШЗв§ЗЂЕФОоЪЩЯИАћгыОоЪЩЯИАћГЌДиаЮГЩжЎМфЕФЯрЛЅзїгУЁЃКЯАћОоЪЩЯИАћЕФГЄЦкУќдЫЩаВЛЧхГўЁЃЪТЪЕЩЯЃЌЪЧЗёгаПЩФмЭъШЋЛжИДНтЦЪбЇКЭЙІФмадИЮдрЃЌЛђепетаЉКЯАћЬхЪЧЗёГЪЯжГжОУЕФБфЛЏЩаВЛЧхГўЁЃ
PeiselerЕШШЫЕФЙлВьНвЪОСЫЪмЫ№аЁЪѓИЮдрЕФЯдзХЪЪгІЃЌвдЮЌГжЦфЧхГ§бЛЗВЁдЬхЕФФмСІЁЃзїепЛЙдкЛМВЁЕФШЫИЮдржаЗЂЯжСЫОоЪЩЯИАћКЯАћЬхЃЌетБэУїСЫвЛжжНјЛЏБЃЪиЕФЛњжЦЁЃдкзщжЏбзжЂЕФБГОАЯТЃЌШЮКЮзщжЏжаЕФзщжЏзЄСєОоЪЩЯИАћЩэЗнКЭЙІФмЪЧЗёЪЧПЩФцЕФ - ОЭЯёИЮдрЕФПтЦеИЅЯИАћвЛбљ - ЩаВЛЧхГўЁЃШчЙћЪЧетбљЃЌетжжШЅЗжЛЏПЩФмЛсгАЯьИїжжЫ№ЩЫЛЗОГжаЕФзщжЏзЄСєОоЪЩЯИАћЃЌВЂПЩФмОпгаКмДѓЕФСйДВЯрЙиадЁЃ
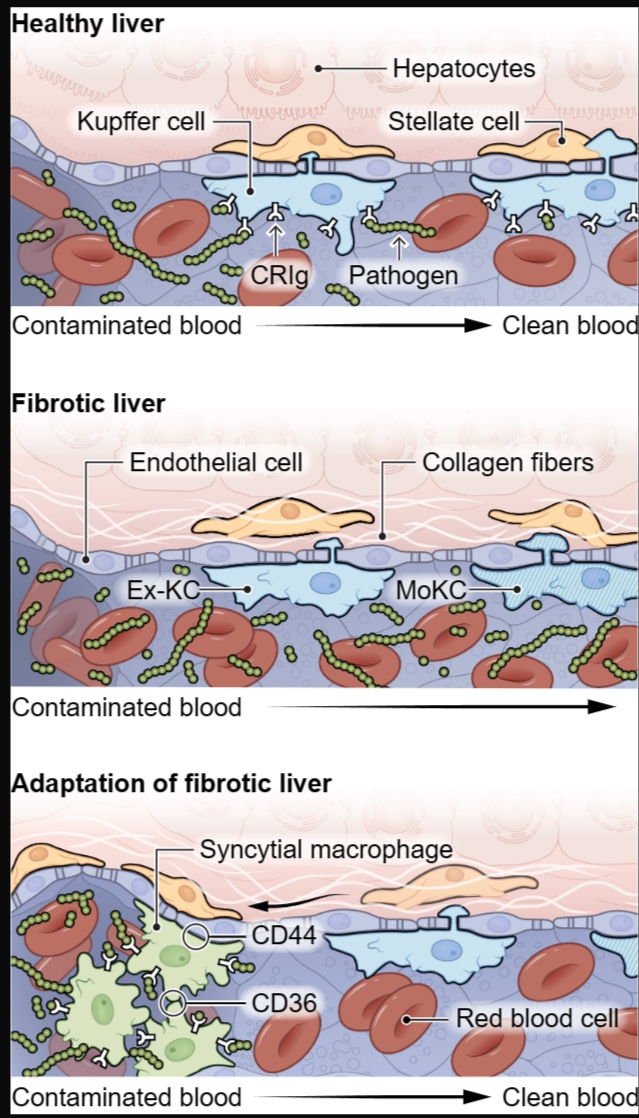
ЯЫЮЌЛЏИЮдрЕФЪЪгІ
дкНЁПЕЕФИЮдрЃЈЖЅВПЃЉжаЃЌПтЦеИЅЯИАћБЛаЧзДЯИАћЃЌФкЦЄЯИАћКЭИЮЯИАћгЁМЧЃЌвдЪЙгУВЙЬхУтвпЧђЕААзЪмЬхЃЈCRIgЃЉВЖЛёбЊдДадВЁдЬхЁЃдкЯЫЮЌЛЏИЮдржаЃЌгЁМЃЪЇАмЃЌЕМжТЧАПтЦеИЅЯИАћЃЈЧАKCsЃЉКЭЕЅКЫЯИАћРДдДЕФПтЦеИЅЯИАћЃЈmoKCsЃЉШБЗІCRIgЃЌвђДЫЮоЗЈЭЬЪЩВЁдЬхЃЈжаЃЉЁЃИЮдрЭЈЙ§аЮГЩБэДяCRIgЕФОоЪЩЯИАћДиЛђКЯАћЬхРДЪЪгІЃЈЕзВПЃЉЃЌДгЖјБЃГжЙ§ТЫФмСІЁЃетаЉОоЪЩЯИАћгыбЊаЁАхЬЧЕААз4ЃЈCD36ЃЉЯрЛЅИНзХЃЌВЂгыCD44ИНзХдкаЁОВТіЛђВржЇФкЦЄЯИАћЩЯЁЃ
Kupffer cellЈClike syncytia replenish resident macrophage function in the fibrotic liver | Science
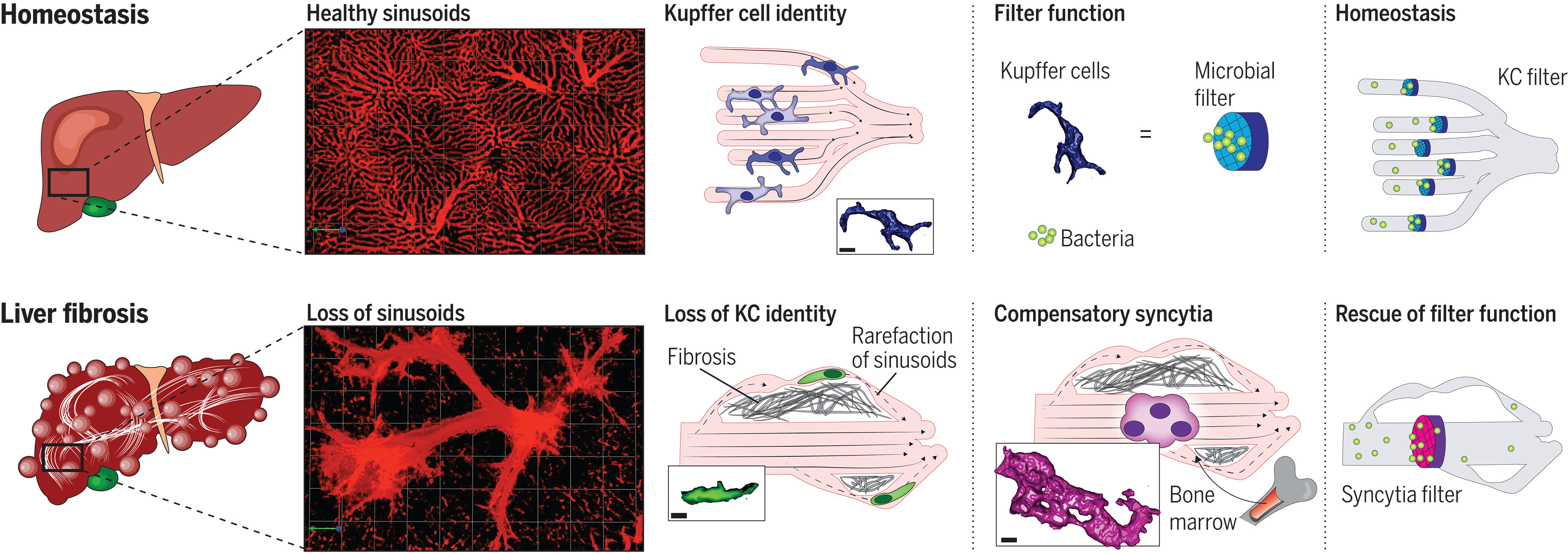
ТлЮФеЊвЊ
НщЩм
ОжВПЛЗОГЖдгкШЗЖЈИјЖЈЦїЙйФкОоЪЩЯИАћЕФБэаЭжСЙиживЊЁЃдкИЮдржаЃЌГЃзЄОоЪЩЯИАћдкгЩИЮЯИАћЁЂФкЦЄЯИАћКЭаЧзДЯИАћзщГЩЕФЩњЬЌЮЛжаНгЪежИЕМадЯпЫїЁЃетаЉЯпЫїМЄЛюЬиЖЈЕФзЊТМвђзгЃЌИГгшетаЉОоЪЩЯИАћПсЪЯЯИАћЃЈKCЃЉЁАЩэЗнЁБЁЃKCsЭЈЙ§зЈУХЕФЪмЬхЃЈАќРЈВЙЬхЪмЬхCRIgЃЉжДааДгбЊвКжаВЖЛёВЁдЬхЕФЙиМќЙІФмЁЃИЮЯЫЮЌЛЏКЭИЮгВЛЏЪЧИїжжТ§адИЮВЁЕФГЃМћжеФЉЦкЃЌЕМжТЪмгАЯьИіЬхЕФДѓСПЗЂВЁТЪКЭЫРЭіТЪЁЃОЁЙмВЁвђВЛЭЌЃЌЕЋНјеЙЯрЫЦЃЌИЮЯИАћЫРЭіКЭИЮёМжмЮЇНКдГСЛ§ЃЌЕМжТбЊСїжиаТЗжХфЕНаТЕФКЭРЉДѓЕФИЮФкКЭИЮЭтВржЇбЊЙмЁЃ
РэгЩ
ФПЧАЩаВЛЧхГўЩњЬЌЮЛЛЗОГЕФЯЫЮЌЛЏжиЫмШчКЮгАЯьKCИєЪвЁЃдкетЯюбаОПжаЃЌЮвУЧЪЙгУИїжжЦзЯЕзЗзйФЃаЭКЭЛюЬхЯдЮЂОЕРДПЩЪгЛЏЁЂИњзйКЭЙІФмЦРЙРЯЫЮЌЛЏИЮдрЛЗОГжаЕФЕЅКЫЯИАћКЭ KCЁЃ
НсЙћ
ЪЙгУзюГЃМћЕФИЮЯЫЮЌЛЏаЁЪѓФЃаЭ - ЫФТШЛЏЬМЖОад - ЮвУЧЙлВьЕНИЮдрЕФЩюПЬНсЙЙБфЛЏЁЃетжжжиЫмАќРЈВржЇбЊЙмКЭе§ЯвжмЮЇНКдЕААзГСЛ§ЕФДѓСПдіМгЃЌетЕМжТKCsгыжмЮЇЛЗОГЪЇШЅСЊЯЕЁЃетЗДЙ§РДгжЕМжТЙиМќзЊТМвђзгКЭФЄЕААзЃЈШчCLEC4FЃЌCRIgКЭTIM-4ЃЉЕФЯТЕїЃЌЫќУЧЙВЭЌОіЖЈСЫKCЩэЗнЁЃОЁЙметаЉБфЛЏЕМжТKCЙІФмЪмЫ№ЃЌОЁЙмKCЩэЗнЩЅЪЇЃЌИЮдрШдМЬајГфЕБбЊдДадЯИОњЕФжївЊЙ§ТЫЦїЁЃ
ИЮдрДгбЊвКеаФМДѓСПЕФЕЅКЫЯИАћЃЌгЩгкГІЕРЮЂЩњЮяШКЧ§ЖЏЕФФкЦЄЯИАћеГИНаддіМгЃЌетаЉЯИАћжївЊЭЈЙ§CD44еГИНЕНДѓЕФИЮФкбЊЙмЩЯЁЃЕЅКЫЯИАћдкВржЇбЊЙмФкаЮГЩДѓДиВЂПЊЪМБэДяKCБъжОЮяЁЃетаЉЕЅКЫЯИАћЙЙГЩСЫвЛЯЕСаНсЙЙЃЌДгЕЅИіЯИАћДиЕНШкКЯЕФЖрКЫОоЯИАћЃЌетаЉОоЯИАћЙВЭЌБэЯжЮЊKCбљКЯАћЬхЁЃЫфШЛЕЅИіKCsЮоЗЈВЖЛёдкНЯДѓбЊЙмФкСїЖЏЕФЯИОњЃЌЕЋKCбљКЯАћЬхФмЙЛВЖЛёДѓСПбЛЗЯИОњЁЃЪЙгУзЊТМзщбЇЗжЮіЃЌЮвУЧНЋCD36ШЗЖЈЮЊКЯАћЬхШкКЯЕФЙиМќЗжзгЃЌВЂНЕЕЭСЫЖдИаШОЕФвзИаадЁЃБэДяCRIgЕФбЊЙмФкОоЪЩЯИАћКЯАћЬхвВМћгкВЛЭЌВЁвђЕФШЫИЮгВЛЏЁЃ
НсТл
гыЯЫЮЌЛЏЩњЬЌЮЛжаЕФЪЕжЪЯИАћЪЇШЅНгДЅЛсЕМжТе§ГЃзЄСєЕФKCЪЇШЅЩэЗнКЭЙІФмЁЃгЩгке§ГЃЕФKCВЙГфМИКѕУЛгагУДІЃЌвђДЫЕЅКЫЯИАћзёбШЦЙ§ИЮёМЕФВржЇбЊЙмЕФаЮГЩЃЌдкФЧРяЫќУЧаЮГЩKCбљКЯАћЬхЃЌОпгаДгбЊвКжаВЖЛёЯИОњЕФФмСІЁЃвђДЫЃЌдкИФБфЕФЯЫЮЌЛЏЩњЬЌЮЛЛЗОГжаЕФKCЪЪгІВЛСМБЛаЮГЩKCбљКЯАћЬхЕФЕЅКЫЯИАћеќОШвдВЖЛёЯИОњЁЃетаЉЯИАћНсЙЙПЩФмЗЂЛгЙиМќЕФНјЛЏзїгУЃЌЪЙВИШщЖЏЮяФмЙЛГаЪмИЮдржаЕФбЯжиТ§адЫ№ЩЫЁЃ
https://blog.sciencenet.cn/blog-41174-1402086.html
ЩЯвЛЦЊЃКХЕБДЖћвНбЇНБЕФдЄШШЃКвШИпбЊЬЧЫибљыФ-1
ЯТвЛЦЊЃКФдЮэПЩФмЪЧФ§бЊЙІФмПКНјЕФКѓЙћ