博文
抗体偶联药物 ADC 和自身免疫性疾病_MCE(MedChemExpress)
|
Section.01
RA 发病机制
类风湿性关节炎 (RA) ,其病理核心在于免疫耐受失衡——机体免疫系统未能正确区分“自身”与“异己”,打破了免疫稳态,导致对自身组织产生免疫攻击。
正常情况下,免疫系统能区分自身与异物。但在类风湿患者体内,免疫细胞误将关节滑膜中的瓜氨酸化蛋白识别为“外来敌人”。这种免疫系统“认错人”的现象,导致炎症细胞的快速增殖和活化,主要炎症部位是滑膜。
滑膜组织异常扩张,伴有新生血管形成、内膜过度增生,机体产生类风湿因子 (RF)、抗瓜氨酸化蛋白抗体 (ACPA) 等针对自身组织的抗体,并持续释放 TNF-α、IL-1 等大量促炎因子,从而导致滑膜出现持续性炎症,进而引发关节软骨和骨破坏[1]。类风湿性关节炎患者的关节肿胀反映了由于免疫激活而引起的滑膜炎症。
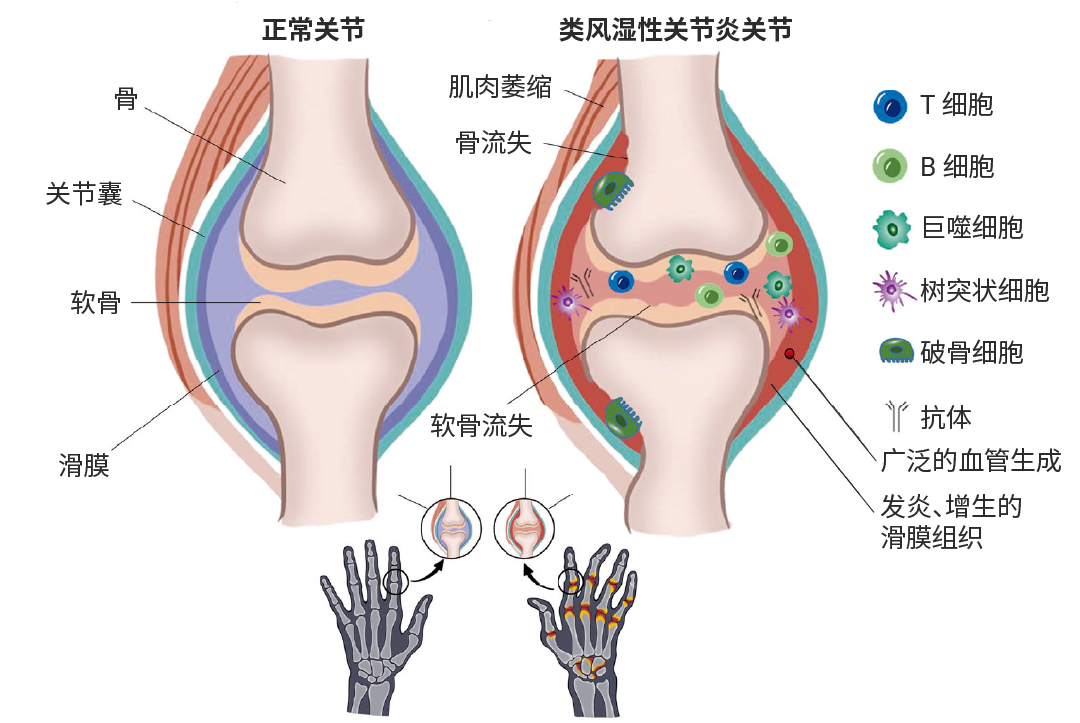
图 1. 正常关节与类风湿性关节炎关节[1]。
Section.02
RA 药物发展
在 20 世纪 90 年代初,糖皮质激素 (Cs) 或 NSAIDs (非甾体抗炎药)、是治疗类风湿关节炎的主要手段。

近几十年来,则以改善病情抗风湿药 (DMARDs) 为基础,作为 RA 的一线治疗方案。其中,传统合成 DMARDs (csDMARDs) 包括甲氨蝶呤 (MTX) 和羟氯喹(HCQ) 等药物。它们能够减轻炎症、缓解疼痛并延缓关节破坏。甲氨蝶呤是 RA 药物治疗中最广泛应用的药物。

新型生物制剂 DMARDs (bDMARDs),是靶向蛋白信使分子或细胞单克隆抗体和可溶性受体的一类药物, 包括英夫利昔单抗、 依那西普等[2]。

自 bDMARD 兴起之后,tsDMARD (靶向合成 DMARDs)——小分子靶向药物,如 JAK 抑制剂——在类风湿性关节炎临床治疗中的地位逐年提升。2012 年,托法替布获得美国食品药品监督管理局 (FDA) 批准,用于成人中重度类风湿性关节炎的治疗,成为全球首个用于 RA 治疗的 tsDMARDs。
 图 1.流式细胞术原理图[1]。
图 1.流式细胞术原理图[1]。尽管不同类别的药物已证明具有改善 RA 相关症状或预防疾病进展的潜力,但每类药物都有其局限性[3]。
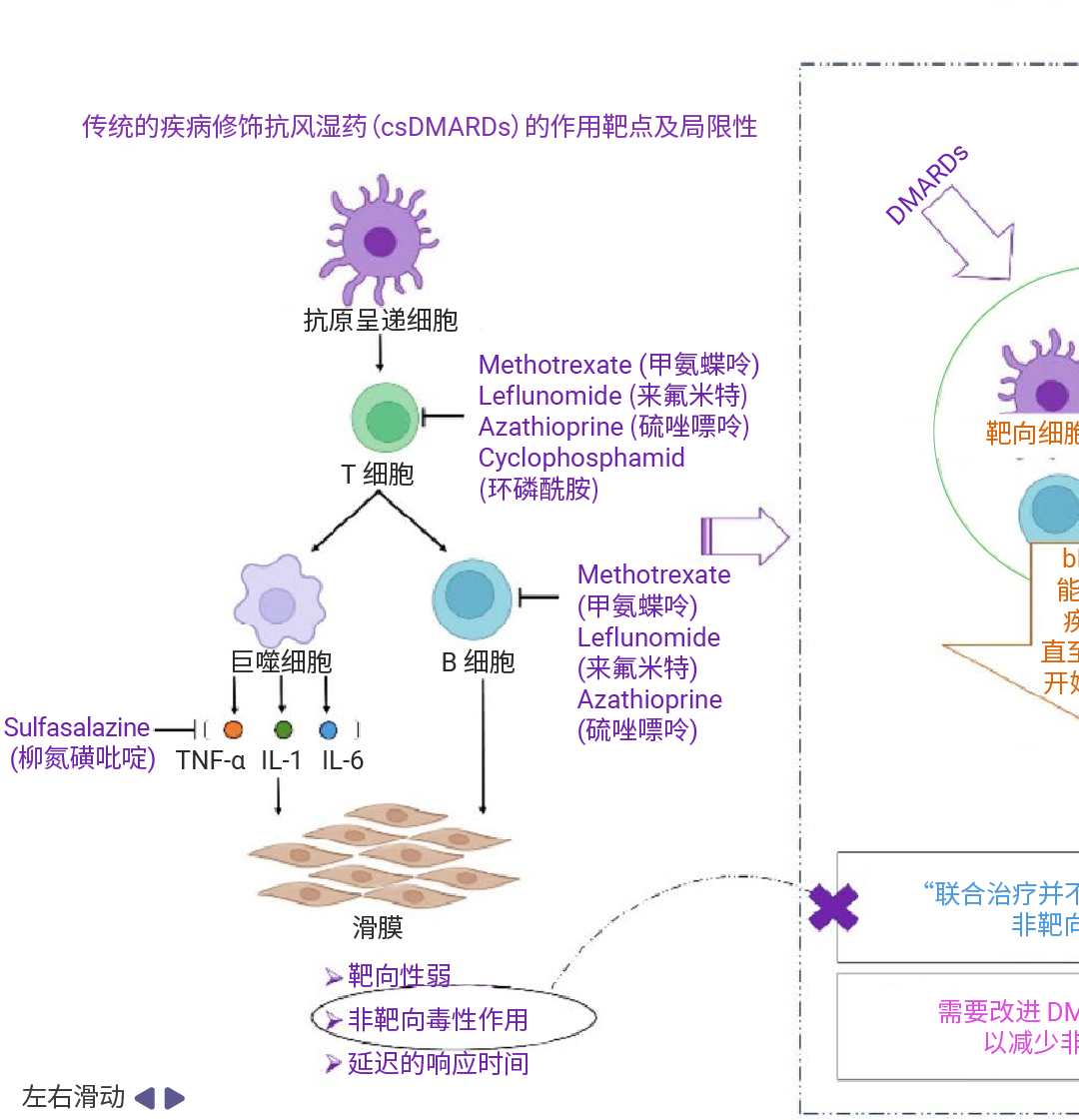
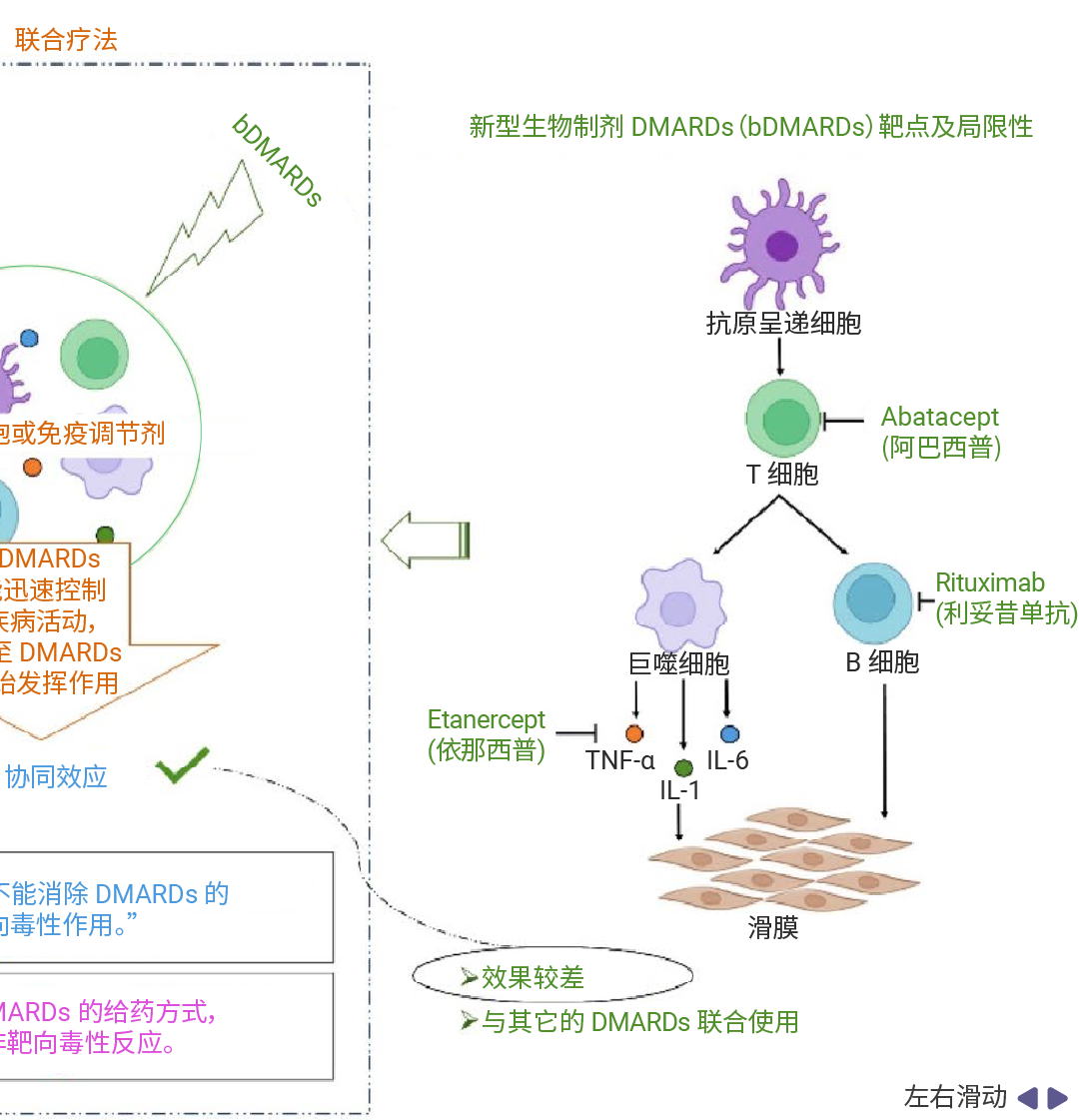
图 2. 与 DMARDs、bDMARDs、联合疗法相关的局限性[3]。
Section.03
靶向干预: ADCs
为了克服这些相关的限制并保留抗炎特性,研究人员开始探索靶向疗法。
抗体药物偶联物(ADC)
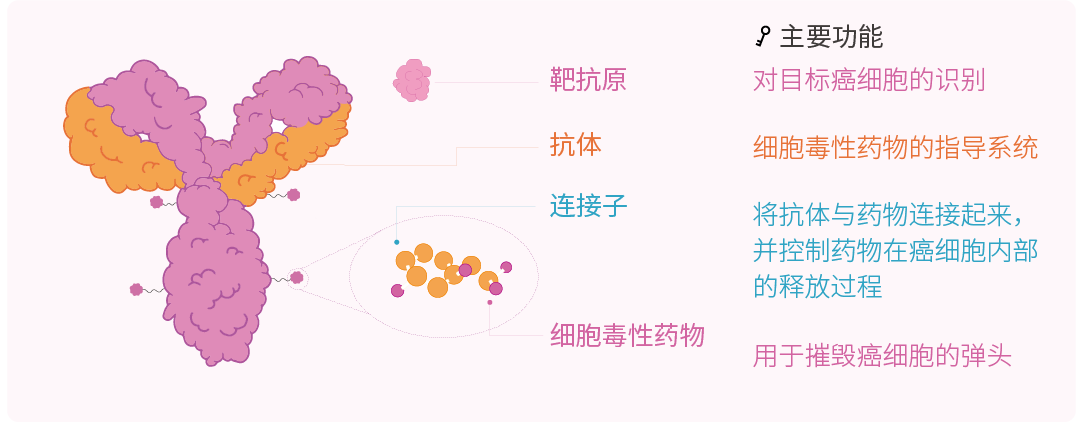
抗体药物偶联物 (Antibody-drug conjugates, ADC),这一新概念的开发,旨在克服单独使用单克隆抗体 (mAb) 的局限性。
ADC 是将单克隆抗体与强效细胞毒性有效载荷通过化学连接子偶联而成。
这种靶向给药方法结合了有效载荷的细胞毒性作用 (有效载荷本身毒性过大,通常无法全身给药) 和 mAb 靶向部分的精准性。
通过限制有效载荷与健康组织的接触,ADC 可以降低脱靶毒性,并有可能扩大治疗窗口,已有多种 ADC 获得 FDA 批准用于肿瘤治疗。
目前正在进行 RA 治疗临床试验的 ADC 通常以糖皮质激素、双膦酸盐类药物或抗有丝分裂药物作为有效载荷。然而,这些药物并不能直接抑制 RA 的进展。
有研究提出一种独特的 ADC 合成策略,即利用针对 RA 发病机制中相关细胞或免疫调节剂的单克隆抗体作为递送载体,并以 DMARD 作为有效载荷,有效靶向并破坏参与类风湿性关节炎发病机制的靶 B 细胞、T 细胞、巨噬细胞或免疫调节剂。最终导致细胞死亡,从而提供高精度给药,最大限度地减少脱靶效应,并提高治疗效果 (图[3])。
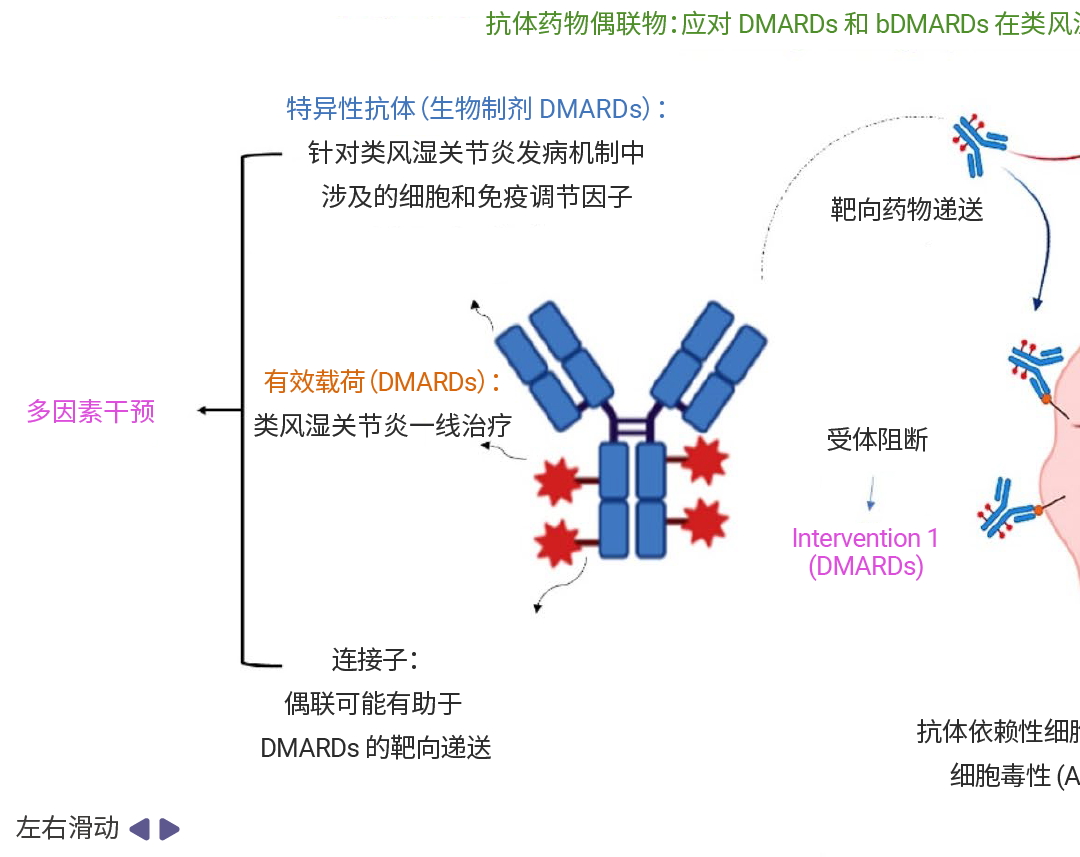
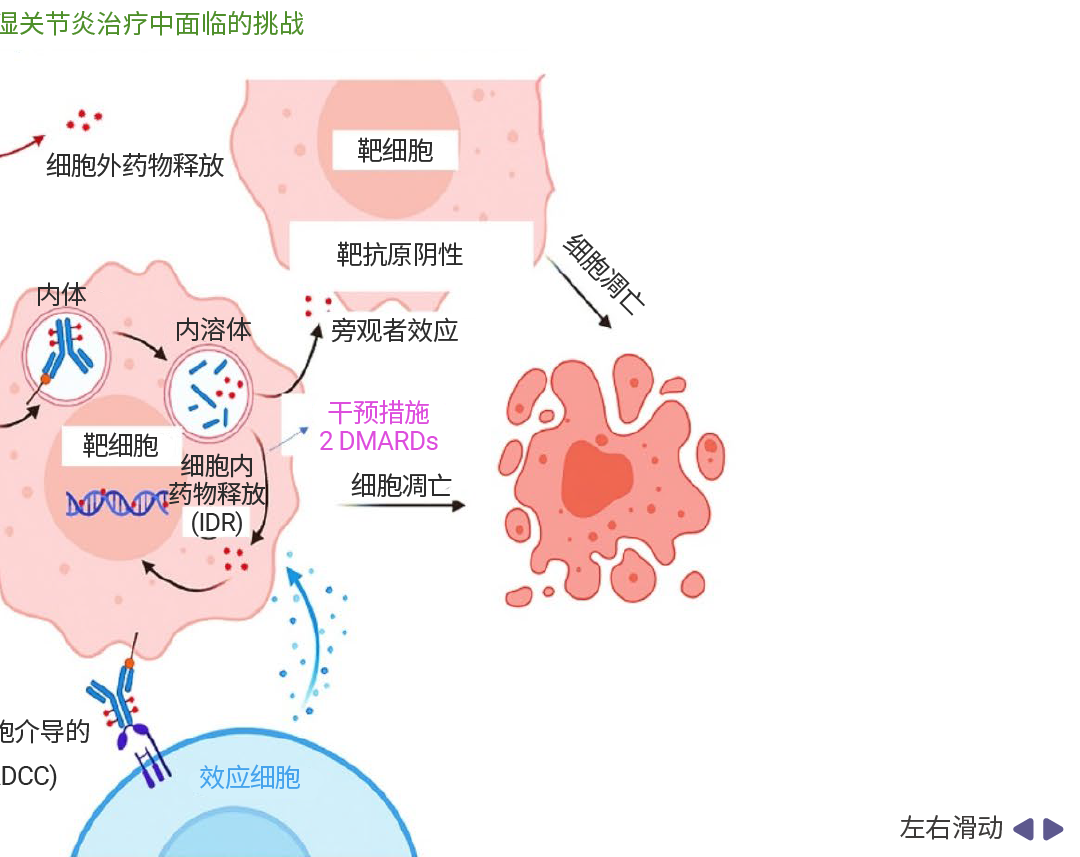
图 3. ADC 增加 RA 治疗的策略[3]。
DMARDs 可以通过抗体与靶细胞表面的特定抗原结合,直接递送至靶细胞。结合后,ADC 通过内吞作用进入细胞,形成内体。内体进化成内溶酶体,DMARDs 在酸性环境或酶促降解作用下被释放到细胞外。这一过程确保 DMARDs 在靶细胞内准确释放。
抗 TNF-GRM ADC (ABBV-3373) 的 IIa 期研究数据是 RA 治疗方面关于新型 ADC 的首次结果报道。
抗 TNF-GRM ADC (ABBV-3373),是由抗 TNF 抗体 (阿达木单抗, ADM) 和糖皮质激素受体调节剂 (GRM) 通过连接子连接而成。在关节炎诱导的小鼠模型中进行测试时,与单独的抗 TNF 抗体相比,ADC 在抑制炎症方面表现出增强的功效。在临床试验中,与阿达木单抗组相比,ABBV-3373 组显示出显著改善。在安全性方面,ABBV-3373 中上呼吸道感染、过敏性休克和非心源性胸部扭曲等副作用的发生率较低 (35% vs. 71%) [4]。
Section.04
ADC 的设计
为了尽可能提高药物的有效性和安全性,在设计 ADC 时必须考虑几项关键要素,包括靶点的选择、靶向特异性抗体、有效载荷以及连接子。
产品推荐
ADC
ADC antidiv
Glucocorticoid receptor agonist-2 Ala-Ala-Mal (HY-148436)
Drug-Linker Conjugates for ADC
ADC
Glucocorticoid receptor agonist-1 phosphate Gly-Glu-Br (HY-137883)
Drug-Linker Conjugates for ADC
ADC Protease Cleavable Linker
DBCO-Val-Cit-PABC-PNP (HY-130937)
ADC Protease Cleavable Linker
ADC Protease Cleavable Linker
Mc-Gly-Gly-Phe-Gly-PAB-OH (HY-136432)
ADC Protease Cleavable Linker
ADC Payload
ADC Payload
ADC Payload
ADC Payload
Drug-Linker Conjugates for ADC
Drug-Linker Conjugates for ADC
Drug-Linker Conjugates for ADC
Drug-Linker Conjugates for ADC
Drug-Linker Conjugates for ADC
参考文献
[1] Ding Q, et al. Signaling pathways in rheumatoid arthritis: implications for targeted therapy. Signal Transduct Target Ther. 2023 Feb 17;8(1):68.
[2] 崔涵姝,刘斌.应用改善病情抗风湿药物治疗骨关节炎之争[J].协和医学杂志,2025,16(1):13?18.
[3] Dixit T, et al. Therapeutic potential of antibody-drug conjugates possessing bifunctional anti-inflammatory action in the pathogenies of rheumatoid arthritis. Arthritis Res Ther. 2024 Dec 19;26(1):216.
[4] Buttgereit F, et al. Efficacy and Safety of ABBV-3373, a Novel Anti-Tumor Necrosis Factor Glucocorticoid Receptor Modulator Antibody-Drug Conjugate, in Adults with Moderate-to-Severe Rheumatoid Arthritis Despite Methotrexate Therapy: A Randomized, Double-Blind, Active-Controlled Proof-of-Concept Phase IIa Trial. Arthritis Rheumatol. 2023 Jun;75(6):879-889.

https://blog.sciencenet.cn/blog-3536222-1531576.html
上一篇:蛋白激酶家族:药物研发的关键靶点_MCE(MedChemExpress)