博文
蛋白激酶家族:药物研发的关键靶点_MCE(MedChemExpress)
|
Section.01
激酶组分类
人类基因组编码的激酶统称为激酶组,对人类激酶组的系统性认知,是靶向药物开发的基石。
根据 Manning 团队的开创性研究,人类蛋白激酶组包含 518 个成员[1]。后续研究进一步扩展了这一图谱,将更多非典型激酶 (aPKs) 纳入其中,目前在 KinBase 等权威数据库中注释的蛋白激酶总数已达 538 种。
理解如此庞大的激酶家族,可从两个相互关联的维度入手:一是根据其催化的生化反应——磷酸化什么底物?;二是根据其蛋白结构的进化关系与序列同源性——属于哪个家族?
一、根据磷酸化底物分类
根据其作用的底物类型,激酶主要可分为四类:蛋白激酶、脂质激酶、碳水化合物激酶和核酸激酶。其中,蛋白激酶因其成员数量最多、调控网络最复杂、与疾病发生发展的关联最为直接,成为药物研发的绝对焦点。通常所说的“激酶靶点”,绝大多数即指蛋白激酶。
表1. 根据磷酸化底物对激酶分类[1]。
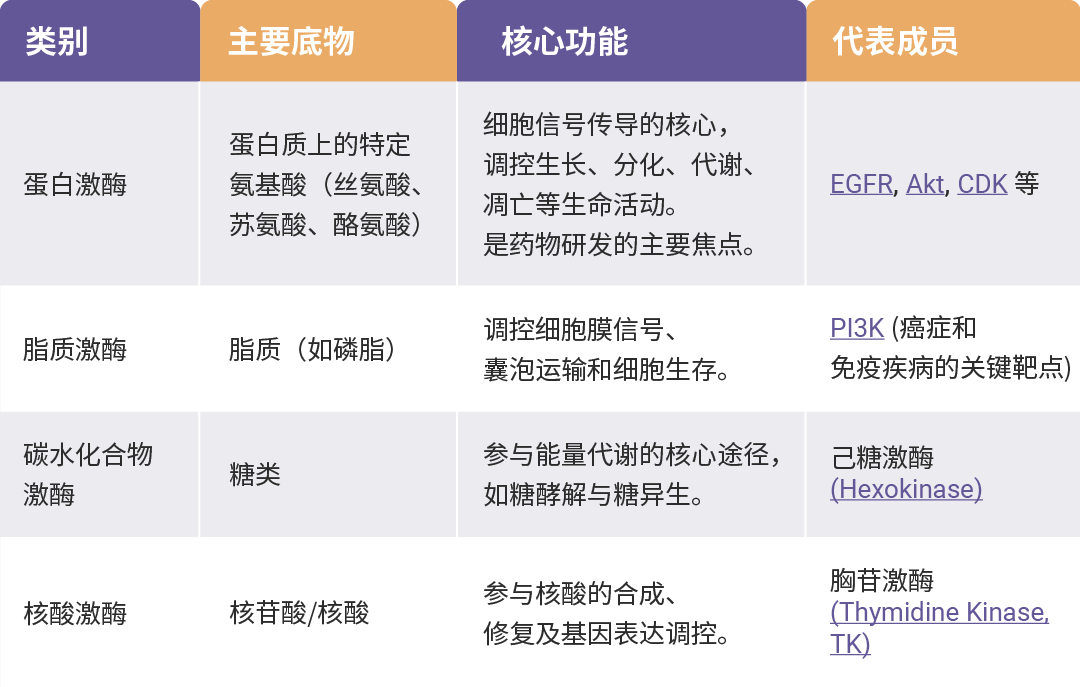
二、根据序列与进化导向分类
基于对激酶催化结构域序列与功能的系统研究,人类激酶组又可分为两大范畴:典型蛋白激酶 (ePKs) 与非典型蛋白激酶 (aPKs)。
典型蛋白激酶的共同特征是拥有一个同源且催化机制明确的真核蛋白激酶结构域。30 年前,一篇里程碑式的文章发表了首个蛋白激酶 (蛋白激酶 A, PKA) 的晶体结构,该结构揭示了蛋白激酶保守的结构核心,约 250-300 个氨基酸组成,包含一个 β-折叠为主的 N 端小叶和一个 α-螺旋为主的 C 端小叶,ATP 分子就结合在两者之间的裂隙中[2][3]。
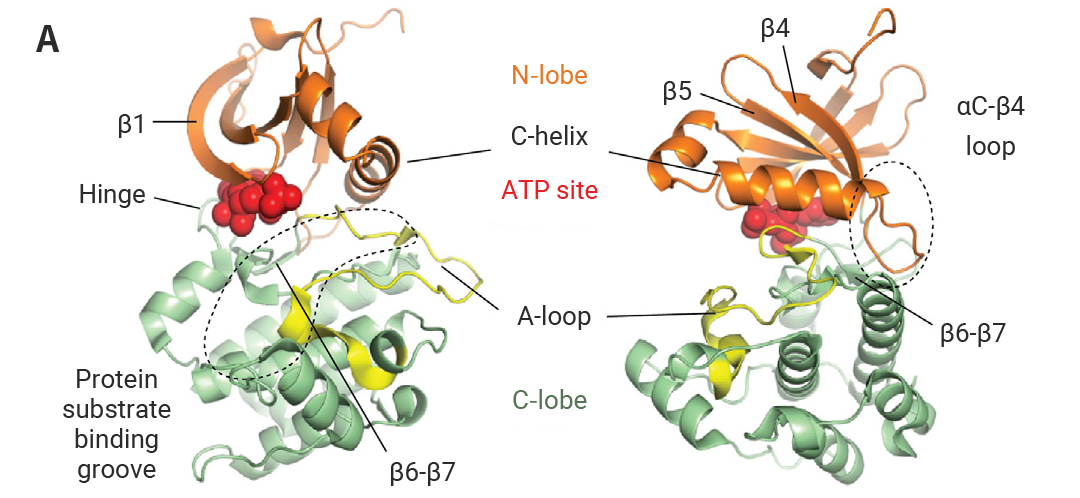
图 1. 激酶结构域的关键结构特征[2]。
该结构域由 N 端叶 (橙色) 和 C 端叶 (绿色) 组成,两者通过铰链序列连接。ATP 结合位点 (红色) 位于两个叶的界面处。
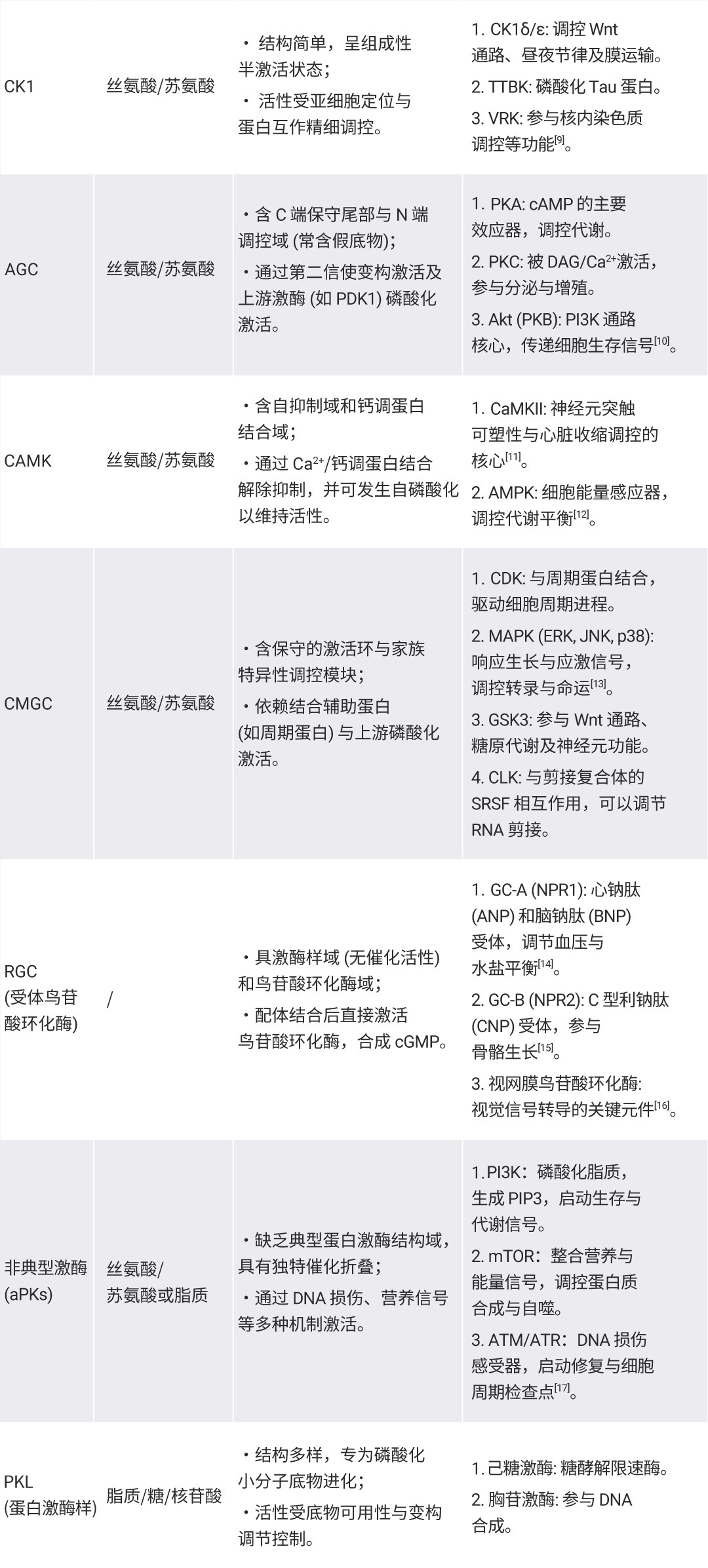
根据该结构域的序列相似性,可进一步划分为八个主要家族:TK、TKL、STE、CK1、AGC、CAMK、CMGC 和 RGC。这些家族构成了细胞信号转导的核心框架。非典型蛋白激酶虽具有激酶活性,但其催化结构域与典型激酶不同,体现了激酶在进化过程中的功能多样性,其中包含 PI3K、mTOR 等多个关键药物靶点[4][5][6]。
表2. 根据催化结构域的序列相似性与系统进化关系对激酶分类[4][5][6]。

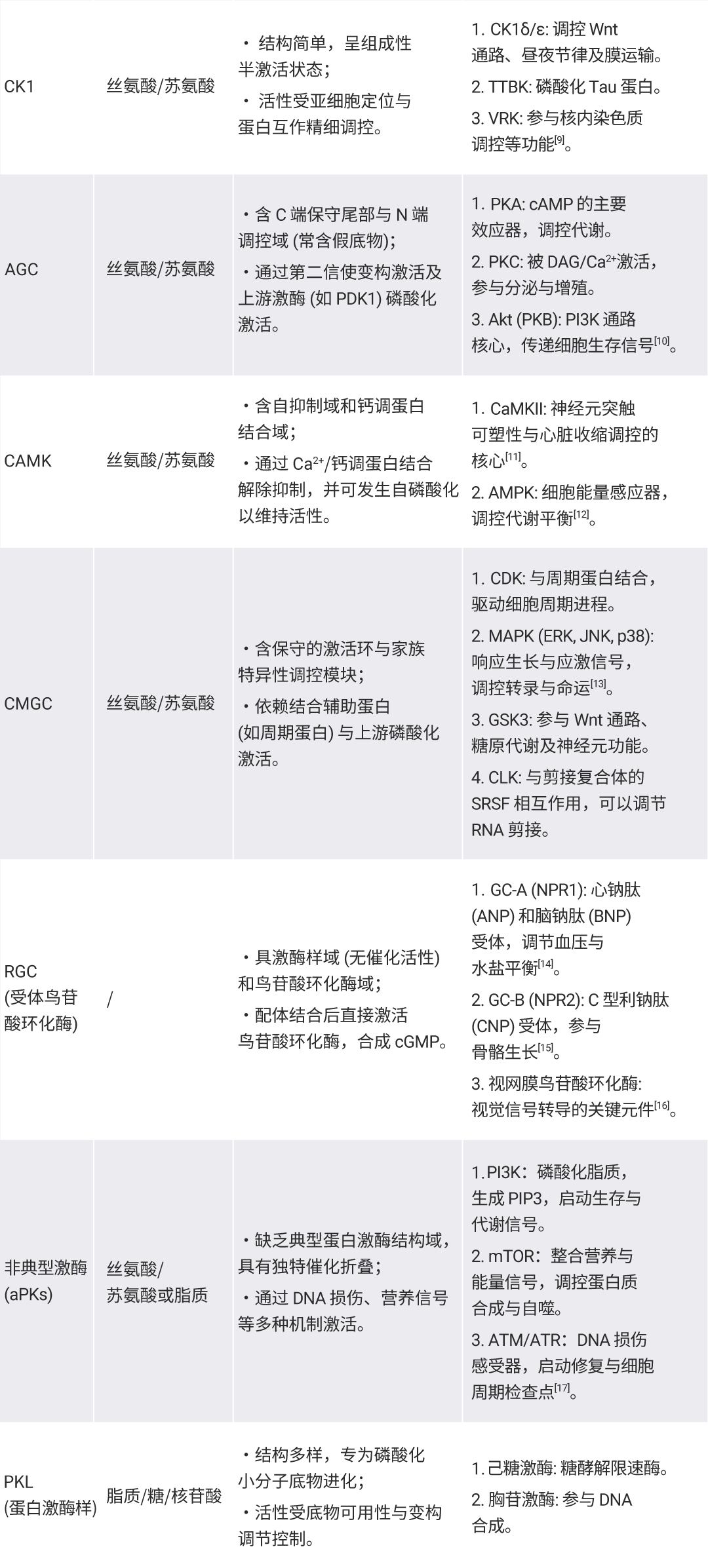
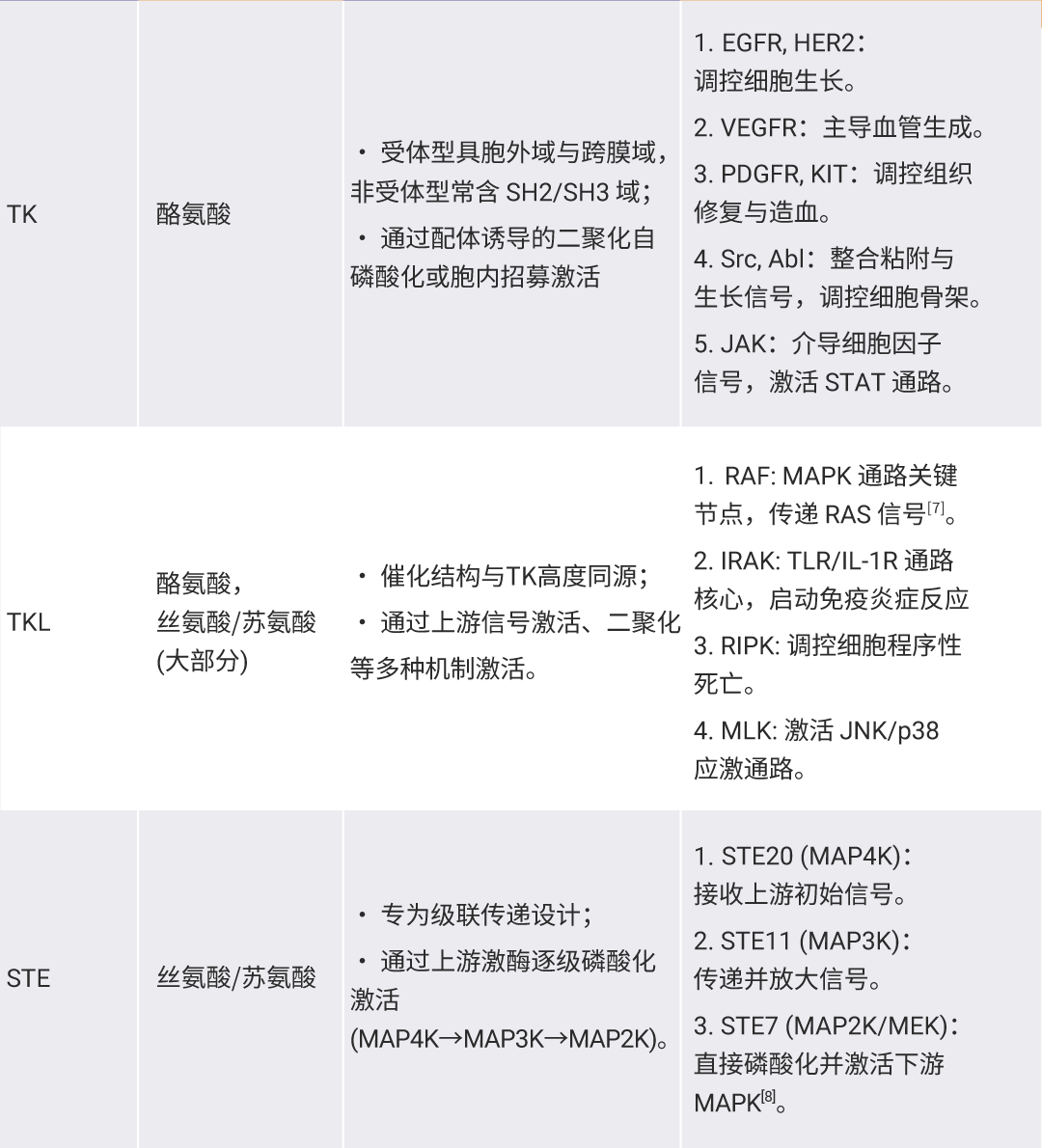
Section.02
激酶抑制剂
正因激酶的异常活化与重大疾病密切相关,针对它的靶向药物开发取得了空前成功。
激酶的分类不仅阐明其生物学功能,更直接指引了药物开发方向。2025 年 11 月 Nature Reviews Drug Discovery 期刊发文,FDA 批准了第 100 个小分子激酶抑制剂[18]。这标志着这类药物发展进入新阶段。
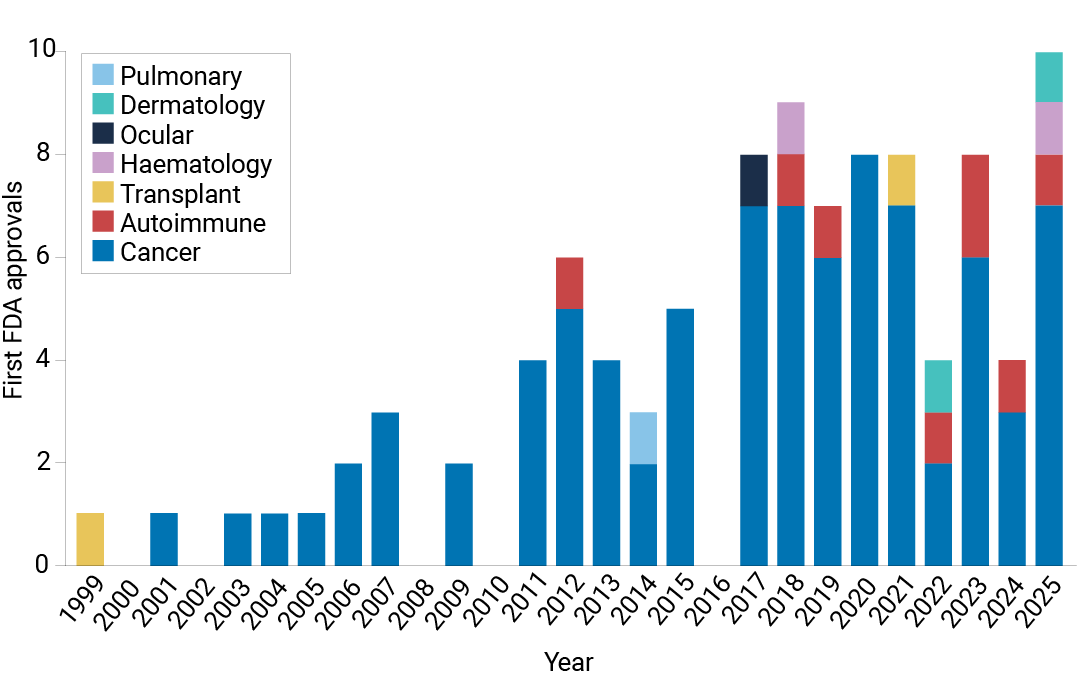
图 2. FDA 激酶抑制剂批准情况,按年份和治疗领域划分[18]。
如何查询最权威的实时信息?
1. 美国 FDA 官方数据库 (Drugs@FDA):可使用“激酶抑制剂”等关键词进行搜索。
2. 专业统计机构:如 Blue Ridge Institute for Medical Research (BRIMR) 网站,会定期更新并列出所有获批的蛋白激酶抑制剂清单。
根据统计分析,这些药物的靶点分布呈现出明显集中的特点,主要集中在少数几个关键的激酶家族上[19]。
表3. 获批激酶抑制剂的靶点分布[19]。
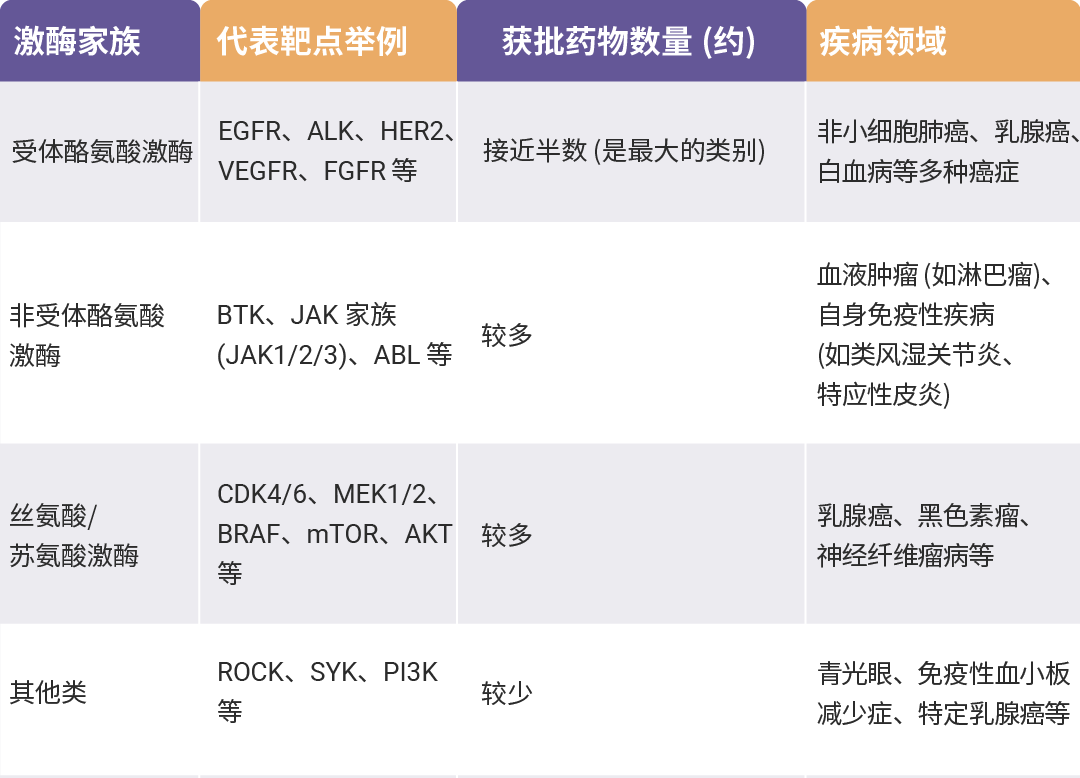
总的来说,已获批激酶抑制剂的靶点分布高度集中于驱动癌症和自身免疫性疾病的关键信号通路上,尤其是酪氨酸激酶家族。
MCE 相关产品
一、主要激酶家族的重组蛋白:含常见突变体如 EGFR L858R/T790M/C797S、预复合物形式如 CDK4-CCND1 等。
二、激酶系列化合物库及激酶谱筛选服务: 可一站式支持您从靶点验证、苗头化合物发现到抑制剂活性与选择性优化的全流程研究,助力加速激酶靶向药物的研发与转化。
三、激酶大环虚拟化合物库,可供虚拟筛选以及定制合成。由于大环的半刚性结构可限制构象与提升亲和力以及优化药代动力学性质,大环化策略是激酶抑制剂优化的理想手段。
产品推荐
表皮生长因子受体,激活后可启动 RAS/MAPK 与 PI3K/AKT 等多条下游通路,是调控细胞增殖、存活与迁移的核心分子。
糖原合成酶激酶-3β,是 Wnt 信号通路的关键负调控因子,广泛参与代谢、发育、细胞周期及神经功能的调节。
Polo 样激酶 1,是有丝分裂进程的核心调控者,对中心体成熟、纺锤体组装和胞质分裂至关重要。
细胞外信号调节激酶 2,是 RAS-MAPK 信号通路的终端效应激酶,主要响应生长信号,促进细胞增殖与存活。
TGFBR1/ALK-5, Human (HY-P74522)
TGF-β I 型受体,是 TGF-β/SMAD 信号通路的门户,在细胞分化、免疫调节及纤维化过程中发挥核心作用。
CaMKII alpha/CAMK2A, Human (HY-P76761)
钙/钙调蛋白依赖性激酶 II α,是解码钙信号并产生“分子记忆”的关键酶,为神经可塑性及心脏功能所必需。
激酶大环虚拟化合物库/Kinase Macrocyclic Compound Virtual Library (HY-L932V0)
收集上千个已报道的上市或进入临床的激酶抑制剂,以这些激酶片段作为起始片段,进行环化生成,通过可合成性以及理化性质评估,最终构建百万级的大环虚拟化合物库,可用于靶向激酶类靶点的虚拟筛选和AI筛选
参考文献
[1] Manning G, et al. The protein kinase complement of the human genome. Science. 2002 Dec 6;298(5600):1912-34.
[2] Arter C, et al. Structural features of the protein kinase domain and targeted binding by small-molecule inhibitors. J Biol Chem. 2022 Aug;298(8):102247.
[3] Knighton DR, et al. Crystal structure of the catalytic subunit of cyclic adenosine monophosphate-dependent protein kinase. Science. 1991 Jul 26;253(5018):407-14.
[4] Wang B, et al. An overview of kinase downregulators and recent advances in discovery approaches. Signal Transduct Target Ther. 2021 Dec 20;6(1):423.
[5] Duong-Ly KC, et al. The human kinome and kinase inhibition. Curr Protoc Pharmacol. 2013 Mar;Chapter 2:Unit2.9.
[6] Kanev GK, et al. The Landscape of Atypical and Eukaryotic Protein Kinases. Trends Pharmacol Sci. 2019 Nov;40(11):818-832.
[7] Jeon H, et al. Signaling from RAS to RAF: The Molecules and Their Mechanisms. Annu Rev Biochem. 2024 Aug;93(1):289-316.
[8] Morrison DK, et al. Protein kinases and phosphatases in the Drosophila genome. J Cell Biol. 2000 Jul 24;150(2):F57-62.
[9] McKay RM, et al. The casein kinase I family in Wnt signaling. Dev Biol. 2001 Jul 15;235(2):388-96.
[10] Arencibia JM, et al. AGC protein kinases: from structural mechanism of regulation to allosteric drug development for the treatment of human diseases. Biochim Biophys Acta. 2013 Jul;1834(7):1302-21.
[11] Takemoto-Kimura S, et al. Calmodulin kinases: essential regulators in health and disease. J Neurochem. 2017 Jun;141(6):808-818.
[12] Trefts E, et al. AMPK: restoring metabolic homeostasis over space and time. Mol Cell. 2021 Sep 16;81(18):3677-3690.
[13] Cargnello M, et al. Activation and function of the MAPKs and their substrates, the MAPK-activated protein kinases. Microbiol Mol Biol Rev. 2011 Mar;75(1):50-83.
[14] Sangaralingham SJ, et al. Natriuretic peptide pathways in heart failure: further therapeutic possibilities. Cardiovasc Res. 2023 Feb 3;118(18):3416-3433.
[15] Potter LR. Phosphorylation-Dependent Regulation of Guanylyl Cyclase (GC)-A and Other Membrane GC Receptors. Endocr Rev. 2024 Sep 12;45(5):755-771.
[16] Bose A, et al. The pseudokinase domain in receptor guanylyl cyclases. Methods Enzymol. 2022;667:535-574.
[17] Gong GQ, et al. Making PI3K superfamily enzymes run faster. Adv Biol Regul. 2025 Jan;95:101060.
[18] Mullard A. FDA approves 100th small-molecule kinase inhibitor. Nat Rev Drug Discov. 2025 Dec;24(12):891-895.
[19] Roskoski R Jr. Properties of FDA-approved small molecule protein kinase inhibitors: A 2025 update. Pharmacol Res. 2025 Jun;216:107723.

https://blog.sciencenet.cn/blog-3536222-1531521.html
上一篇:Nature 重磅 | 地塞米松——"老药新用"的便捷之路_MCE (MedChemExpress)