博文
免疫组织化学 (IHC) 常用的肿瘤标志物抗体_MCE 中国
|
Section.01
肺癌标志物
PD-L1
PD-L1——免疫检查点分子,属于 B7-CD28 免疫调节超家族。
定位:细胞膜。
功能:PD-L1 是一种跨膜蛋白。其主要生理功能是在免疫突触中与免疫 T 细胞表面的 PD-1 受体结合,传递抑制性信号,通过抑制 T 细胞活化和增殖来发挥作用。
肿瘤细胞或肿瘤微环境中的免疫细胞会高表达 PD-L1,与浸润 T 细胞的 PD-1 结合,从而“关停” T 细胞的杀伤功能,实现免疫逃逸。在非小细胞肺癌中,PD-L1 的表达水平是预测免疫检查点抑制剂疗效的关键生物标志物[1]。
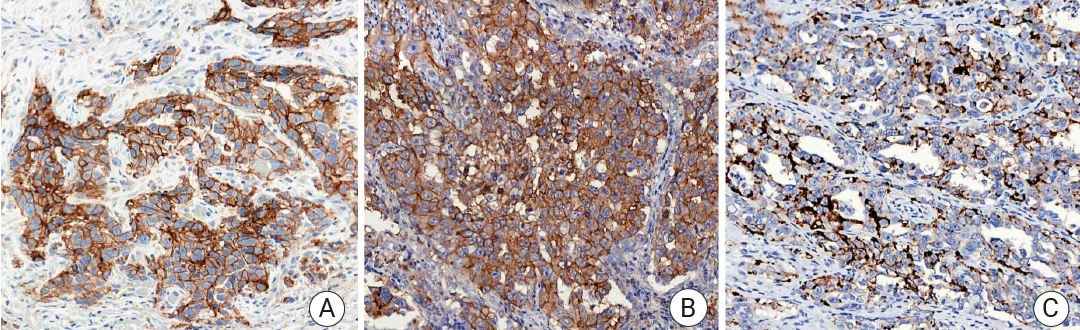
图 1. 人肺癌组织的 PD-L1 免疫组化分析[2]。
TTF-1
TTF-1——甲状腺转录因子-1,属于 NKX2 转录因子家族。
定位:细胞核。
功能:TTF-1 是调控肺组织和甲状腺器官特异性基因表达的核转录因子,对肺泡上皮细胞的终末分化和表面活性物质的分泌至关重要。
TTF-1 是关键的核转录因子,表达具有高度组织特异性。它在肺腺癌和甲状腺癌中高表达,是诊断这些原发癌的核心标志物[3]。其临床价值在于鉴别转移癌的原发部位:若 TTF-1 阳性,强烈提示肿瘤来源于肺或甲状腺。值得注意的是,肺鳞癌中 TTF-1 通常为阴性,需结合其他标志物来进一步确认[4]。
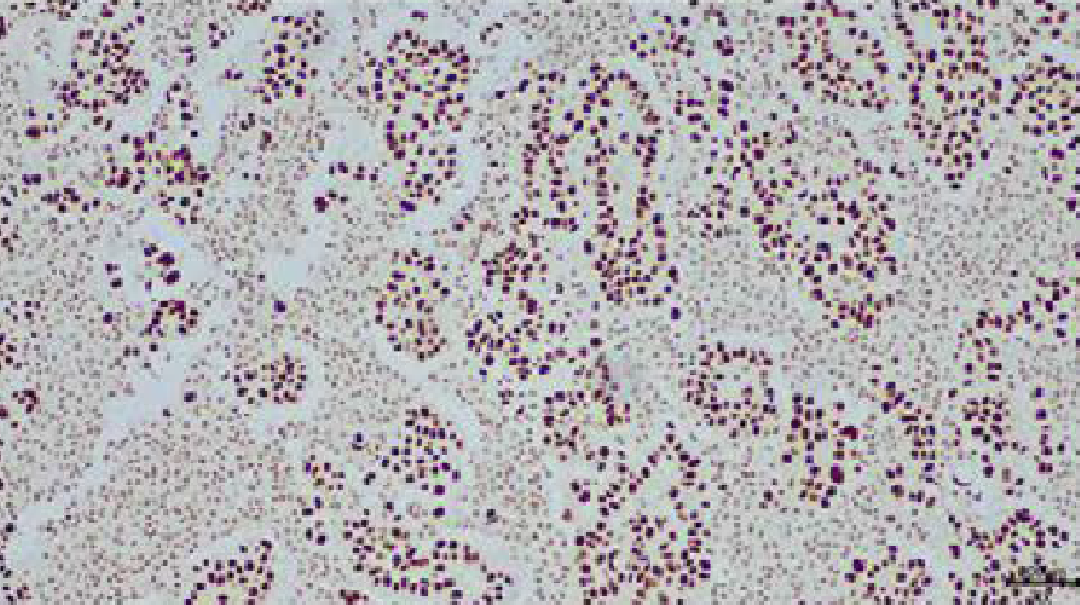
图 2.人肺癌组织的 TTF-1 免疫组化分析[5]。
MET
MET——MET 基因是定位在人类第 7 号染色体上的一个原癌基因,其编码生成的 c-Met 蛋白属于受体酪氨酸激酶家族。
定位:细胞膜。
功能:MET 是肝细胞生长因子 (HGF) 的受体。正常的 HGF/MET 信号通路精密调控胚胎发育、组织再生和损伤修复过程中的细胞增殖、分化和迁移。
在肺癌中,MET 可通过基因扩增、蛋白过表达或 14 号外显子 (METex14) 跳跃突变等方式异常激活,导致下游促生长和生存信号通路持续活化,驱动肺癌的生长、存活和转移。MET 扩增/过表达是 EGFR 靶向治疗获得性耐药的重要机制之一[6]。
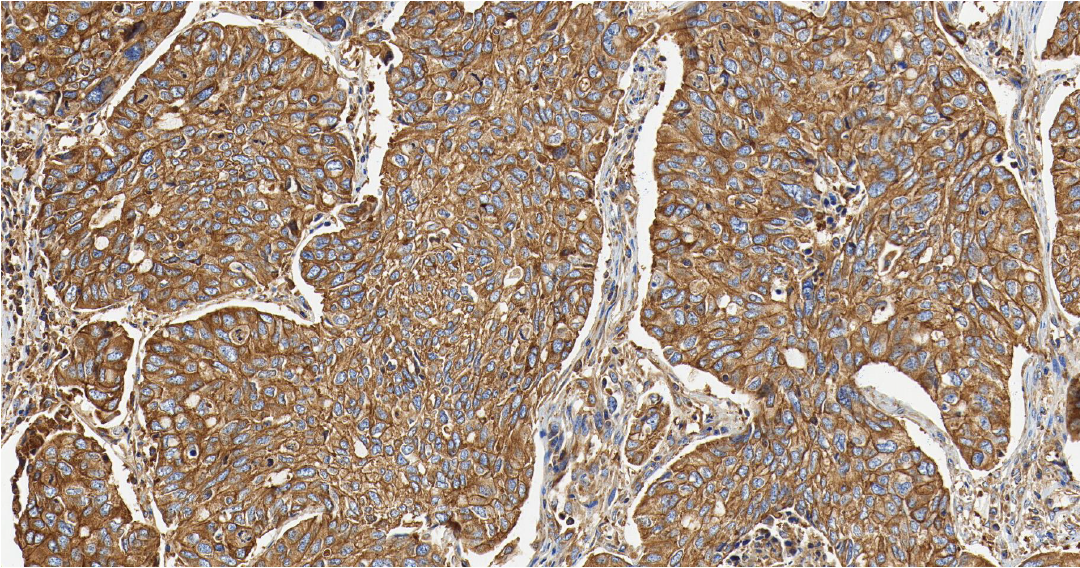
Section.02
乳腺癌标志物
ERα
ERα——雌激素受体,属于核激素受体超家族。
定位:细胞核。
功能:雌激素受体是一种位于细胞核内的配体依赖性转录因子。当雌激素与其结合后,受体被激活,进而调控与细胞增殖、分化相关的靶基因转录,主导女性第二性征发育,并参与月经周期中乳腺和子宫内膜的生理性变化。
Carol E DeSantis 等在 2019 年统计,雌激素受体 α 阳性 (ERα+) 乳腺癌占全球报告病例的 79%[7]。这类癌细胞的生长高度依赖雌激素信号通路。ER 阳性状态是乳腺癌预后相对较好的重要指标,也是选择内分泌治疗的直接靶点。
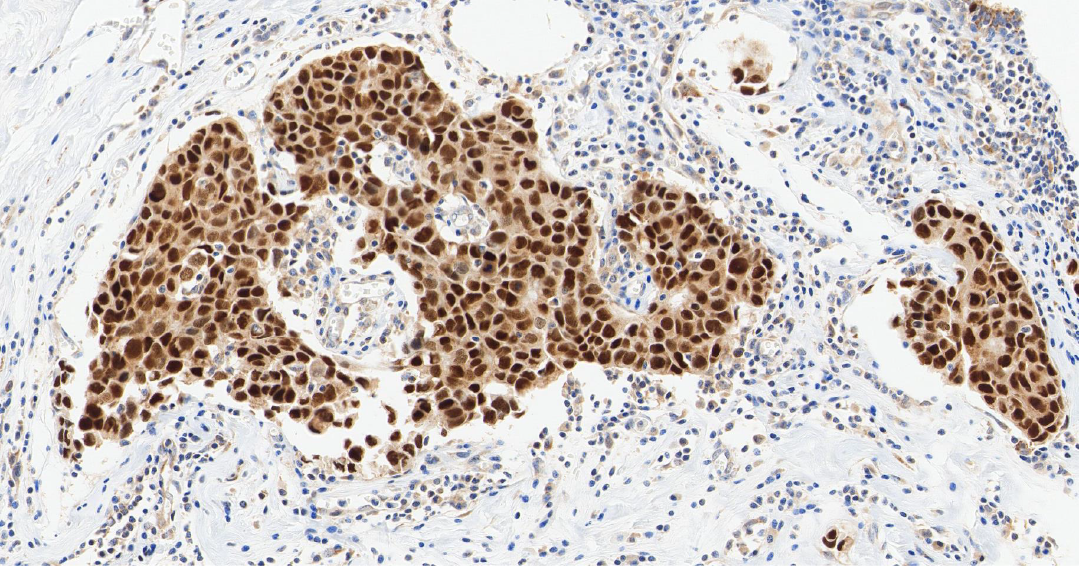
PR
PR——孕激素受体,属于核激素受体超家族。
定位:细胞核。
功能:孕激素受体是一种核内转录因子,当与孕激素结合后,主要调控子宫内膜向分泌期转化及平衡雌激素驱动的乳腺增生。
PR 表达依赖完整 ER 信号通路。在 ER 阳性的乳腺癌中,PR 阳性进一步证实了激素信号通路的活跃性,是预测内分泌治疗反应性的重要辅助指标,通常与更好的预后和更高的内分泌治疗有效率相关[8]。
Section.05
小结
好啦,今天关于肿瘤标志物就先介绍到这里了~MCE 提供大量肿瘤标志物抗体,快来 MCE 官网挑选你心仪的抗体吧!点击直达官网。
小伙伴还需要注意:每一个肿瘤标志物,都不是孤立的“判决书”,一定要结合多种检测指标联合判断,才能更准确。
产品推荐
PD-L1 Antibody (YA4674)(HY-P84982)
兔来源、无偶联标记、抗 PD-L1 的 IgG 单克隆抗体。
Estrogen Receptor alpha Antibody (YA450)(HY-P80663)
兔来源、无偶联标记、抗 Estrogen Receptor alpha 的 IgG 单克隆抗体
CDX2 Antibody (YA3498)(HY-P80983)
兔来源、无偶联标记、抗 CDX2 的 IgG 单克隆抗体。
p63 Antibody (YA1531)(HY-P81786)
兔来源、无偶联标记、抗 p63 的 IgG 单克隆抗体。
FOLR1 Antibody (YA1099)(HY-P81354)
兔来源、无偶联标记、抗 FOLR1 的 IgG 单克隆抗体。
Smad4 Antibody (YA074)(HY-P80326)
兔来源、无偶联标记、抗 Smad4 的 IgG 单克隆抗体
参考文献
[1] Velcheti V, et al. Programmed death ligand-1 expression in non-small cell lung cancer. Lab Invest. 2014;94:107–116. [2] Kim H, et al. PD-L1 Testing in Non-small Cell Lung Cancer: Past, Present, and Future. J Pathol Transl Med. 2019 Jul;53(4):199-206. [3] Phelps C. A., et al. Roles of thyroid transcription factor 1 in lung cancer biology. Vitamins and Hormones . 2018;106:517–544.[4] Kaufmann O., et al. Thyroid transcription factor-1 is the superior immunohistochemical marker for pulmonary adenocarcinomas and large cell carcinomas compared to surfactant proteins A and B. Histopathology . 2000;36(1):8–16.[5] Sun J, et al. TTF-1 and p40 co-expressing non-small cell lung cancer with ERBB2 and TP53 gene mutations: A case report and review of the literature. Medicine (Baltimore). 2025 Feb 7;104(6):e41290. [6] uo R, et al. MET IHC Is a Poor Screen for MET Amplification or MET Exon 14 Mutations in Lung Adenocarcinomas: Data from a Tri-Institutional Cohort of the Lung Cancer Mutation Consortium. J Thorac Oncol. 2019 Sep;14(9):1666-1671.[7] DeSantis CE, et al. Breast cancer statistics, 2019. CA Cancer J Clin. 2019 Nov;69(6):438-451.[8] Valerie-Jeanne Bardou et al.Progesterone Receptor Status Significantly Improves Outcome Prediction Over Estrogen Receptor Status Alone for Adjuvant Endocrine Therapy in Two Large Breast Cancer Databases. J Clin Oncol 21, 1973-1979(2003).[9] Trenker R., et al. Structural Dynamics of the Active HER4 and HER2/HER4 Complexes Is Finely Tuned by Different Growth Factors and Glycosylation. Cold Spring Harbor Laboratory; Laurel Hollow, NY, USA: 2023.[10] Iqbal N., et al. Human Epidermal Growth Factor Receptor 2 (HER2) in Cancers: Overexpression and Therapeutic Implications. Mol. Biol. Int. 2014;2014:852748.[11] Cheng X. A Comprehensive Review of HER2 in Cancer Biology and Therapeutics. Genes (Basel). 2024 Jul 11;15(7):903.[12] Sun X, et al. Ki-67: more than a proliferation marker. Chromosoma. 2018 Jun;127(2):175-186.[13 ]S?rlie T, et al. Gene expression patterns of breast carcinomas distinguish tumor subclasses with clinical implications Proc Natl Acad Sci U S A. 2001;98:10869–74.[14] Sun, et al. AMPK improves gut epithelial differentiation and barrier function via regulating Cdx2 expression. Cell Death and Differentiation. 2017; 24:819-831[15] Badia-Ramentol J, et al. The prognostic potential of CDX2 in colorectal cancer: Harmonizing biology and clinical practice. Cancer Treat Rev. 2023 Dec;121:102643.[16] Roy SK, et al. SATB2 is a novel biomarker and therapeutic target for cancer. J Cell Mol Med. 2020 Oct;24(19):11064-11069. [17] Sirni? P, et al. CDX2 and SATB2 loss are associated with myeloid cell infiltration and poor survival in colorectal cancer. Cancer Immunol Immunother. 2025 Feb 25;74(4):111. [18] Roy SK, et al. SATB2 is a novel biomarker and therapeutic target for cancer. J Cell Mol Med. 2020 Oct;24(19):11064-11069. [19] Ristau BT, et al. The prostate-specific membrane antigen: lessons and current clinical implications from 20 years of research. Urol Oncol. 2014;32(3):272–279. [20] Zou S, et al. Time point-independent tumor positivity of 68Ga-PSMA-PET/CT pre- and post-biopsy in high-risk prostate cancer. Ann Nucl Med. 2022 Jun;36(6):523-532.[21] Houshmand S, et al. PSMA PET imaging in the diagnosis and management of prostate cancer. Abdom Radiol (NY). 2023 Dec;48(12):3610-3623. [22] Singh V, et al. Diagnostic utility of p63 and α-methyl acyl CoA racemasein resolving suspicious foci in prostatic needle biopsy and transurethral resection of prostate specimens. J Can Res Ther. 2014;10:686–92. [23] Alinezhad S, et al. Global expression of AMACR transcripts predicts risk for prostate cancer - a systematic comparison of AMACR protein and mRNA expression in cancerous and noncancerous prostate. BMC Urol. 2016 Feb 29;16:10.
https://blog.sciencenet.cn/blog-3536222-1530687.html
上一篇:国自然, “人工智能×类器官“ 的双重Buff_MCE 中国
下一篇:病毒载体——慢病毒、腺病毒、AAV, 你的细胞实验该选谁_MCE(MedChemExpress)
全部作者的其他最新博文
- • SMAD6抗体是IgG1 单克隆抗体_MCE(MedChemExpress)
- • Glepaglutide,914009-86-2 是一种 GLP-2R 激动剂_MCE(MedChemExpress)
- • Fmoc-Gly-OH-13C2,15N,285978-13-4 用于化合物合成_MCE(MedChemExpress)
- • Trimethylamine oxide-15N是 Trimethylamine N-oxide 的氘代物_MCE
- • L-Histidine-13C6 hydrochloride,L-组氨酸 13C6 , 201740-88-7_MCE
- • Citric acid-13C3,柠檬酸-13C3诱导 HaCaT 细胞凋亡_MCE(MedChemExpress)