博文
Nature 重磅 | 地塞米松——"老药新用"的便捷之路_MCE (MedChemExpress)
|
Section.01
Nature 重磅:
首次揭示禁食抗癌核心机制
近期,Nature 杂志上发表了一项重磅研究,来自荷兰癌症研究所和意大利热那亚大学的研究团队首次揭示:禁食之所以能够增强乳腺癌内分泌治疗的疗效,核心在于激活了糖皮质激素受体 (GR)。更重要的是,他们证实临床常用的糖皮质激素药物——,完全可以替代禁食,产生同等的抗肿瘤效果[1]。这项研究不仅为"食疗抗癌"提供了分子机制解释,更为 HR+乳腺癌的联合治疗开辟了"老药新用"的便捷之路。

Section.02
GR 激活:
禁食增强疗效的分子开关
该研究的核心发现建立在系统的多组学分析基础之上。研究团队利用 MCF7 人源 HR+乳腺癌细胞系建立小鼠异种移植模型,采用每周 48 小时禁食联合 (Tamoxifen, TMX, 他莫昔芬是最常用的内分泌治疗药物之一) 的治疗方案,通过染色质免疫共沉淀测序 (ChIP-seq)、转录组测序 (RNA-seq)、蛋白质组学及免疫组织化学等技术,全面解析了禁食对肿瘤表观基因组和转录组的深刻影响。
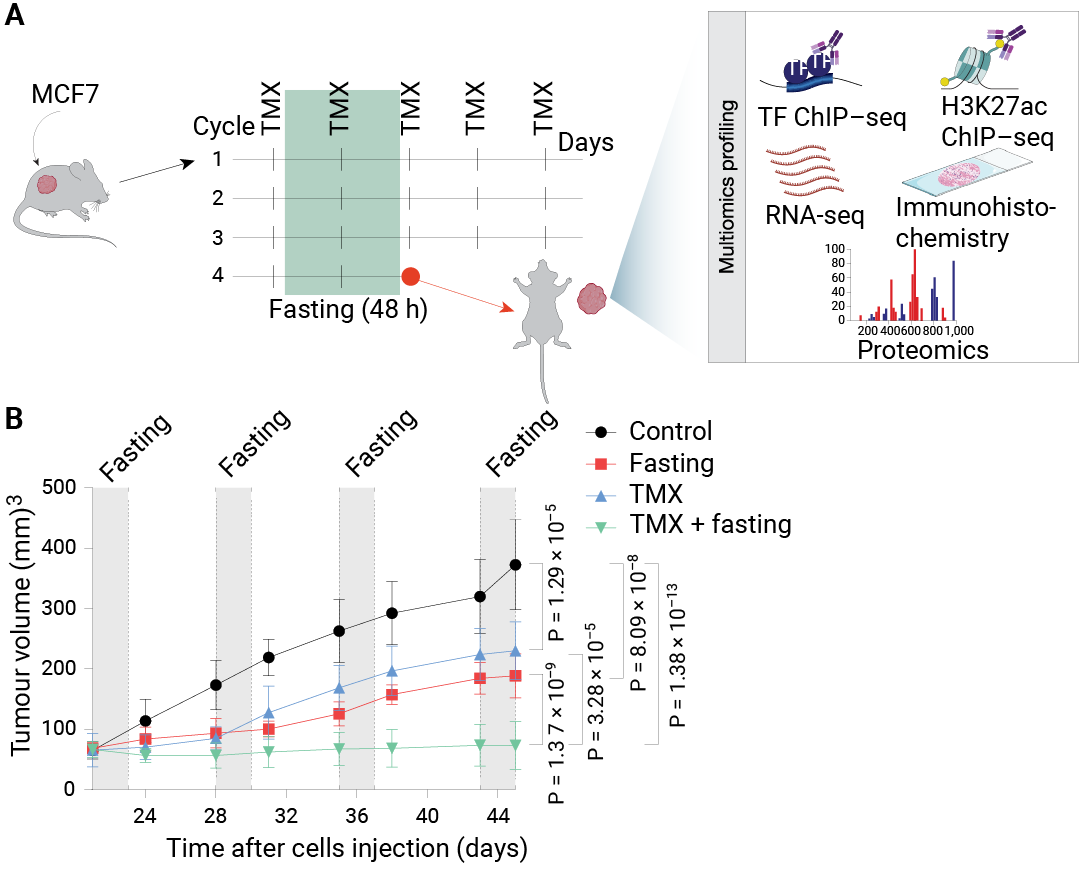
图 1. MCF7 异种移植小鼠治疗周期示意图 (A) 与 6-8 周龄雌性无胸腺裸鼠异种移植肿瘤生长情况 (B)[1]。
表观基因组重编程与转录因子转换是研究揭示的第一个关键机制。H3K27ac 作为活跃增强子/启动子的标志,其 ChIP-seq 分析显示,禁食联合 TMX 治疗导致了肿瘤表观基因组的广泛重编程。具体而言,禁食使 TMX 治疗下的肿瘤丧失了 289个 H3K27ac 富集区域,同时获得了 291 个新的 H3K27ac 位点。深入分析发现,丢失的 H3K27ac 位点显著富集于 AP-1 转录因子家族成员 (包括 FOSL2、JUN、FOSL1、FOS 和 JUND) 的结合 motif,这些转录因子已知能够促进乳腺癌细胞增殖和肿瘤生长。相反,新获得的 H3K27ac 区域则富集于类固醇激素受体 (Steroid Hormone Receptors, SHRs) 的结合位点,包括糖皮质激素受体 (GR) 、孕激素受体 (PR) 和雄激素受体 (AR)。
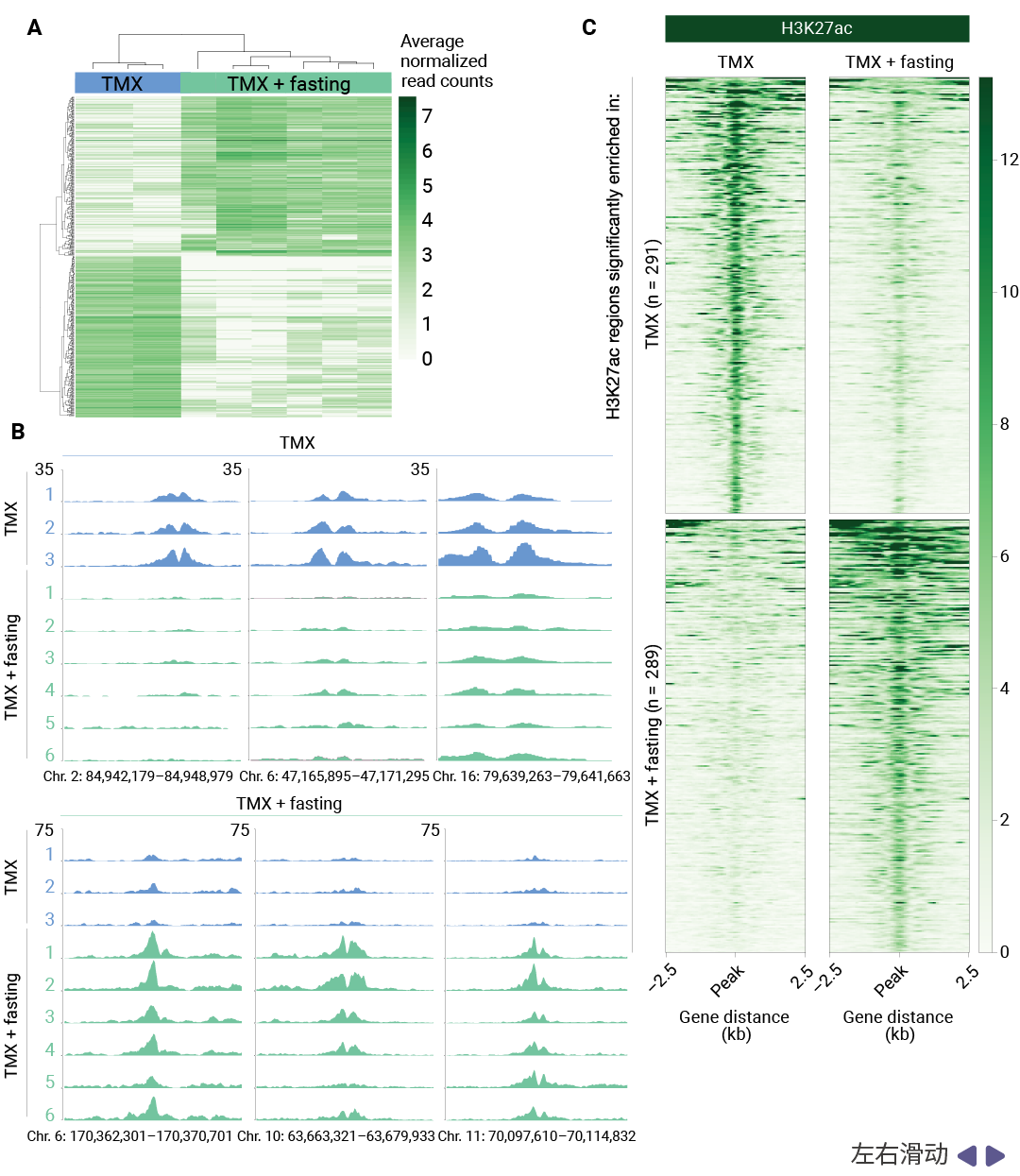
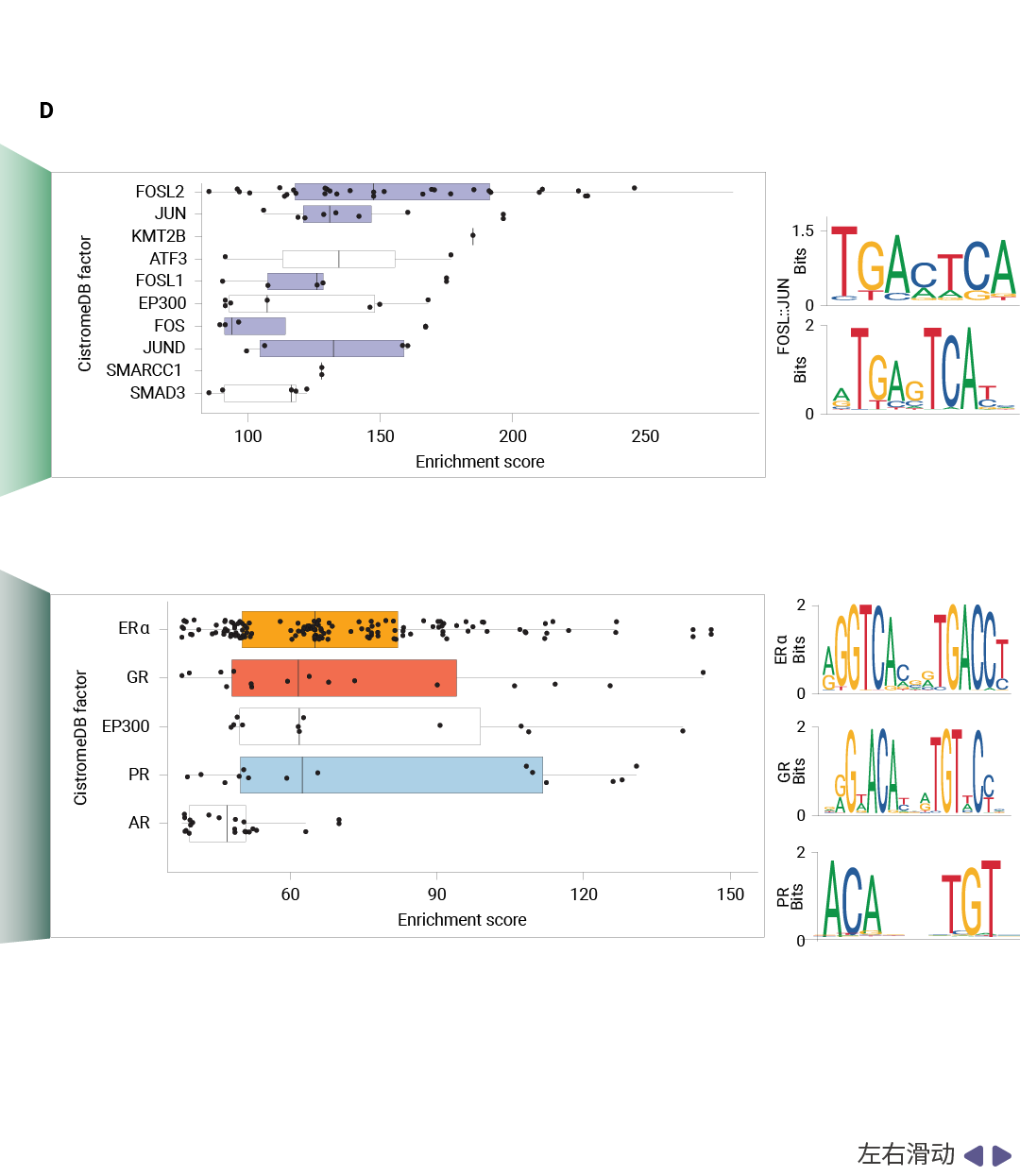
图 2. 禁食重编程癌症表观基因组[1]。
这一发现提示禁食可能通过"开关转换"机制调控肿瘤转录程序:一方面抑制促增殖的 AP-1 信号,另一方面激活具有肿瘤抑制功能的 SHRs 信号。免疫组化分析进一步证实,单独禁食或联合 TMX 均显著增加了 GR 的核定位,这是 GR 激活的典型标志,而 ERα 和 PR 的亚细胞定位则未受影响。ChIP-seq 实验直接证明了禁食诱导了 GR 和 PR 的染色质结合显著增强,而 JUN 在新获得的 H3K27ac 位点上并无 occupancy,说明禁食确实实现了从 AP-1 驱动到 GR/PR 驱动的转录程序转换。
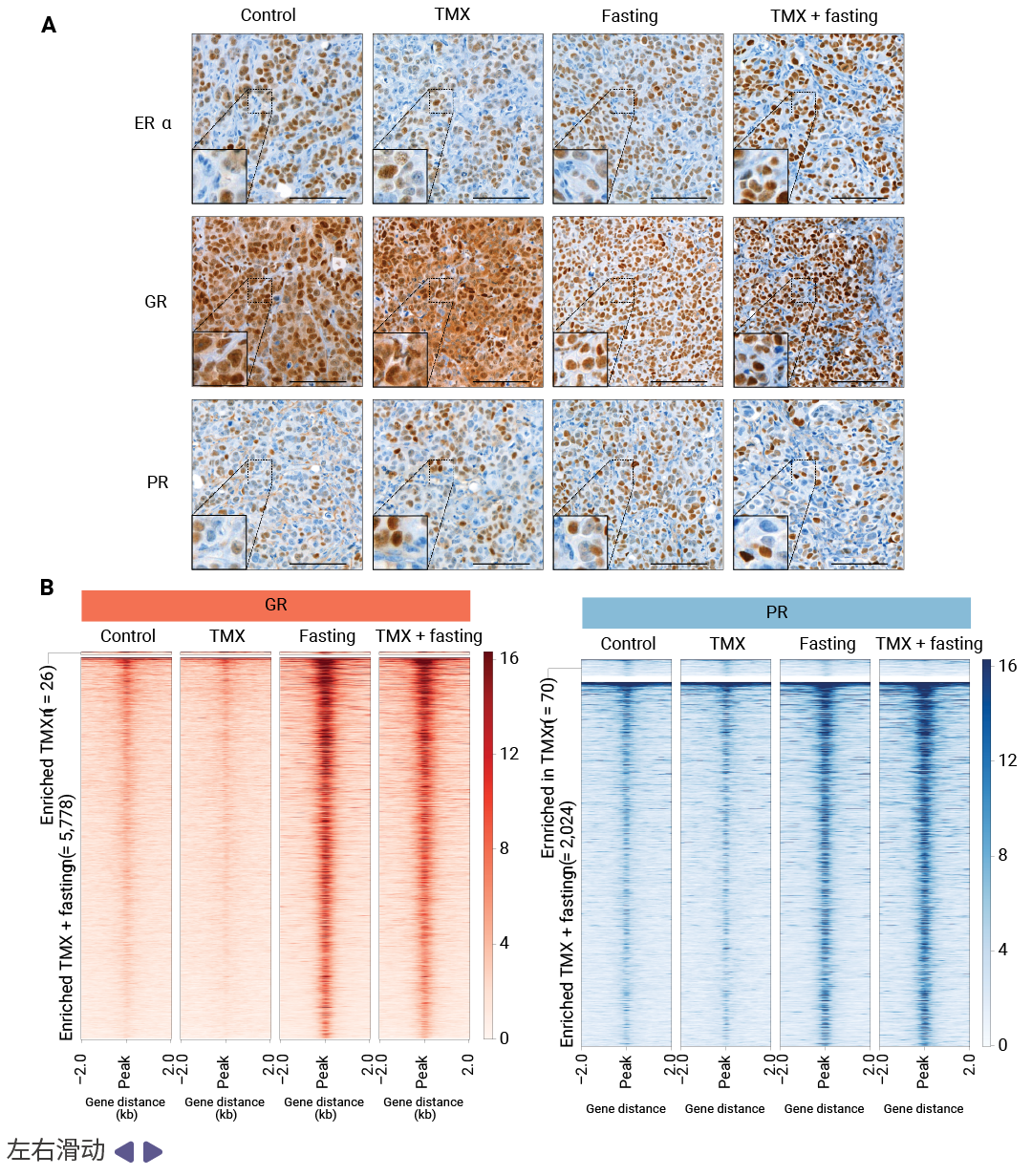
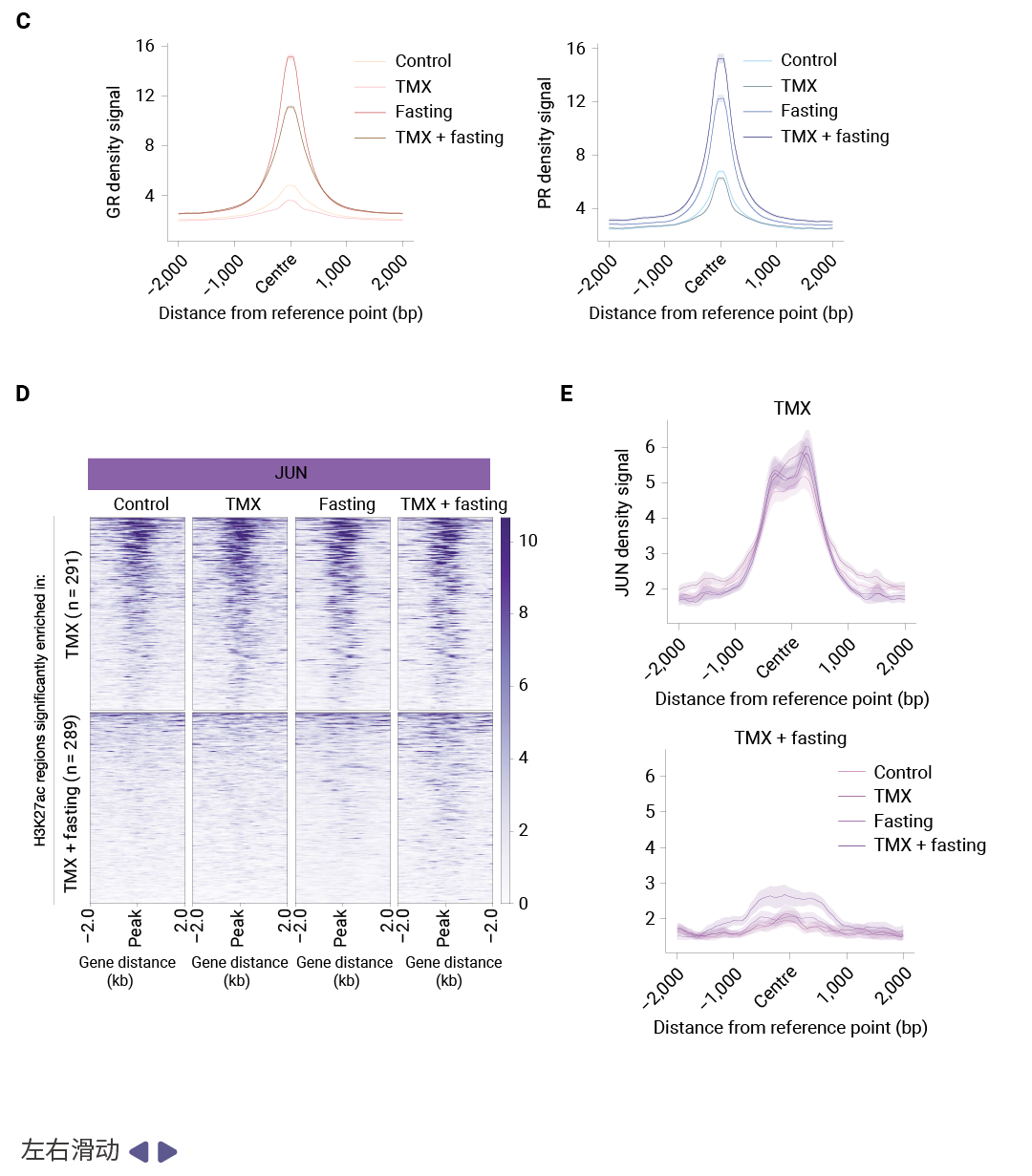
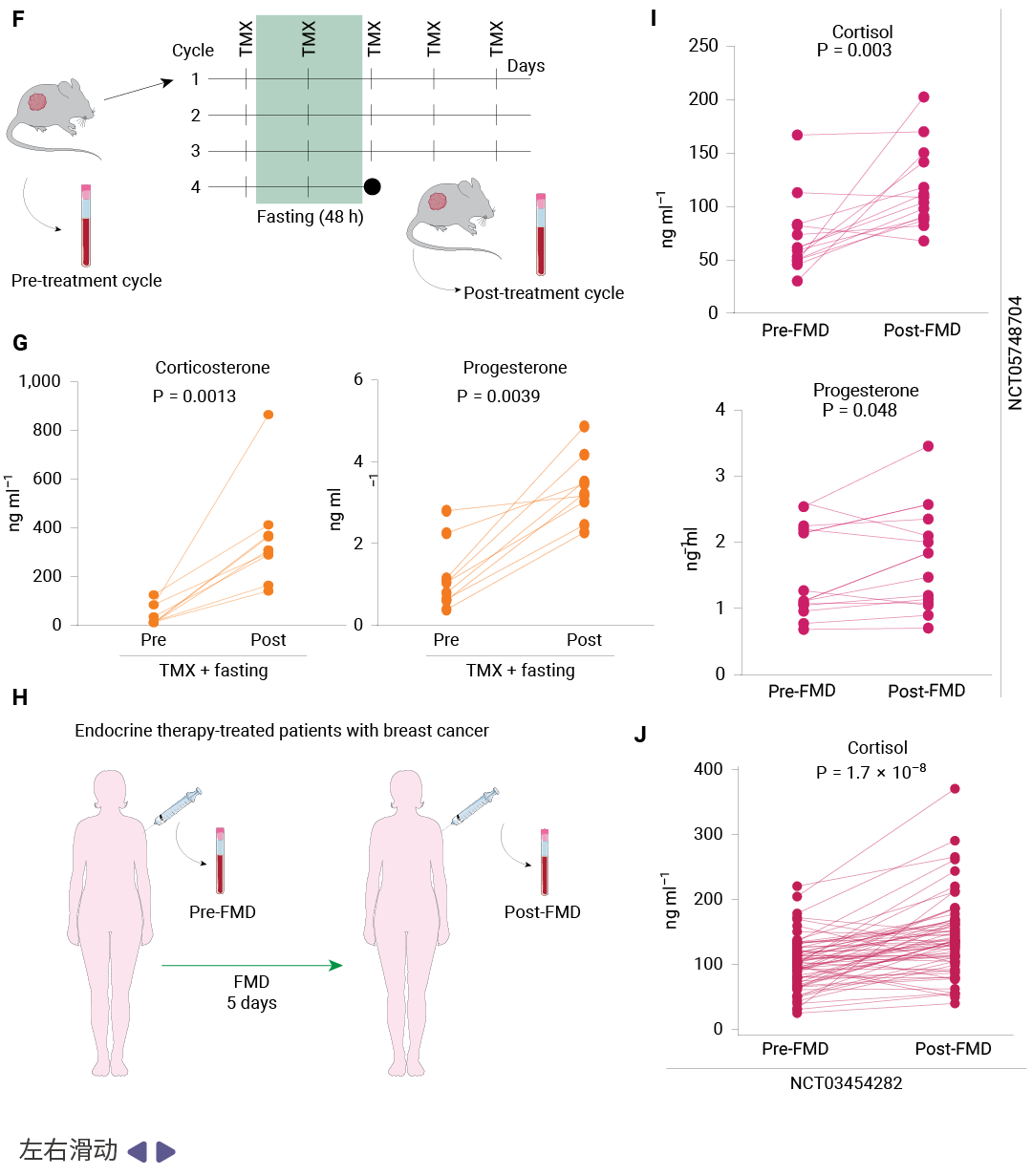
图 3. 禁食增强 GR 和 PR 染色质结合并降低 JUN 位点的增强子活性[3]。
GR 激活的转录程序与抗肿瘤效应是第二个关键发现。RNA-seq 分析显示,禁食联合 TMX 显著抑制了 MYC 靶基因和 E2F 靶基因等增殖相关通路,同时 mTOR 信号活性降低。研究团队利用泛癌适用的 GR 活性基因特征 (GR-activity signature) 分析发现,TMX 单独治疗实际上降低了 GR 转录活性,而禁食联合 TMX 则显著激活了 GR 驱动的基因表达程序。值得注意的是,转录抑制因子 ZBTB16 (又称 PLZF) 是禁食诱导上调的第二高表达基因,该基因已被报道介导 GR 的抗肿瘤效应。
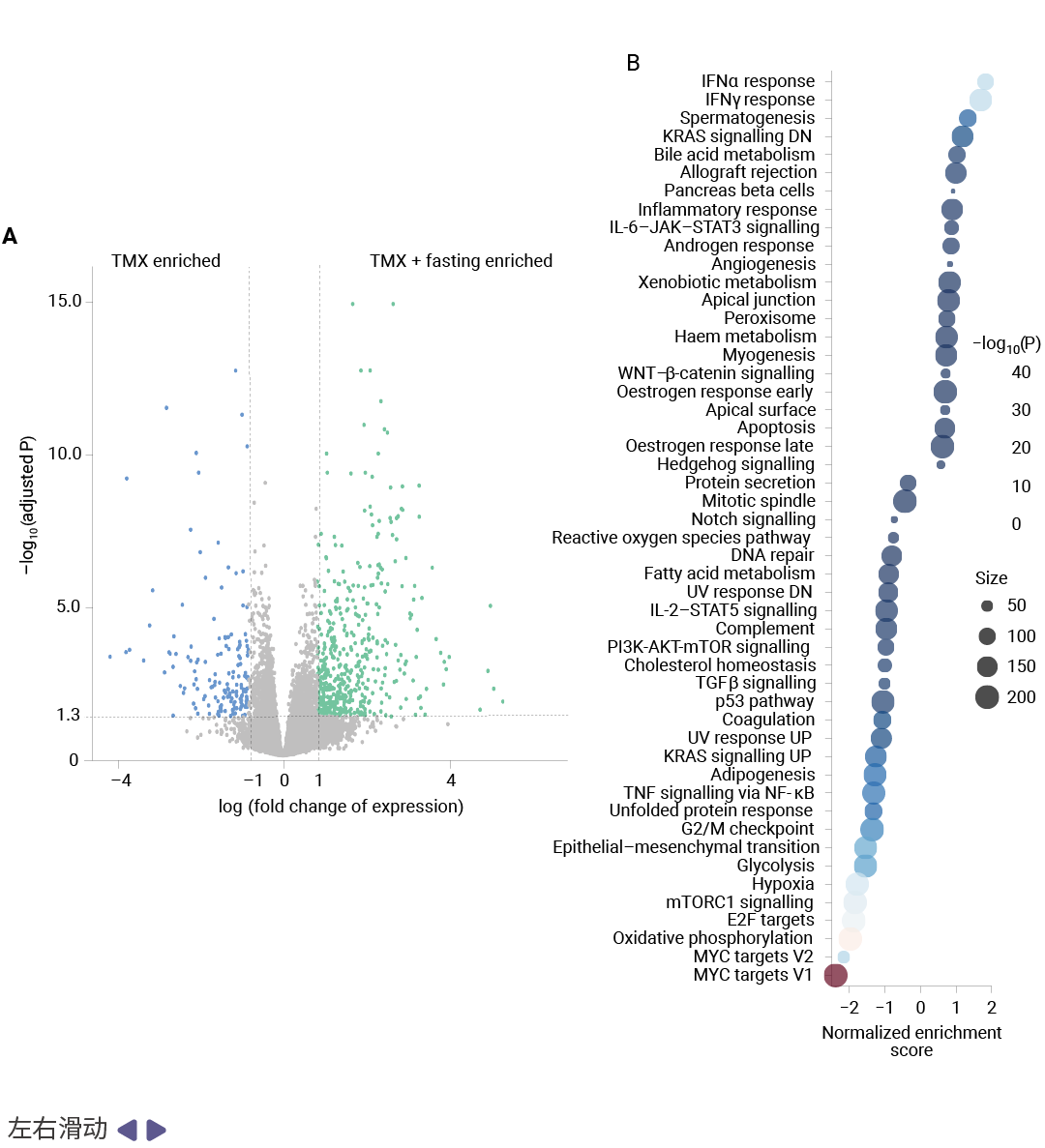
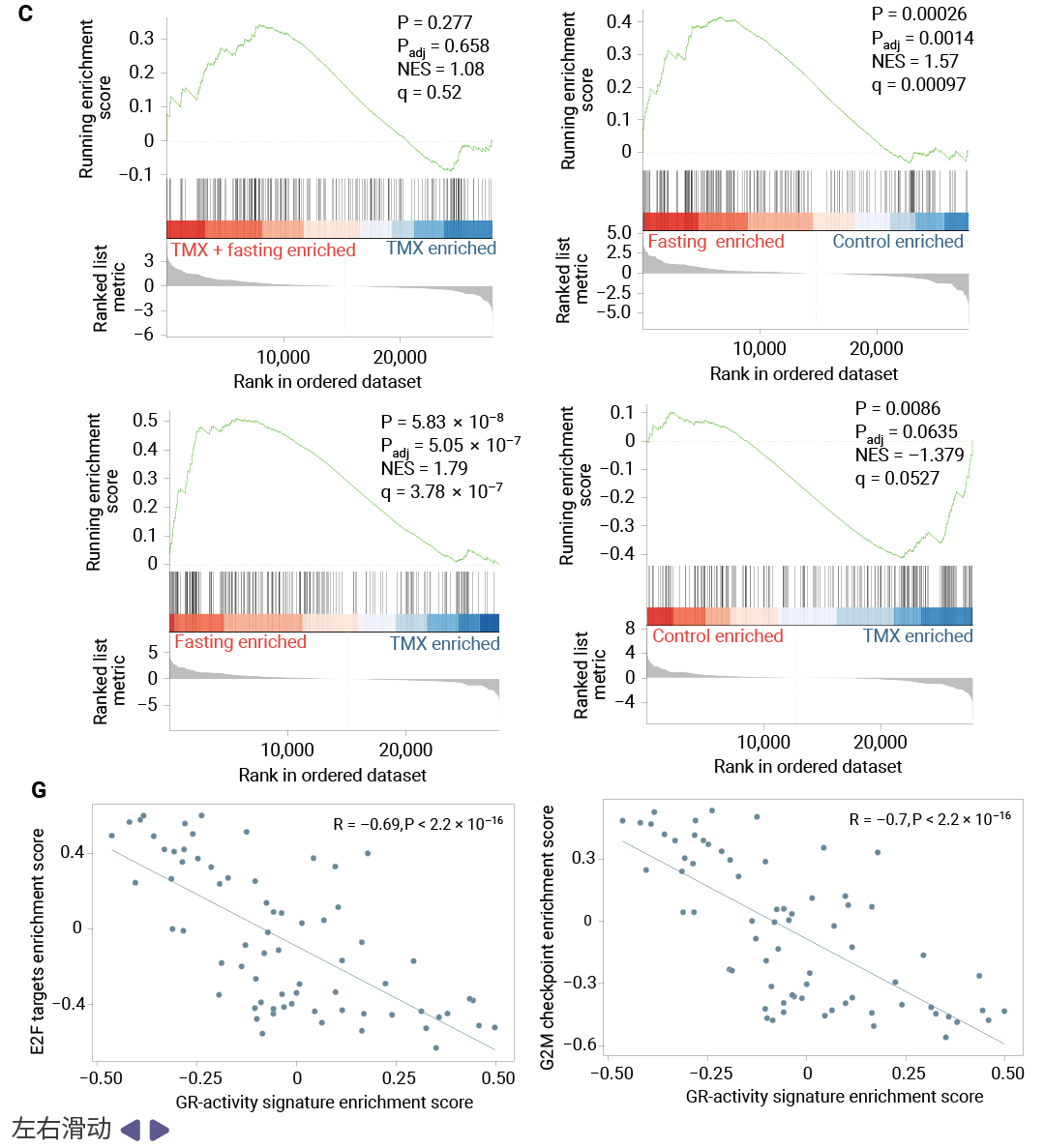
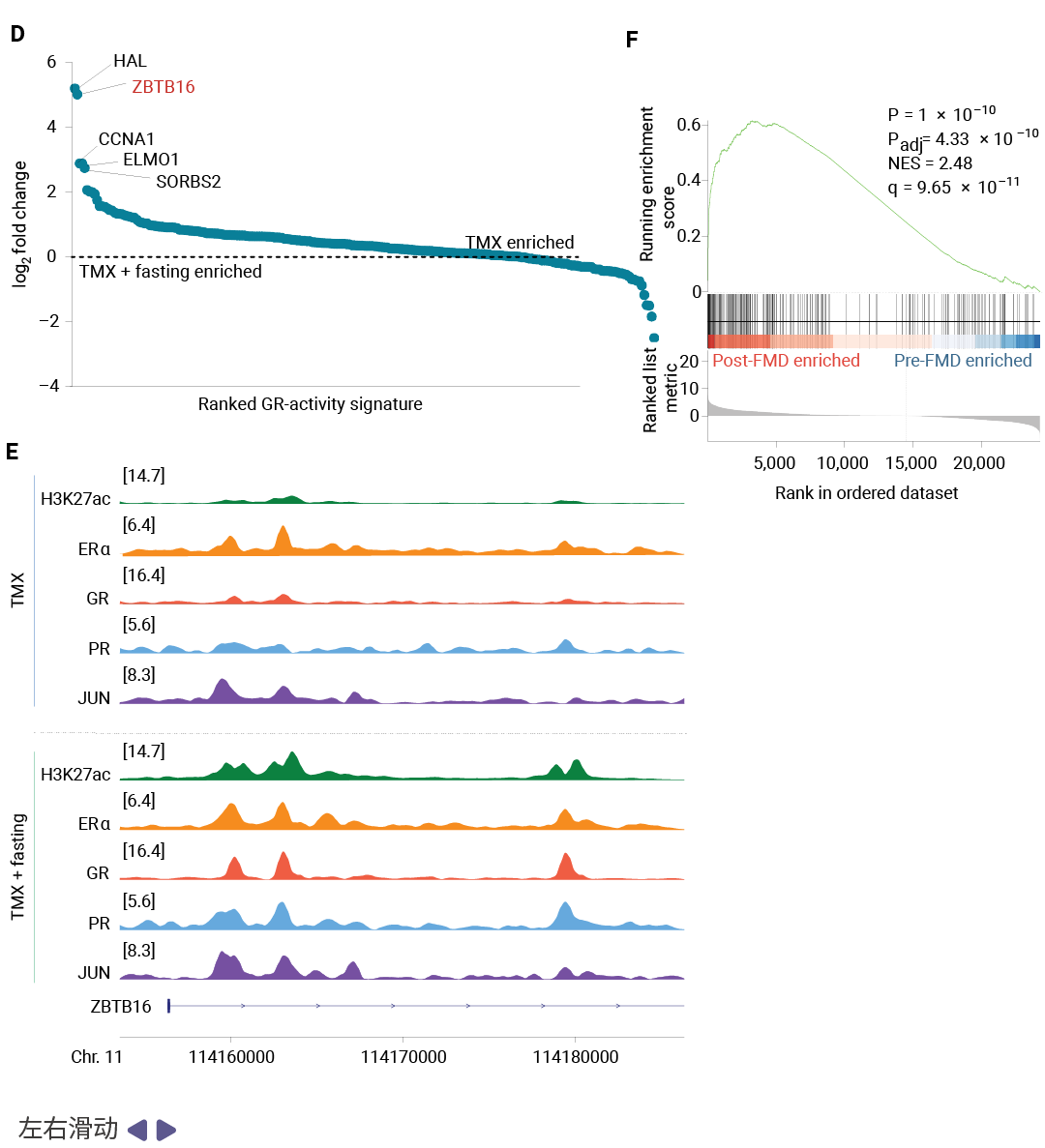
图 4. 禁食增强 GR 转录活性并增加转录抑制因子 ZBTB16 的表达[1]。
为验证 GR 在禁食增效中的必要性,研究团队利用 CRISPR-Cas9 技术构建了 GR 敲除 (GR-KO)的 MCF7 细胞。体内实验结果令人信服:在野生型 MCF7 移植瘤中,禁食联合TMX产生了协同抗肿瘤效应,肿瘤生长受到显著抑制;而在 GR-KO移植瘤中,这一协同效应完全消失,禁食不再能够增强 TMX 的疗效。这一遗传学证据确凿地证明了 GR 是禁食增强内分泌治疗疗效所必需的关键介质。
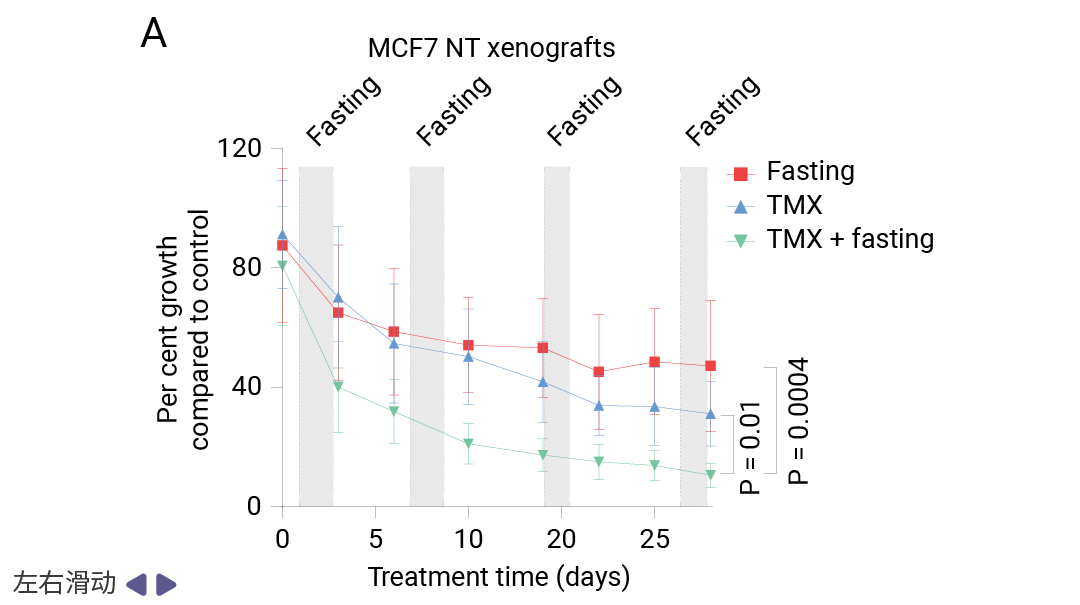
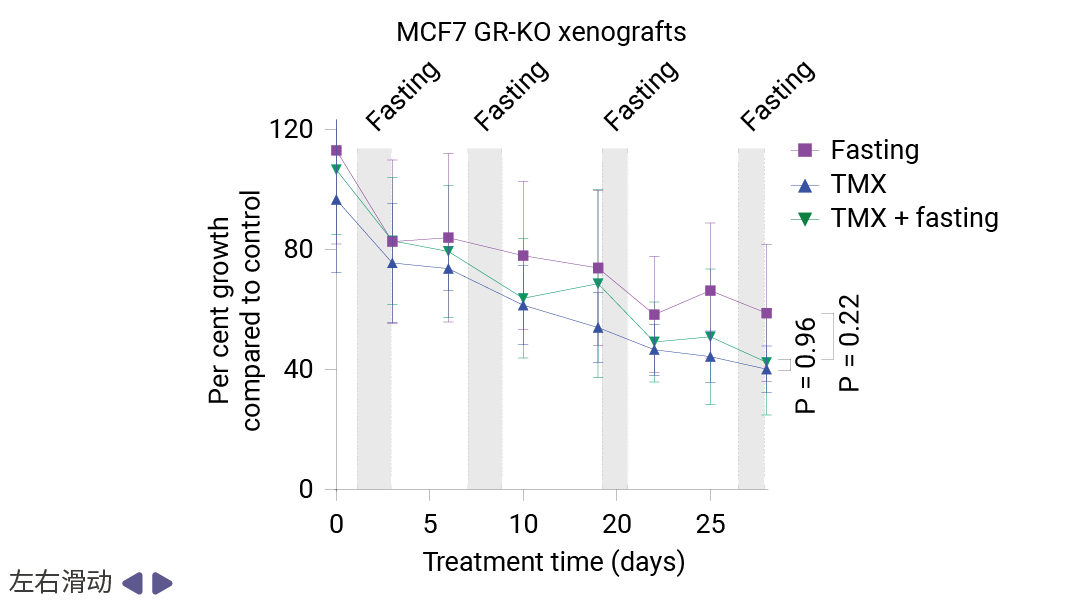
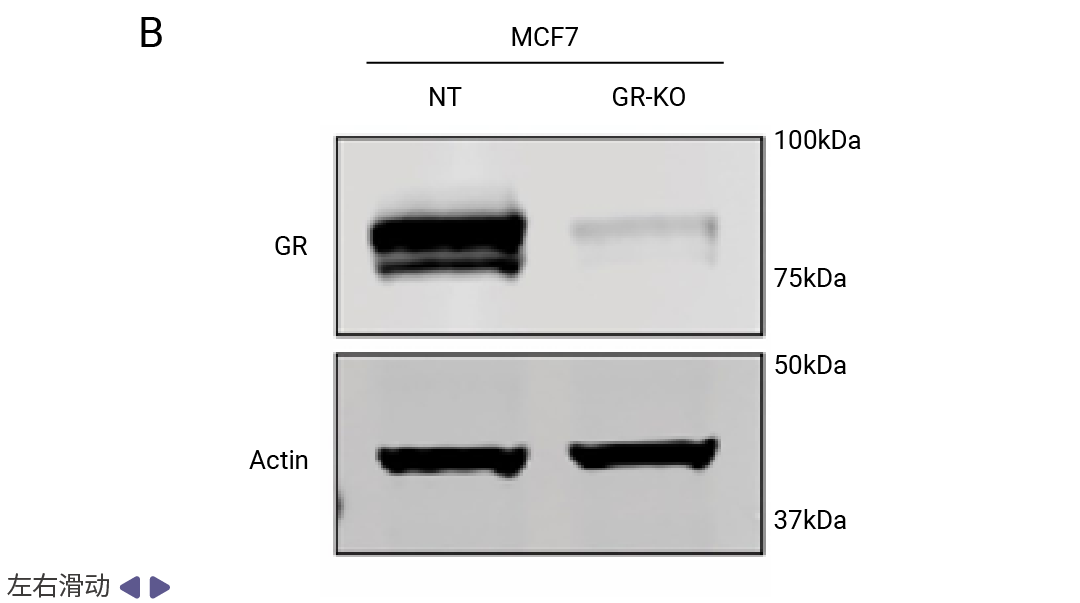
图 5. 非靶向对照 (NT) 或 GR 敲除 (GR-KO) MCF7 异种移植肿瘤在 6-8 周龄雌性无胸腺裸鼠中的生长 (A);NT (非靶向) 和 GR-KO MCF7 细胞中 GR 的蛋白质印迹 (B) [1]。
Section.03
地塞米松:
禁食的"替代者"
基于 GR 的核心作用,研究团队提出了一个具有重要临床意义的假设:外源性给予 GR 激动剂是否能够模拟禁食的抗肿瘤增效作用?为验证这一点,他们选择了临床广泛使用的合成糖皮质激素——地塞米松 (Dexamethasone, Dexa) 进行测试。
地塞米松完美复制禁食的抗肿瘤效应。在 MCF7 异种移植模型中,Dexa 单独使用对肿瘤生长影响有限,但与 TMX 联合使用时,其抗肿瘤活性与禁食联合 TMX 相当,均显著优于 TMX 单药治疗。更重要的是,禁食会导致小鼠体重明显下降,而Dexa 治疗组体重保持稳定,这一优势对于需要长期治疗的癌症患者尤为重要。该效应在第二种 HR+细胞系 T47D 以及患者来源的异种移植 (PDX) 模型 IDC186 中均得到验证,证明了策略的普适性、长期获益与免疫微环境调节。
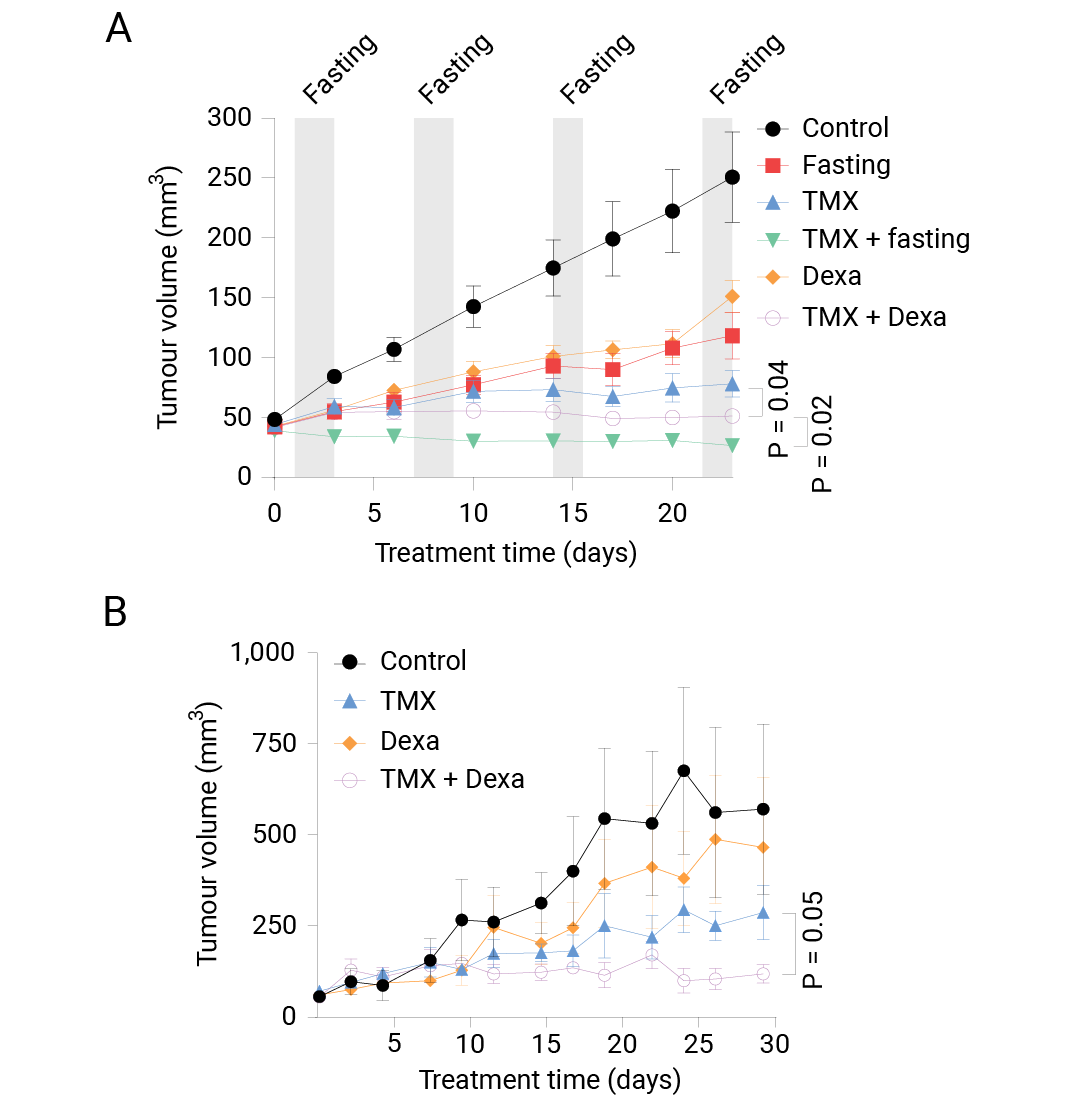
图 6. 6-8 周龄雌性无胸腺裸鼠不同治疗组中 MCF7 异种移植瘤的生长情况[1]。
(A) 与 6-8 周龄雌性 NSG 小鼠不同治疗组中 HR+乳腺癌患者来源异种移植瘤 (PDX) 的生长情况 (B) 。
研究还发现,为期一个月的 Dexa 联合 TMX 治疗在停药后仍能产生持续的"carry-over"抗肿瘤效应,肿瘤生长延迟时间较禁食或 TMX 单药延长两倍。在免疫健全的 TSAE1 同基因移植模型中,Dexa 联合 TMX 不仅显著抑制肿瘤生长,还延长了小鼠生存期。免疫表型分析显示,联合治疗降低了中性粒细胞、非经典单核细胞和树突状细胞表面的 PD-L1 表达,提示 Dexa 可能通过调节肿瘤免疫微环境发挥额外的抗肿瘤作用,且未引起明显的免疫抑制。
研究团队分析了两项临床试验的患者数据:NCT05748704 试验中,接受 FMD 联合内分泌治疗的乳腺癌患者血清皮质醇和孕激素水平显著升高;NCT03454282 (DigesT 研究) 的肿瘤样本 RNA-seq 分析显示,FMD 后 GR 活性特征评分显著升高,且与 E2F 靶点和 G2M 检查点等增殖标志物呈负相关。这些临床数据与动物模型发现高度一致,证实了 GR 激活在人体内的相关性。
该研究的临床转化价值在于:地塞米松作为已上市数十年的老药,其药代动力学、安全性和给药方案已非常明确,可直接进入临床试验验证,无需漫长的药物开发周期。研究团队指出,鉴于 GR 激动剂在三阴性乳腺癌中可能促进转移,未来临床试验应严格筛选 HR+ 乳腺癌患者,并参考 PIONEER 试验 (NCT03306472) 中 PR 激动剂的评估经验,设计合理的给药剂量和时间方案。
产品推荐
Tamoxifen 是一种口服有效的,选择性雌激素受体调节剂,可阻断乳腺细胞中的雌激素作用,并可激活其他细胞如骨骼,肝脏和子宫细胞中的雌激素活性。
4-Hydroxytamoxifen 是一种口服有效,选择性的雌激素受体调节剂,也是 Tamoxifen (HY-13757A) 在体内的活性代谢形式,可用于诱导 CreER 转基因小鼠的基因敲除。
Dexamethasone 是糖皮质激素受体 (glucocorticoid receptor) 激动剂、凋亡诱导剂、以及常见的实验动物的疾病诱导剂,可构建肌肉萎缩、高血压和抑郁模型。
SR 11302 是激活蛋白-1 (AP-1) 转录因子抑制剂。SR 11302 是一种类视黄醇,可特异性抑制 AP-1 活性,而不会激活视黄酸反应元件 (RARE) 的转录。
参考文献
[1] Padr?o N, et al. Fasting boosts breast cancer therapy efficacy via glucocorticoid activation. Nature. 2026 Jan;649(8098):1013-1021.

https://blog.sciencenet.cn/blog-3536222-1531435.html
上一篇:ZBP1 降解新工具!南开大学团队开发共价 PROTAC_MCE(MedChemExpress)