博文
Cells:NF-κB作为中枢神经系统炎症的可诱导调节因子
||
NF-κB (nuclear factor K-light-chain-enhancer of activated B cells) 转录因子家族是调控免疫介导炎症反应的核心因子。2024年发表于Cells的一篇综述“NF-κB as an Inducible Regulator of Inflammation in the Central Nervous System”系统总结了NF-κB在中枢神经系统不同细胞类型中的功能差异及其在神经炎症性疾病中的作用机制。
主要内容
NF-κB信号通路概述
NF-κB家族由 15 个已知的同源或异源二聚体组成,这些二聚体来源于五个蛋白质亚基:p65 (RelA)、c-Rel、RelB、p50/p105 (NF-κB1) 和 p52/p100 (NF-κB2)。NF-κB激活可分为经典与非经典两条通路,如图1所示。
经典通路:响应急性炎症刺激快速激活,介导先天免疫。激活信号包括细菌或病毒产物 (例如脂多糖或病毒蛋白)、炎症细胞因子 (主要是 TNFα、IL-1 和 IL-6)以及物理或化学应激。信号经TAK1汇聚后激活IKK复合物,后者磷酸化IκBα使其被泛素化后降解,释放NF-κB转位至核内,启动炎症相关基因转录。
非经典通路:反应缓慢持久,介导适应性免疫,参与淋巴器官发生及B细胞分化。由特定TNFR家族成员 (CD40、RANKL等) 触发,激活NIK进而磷酸化IKKα。该通路依赖p100加工:p100被IKKα磷酸化后泛素化降解,此时激活的NF-κB2 (包含p52、RelB亚基) 转位入核,调控炎症、细胞存活及免疫发育相关基因。
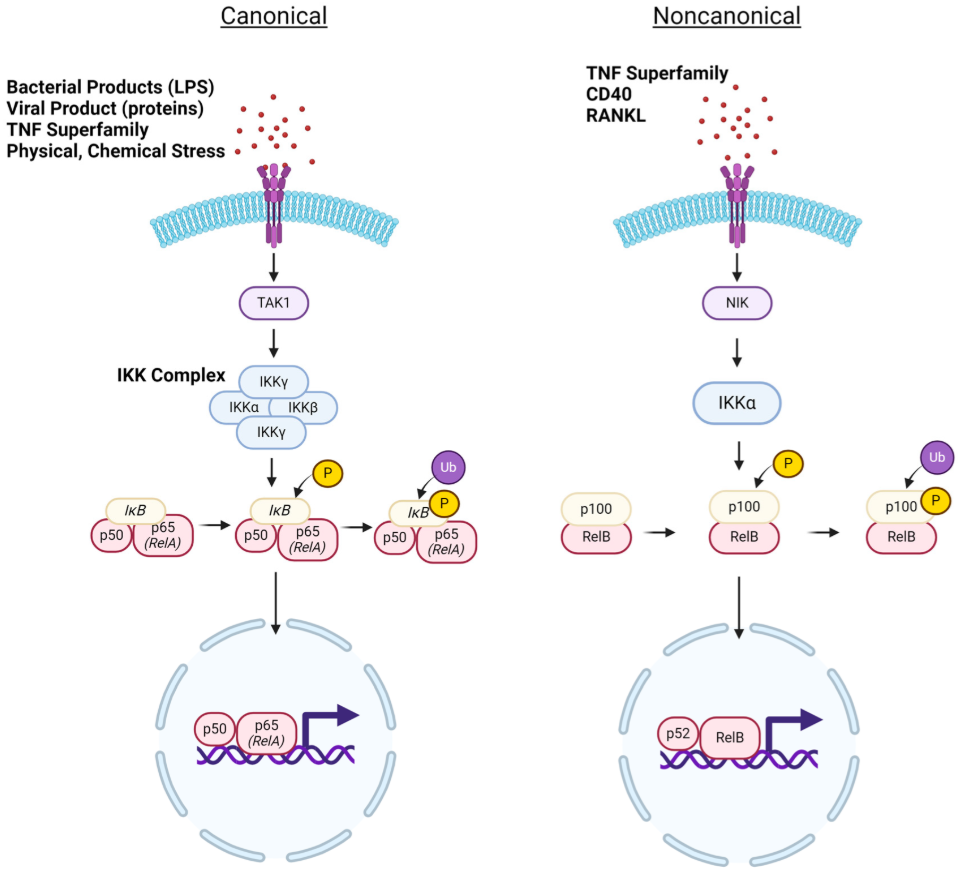
图1. 经典和非经典 NF-κB信号通路
中枢神经系统中NF-κB的细胞特异性作用
神经元:NF-κB兼具保护与毒性双重作用。保护方面,诱导抗凋亡基因 (TRAF1/2、Bcl-2、SOD) 表达,抵抗氧化应激;发育中感觉神经元存活依赖p65。毒性方面,脑缺血模型中p50/p65核转位与神经元死亡一致;TNF-α/NF-κB/p53轴诱导多巴胺能神经元死亡。功能差异可能与亚基组成有关:p65促凋亡,c-Rel促存活。
少突胶质细胞:目前的研究尚存争议。部分显示NF-κB激活减少凋亡、促进成熟;EAE模型中抑制NF-κB加剧细胞死亡和脱髓鞘。亦有研究表明NF-κB非必需,慢性激活诱导衰老表型导致白质变性。差异可能与PERK等非经典通路有关。
星形胶质细胞:生理条件下参与神经干细胞向星形胶质细胞分化。病理条件下与炎症加剧相关:脊髓损伤后p50/p65表达升高;选择性抑制NF-κB可减小损伤体积、保留白质、改善运动功能。
小胶质细胞:NF-κB激活诱导促炎表型。生理条件下参与分化与稳态维持:PDCD11缺失导致小胶质细胞分化减少;IKKβ缺失后细胞再殖能力受损。
小胶质细胞NF-κB在中枢神经系统疾病中的作用
作为中枢神经系统固有免疫细胞,小胶质细胞的NF-κB激活主要诱导促炎表型转化。在阿尔茨海默病中,β淀粉样蛋白通过ERK/MAPK信号激活小胶质细胞NF-κB,促进炎症因子释放;tau蛋白病模型中,小胶质细胞特异性敲除NF-κB可预防学习记忆缺陷并减少tau蛋白扩散。在ALS小鼠模型中,抑制小胶质细胞NF-κB可降低促炎标志物并延长生存期。在缺氧缺血性脑病模型中,早期抑制小胶质细胞NF-κB可减轻脑损伤并改善运动功能。
总结
NF-κB信号通路在中枢神经系统不同细胞类型中呈现功能多样性,其在小胶质细胞中的激活是神经炎症反应的关键驱动因素。小胶质细胞特异性NF-κB抑制在多种神经疾病模型中显示出保护效应,但介导这一作用的细胞间及分子间相互作用仍需进一步研究。现有证据表明,NF-κB在不同细胞类型、不同疾病阶段甚至不同亚基组成下可能呈现截然相反的功能,这提示未来治疗策略需要精准靶向特定细胞类型或特定亚基,而非全局性抑制。深入理解NF-κB信号的组织与细胞特异性调控机制,将为开发靶向神经炎症的干预策略提供理论基础。
阅读英文原文:https://www.mdpi.com/2073-4409/13/6/485
Cells 期刊介绍
主编:Cord Brakebusch, The University of Copenhagen, Denmark; Alexander E. Kalyuzhny, University of Minnesota, USA
期刊涵盖细胞生物学、分子生物学和生物物理学等方面的研究。目前已被SCIE (Web of Science)、PubMed、MEDLINE、PMC等数据库收录。
2024 Impact Factor:5.2
2024 CiteScore:10.5
Time to First Decision:15.5 Days
Acceptance to Publication:2.8 Days
期刊主页:https://www.mdpi.com/journal/cells

https://blog.sciencenet.cn/blog-3516770-1532340.html
上一篇:Cryptography:天津大学宗传明教授揭示格密码背后的数学问题
下一篇:IJMS:“大分子”栏目 | MDPI 栏目推荐