博文
Pharmaceutics乌普萨拉大学Erik Sjögren:基于全身生理的GalNAc偶联siRNA药代动力学模型
||
研究简介
小干扰RNA (siRNA) 疗法借助基因沉默机制,在治疗遗传性疾病方面展现出了巨大潜力。乙酰半乳糖胺 (GalNAc) 偶联技术靶向肝脏去唾液酸糖蛋白受体 (ASGPR),是目前应用最成熟的递送方案之一。然而,在药物开发过程中,如何将动物实验中的药代动力学 (PK) 数据准确外推至人体临床仍极具挑战。与此同时,GalNAc-siRNA的体内动态还涉及受体结合饱和、复杂的内吞转运及胞内逃逸过程。针对这一瓶颈,瑞典乌普萨拉大学 Erik Sjögren 教授团队在 Pharmaceutics 发表研究,构建了一套先进的全身生理药代动力学-药效学 (WB-PBPK-PD) 模型,为核酸药物的给药方案优化与临床转化提供了有力工具。
研究过程与结果
本研究构建了一个整合了15个组织器官的PBPK模型,并深入建立了涵盖药物与ASGPR受体结合、内吞转运及胞内降解的详细细胞动力学框架。通过引入受体周转 (turnover) 参数,模型成功解析了高剂量给药下受体介导摄取的饱和动力学特征。该模型在小鼠、大鼠、食蟹猴及人类等多个物种的实验数据中得到了严谨验证,展示了其在静脉和皮下给药途径下卓越的种属外推能力,能够一致性地预测跨物种的血浆药代动力学行为。
在机制层面,模型定量阐明了GalNAc-siRNA极强的肝脏靶向性及其被肝实质细胞捕获并加载至RISC复合体的动态全过程,为评估长效基因沉默效能提供了关键指标。通过参数敏感性分析,研究明确了ASGPR表达水平、受体亲和力及内吞速率是决定肝脏暴露量的核心驱动因素。这一发现不仅揭示了影响药物体内命运的关键生理与化学环节,也为通过精准化学修饰优化下一代siRNA递送系统提供了明确的理论支撑与设计导向。
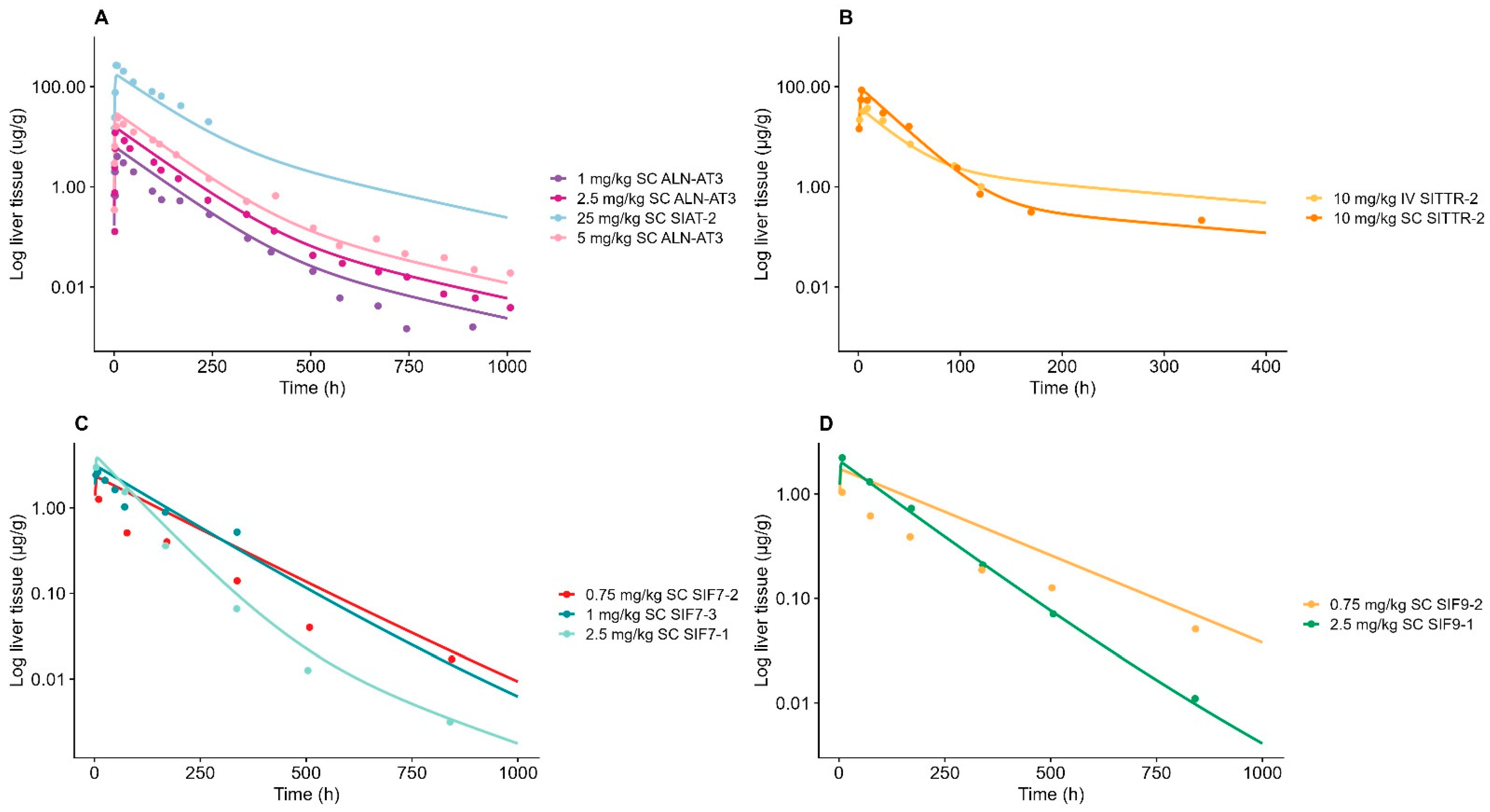
图片展示了靶向抗凝血酶的GalNAc-siRNA与靶向甲状腺素运载蛋白SITTR-2的模型模拟的肝组织分布与观察数据。
研究总结
本研究构建了首个涵盖全身多器官分布及胞内微观动态的GalNAc-siRNA通用型WB-PBPK-PD模型,实现了从宏观组织暴露到微观受体介导转运的机制化衔接。该模型不仅克服了传统房室模型难以刻画受体饱和及内吞动力学的技术瓶颈,更通过对胞内RISC加载过程的量化,揭示了决定基因沉默效能的深层逻辑。
跨物种验证的成功充分证明了该模型在临床前研究与人类临床预测之间的桥梁作用,为精准确定首次人体给药剂量、优化长效给药间隔以及解析个体差异对药效的影响提供了坚实的定量科学依据。这一研究成果显著增强了对核酸类递送系统体内行为的预判能力,不仅为GalNAc偶联药物的研发提供了强有力的计算平台,更为推动下一代精准肝脏靶向药物的临床转化与分子设计树立了新的典范。
阅读英文原文:https://www.mdpi.com/1999-4923/17/1/69
Pharmaceutics 期刊介绍
主编:Patrick J. Sinko, Rutgers University, Piscataway, USA
期刊领域涵盖生物制药、药物递送、药物控释、药物制剂、药物靶向、药代动力学、纳米医学、药物遗传学、药物基因组学、药效学等。目前期刊已被SCIE、Scopus和PubMed等数据库收录,位列JCR“药理学与药学”学科领域Q1区。
2024 Impact Factor:5.5
2024 CiteScore:10.0
Time to First Decision:15.7 Days
Acceptance to Publication:3.5 Days
期刊主页:https://www.mdpi.com/journal/pharmaceutics

https://blog.sciencenet.cn/blog-3516770-1530152.html
上一篇:东北农业大学李翰宇副教授和张华江教授主持特刊——禽蛋科学:营养成分、加工品质与微生物风险探究
下一篇:JoF 中国科学院微生物研究所:篮状菌属 (Talaromyces) 新分类系统的建立与新物种的发现