博文
新发现的细胞内电活动可能会改变研究人员对生物化学的看法
||
新发现的细胞内电活动可能会改变研究人员对生物化学的看法
诸平
Credit: Pixabay/CC0 Public Domain
据美国杜克大学(Duke University, Durham, NC, USA)2023年4月28日提供的消息,新发现的细胞内电活动可能会改变研究人员对生物化学的看法(Newly discovered electrical activity within cells could change the way researchers think about biological chemistry)。
人体很大程度上依赖于电荷。像闪电一样的能量脉冲飞过大脑和神经,大多数生物过程都依赖于穿越我们身体每个细胞膜的离子。
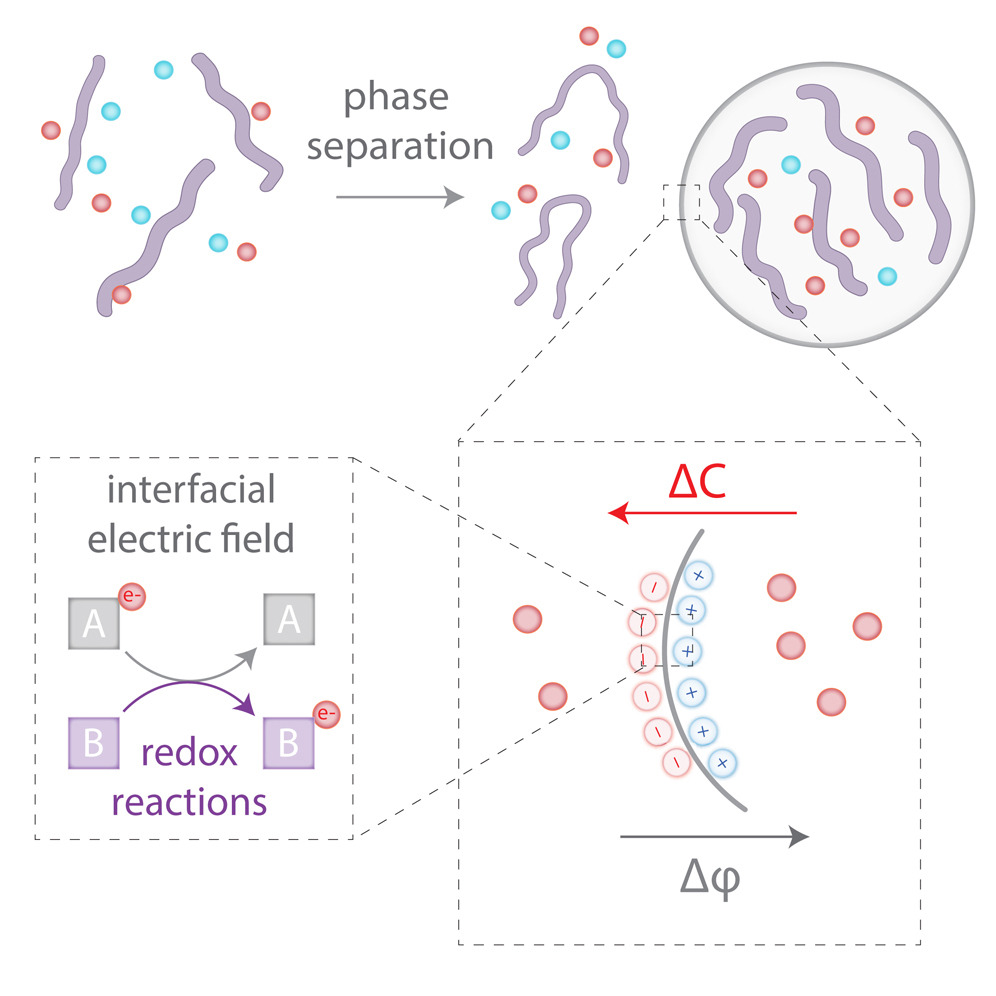
这些电信号(electrical signals)是可能的,部分原因是存在于细胞膜两侧的电荷不平衡。直到最近,研究人员认为膜是造成这种不平衡的重要组成部分。但是,当美国斯坦福大学(Stanford University)的研究人员发现,在微水滴和空气之间也存在类似的不平衡电荷时,这种想法被颠覆了。现在,美国杜克大学的研究人员发现,这些类型的电场也存在于另一种称为生物凝聚体(biological condensates)的细胞结构内部和周围。就像浮在水中的油滴一样,这些结构的存在是因为密度的不同。它们在细胞内形成隔室,而不需要膜的物理边界。
先前的研究表明,微水滴与空气或固体表面相互作用会产生微小的电不平衡,受此启发,研究人员决定看看小型生物凝聚物是否也是如此。他们还想看看这些不平衡是否会像其他系统一样引发活性氧“氧化还原”反应("redox," reactions)。相关研究结果于2023年4月28日已经在《化学》(Chem)杂志网站发表——Yifan Dai, Christian F. Chamberlayne, Marco S. Messina, Christopher J. Chang, Richard N. Zare, Lingchong You, Ashutosh Chilkoti. Interface of biomolecular condensates modulates redox reactions. Chem, 2023. DOI: 10.1016/j.chempr.2023.04.001. Available online 28 April 2023. https://doi.org/10.1016/j.chempr.2023.04.001. 他们的基础性发现可能会改变研究人员对生物化学(biological chemistry)的看法。它还可以提供线索,说明地球上的第一批生命是如何利用所需的能量产生的。
参与此项研究的除了来自美国杜克大学的研究人员之外,还有来自美国斯坦福大学(Stanford University, Stanford, CA, USA)和美国加州大学伯克利分校(University of California, Berkeley, Berkeley, CA , USA)的研究人员。
杜克大学博士后研究者戴一凡(Yifan Dai音译)问道:“在没有酶催化反应的益生元环境中,能量从哪里来?”戴一凡在艾伦·卡加沃夫生物医学工程特约教授(Alan L. Kaganov Distinguished Professor of Biomedical Engineering)阿素托史·奇尔科蒂(Ashutosh Chilkoti)和詹姆斯·梅里亚姆生物医学工程特约教授(James L. Meriam Distinguished Professor of Biomedical Engineering)尤凌冲(Lingchong You音译)的实验室工作。
戴一凡说:“这一发现为反应能量的来源提供了一个合理的解释,就像电场中的点电荷所传递的势能一样。”
当电荷在一种物质和另一种物质之间跳跃时,它们可以产生分子片段,这些分子片段可以配对并形成羟基自由基(hydroxyl radicals),其化学式为OH。然后,它们可以再次配对,形成少量但可检测的过氧化氢(H2O2)。
戴一凡说:“但是除了细胞膜之外,很少有人在生物学机制中研究界面,而细胞膜是生物学中最重要的部分之一。所以我们想知道在生物冷凝物的界面上可能发生了什么,也就是说,是否它也是一个不对称系统。”
细胞可以构建生物凝聚体,将某些蛋白质和分子分离或聚集在一起,从而阻碍或促进它们的活性。研究人员刚刚开始了解凝聚物的工作原理以及它们的用途。
由于阿素托史·奇尔科蒂实验室专门从事制造天然生物凝聚物的合成版本,研究人员很容易为他们的理论创建一个测试平台。在博士后学者马可·梅西纳(Marco Messina)的帮助下,将正确的积木配方结合起来,创造出微小的凝聚物。克里斯多夫·张(Christopher J. Chang)在加州大学伯克利分校(University of California—Berkeley)的研究小组,他们在系统中加入了一种染料,在活性氧存在的情况下会发光。
他们的预感是对的。当环境条件( environmental conditions)合适时,凝聚物的边缘开始发出固体辉光,证实了一种以前未知的现象正在起作用。戴一凡接着与斯坦福大学玛格丽特·布莱克·威尔伯化学教授(Marguerite Blake Wilbur Professor of Chemistry at Stanford)理查德·扎尔(Richard Zare)进行了交谈,他的团队建立了水滴的电行为。听到生物系统中的新行为,理查德·扎尔很兴奋,并开始与团队一起研究其潜在机制。
理查德·扎尔说:“受到先前对水滴的研究的启发,我的研究生克里斯蒂安·张伯伦(Christian Chamberlayne)和我认为,同样的物理原理可能适用并促进氧化还原化学,例如过氧化氢分子的形成。这些发现说明了为什么凝聚物(condensates)在细胞功能中如此重要。”
阿素托史·奇尔科蒂说:“以前大多数关于生物分子凝聚体的研究都集中在它们的内部。戴一凡发现生物分子凝聚物似乎具有普遍的氧化还原活性,这表明凝聚物并不是像人们通常理解的那样简单地进化为执行特定的生物功能,而是它们也被赋予了对细胞至关重要的关键化学功能。”
虽然我们细胞内这种持续反应的生物学含义尚不清楚,但戴一凡指出了一个益生元的例子(a prebiotic example),说明它的影响可能有多强大。我们细胞的能量发电站,叫做线粒体(mitochondria),通过相同的基本化学过程为我们所有的生命功能创造能量。但在线粒体甚至是最简单的细胞存在之前,必须有某种东西为生命最初的功能提供能量,使其开始运作。
研究人员提出,这种能量是由海洋或温泉中的热喷口提供的。另一些人则认为,发生在微水滴中的这种氧化还原反应是由海浪的喷射产生的。
但为什么不是冷凝物呢?(But why not condensates instead?)
戴一凡说:“当物质变得很小,界面体积相对于其体积变得巨大时,就会发生奇迹。我认为这对许多不同的领域都很重要。”
本研究得到了美国空军科学研究办公室(Air Force Office of Scientific Research: FA9550-20-1-0241 and FA9550-21-1-0170)、美国国立卫生研究院{NIH: MIRA R35GM127042; R01EB031869; R01 GM 79465, R01 GM 139245, R01 ES 28096;NIH MOSAIC K99/R00 (K99GM143573) award}、加州大学校长博士后奖学金计划(UC President’s Postdoctoral Fellowship Program)以及奇努克-伯克利博士后奖学金计划(Chinook-Berkeley Postdoctoral Fellowship Program)的资助。
上述介绍,仅供参考。欲了解更多信息,敬请注意浏览原文或者相关报道。
Synthetic compartments stop pathogens from sharing antibiotic resistance genes
• Phase transition of biomacromolecules can result in an ion density gradient
• The interface of biomolecular condensates possesses an electric potential
• Interfacial electric field can drive redox reactions
Biomolecular condensates mediate diverse cellular processes. The density-transition process of condensate formation results in the selective partitioning of molecules, which defines a distinct chemical environment within the condensates. However, the fundamental features of the chemical environment and the mechanisms by which such an environment can contribute to condensate functions have not been revealed. Here, we report that an electric potential gradient, thereby an electric field, is established at the liquid-liquid interface between the condensate and the bulk environment as a result of the density transition of ions and molecules brought about by phase separation. We find that the interface of condensates can drive spontaneous redox reactions in vitro and in living cells. Our results uncover a fundamental physicochemical property of the interface of condensates and the mechanism by which the interface can modulate biochemical activities.
https://blog.sciencenet.cn/blog-212210-1386445.html
上一篇:替代电池技术的进展
下一篇:新观察到的效应使原子对某些频率的光透明