博文
恭喜!1区Top、IF 9.3 的生物学期刊JIPB已经顺利发表!
|
文章已发表在SCI期刊 Journal of Integrative Plant Biology(生物学1区Top ,IF 9.3),评论可以沾沾好运~标题为:The VvPUB8–VvbHLH93–VvMYB15/VvMYB5a module inhibits the synthesis of anthocyanins in grape in response to MeJA
花青素是影响葡萄品质的关键因素。在不同浓度下,茉莉酸甲酯对葡萄花青素含量表现出浓度依赖性效应,但其分子机制尚不清楚。本研究鉴定了一个响应茉莉酸甲酯的E3泛素连接酶VvPUB8,并通过在“佳美”葡萄愈伤组织中过表达和突变体载体转化,验证了该基因负向调控葡萄花青素合成的功能。
进一步研究发现,VvPUB8与转录因子VvbHLH93直接互作,而VvbHLH93可通过激活VvMYB15和VvMYB5a启动子正向调控花青素合成。蛋白质的稳定性或活性受泛素化修饰类型和数量的调控。
本研究表明VvPUB8通过催化VvbHLH93发生K6和K33连接的泛素化修饰,进而促进其降解。外源茉莉酸甲酯处理加速了VvbHLH93蛋白降解并抑制VvMYB15启动子活性,最终导致葡萄花青素合成受阻。
本研究揭示了在茉莉酸甲酯响应过程中,VvPUB8通过差异性多聚泛素链修饰调控VvbHLH93稳定性,进而调节VvMYB15和VvMYB5a启动子活性,最终抑制花青素合成的分子机制。
研究结果(部分)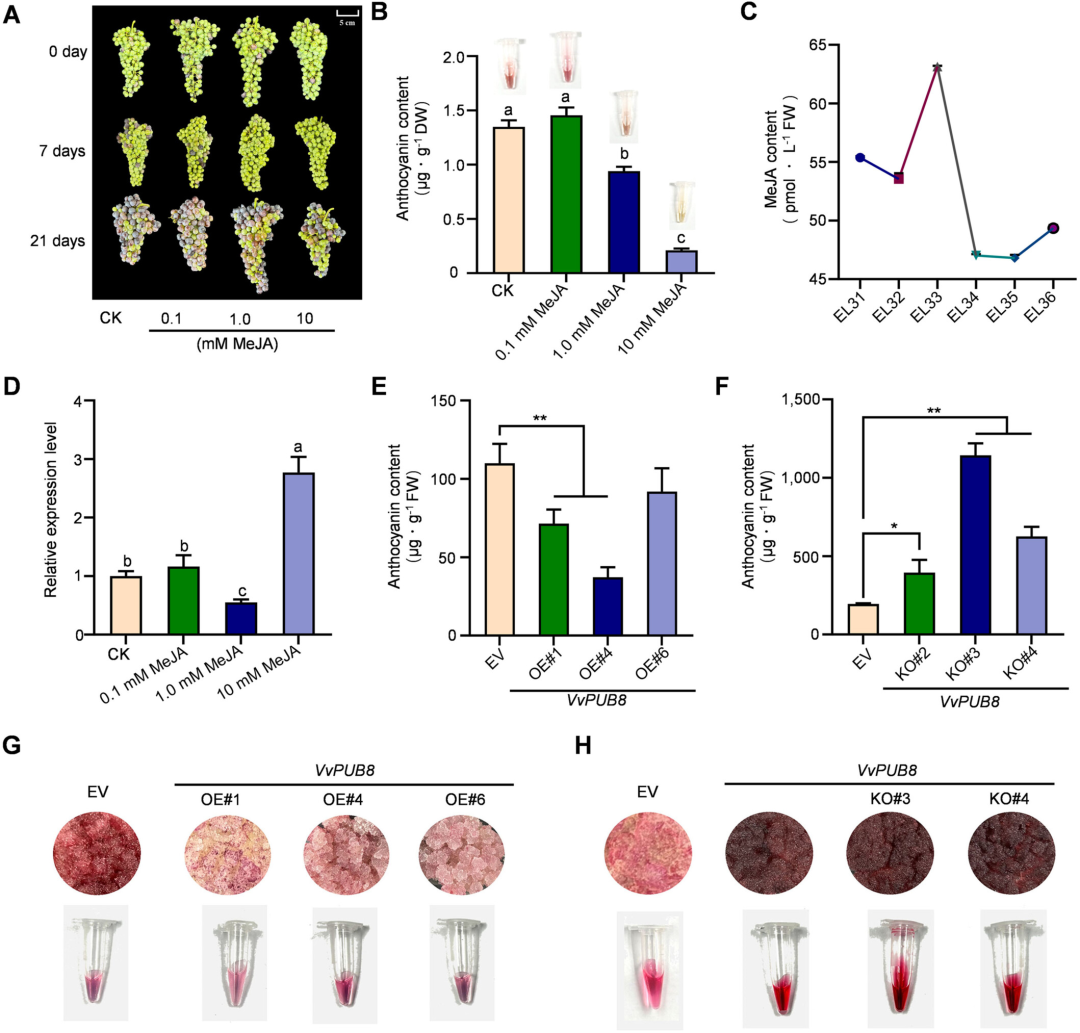
图1. 茉莉酸甲酯诱导VvPUB8抑制葡萄花青素合成。
(A)不同浓度茉莉酸甲酯(0、0.1、1.0和10 mM)处理“赤霞珠”葡萄果实的表型分析。比例尺=5 cm。
(B)MeJA处理后“赤霞珠”葡萄果实花青素含量测定。
(C)EL31–EL36时期葡萄果实内源MeJA含量。
(D)不同浓度MeJA对VvPUB8基因表达水平的影响。MeJA处理6 h后采集样品,立即用液氮冷冻进行RT-qPCR分析。
(E)VvPUB8过表达“佳美”愈伤组织的花青素含量及提取液颜色。
(F)VvPUB8敲除“佳美”愈伤组织的花青素含量及提取液颜色。
(G)VvPUB8过表达“佳美”愈伤组织的表型观察及提取液颜色。
(H)VvPUB8敲除“佳美”愈伤组织的表型观察及提取液颜色。OE#1、OE#4和OE#6为三个过表达VvPUB8的株系;KO#2、KO#3和KO#4为三个CRISPR/Cas9敲除VvPUB8的株系。pRI101-AN-GFP和CRISPR/Cas9空载体作为对照。
数据为平均值±标准差;n=3个生物学重复。不同字母表示经单因素方差分析(Tukey检验)差异显著(P < 0.05)。
星号表示与空载体对照相比有显著差异(*P < 0.05,**P < 0.01,双尾Student t检验)。
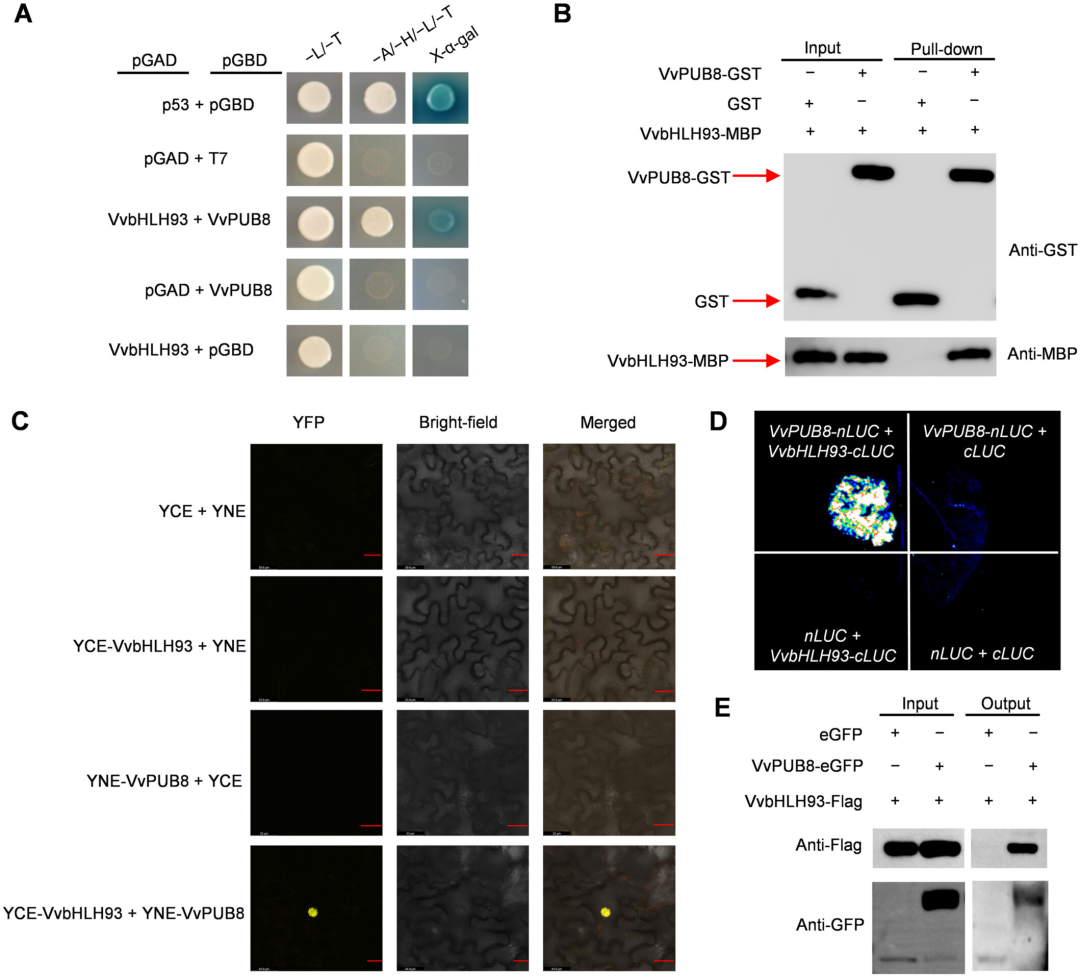
图2. VvPUB8与VvbHLH93在体内和体外的互作验证。
(A)酵母双杂交试验。共转化pGBD-p53与pGAD−T7及pGBD-p53与pGAD+T7作为阳性对照,共转化pGBD-VvPUB8+pGAD及pGBD+pGAD-VvbHLH93作为阴性对照。将共转化pGBD-VvPUB8+pGAD-VvbHLH93的酵母细胞培养于添加20 mg mL⁻¹ X-α-Gal的营养缺陷型培养基(SD/−Trp−Leu−His−Ade)上。
(B)Pull-down试验。将纯化的重组蛋白VvPUB8-GST和GST分别与VvbHLH93-MBP蛋白孵育,并用谷胱甘肽琼脂糖珠固定。使用抗GST和抗MBP抗体检测蛋白。
(C)双分子荧光互补试验。将pSPYNE-VvPUB8与pSPYCE-VvbHLH93瞬时共转化本氏烟叶片。以pSPYNE与pSPYCE-VvbHLH93共转化及pSPYNE-VvPUB8与pSPYCE共转化作为阴性对照,通过共聚焦显微镜观察黄色荧光蛋白信号。比例尺=25 μm。
(D)荧光素酶互补成像试验。将VvPUB8-nLUC与VvbHLH93-cLUC在本氏烟叶片中瞬时共表达,以VvPUB8-nLUC与cLUC共转化及VvbHLH93-cLUC与nLUC共转化作为阴性对照。使用植物体内分子标记成像系统观察荧光信号。
(E)免疫共沉淀试验显示VvPUB8与VvbHLH93在体内的互作。
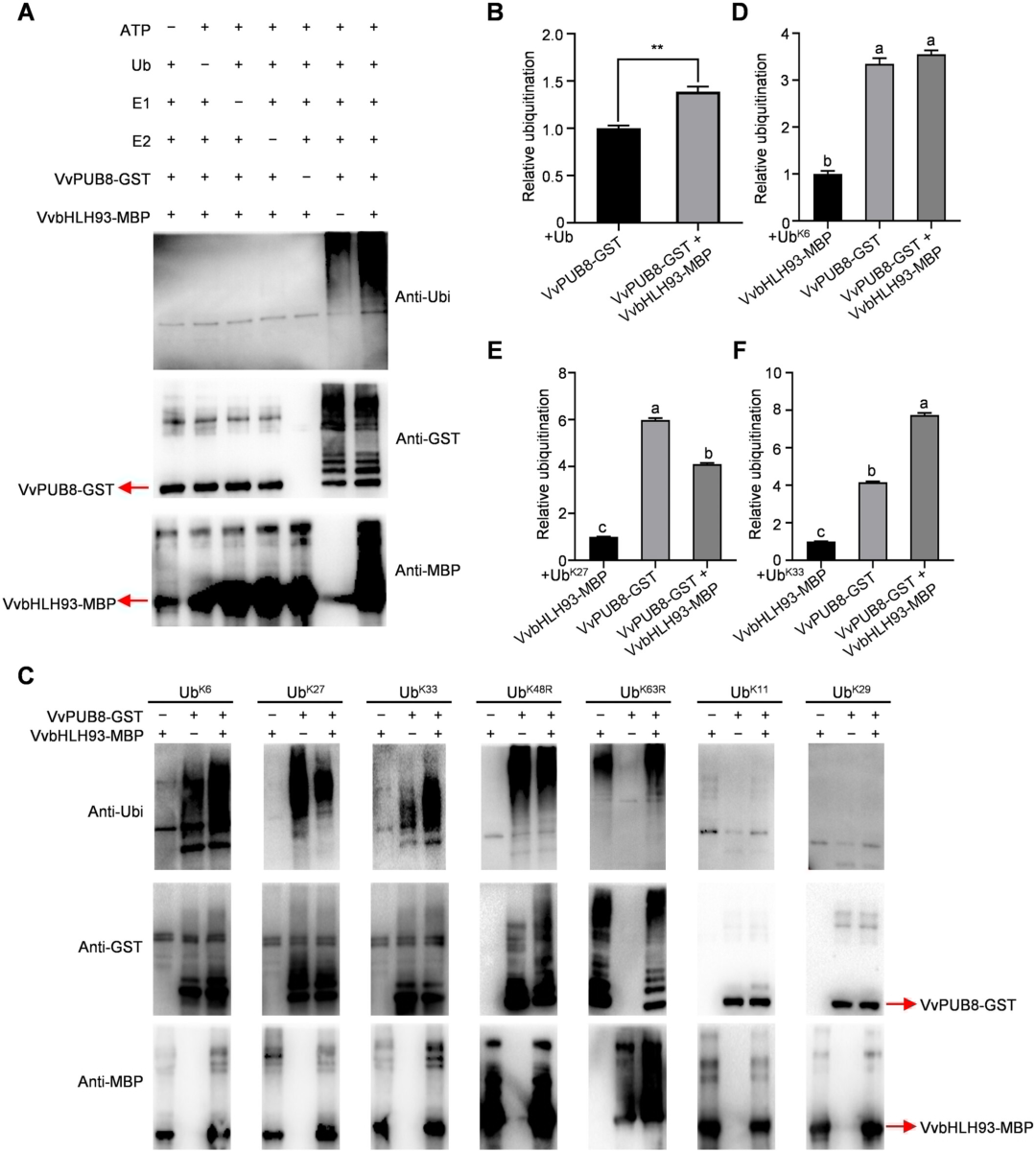
图4. VvPUB8在体外对VvbHLH93进行泛素化修饰。
(A、B)VvPUB8具有E3泛素连接酶活性,可在体外对VvbHLH93进行泛素化修饰。将纯化的原核蛋白VvPUB8-GST和VvbHLH93-MBP与E1、E2及Ub在泛素化反应缓冲液中于37°C孵育2小时。
反应结束后,在(A)中使用抗GST、抗MBP和抗Ubi抗体检测蛋白质的泛素化水平。在(B)中使用ImageJ软件对抗Ubi抗体的Western blot检测结果进行定量分析,计算相对泛素化水平。以VvPUB8-GST蛋白水平设为1.0。星号表示与对照组相比差异显著(**P < 0.01,双尾Student t检验)。
(C–F)同样,在体外泛素化反应缓冲液中添加不同类型泛素(UbK6、UbK27、UbK33、UbK48R、UbK63R、UbK11和UbK29),以鉴定VvPUB8对VvbHLH93进行泛素化修饰的泛素链类型。独立重复三次实验,结果相似。
使用ImageJ软件对抗Ubi抗体的Western blot检测结果进行定量分析。以VvbHLH93-MBP蛋白水平设为1.0。不同字母表示经单因素方差分析(Tukey检验)差异显著(P < 0.05)。
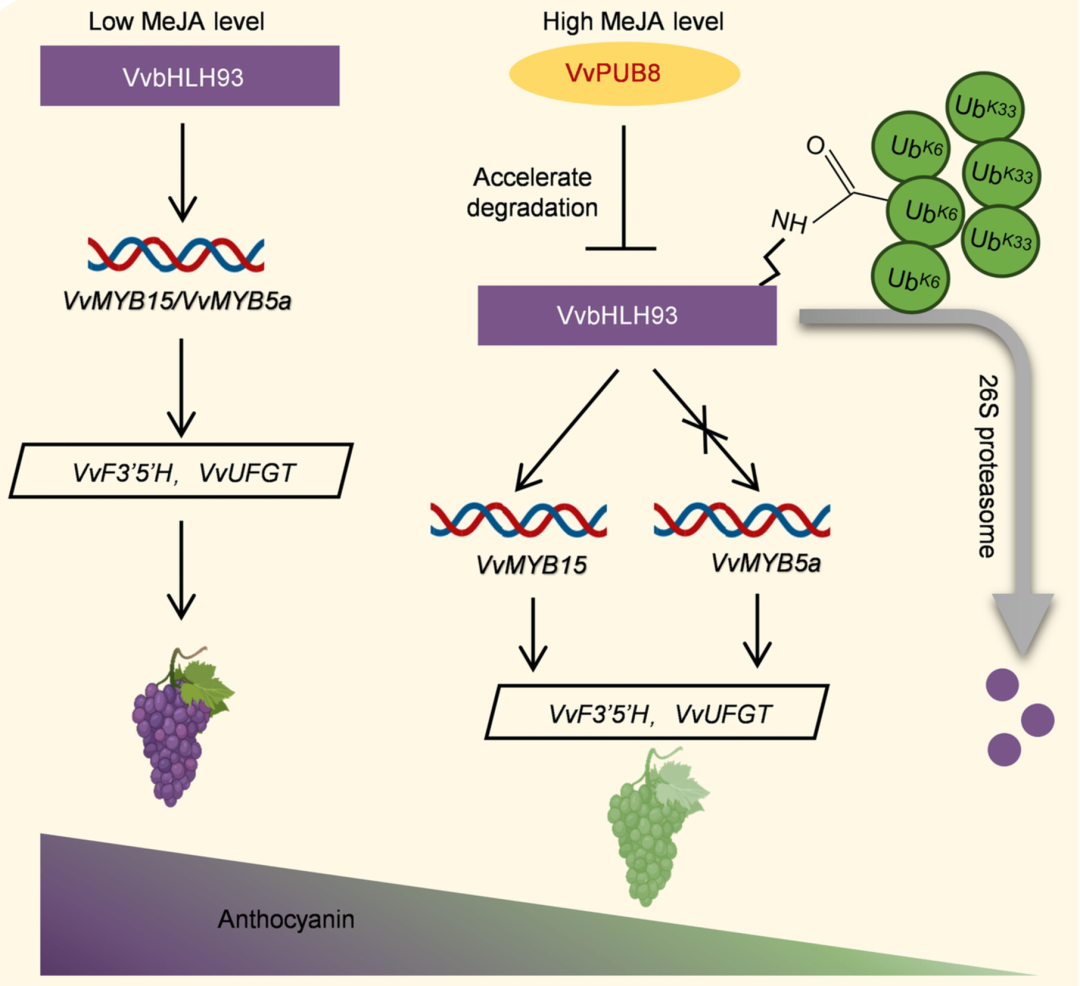
图8. VvPUB8响应MeJA调控VvbHLH93抑制葡萄花青素合成的分子模型。
在低浓度MeJA条件下,VvbHLH93通过激活转录因子VvMYB15和VvMYB5a启动子活性,正向调控葡萄花青素合成。当存在高浓度MeJA时,VvPUB8表达显著诱导;VvPUB8通过K6和K33两种泛素链对VvbHLH93进行泛素化修饰,加速VvbHLH93蛋白降解,并抑制VvbHLH93对VvMYB15转录因子启动子的激活作用,从而阻断葡萄花青素合成。
总结
总之,我们提出了一个模型,阐明VvPUB8–VvbHLH93–VvMYB15/VvMYB5a模块通过MeJA信号通路调控葡萄花青素合成(图8)。在正常条件下,VvbHLH93通过激活VvMYB15和VvMYB5a启动子正向调控花青素合成。当存在高浓度MeJA时,VvPUB8被显著诱导表达。随后,VvPUB8通过两种泛素链类型(K6和K33)对VvbHLH93进行泛素化修饰,加速VvbHLH93降解,并抑制其对VvMYB15启动子的激活作用。该过程最终抑制了葡萄花青素的合成。
本研究揭示了E3泛素连接酶VvPUB8与转录因子VvbHLH93响应MeJA处理抑制葡萄花青素合成的分子机制,为MeJA激素调控葡萄花青素合成提供了新视角。
作者致谢本研究得到国家自然科学基金、生物育种与农产品精深加工专项、科技人才与平台计划以及国家葡萄产业技术体系的资助。感谢LetPub(www.letpub.com.cn)在论文准备过程中提供的语言协助。

已发表文章的好评与致谢
 更多网友投稿经验,查看:https://www.letpub.com.cn/index.php?journalid=4694&page=journalapp&view=detail
更多网友投稿经验,查看:https://www.letpub.com.cn/index.php?journalid=4694&page=journalapp&view=detail好消息!!! LetPub重磅推出4大核心投稿套餐,覆盖不同科研投稿场景
LetPub重磅推出4大核心投稿套餐,覆盖不同科研投稿场景

📢LetPub结合15年SCI论文编辑服务经验,推出四大投稿套餐,从语言润色、中译英翻译、行文逻辑结构优化、专家预审、材料准备到投稿系统指导,一站式支持您顺利投出高质量稿件!


SCI论文润色│SCI论文翻译│SCI论文润色哪家好│SCI论文润色价格|SCI论文修改|SCI论文润色公司│SCI论文查重│联系我们
https://blog.sciencenet.cn/blog-1232242-1529825.html
上一篇:Energy Strategy Reviews冷暖超和谐配色
下一篇:SCI作者要注意了!期刊正在检测AI幻觉引用