博文
《自然—神经科学》:首次发现!西湖大学贾洁敏团队揭示连接神经元与血管间“新桥梁”
||
北京时间2024年1月2日,西湖大学生命科学学院贾洁敏团队在Nature Neuroscience上发表最新成果“Synaptic-like transmission between neural axons and arteriolar smooth muscle cells drives cerebral neurovascular coupling”,发现了一座横架在神经元与血管之间“新桥梁”——“类突触连接(NsMJ)”。
通过这种类突触信息传递方式,谷氨酸能神经元活化后分泌的神经递质谷氨酸,可以直接作用于动脉血管平滑肌细胞,进而导致动脉舒张,诱发大脑功能性充血。
“这种类突触结构及其对功能性充血调控作用的发现,是对现有脑血流调控机制的进一步完善和补充,是对实现脑血流快速和精准调控的一个全新认知。”贾洁敏表示,这项研究丰富了人们对脑血流受神经支配机制多样性的认识,也为临床上有效的治疗缺血性低灌注损伤,提供了潜在的策略。
发现——连接神经元与血管的新桥梁
神经元传递信息,势必需要能量供给,能量从哪里来?答案藏在长达10万英里的血管中,血液可以为大脑提供葡萄糖和氧气,同时排出代谢废物和二氧化碳。
神经元之间沟通路径已然明朗,那么,神经元与血管间该如何对话?换句话说,大脑如何快速和精准地告诉血管及时为其提供能量?当大脑血供出现异常时,我们又该如何调节脑血供,来治疗这些脑血管疾病?
血管周存在着各种各样的脑细胞,如星形胶质细胞,神经元,小胶质细胞,和血管壁细胞(包括周细胞和血管平滑肌细胞)。这些细胞组成了脑组织和血液进行物质交换的基本单元,被称为神经血管单元。
这些细胞中,难道会藏有大脑调节血供的密码吗?
生命科学学院的贾洁敏团队长期从事大脑中神经与血管之间相互作用的研究,神经元对脑血流的精准调控,是为神经元及时保证能量供给的关键。对此,他们展开了长达6年的深入探究。
已有的研究表明,神经元可以作用于神经胶质细胞继而调节血管血流,但是目前证据仍不充分,于是,他们思考,或许除了这种间接的调控方式,会不会有一种直接的调控方式?
结构决定功能,基于结构探索功能。想要了解一个事物的功能,第一步就是要先“看清”它的全貌。
通过大体积三维扫描电镜和光电联合技术,贾洁敏团队全面地解析了小鼠躯体感觉皮层中约480 μm长的穿支动脉血管及血管周脑组织细胞的超微结构。他们发现,星形胶质细胞终足对穿支动脉的包裹率并不是100%,反而有“漏洞”。这些漏洞为脑内其他细胞的亚细胞结构,如小胶质细胞突起,神经元胞体,树突和轴突,提供了可以直接与血管进行信息交流的可能。也就是说,血管并非被终足全部包裹,神经元很有可能穿过这些裸露的部分,与血管直接“对话”。
对话不可能凭空产生,势必有一个中介,或者说,载体。
从样本制备、采集数据到分析数据,贾洁敏团队花了近三年的时间终于看清,血管周神经元的轴突含有子母突触前,母突触前与神经元的树突脊形成经典的突触,同时子突触前穿过星形胶质细胞终足的漏洞,插入血管平滑肌细胞外围的基底膜,与血管平滑肌细胞形成“类突触”,他们首次将这一结构定义为NsM,从而传递一个新认知:神经元除了和骨骼肌之间会形成经典NMJ(神经肌肉接头)外,也会与血管平滑肌形成类突触。

图1:神经元与动脉血管平滑肌细胞之间形成一种“类突触(NsMJ)”
第一次,贾洁敏团队看清了神经元与血管之间存在一座从来没有发现过的“新桥梁”。但随之而来的是更多问题:眼见不一定为实,这座连接神经元与血管平滑肌细胞的新桥梁可以传输信息吗?还是只是一个没有功能的结构?
这需要实验进一步来验证。
验证——类突触样连接可调节大脑血管收缩舒张
实验第一步,研究血管平滑肌细胞是否具有接收神经递质信号的信号接收器
结合细胞纯化和测序、免疫组化验证以及钙成像和电生理记录等多种技术,证明脑内血管平滑肌细胞,竟然能表达多种神经递质受体,其中包括具有通透钙离子等谷氨酸神经递质受体NMDAR (图2)。
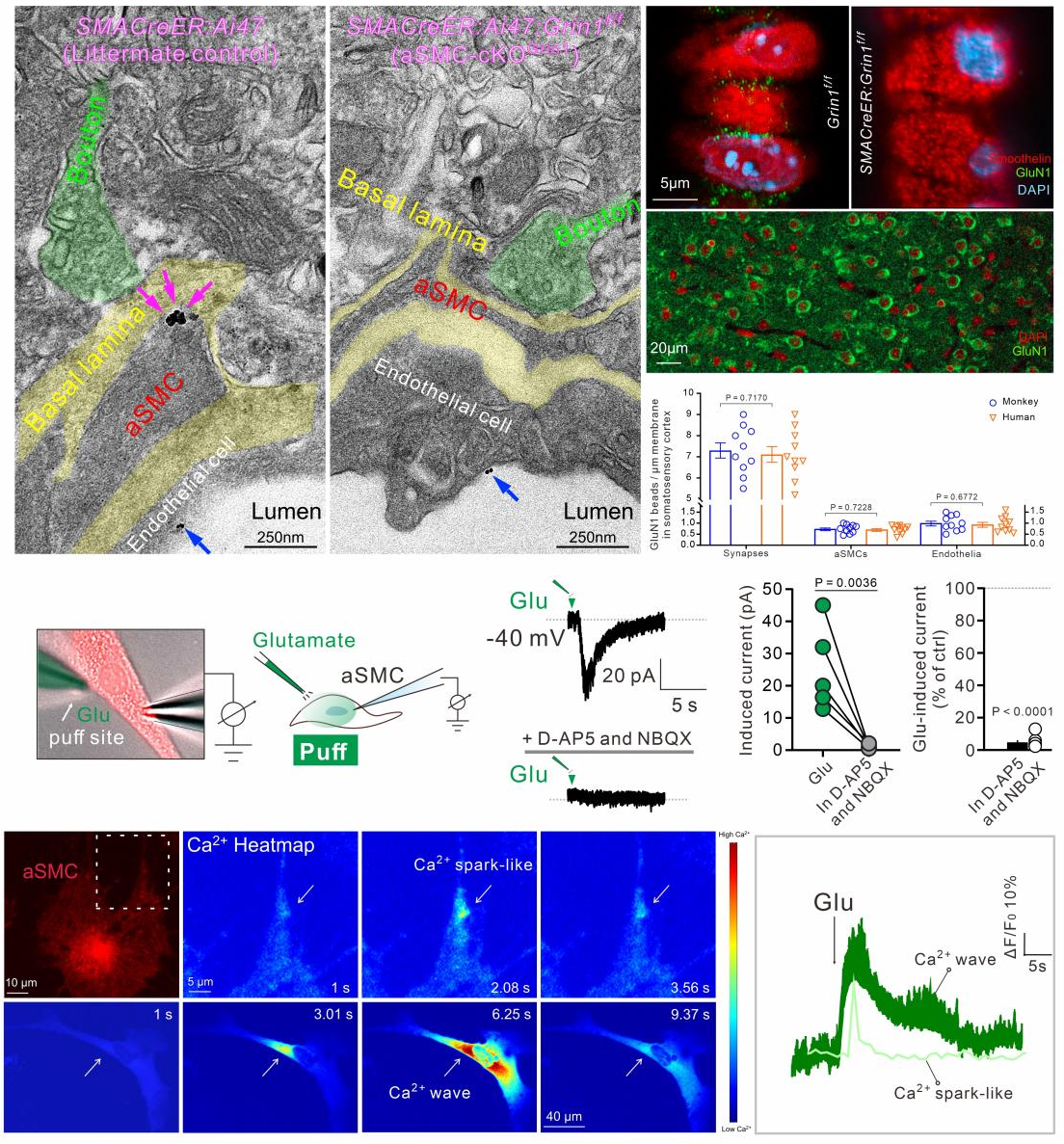
图2:功能性NMDAR亚基GluN1富集在类突触后膜(血管平滑肌细胞膜)
实验第二步,整体水平精确瞄准激活谷氨酸能轴突,激活类突触的突触前膜。
目前,化学遗传学和常规光遗传学,都无法精准激活单个神经元胞体,更别提激活比其直径小几十倍之差的神经元局部的树突和轴突。
贾洁敏团队创新双光子光遗传学,开创了颅内单根轴突和树突光遗传学激活,并且同时跟踪靶向动脉的直径变化,进而研究类突触在整体水平对脑血流的调控能力。此实验范式属于世界首创,打破了绝大多数实验室依赖已丧失血流血压的“脑片”实验体系,将单根轴突激活和真实的血流相结合 。贾洁敏研究团队使用该范式成功诱发动脉血管舒张,直径可增大近15%;但该范式在缺失NMDAR受体的条件性敲除小鼠却无法诱发舒张,证明的确是通过NsMJ引发舒张。该结果又被经典胡须刺激诱导功能性充血的实验所验证。由此推断,在整体水平,类突触NsMJ是大脑功能性充血的主要机制者之一。
实验第三步,明确类突触NMDAR如何调控动脉血管直径的分子机制。
他们进一步发现NMDAR亚基GluN1和钙离子依赖的钾离子通道(BK)形成复合体。当NMDAR激活时内流的钙离子进而开启钾离子通道,引发钾离子外流,导致细胞超极化(图3),而超级化可以舒张血管平滑肌细胞。
至此,从现象、结构、功能、分子机制等多水平,贾洁敏团队全方面证实了神经元的类突触可调节大脑血管收缩和舒张。
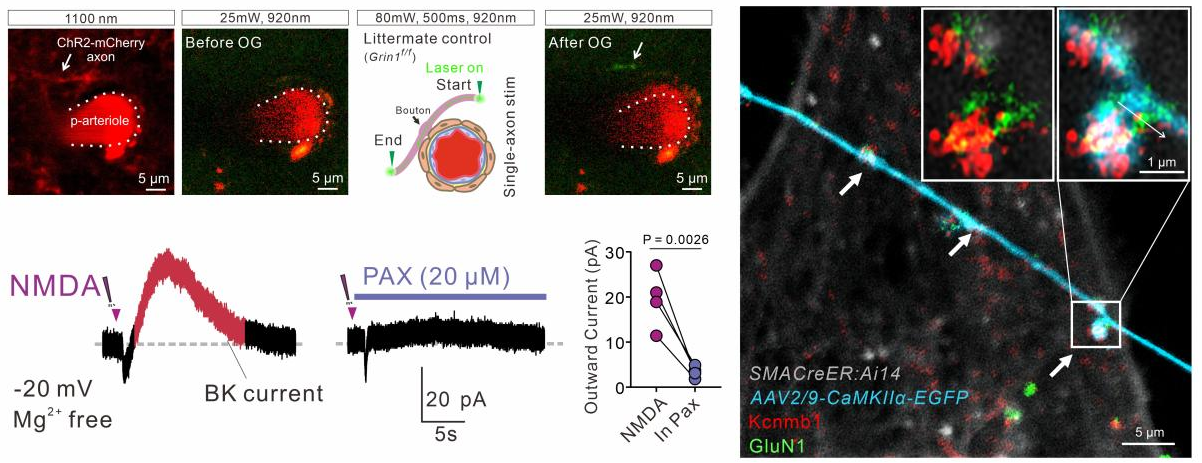
图3:类突触样连接是大脑功能性充血的重要贡献者
意义——为研究大脑缺血造成的损伤提供新的研究思路
脑卒中是血管源性障碍而引发脑血流异常的疾病。贾洁敏实验室发现了的这条神经元调控大脑血液的新路径是否能会对脑卒中如何引发大脑损伤提供新的思考角度?
生理正常状态时,神经元通过类突触可以与大脑血管正常对话;但是如果桥对岸“堵车”了,信号还能继续传递过去吗?
当大脑中的血管发生堵塞,形成血栓,导致大脑血液供给不足,发生缺血缺氧,这时“堵车”就发生了。此时,脑内谷氨酸水平会急剧增高,从而产生兴奋性毒性。该毒性的确引发神经元的死亡,但其是否会动脉带来毒性确实全然未知的。
通过细胞膜片钳技术,贾洁敏团队发现在高浓度谷氨酸灌注刺激下,血管平滑肌细胞会大量去极化,血管因此收缩。随后,通过小鼠大脑中动脉阻塞模型(MCAO)验证,谷氨酸被大量释放作用与动脉平滑肌细胞,会使得其钙离子超载,导致血管急性收缩,即产生了动脉毒性。该毒性会继而二次缺血。如何有效避免二次缺血呢?团队发现,通过特异性敲除动脉平滑肌细胞上NMDAR亚基GluN1,可以缓解动脉毒性和后续的脑萎缩程度,增强了小鼠的运动恢复,降低死亡率(图4)。
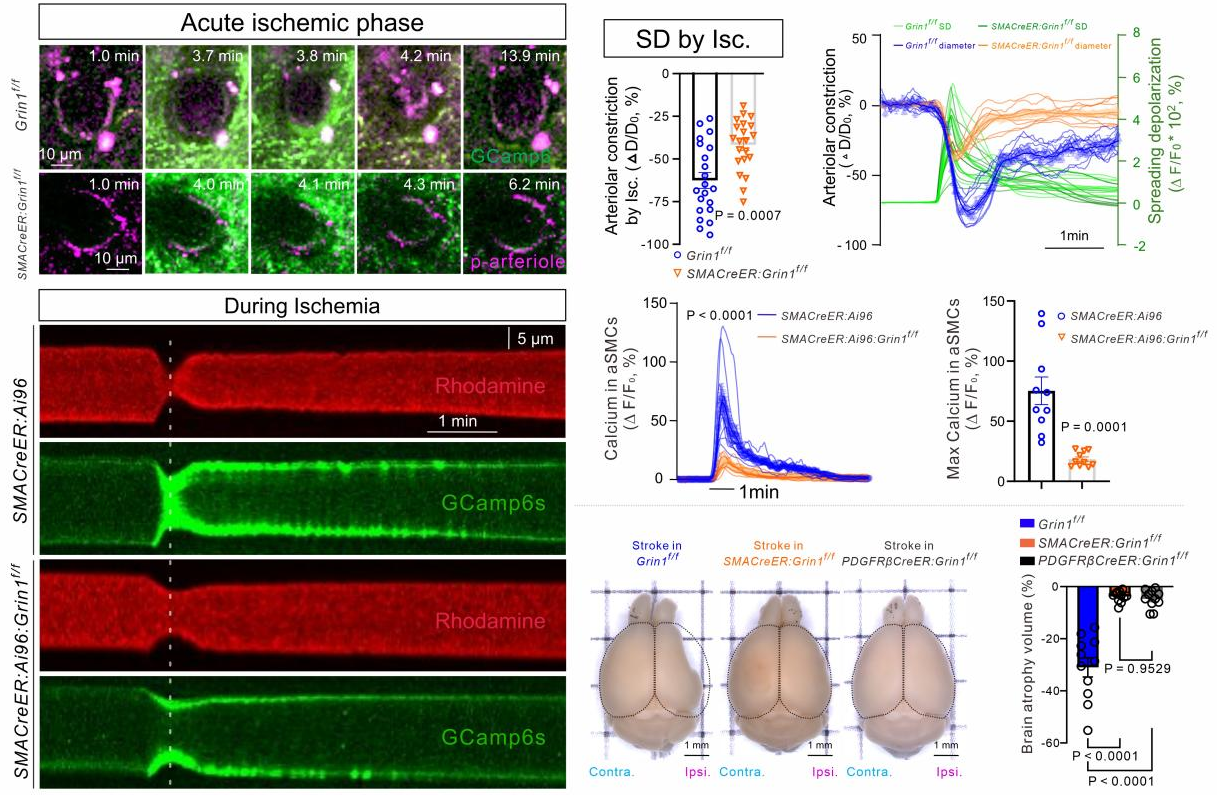
图4:动脉平滑肌细胞上表达的谷氨酸NMDA受体介导了兴奋性毒性对动脉的二次损伤及其神经损伤
通过严谨的实验和分析,贾洁敏团队揭示了大脑中神经元与动脉血管平滑肌细胞之间存在的“类突触(NsMJ)”。该研究从超微结构组成、分子富集特性、体外和体内的功能体现,以及疾病发生发展等方面,对这种类突触信息传递进行了深入探讨。这些发现为深入理解大脑的血供机制提供了新的视角,并为开发针对此类连接的脑卒中治疗策略提供了新的思路。
“西湖一期”博士生张冬冬与他的导师贾洁敏,都是最早一批加入西湖大学的研究人员。花费6年时间,专注在这个课题上,张冬冬坦言,压力山大,但是正如他们坚信神经元与血管之间必然存在着连接一样,坚持与收获之间,或许应该也存在着一些冥冥之中的连接。
西湖大学生命科学学院特聘研究员贾洁敏为论文通讯作者,西湖大学2017级博士研究生张冬冬为本文第一作者。第二作者为博士研究生阮家宇,他负责了分子表达验证实验和小鼠交配策略制定和管理工作,为项目的稳定推进做出了不可或缺的贡献。讲席教授许田实验室彭诗宇副研究员在电生理记录方面为项目推进做出了重要贡献。四位博士研究生胡旭,李旭召,李廷波,周丽丽,两位助理研究员李金泽和朱珠,参与了部分研究工作。临床样本研究是与复旦大学附属华山医院神经外科吴劲松主任和李文生团队合作完成。
该工作得到了西湖大学生命科学学院许田老师,北京脑科学与类脑研究所戈鹉平和孙文智两位老师的大力支持。本项目获得了国家自然基金委、西湖实验室以及西湖教育基金会的资助;项目实施过程中得到了西湖大学成像平台、超算平台、流式平台以及实验动物中心的大力支持。
相关论文信息:
DOI:10.1038/s41593-023-01515-0
https://blog.sciencenet.cn/blog-3423233-1416415.html
上一篇:《细胞—干细胞》:陈水冰团队开发新的靶向KRAS突变抑制剂
下一篇:《自然—生物技术》:何川团队开发出超快速精准检测微量DNA与RNA中5-甲基胞嘧啶的新方法