博文
不止基因与蛋白,糖代码正成为疾病诊疗新密钥_MCE(MedChemExpress)
|
Section.01
糖是什么?
糖是一类由碳 (C) 、氢 (H) 和氧 (O) 组成的天然有机化合物,常常被归类为碳水化合物。在结构上,这些分子同时含有多个羟基 (—OH) 以及一个醛基 (—CHO) 或酮基 (C=O) ,因此糖也被称为多羟基醛或多羟基酮及其衍生物。
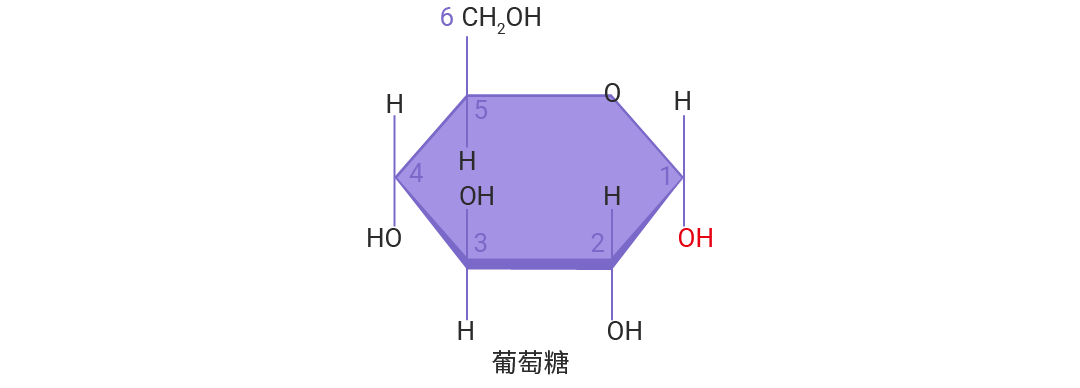
最简单的糖结构称为单糖,如我们熟知的葡萄糖、果糖等,它们是糖类的基本单元,在生命体中既是能量来源,也是许多生物分子的原料。
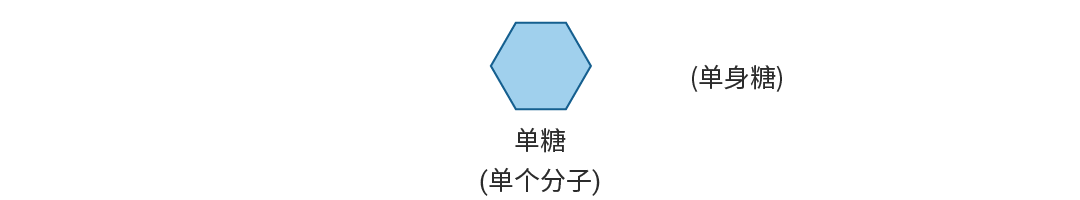 图 1. 单糖结构示意图。
图 1. 单糖结构示意图。
当两个单糖通过糖苷键连接在一起时,就形成了二糖,常见的例子包括蔗糖、乳糖和麦芽糖等。
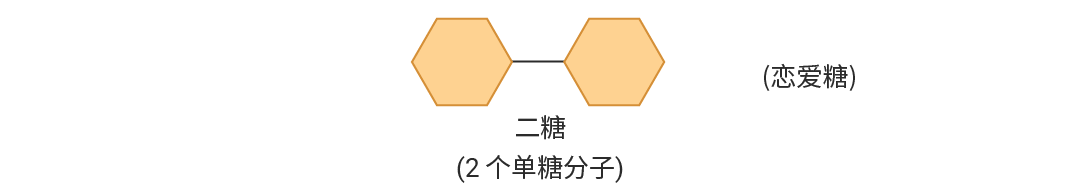 图 2. 二糖结构示意图。
图 2. 二糖结构示意图。
大量的单糖通过类似方式反复连接起来,就构成了多糖,例如淀粉、纤维素和糖原等。
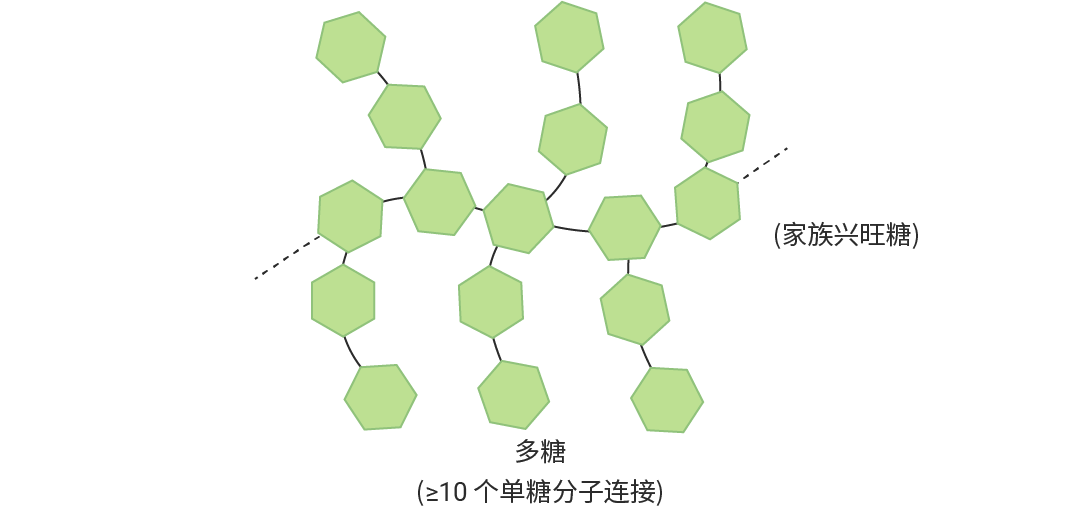 图 3. 多糖结构示意图。
图 3. 多糖结构示意图。
多种多样的糖除了提供能量外,还具有结构性生理学功能。比如纤维素、甲壳素都是葡萄糖通过 β-1,4- 糖苷键连接得到的线性多糖,分子内和分子间氢键使其内部形成高度有序的微纤丝结构,给整体结构带来坚固的机械支撑力。
纤维素作为植物细胞壁的主要成分,为植物体提供结构支撑。
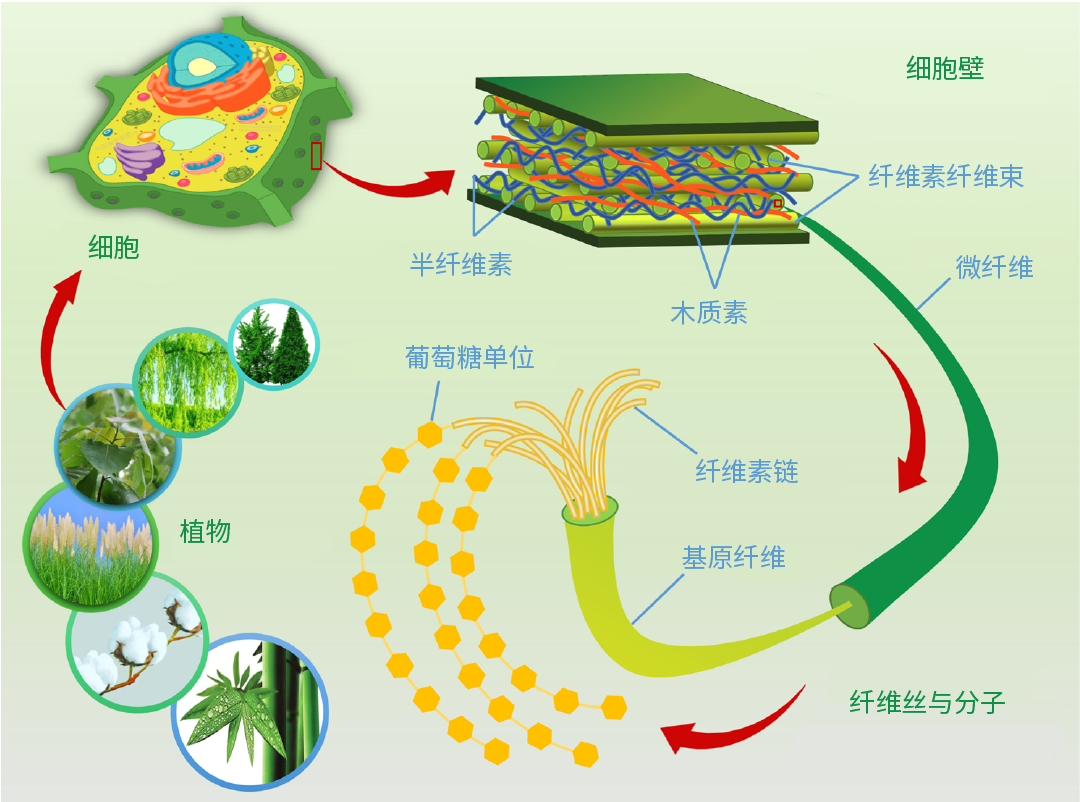
图 4. 植物的等级结构[1]。
甲壳素作为构成甲壳类动物外骨骼的主要多糖,为甲壳动物提供保护和刚性支撑[2]。
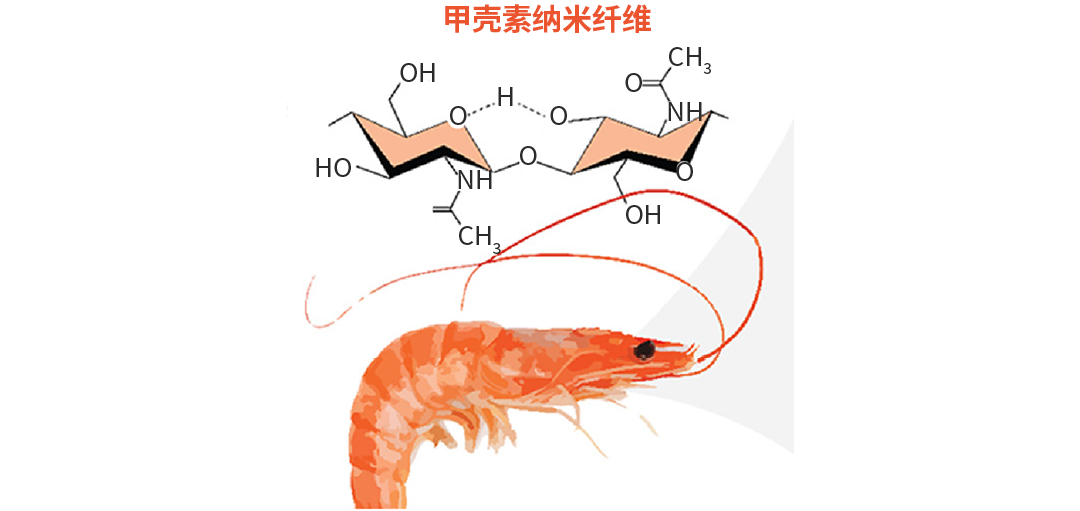
图 5. 虾源甲壳素纳米纤维[3]。
此外,细胞表面存在一层高度动态且结构复杂的糖类富集层,称为糖萼 (Glycocalyx) 。糖萼是由细胞膜表面的蛋白质或脂质发生 N- 糖基化/O- 糖基化修饰后形成的糖缀合物聚集层,是细胞与外界环境进行物质交换、信号识别与免疫应答的重要分子界面,甚至可以作为细胞的身份信息特征[4]。细胞表面的糖缀合物还可以直接影响受体构象、配体结合及信号级联等关键生物过程。
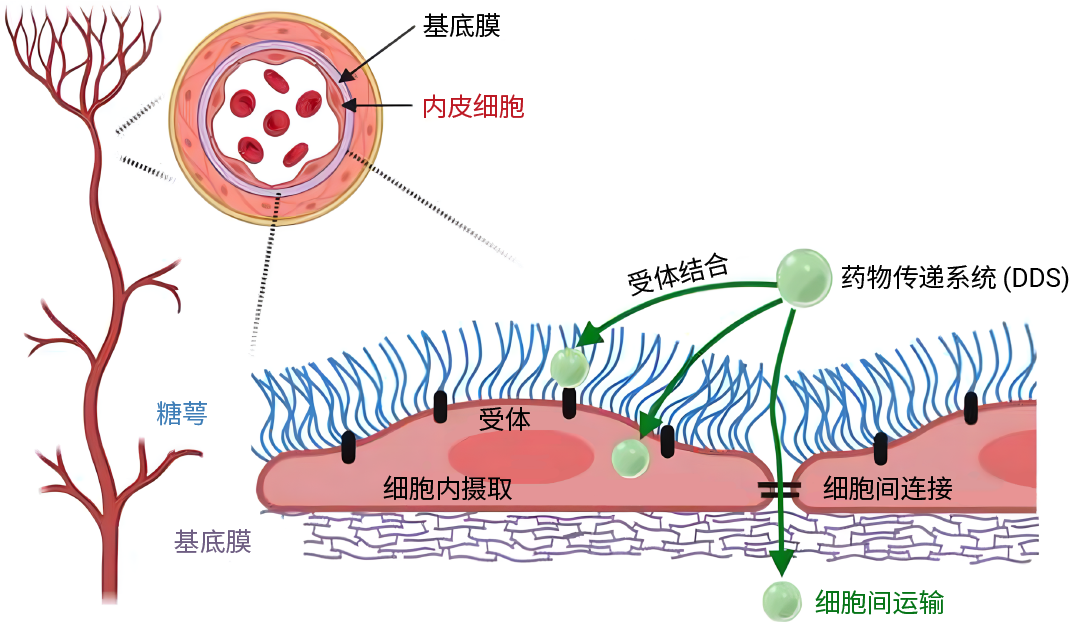
图 6. 细胞表面糖萼在药物进入和通过内皮中的作用[5]。
Section.02
糖基化
糖萼哪来的?
——其形成是来源于生命体内最常见、也最关键的翻译后修饰之一:糖基化!
糖基化是指在糖基转移酶催化下,单糖或糖链通过糖苷键与蛋白质、脂质、RNA 等生物大分子结合的过程。这一过程主要在内质网和高尔基体两个细胞器内发生,蛋白质经糖基化修饰后形成糖蛋白,其结构和功能都可能受到影响。
糖基化可分为两大主要类型:N- 糖基化和O- 糖基化。
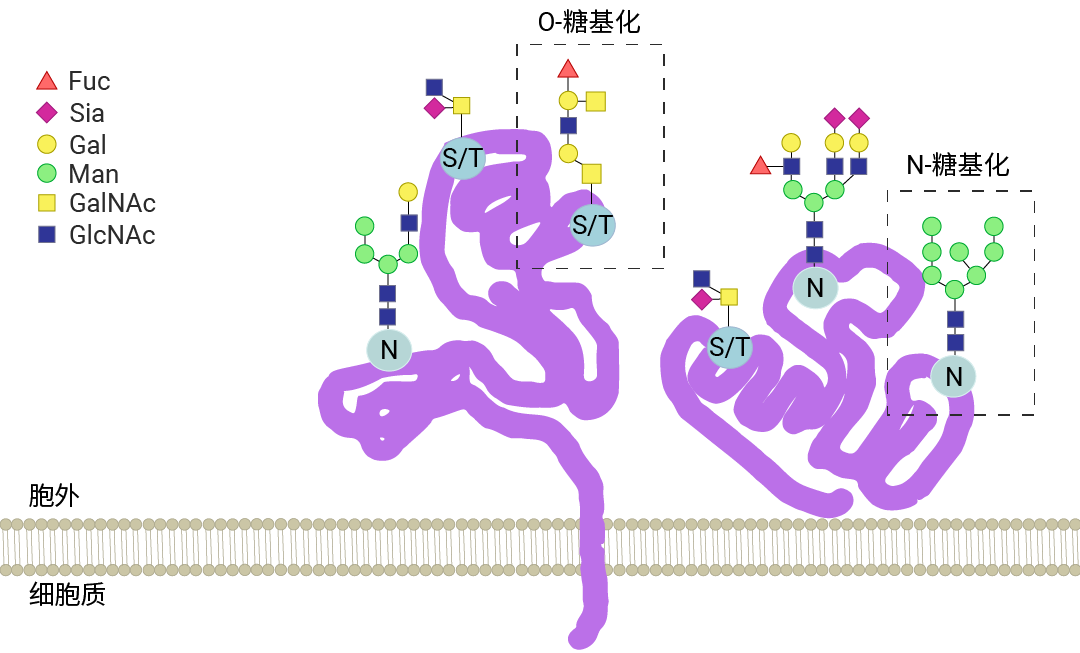 图7. N-糖基化/O-糖基化。
图7. N-糖基化/O-糖基化。
二者异同
N- 糖基化发生在天冬氨酸 (Asn) 残基上,预先组装的核心寡糖结构在新生肽链进入内质网后被寡糖转移酶转移到蛋白上,内质网对糖蛋白进行初步加工后将其运输至高尔基体修建完成修饰过程,N- 糖链的结构相对固定,主要可以分为高甘露糖型、复合型和杂合型。
O- 糖基化发生在丝氨酸 (Ser) 或苏氨酸 (Thr) 残基上,直接在高尔基体中将单糖逐个转移到蛋白中加工,并在此基础上延伸和修饰糖链,O- 糖链的结构没有相对固定的结构范式,因此预测和研究难度较大。
前文已经提到,糖基化的本质是一种酶促反应,因此负责催化这一过程的两类酶——糖基转移酶 (GlycosylTransferases, GTs) 和糖苷酶 (Glycoside Hydrolases, GHs) ——是糖生物学中重要的研究对象。
糖基转移酶:负责将糖从供体底物转移至受体来催化糖苷键合成。
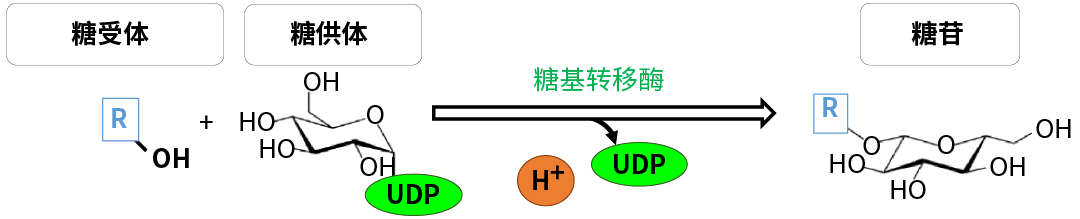
图 8. 糖基转移酶催化糖基转移至受体,形成糖苷键[6]。
糖苷酶:执行相反的功能,通过水解已经形成的糖苷键来拆解糖缀合结构,还在细胞内部糖链加工、质量控制和能量代谢等过程中发挥关键作用。
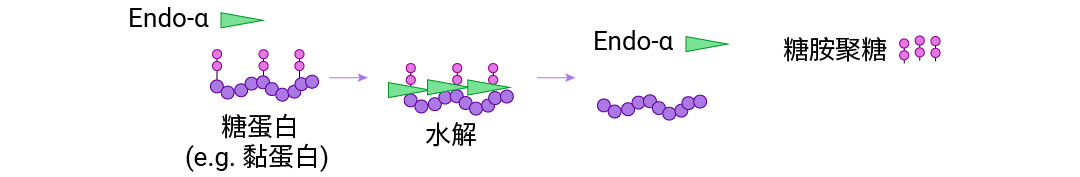 图 9. 内切糖苷酶 (Endo-α) 识别寡糖的内部结构,酶切寡糖的共有基序得到对应寡糖分子。
图 9. 内切糖苷酶 (Endo-α) 识别寡糖的内部结构,酶切寡糖的共有基序得到对应寡糖分子。
酶信息去哪找?
Carbohydrate-Active enZyme (CAZy) 数据库专门收录整理了与碳水化合物代谢相关酶的信息,其中包含 138 个家族的超一百五十万个糖基转移酶序列以及包含 189 个家族的超一百八十万个糖苷酶序列,其中人源糖苷酶序列 95 个,糖基转移酶序列 249 个。
言归正传!糖基化是生命过程中最重要的翻译后修饰调控之一。在真核生物中有超 50% 的蛋白质会发生糖基化修饰,而人类基因组中有至少 1% 的基因参与到聚糖的合成、代谢等生理过程。
糖基化参与到细胞-细胞间信号识别、细胞黏附、内吞及胞吐、清除细胞异物等重要的生理过程中,蛋白质的糖基化会显著影响蛋白质的折叠、空间定位、稳定性和功能,改变蛋白质的三维构象和表面性质,使其在细胞内部或细胞间发挥特定的生物学作用。
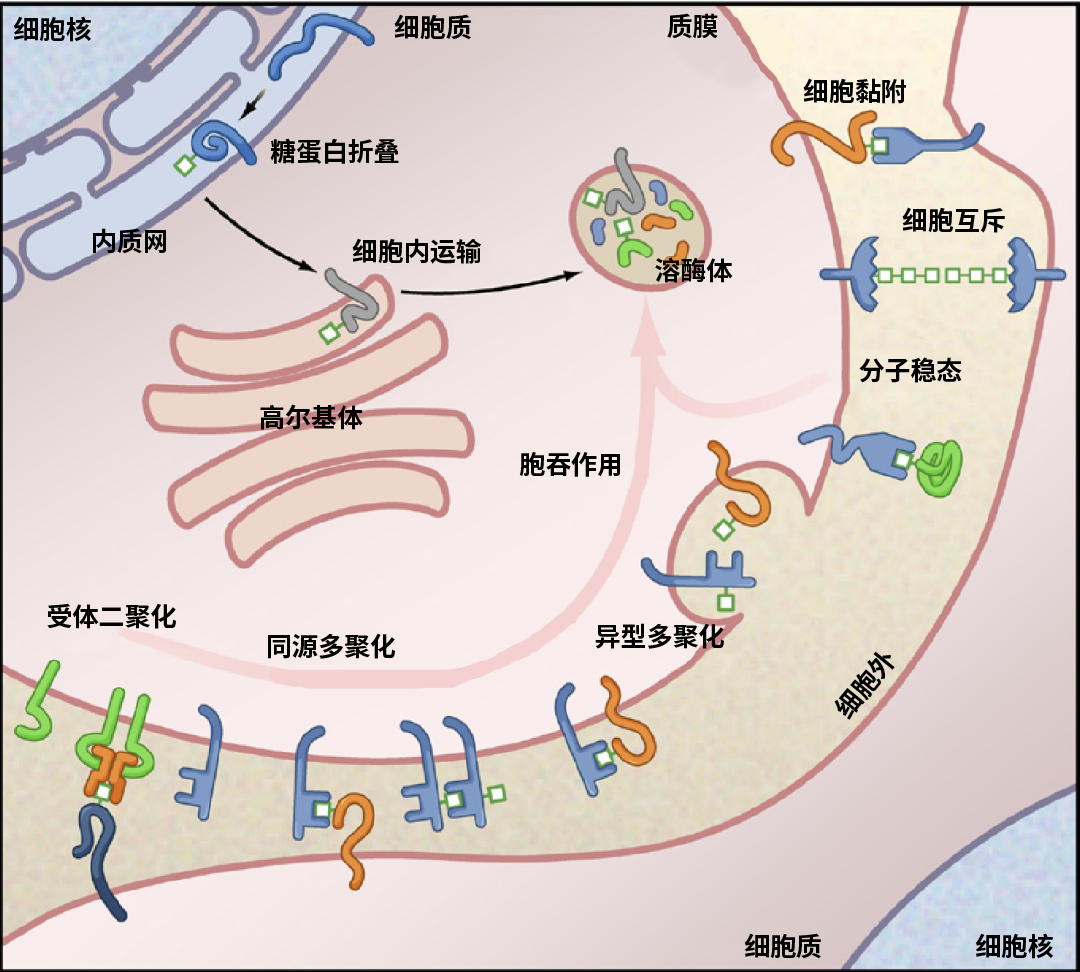
图 10. 糖基化的细胞生物学功能[7]。
广泛存在的糖基化修饰对蛋白质功能和细胞行为有深远的影响,由此带来异常糖基化与多种疾病的密切关联。
在神经系统中,糖基化异常可能干扰神经元间的信号交流。肿瘤细胞也常表现出异常的糖基化模式,例如整体唾液酸化水平升高,这会改变细胞间黏附和信号识别,有助于肿瘤细胞的迁移和侵袭性表型的增强。
目前,临床上已开发出一系列糖类抗原 (Carbohydrate antigens) 作为肿瘤标志物用于辅助诊断和病情监测。例如,CA15-3 常用于乳腺癌的辅助监测;CA19-9 则在胰腺癌及部分胃肠道肿瘤中常显著升高,被用于辅助诊断和疗效监测。
Section.03
如何检测糖?
尝一尝?NO!
对糖进行精确的检测分析需要上设备!
游离的单糖、多糖可以通过常规的化学比色法、LC-MS、NMR 等手段进行定性定量检测。而在生物体内,面对复杂糖基化修饰后形成的糖链,则需要专门的识别和分析策略。
凝集素
一种常用且灵敏的工具是凝集素 (lectins) ——这是一类天然存在的碳水化合物结合蛋白,能够特异性识别特定的糖链结构。
凝集素的糖识别域 (CRD) 可以可逆性地结合具有特定终端残基的糖链,例如甘露糖、岩藻糖或唾液酸等。基于这种特异性识别,将荧光团、生物素等标签偶联到凝集素分子上,就可以实现对特定结构糖链的检测、定位和富集。
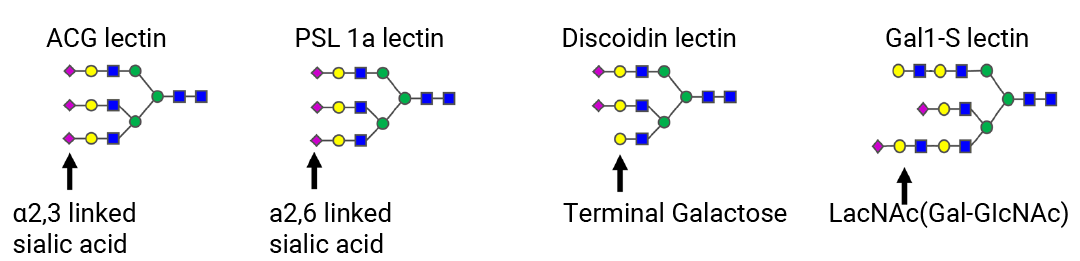
图 11. 凝集素及对应识别糖链示意图[8]。
这一策略在糖组学分析、糖修饰蛋白的分离鉴定以及细胞表面糖结构的表征中得到了广泛应用。
除了作为检测工具外,糖链与凝集素之间的特异性结合还被用于靶向递药。将 GalNAc 作为配体共价偶联到 siRNA 或反义核酸 (ASO) 药物分子上,可以显著提高这些药物的肝脏靶向性,使其通过 ASGPR 介导的途径特异性进入肝细胞。这一策略已成为目前最成熟、临床验证最多的小核酸药物递送技术之一。例如,多款 GalNAc-siRNA 药物 (如 Givosiran、Lumasiran 和 Inclisiran 等) 已经获批上市,覆盖遗传性代谢病和心血管疾病等适应症。
Section.04
小结
随着高分辨率质谱、液相色谱、人工智能和大数据等技术的融合,糖组学和糖基化研究正快速向精细化、动态化和临床化方向迈进。糖链结构的精准解析将在疾病早期诊断、个性化治疗和靶向药物开发中发挥更大作用,而基于糖代码 (glyco-code) 的免疫调控、糖工程细胞疗法等新兴方向也正在成为转化医学的新热点。糖生物学不仅会继续深化我们对生命机制的理解,而且有望成为精准医学、合成生物学和下一代生物材料等领域的重要推动力量,开启“糖代码”在健康与疾病管理中的全新应用篇章。
产品推荐
含叠氮基的代谢糖蛋白标记试剂,选择性修饰 N-糖基化蛋白质。常用于细胞标记、跟踪和蛋白质组学分析。
Lens Culinaris Agglutinin (LCA) (HY-NP087)
小扁豆凝集素,优先结合 α-甘露糖和 α-葡萄糖
催化寡糖中内部糖苷键的裂解,可以在糖分析工作流程中从糖蛋白中释放 N-聚糖。
对 N-糖蛋白中的高甘露糖,复杂型和某些杂合型寡聚糖的壳二糖核心结构进行切割,去除糖蛋白中的 N-连接高甘露糖。
包含 O-Glycosidase及α2-3,6,8,9 Neuraminidase,组合用于糖蛋白 O-糖链的酶切释放。
参考文献
[1] Liu K, et al. Recent advances in cellulose and its derivatives for oilfield applications. Carbohydr Polym. 2021 May 1;259:117740.
[2] Rodrigues Reis CE, et al. Lignocellulosic biomass-based glycoconjugates for diverse biotechnological applications. Biotechnol Adv. 2023 Nov;68:108209.
[3] Bai L, et al. Nanochitin: Chemistry, Structure, Assembly, and Applications. Chem Rev. 2022 Jul 13;122(13):11604-11674.
[4] Gomez Toledo A, et al.Endothelial Glycocalyx Turnover in Vascular Health and Disease: Rethinking Endothelial Dysfunction. Annu Rev Biochem. 2025 Jun;94(1):561-586.
[5] Fu L, et al. The role of the cell surface glycocalyx in drug delivery to and through the endothelium. Adv Drug Deliv Rev. 2022 May;184:114195.
[6] McGraphery K, et al. Comparative Analysis of High-Throughput Assays of Family-1 Plant Glycosyltransferases. Int J Mol Sci. 2020 Mar 23;21(6):2208.
[7] Ohtsubo K, et al.Glycosylation in cellular mechanisms of health and disease. Cell. 2006 Sep 8;126(5):855-67.
[8] Matsumoto T, et al. Serum N-glycan profiling is a potential biomarker for castration-resistant prostate cancer. Sci Rep. 2019 Nov 14;9(1):16761.
[9] Parle DR, et al.Metabolic Glycan Labeling of Cancer Cells Using Variably Acetylated Monosaccharides. Bioconjug Chem. 2022 Aug 17;33(8):1467-1473.
[10] Nanni P, et al. Mass Spectrometry in Proteomics: Technologies, Methods, and Research Applications for the Life Sciences. Chimia (Aarau). 2022 Feb 23;76(1-2):73-80.
https://blog.sciencenet.cn/blog-3536222-1531747.html
上一篇:类器官多维鉴定(基因测序等)__ MCE (MedChemExpress)