博文
hLife | 佐治亚大学林晓蓉团队描绘真菌mRNA疫苗:从“首次验证”到“破局路线图”
|
每年,超过380万人的死亡与真菌感染相关。其中HIV/AIDS患者、器官移植受者及恶性肿瘤患者等免疫功能低下人群,是侵袭性真菌病的主要易感群体。在美国,真菌病造成的年经济负担已超过110亿美元。然而,面对这一严峻威胁,全球范围内尚无一款获批的真菌疫苗。病原真菌是人类健康的狡猾的对手。作为复杂的真核生物,它们进化出了精密的免疫逃逸机制:例如新生隐球菌用荚膜“隐身”,烟曲霉破坏吞噬体成熟,念珠菌分泌抑制因子干扰干扰素信号等。真菌疫苗研发已走过三十余年,传统全细胞疫苗免疫原性强但安全性存疑,重组亚单位疫苗安全但模拟抗原能力有限。mRNA技术的出现,为突破这一僵局带来了新机,正被推向抗真菌防治的前沿。近日,美国佐治亚大学林晓蓉研究团队在hLife发表题为“Prospects for using mRNA vaccines against fungal infections”观点文章(图1),总结了真菌疫苗研究并对mRNA技术在这一领域的应用进行了前瞻性展望。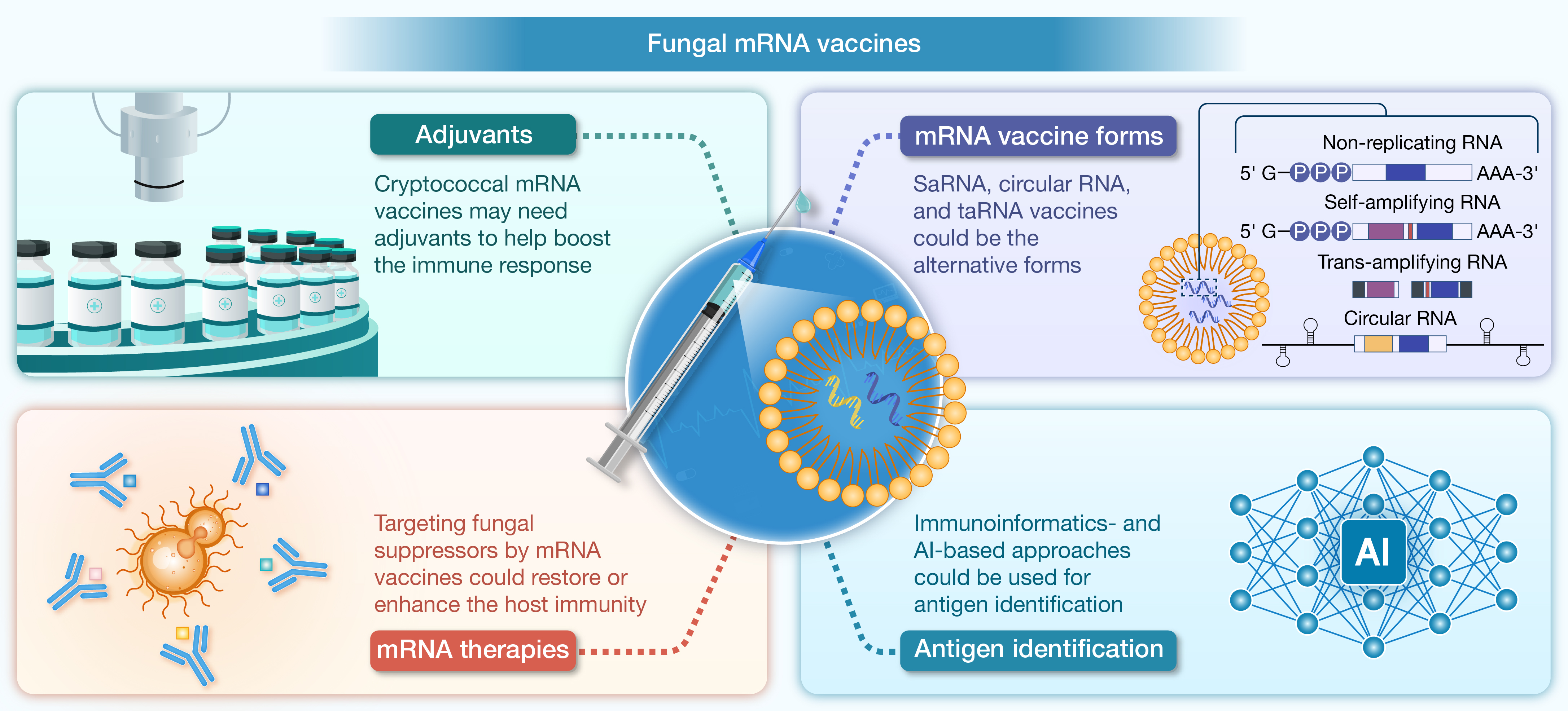
https://blog.sciencenet.cn/blog-3552961-1526656.html
上一篇:hLife | Call for Papers: Immune Reprogramming and Microenvir
下一篇:hLife Collection | Oncology

图1 论文标题及作者信息
真菌mRNA疫苗的“首次验证”。2025年,佐治亚大学研究团队首次报道了一款针对隐球菌病的mRNA-LNP疫苗。研究中发现一个耐人寻味的现象:单独使用编码几丁质脱乙酰酶1(Cda1)抗原的mRNA-LNP,在所测试剂量下未能提供保护;而当同时添加纯化的隐球菌荚膜成分时,保护性免疫被成功诱导。这一结果揭示了一个核心命题:病毒mRNA疫苗的成功经验,可能无法直接平移至真菌。该发现为真菌mRNA疫苗开辟了“优化之门”。借助mRNA平台固有的灵活性,以下四个战略方向值得系统探索(图2)。

图2 真菌mRNA疫苗未来发展的潜在优化方向
佐剂是成败的关键。在病毒疫苗中常被视为“锦上添花”的佐剂,在真菌mRNA疫苗中,可能成为成败的关键。CDA1-LNP单独无效,加荚膜后有效,这一对比使佐剂成为关键因素。核心问题随之浮现:真菌mRNA疫苗需要什么佐剂?全细胞隐球菌疫苗的经验指向IFN-γ/TNF-α,其表达水平与保护效果明确相关,但这一相关性在mRNA平台仍是未知。唯有找到真菌mRNA疫苗的免疫保护相关因子,佐剂选择才有“导航仪”。平台不止线性一条路。传统线性mRNA之外,三员新将已登场:saRNA,细胞内自我扩增,抗原产量更高、更持久,剂量可更低;环状RNA,闭环结构,耐降解,表达窗口更长;taRNA, saRNA的“分体版”,扩增与抗原编码分离,调控更灵活。这可能是研制真菌mRNA疫苗低成本、低剂量、长持效的突破口。抗原筛选从“海捞”到“智选”。真菌基因数量庞大,选抗原如大海捞针;传统方法贡献不小,但效率有限。AI正在改写规则,深度学习可扫描已知抗原的表位特征,预测候选者。然而瓶颈依然存在:高质量的保护性抗原数据太少。AI再强,也需“喂料”。动物实验这个“笨办法”,依然是从预测走向保护不可绕过的关卡。mRNA疫苗从预防到治疗。真菌不只是“入侵者”,更是免疫破坏者:新生隐球菌借助Cpl1蛋白驱动M2极化,诱导2型免疫;白色念珠菌利用Cmi1蛋白干扰I型干扰素;烟曲霉则通过HscA蛋白抑制吞噬体成熟,实现免疫逃逸。这些免疫抑制因子,恰可作为治疗性疫苗的理想靶点。若用mRNA编码这些因子的失效版本,诱导机体产生中和抗体,便能卸掉真菌的“免疫刹车”,重启宿主防御。肿瘤mRNA疫苗已走通这条路,因此真菌治疗性疫苗不该被落下。总结与展望前方障碍不少:真菌太复杂,保护性抗原数据太少,佐剂规则待厘清。但工具箱正在快速丰富:saRNA/环状RNA拉低剂量门槛,AI加速抗原发现,中和抗体策略打开治疗新窗。把mRNA技术的迭代速度,与真菌—宿主互作机制的深层理解拧成一股绳。定制化真菌mRNA疫苗,已在路上。
✦ +
+
作者简介
李业奇 博士后
第一作者、通讯作者
机构:佐治亚大学
研究方向:病原真菌抗原鉴定及疫苗研发林晓蓉 教授
通信作者
机构:佐治亚大学
研究方向:病原真菌发育与分化、致病机制、预防与治疗
引用格式: Li Y, Lin X. Prospects for using mRNA vaccines against fungal infections. hLife 2026. https://doi.org/10.1016/j.hlife.2026.02.002.https://blog.sciencenet.cn/blog-3552961-1526656.html
上一篇:hLife | Call for Papers: Immune Reprogramming and Microenvir
下一篇:hLife Collection | Oncology
扫一扫,分享此博文