博文
癌症血液检测随处可见,它们真的有效吗?  精选
精选
|
癌症血液检测随处可见,它们真的有效吗?
研发厂商宣称这些检测能发现数十种癌症,但部分科学家表示,它们可能漏检大量癌症,或是给出错误诊断。
从人左臂抽取血样的特写镜头。
数十种血液检测(部分已上市销售)号称能捕捉癌症的特征信号。
一名男子坐在车里低头看着手机,屏幕上显示一行信息:未检测到癌症信号。男子闭上眼睛,如释重负地笑了。
这则电视广告上月在美国橄榄球“超级碗”期间播出,推广一款简易血液检测,宣称能发现50多种癌症的早期迹象,或是给出“一切正常”的安心结果。
这款名为Galleri的检测,是全球约40种多癌早筛(MCED) 检测之一,其中部分已上市,其余仍在研发中。但这些检测中,极少经过随机对照试验(RCT)——这一被视为检测“金标准”的验证,且尚无一款获得监管机构批准。
上月,Galleri的研发方、加州门洛帕克的生物技术公司Grail,公布了全球首个多癌早筛随机对照试验的部分细节。该试验与英国国民保健制度(NHS)合作开展,旨在探究:在现有筛查项目基础上联合使用Galleri,能否通过减少晚期癌症检出量来改善预后。但结果显示,该检测并未达到这一目标。
支撑这些检测的科学原理并不新鲜:研究人员早已知道,包括癌细胞脱落的DNA片段在内的癌症标志物,会出现在血液、唾液和尿液中。基于与多癌早筛相似技术的液体活检,已被医生广泛用于监测癌症进展、选择最佳治疗方案。然而,早期癌症检测要困难得多,因为血液中的肿瘤DNA含量极低。
部分研究者认为,多癌早筛有潜力彻底改变癌症检测与诊疗,尤其对尚无筛查手段的癌种意义重大。另一些人则持反对意见,指出这类检测会漏检许多甚至大部分早期癌症,对多数人而言,误诊带来的负面影响可能超过少数人从中获得的收益。
“检测结果为阴性固然令人安心,但你体内仍可能藏着癌症。”加州圣迭戈斯克里普斯转化科学研究所创始人、医师研究员埃里克·托波尔说,“就目前已有的数据来看,我认为推广这类检测是不负责任的。”
筛查现状
约五分之一的人一生中会罹患癌症,它是多数国家的主要死因,2022年全球约970万人死于癌症。癌症越早被发现,治疗通常创伤越小、成本越低,生存率也越高。
伦敦大学玛丽女王学院巴茨癌症研究所的癌症生物技术专家尼赞·罗森菲尔德表示,大多数癌症死亡都发生在确诊晚期,此时癌症已进展并扩散到身体其他部位。
“这主要是因为,我们主要依靠人们发现身体异常后再去就医。”他说,“唯一的解决办法,就是在癌症出现症状前就发现它。”
这正是各类筛查项目的目标:如乳腺癌的钼靶检查、结直肠癌的粪便检测与结肠镜检查、宫颈癌的宫颈涂片检查等。
然而,这些筛查项目远非完美。部分人觉得检测痛苦、尴尬或不便,因此参与率参差不齐。绝大多数癌症尚无对应的筛查手段。美国的预防性筛查项目仅能检出14%的确诊癌症,其余主要靠其他筛查或就医发现。
使用多癌早筛检测更多癌种,可能会增加假阳性概率——让无癌人群被告知可能患癌,可能引发焦虑,并需要进行有创的后续检查。对罕见癌症而言,这类风险更高,因为开发对应筛查本就更加困难。
尽管筛查已降低了癌症死亡率,但过去三十多年里,研究人员一直在寻找能进一步减轻疾病负担的新方法。多癌早筛的潜力在于操作简便,且有望更早发现更多癌症。
“我认为它们具有革命性潜力。”罗森菲尔德说,“在最理想的情况下,若有试验结果支持,它们将成为标准诊疗手段。”
血液中的线索
成熟的筛查技术通过生理或分子指标识别特定癌种,如钼靶中乳腺组织密度的变化。而多癌早筛的任务更难:仅靠一份血液样本,识别与多种癌症相关的生物标志物。
科学家早已知道,癌细胞会将自身的细胞和DNA片段释放到血液中。早期开发特定癌症血液检测的许多尝试,都是通过分析这些片段寻找已知的基因突变标志物。但由于这些癌症来源的物质浓度极低(尤其在早期),会被血液中大量其他游离DNA掩盖。例如,循环肿瘤DNA(ctDNA) 在血液游离DNA中占比可低至0.006%。
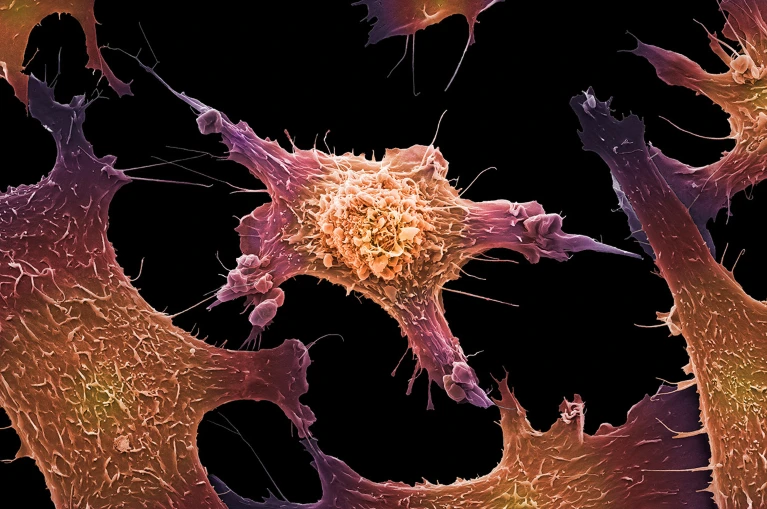
彩色扫描电镜下一团形态不规则的乳腺癌细胞。
肿瘤细胞(如这些乳腺癌细胞)会将DNA片段释放到血液中。
DNA测序速度与精度的提升,在一定程度上攻克了这一难题。2008年,马里兰州巴尔的摩市约翰斯·霍普金斯大学的肿瘤学家伯特·沃格尔斯坦证实,ctDNA可用于检测癌细胞存在,进而预测术后复发。
2014年,沃格尔斯坦及其团队进一步证明,他们能在75%以上的晚期胰腺癌、卵巢癌、结直肠癌、膀胱癌、乳腺癌等患者体内检测到ctDNA,并开发出名为CancerSEEK的检测,同时分析ctDNA与癌症蛋白,旨在检出8种常见癌症。该技术后续迭代为Cancerguard,一款可检测50多种癌症的多癌早筛产品,由威斯康星州麦迪逊市的Exact Sciences公司于去年商业化上市。
(在部分国家,多癌早筛可在无监管批准的情况下销售,但获批后能更方便地纳入保险、由医生开具处方。)
与此同时,血液中癌症DNA含量极低的问题,也促使其他研究者另辟蹊径。
“在血浆中寻找突变,就像在大海捞针,可能百万分之一的概率。”香港中文大学分子生物学家卢煜明说。
卢煜明开始从表观遗传变化——即基因组上开启或关闭基因的化学标记——入手分析血液中的DNA片段。其团队开发出一种可扫描全基因组寻找这类DNA甲基化标记的技术,并证实能定位体内肿瘤位置。
Grail公司于2017年收购了这项技术,并在此基础上开发出构成Galleri核心的检测方案。其他许多多癌早筛也基于血液游离DNA的甲基化模式分析,包括圣迭戈星炎基因的PanSeer、加州燃石医学的OverC等。
卢煜明等人还利用肿瘤DNA片段的物理特征(如片段长度、末端结构等与正常DNA的差异),来判断癌症位置与类型。
部分研发多癌早筛的团队与企业,正结合多种方法以提高准确性。例如,越南胡志明市医学遗传研究所团队开发的SPOT‑MAS,已在东南亚上市销售,该检测联合分析ctDNA的基因突变、甲基化状态与物理特性,可检测肝癌、乳腺癌、结直肠癌、胃癌和肺癌。
检测效果验证
要判断多癌早筛是否适合广泛推广,监管机构(如美国FDA)、医疗体系负责人及保险公司,会依据几项关键指标评估试验结果:
- 灵敏度:癌症患者中检测呈阳性的比例
- 特异度:无癌人群中检测呈阴性的比例
- 阳性预测值:检测阳性者中真正患癌的比例(取决于该病在受试人群中的常见程度)
汇总不同研究的系统评价发现,多癌早筛的特异度很高:能准确排除无癌人群的比例达96%~99.5%。但灵敏度差异较大:正确检出癌症患者的比例为30%~80%。
许多多癌早筛仅在已知患癌人群中开展过试验,这类试验结果未必能代表普通人群。为此,另有研究招募无癌症病史者并长期随访。
其中一项试验在65~75岁无癌女性中评估了CancerSEEK血液检测:它能98.9%准确排除无癌者,联合医学影像后可达99.6%;但研究期间确诊的96例癌症中,仅26例被成功检出。
2023年发表的Galleri试验结果呈现相似趋势:无癌人群的阴性结果准确率为99.1%,但92例阳性结果中,仅38%最终确诊癌症。
去年10月,Grail公布了一项更大规模随访研究的未发表初步结果:在2.3万名50岁以上、无癌史且接受过乳腺癌、宫颈癌、结直肠癌、肺癌标准筛查的人群中,Galleri阳性者最终确诊癌症的概率为61.6%。
“检测阳性时,几乎一半结果其实是假的。”英国牛津大学血液学家、肿瘤学家安娜·舒赫说,她正研发一款结合多种检测手段以提高精度的多癌早筛。
批评者还质疑该公司对数据的部分处理方式:原始研究纳入超3.5万名受试者,但结果仅覆盖其中一部分。包括舒赫在内的9名研究者在致《柳叶刀·肿瘤学》的公开信中写道,媒体基于新闻稿里“精心挑选的性能指标”进行报道,是“受商业驱动、过早将未经同行评审的数据包装成突破性成果”。
Grail发言人上月回应称,分析基于首批2.5万名有一年随访数据的受试者,今年晚些时候计划提交全部3.5万人队列的完整结果用于发表。
 NHS‑Galleri试验是全球首个多癌早筛随机对照试验。
NHS‑Galleri试验是全球首个多癌早筛随机对照试验。
上月,NHS‑Galleri试验也公布了部分核心结果:约14.2万名50~77岁无症状受试者同时接受常规筛查,随机分为两组——一组连续三年每年做Galleri检测,另一组仅抽血不做检测。试验旨在验证:相比单独常规筛查,Galleri能否减少晚期(3、4期)癌症确诊量。
该试验的主要终点未达到统计学显著差异。但公司表示,其他试验数据证明该检测仍有价值。Grail首席科学官兼国际总裁哈帕尔·库马尔称,在同时接受标准筛查的人群中,“每年使用Galleri筛查者的癌症检出率提升了四倍”;在导致三分之二癌症死亡的12种癌种中,4期确诊量也“显著下降”。
英国NHS发言人表示:“这一证据是重要一步,NHS将在未来数月仔细研究这项大型试验的完整结果。”
面临的挑战
即便多癌早筛能成功更早发现癌症,部分批评者仍质疑这能否真正转化为临床获益。例如,检测可能更早发现危险性较低、更易治疗的癌症,却漏检更致命、侵袭性更强的癌症。
“只有能改善患者预后,癌症早筛才有真正意义。”加拿大蒙特利尔麦吉尔大学研究液体活检的分子与细胞生物学家朱莉娅·伯尼尔说,“这类检测是否影响总生存率,仍是悬而未决的问题。”
包括Grail、Exact Sciences在内,多数多癌早筛支持者都表示,这类检测应作为现有筛查的补充,而非替代。但部分公共卫生研究者认为,过早广泛推广仍可能带来严重的意外后果。
英国剑桥大学公共卫生医师、英国国家筛查委员会多癌检测工作组成员汤姆·卡伦德表示,尽管现有多癌早筛覆盖很多癌种,但对已有成熟筛查的癌种,灵敏度并不高。
“风险在于,人们以为自己没事,就不去做已有的标准筛查,这可能导致更多本可避免的死亡。”
Grail与Exact Sciences均表示,其研究中未发现检测会影响标准筛查的依从性。Exact Sciences多癌早筛首席医疗官汤姆·比尔补充道,这类检测满足了未被满足的需求:检出尚无推荐筛查手段的癌症。
部分研究者认为,支撑多癌早筛的技术,在大规模预防性筛查之外可能有更大潜力,例如帮助医生为个体选择最佳治疗方案。2025年5月,英国政府宣布,基于ctDNA的液体活检将通过NHS面向英格兰的肺癌与乳腺癌患者开放。这类检测比传统活检更快确诊和分型肺癌,并能识别出可能受益于靶向治疗的晚期乳腺癌患者。
这类检测也可能适用于癌症高风险人群筛查,如有家族遗传史者。
“我相信未来会出现更精准的检测。”托波尔说,“在高风险人群(如遗传易感者)中,它们会非常有用。”
一个快速发展的方向是:用液体活检判断手术或其他治疗后体内是否仍残留癌细胞,肿瘤学界称之为微小残留病灶检测。多款此类检测已投入临床,更多仍在研发中。
卡伦德表示,多癌血液检测的应用存在争议并不意外,因为该领域仍处于起步阶段。
“我认为我们远未达到广泛推广的阶段,但这是一项令人兴奋的技术。如果应用得当,它未来有望成为癌症防控体系中的重要一环。”
https://blog.sciencenet.cn/blog-41174-1524425.html
上一篇:人工智能能编写基因组——距离创造合成生命还有多久?
下一篇:氢气预防人工皮肤UVA老化的转录组学评估