博文
吸入氢气通过PTEN诱导激酶1 Parkin通路调控SH-SY5Y细胞和小鼠线粒体自噬减轻脑缺血再灌注损伤
||
吸入氢气通过PTEN诱导激酶1 Parkin通路调控SH-SY5Y细胞和小鼠线粒体自噬减轻脑缺血再灌注损伤
背景
脑缺血/再灌注损伤(CIRI)在脑血流恢复后会造成严重的神经元损伤,线粒体功能障碍是该过程的核心病理驱动因素。氢气(H₂)已在多种神经系统疾病模型中展现出良好的神经保护作用,但氢气是否通过调控线粒体自噬及其上游信号通路来减轻CIRI,目前尚不明确。
方法
体内实验:选用雄性C57BL/6小鼠建立大脑中动脉栓塞/再灌注(MCAO/R)模型,随机分为3组:假手术组、MCAO/R组、MCAO/H₂组。
体外实验:人神经母细胞瘤SH-SY5Y细胞建立氧糖剥夺/复氧(OGD/R)模型,分为4组:对照组、OGD/R组、OGD/R+H₂组、OGD/R+H₂+ML385组(ML385为Nrf2特异性抑制剂,OGD前1h预处理)。
检测指标:神经功能缺损评分(Zea-Longa)、TTC染色测脑梗死体积、HE/尼氏/TUNEL染色评估病理损伤与凋亡、CCK-8测细胞活力、流式细胞术检测细胞凋亡、线粒体活性氧(ROS)、线粒体膜电位(MMP)、Western Blot定量蛋白表达。
结果
体内实验显示,吸入氢气显著改善MCAO/R小鼠神经功能缺损、减小脑梗死体积、减轻组织病理损伤、抑制神经元凋亡并促进线粒体自噬。
在SH-SY5Y细胞中,氢气处理显著提高细胞活力、减轻氧化应激与线粒体功能障碍,并通过激活PINK1/Parkin通路增强线粒体自噬。
机制上,氢气维持细胞氧化还原稳态、清除受损线粒体、上调Nrf2/HO-1抗氧化通路、抑制NF-κB介导的炎症信号。值得注意的是,使用ML385抑制Nrf2可显著逆转氢气对OGD/R损伤细胞的线粒体保护与抗凋亡作用。
结论
本研究表明,氢气通过减轻氧化应激、抑制神经元凋亡、改善线粒体功能发挥显著的抗脑缺血/再灌注损伤神经保护作用。这些效应与激活Nrf2/PINK1/Parkin介导线粒体自噬通路密切相关,提示氢气可作为治疗脑缺血/再灌注损伤的潜在方法。
引言
缺血性卒中是全球性公共卫生难题,具有高发病率、高死亡率和高致残率,尤以老年人群最为突出。脑缺血缺氧后,神经元与神经血管单元发生进行性结构和功能损伤。尽快实现闭塞脑血管再通、恢复血流灌注,是挽救缺血半暗带存活神经元的主要临床策略。然而,再灌注过程常引发继发性病理损伤,即脑缺血/再灌注损伤,进一步加重神经功能缺损并降低血管再通治疗效果。
脑缺血/再灌注损伤的发病机制极为复杂,涉及过度氧化应激、炎症反应激活、线粒体功能障碍、凋亡信号级联反应及自噬紊乱等。越来越多的证据证实,过度氧化应激及其继发的线粒体损伤是脑缺血/再灌注损伤发生发展的核心环节。过量活性氧直接激活核因子κB炎症通路,破坏线粒体膜完整性,降低线粒体膜电位,触发内源性凋亡通路,最终导致大量神经元死亡。线粒体是维持细胞能量代谢与氧化还原稳态的关键细胞器,其功能障碍与脑缺血/再灌注损伤的发生密切相关。线粒体自噬是一种选择性自噬,可特异性靶向清除受损线粒体,维持线粒体质量控制与细胞稳态。通过线粒体自噬高效清除受损线粒体,被认为是减轻脑缺血/再灌注损伤的关键治疗靶点。PTEN诱导激酶1(PINK1)/Parkin通路是介导线粒体自噬的经典且研究最为透彻的信号轴。
已有研究证实,核因子E2相关因子2(Nrf2)信号通路是抵御氧化应激与线粒体功能障碍的重要细胞防御机制。Nrf2核内高表达可促进下游抗氧化酶的转录生成,包括血红素氧合酶1(HO-1)、NAD(P)H醌氧化还原酶1(NQO1)和超氧化物歧化酶(SOD),从而减轻氧化损伤并维持线粒体功能。Nrf2与核因子κB的交互作用,共同调控脑缺血损伤中抗氧化反应与炎症进程的平衡,使Nrf2成为脑缺血/再灌注损伤的潜在治疗靶点。
氢气(H₂)是分子量最小且生物学惰性的双原子分子,因其生物安全性好、高透膜性(可透过血脑屏障)及选择性抗氧化特性,成为转化医学领域新型治疗气体。既往研究已证实氢气在脑缺血/再灌注损伤模型中的神经保护作用,但其分子机制尚未完全阐明,尤其是氢气、Nrf2信号与PINK1/Parkin介导线粒体自噬之间的调控关系仍不明确。尽管已有文献报道氢气在脑缺血中的抗氧化与抗凋亡作用,但尚无研究在体内外脑缺血/再灌注损伤模型中系统验证Nrf2-PINK1/Parkin-线粒体自噬这一连续调控轴。
本研究旨在探讨吸入氢气对脑缺血/再灌注损伤的神经保护作用,并揭示其可能通过Nrf2/PINK1/Parkin通路介导线粒体自噬的分子机制,为氢气用于缺血性卒中临床治疗提供新的实验依据。
材料与方法
实验动物
SPF级雄性C57BL/6成年小鼠,体重25±2 g,购自辽宁长生生物技术有限公司(许可证号:SCXK(辽)2020-016)。小鼠饲养于温度22±2℃、湿度55±5%、12 h明暗交替环境,自由摄食饮水,适应性饲养3天后开始实验。采用随机数字表法将小鼠分为3组(每组n=12,共40只);纳入标准为MCAO造模成功(术后神经功能缺损评分≥1分)、体重23–27 g且术前无异常;因手术失败或过早死亡剔除4只,符合预设纳入排除标准。
所有动物实验经哈尔滨医科大学实验动物伦理委员会批准(批准号:2024-DWSYLLCZ-53),并严格遵循ARRIVE指南执行。
大脑中动脉栓塞/再灌注模型制备与氢气处理
所有手术由同一熟练研究者操作以减少误差。腹腔注射戊巴比妥钠(50 mg/kg)麻醉小鼠,颈正中切口暴露右侧颈总动脉、颈外动脉与颈内动脉,采用硅胶线栓法插入颈内动脉阻断大脑中动脉,缺血2 h后拔线栓实现24 h再灌注。假手术组仅进行相同手术操作但不插入线栓;MCAO/H₂组于再灌注0 h和12 h吸入67%氢气+33%氧气混合气体,流量1.5 L/min,每次3 h,在通风防爆通风橱内进行并实时监测气体浓度确保安全,操作区域无明火及静电源。假手术组与MCAO/R组在相同条件下吸入正常空气。再灌注24 h后,深度麻醉下颈椎脱臼处死小鼠,快速取脑组织用于后续检测。实验设计见图1A。
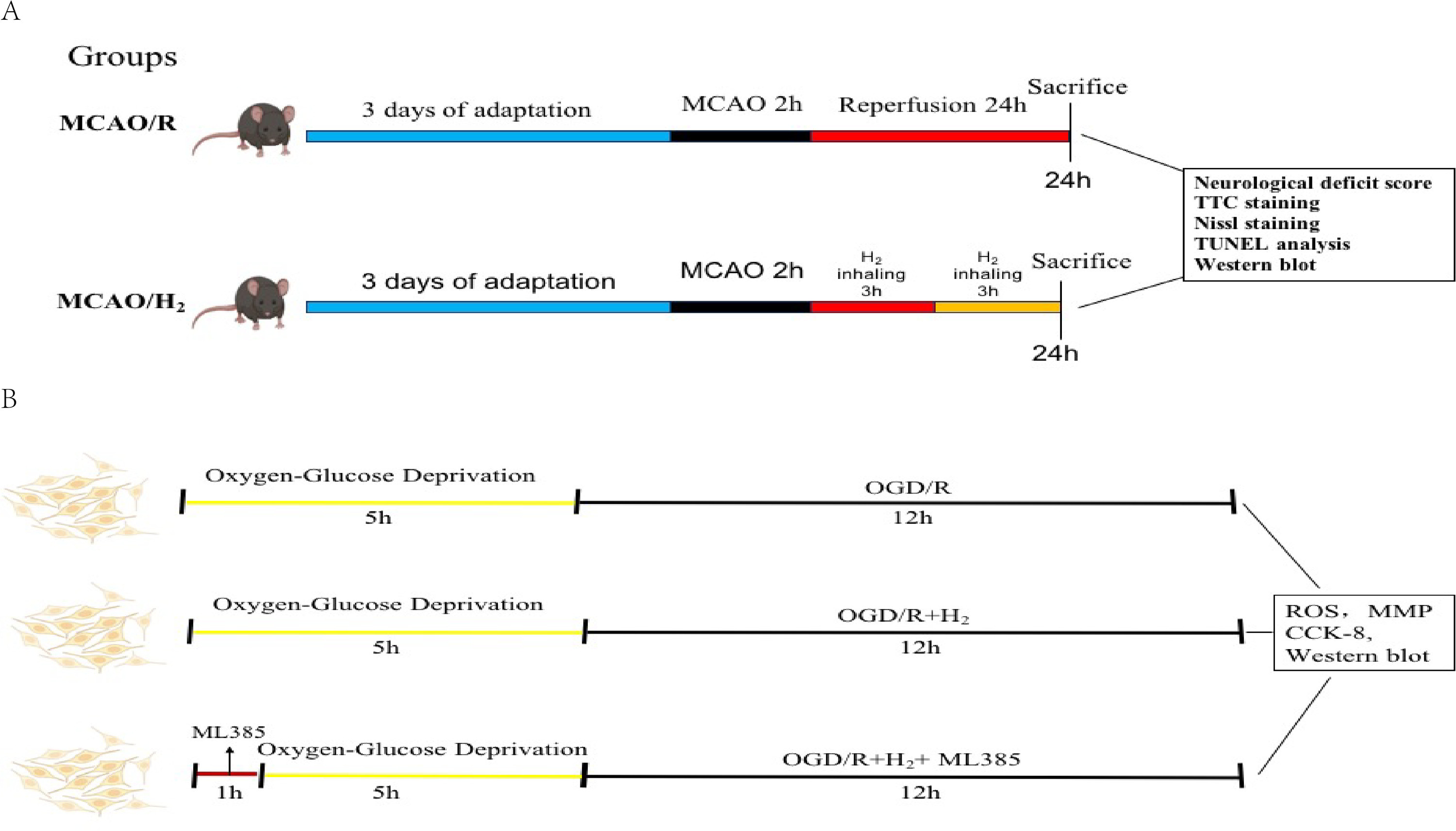
图1 实验设计流程图
(A)大脑中动脉栓塞/再灌注(MCAO/R)小鼠模型及氢气(H₂)吸入治疗的动物实验设计;(B)SH-SY5Y细胞氧糖剥夺/复氧(OGD/R)模型、氢气处理及Nrf2抑制剂干预的体外实验设计。样本量与统计学详情见相应图注。
细胞培养与氧糖剥夺/复氧模型构建
人神经母细胞瘤SH-SY5Y细胞购自碧云天生物技术公司(C6823),培养于含10%胎牛血清及1%青链霉素双抗的DMEM/F12培养基中,置于37℃、5% CO₂培养箱。构建氧糖剥夺/复氧模型模拟体外脑缺血/再灌注损伤:细胞置于无糖DMEM/F12培养基,放入厌氧培养袋建立厌氧环境(O₂浓度<0.1%,5% CO₂)培养5 h,随后恢复正常培养条件复氧12 h。氢气处理组于复氧期间置于67%氢气+33%氧气混合气体环境。抑制实验于氧糖剥夺前1 h加入5 μM Nrf2特异性抑制剂ML385(溶于二甲基亚砜)。细胞分为4组:正常对照组、氧糖剥夺/复氧组、氧糖剥夺/复氧+氢气组、氧糖剥夺/复氧+氢气+ML385组。设置二甲基亚砜溶剂对照组排除溶剂干扰。实验设计见图1B。
神经功能缺损评分
再灌注24 h后,由两名独立盲法评估者采用Zea-Longa 5分制评分法评估神经功能缺损:0分=无神经功能缺损;1分=对侧前肢不能完全伸展;2分=向对侧转圈;3分=向对侧倾倒;4分=无自主活动且意识抑制。
脑梗死体积检测
新鲜脑组织于-80℃冷冻5 min,冠状切为2 mm厚度切片,2% 2,3,5-氯化三苯基四氮唑(TTC)37℃避光染色20–30 min,4%多聚甲醛固定24 h后拍照,采用ImageJ软件定量梗死体积,以损伤区域占全脑体积百分比表示。
组织病理与凋亡分析
脑组织固定、脱水、石蜡包埋后制作4 μm切片,行HE染色与尼氏染色观察神经元形态损伤与尼氏体完整性;TUNEL凋亡检测试剂盒检测神经元凋亡,盲法评估者于光学显微镜200倍下计数TUNEL阳性细胞。
细胞活力、活性氧与线粒体膜电位检测
采用CCK-8试剂盒于450 nm处检测细胞活力,计算公式:细胞存活率=100%×(实验组OD值-空白组OD值)/(对照组OD值-空白组OD值)。DCFH-DA荧光探针试剂盒结合流式细胞术检测线粒体活性氧水平;JC-10试剂盒结合流式细胞术检测线粒体膜电位,评估线粒体膜完整性。所有体外实验至少进行3次独立生物学重复。
蛋白质印迹法
含苯甲基磺酰氟的RIPA裂解液提取细胞与脑组织总蛋白,BCA试剂盒定量蛋白浓度。取20 μg蛋白经10%–12.5% SDS-PAGE电泳分离,转印至硝酸纤维素膜,5%脱脂牛奶封闭,4℃孵育一抗:微管相关蛋白轻链3(LC3)、PINK1、Parkin、Bcl-2、Bax、Caspase-3、Nrf2、血红素氧合酶1(HO-1)、甘油醛-3-磷酸脱氢酶(GAPDH),随后孵育辣根过氧化物酶标记二抗,化学发光成像系统显影,ImageJ软件分析条带灰度值。
统计学分析
所有实验数据采用GraphPad Prism 9.0软件分析,以均数±标准差(x±s)表示。两组间比较采用非配对t检验;多组间比较采用单因素方差分析(ANOVA),后续行Tukey事后检验。P<0.05为差异具有统计学意义。生物学重复数(n)标注于各图注中。所有结局评估与数据分析均采用双盲法进行。
结果
氢气吸入减轻MCAO/R诱导的脑损伤、神经功能缺损与组织病理损伤
为评估氢气对MCAO/R诱导脑损伤的治疗潜力,构建小鼠MCAO模型并给予氢气再灌注治疗24 h。TTC染色显示,与假手术组相比,MCAO/R组脑梗死体积(白色区域)显著增大(P<0.01),而氢气吸入可显著减小MCAO/H₂组梗死体积(P<0.01)(图2A、2B)。MCAO/R组Zea-Longa评分显著高于假手术组(P<0.01),氢气治疗可显著改善神经功能(P<0.05)(图2C)。以上结果表明氢气可改善小鼠MCAO/R诱导的脑损伤。

图2 氢气吸入减轻MCAO/R诱导的脑损伤、神经功能缺损与组织病理损伤
(A、B)各组脑缺血24 h后冠状位TTC染色代表性图像与脑梗死体积定量分析(n=3);(C)各组神经功能缺损评分(Zea-Longa评分,n=3);(D、E)各组缺血皮层与海马区组织病理改变的HE染色与尼氏染色代表性图像(n=3;放大倍数×200,标尺10 μm)。数据以均数±标准差表示。*P<0.05,P<0.01,MCAO/R组与假手术组或MCAO/H₂组比较。
HE与尼氏染色评估神经元组织病理改变。HE染色显示,MCAO/R组出现严重神经元坏死、水肿与结构紊乱,而MCAO/H₂组组织病理损伤显著缓解,神经元形态接近正常(图2D)。尼氏染色显示,MCAO/R组尼氏体大量丢失,氢气治疗可显著恢复尼氏体水平(图2E)。上述结果证实,氢气吸入可有效缓解MCAO/R诱导的脑损伤。
氢气提高SH-SY5Y细胞活力并减轻OGD/R诱导的氧化应激与线粒体损伤
体外进一步验证氢气对脑缺血/再灌注损伤的神经保护作用。缺氧处理后采用CCK-8法检测细胞活力。结果显示,氧糖剥夺/复氧处理使SH-SY5Y细胞活力显著降至34.5±4.45%(P<0.01,与对照组相比),而氢气治疗使细胞活力恢复至68.00±3.08%(P<0.05,与氧糖剥夺/复氧组相比)(图3A)。

图3. 氢气提高SH‑SY5Y细胞活力,减轻氧糖剥夺/复氧诱导的氧化应激与线粒体损伤
(A) CCK‑8法检测SH‑SY5Y细胞活力。(B、C)流式细胞术检测细胞内活性氧(ROS)水平的代表性荧光图与定量分析,对SH‑SY5Y细胞荧光强度进行定量。(D、E)流式细胞术检测线粒体膜电位(MMP)的JC‑10染色代表性图像,低膜电位以统计直方图展示。数据以均数±标准差表示,来自三次独立实验(每组n=3)。*P<0.05,P<0.01,OGD/R组与空白对照组或OGD/R+H₂组比较。
随后检测多项氧化应激与线粒体功能相关标志物,进一步证实氢气的保护作用。流式结果显示,OGD/R显著升高线粒体ROS水平(P<0.05),而氢气处理可使其明显降低(P<0.05)(图3B、C)。OGD/R导致线粒体膜电位显著下降(绿色荧光增强),氢气处理则维持膜电位并使红色荧光增强(P<0.05)(图3D、E)。以上结果表明,氢气可有效抑制OGD/R损伤神经元的氧化应激并改善线粒体功能。
氢气在MCAO/R小鼠中激活Nrf2/HO‑1通路并抑制NF‑κB信号
Nrf2是关键的氧化还原敏感转录因子,可调控多种抗氧化防御基因(如HO‑1)表达,以抵御氧化应激损伤与线粒体功能障碍。为明确Nrf2通路是否参与氢气的神经保护作用,采用蛋白质印迹法检测Nrf2及其下游抗氧化酶HO‑1的表达。
结果显示,MCAO/R组Nrf2与HO‑1蛋白表达上调(P<0.01,与假手术组比),氢气处理可进一步显著升高二者表达(P<0.05、P<0.01,与MCAO/R组比)(图4A、B)。
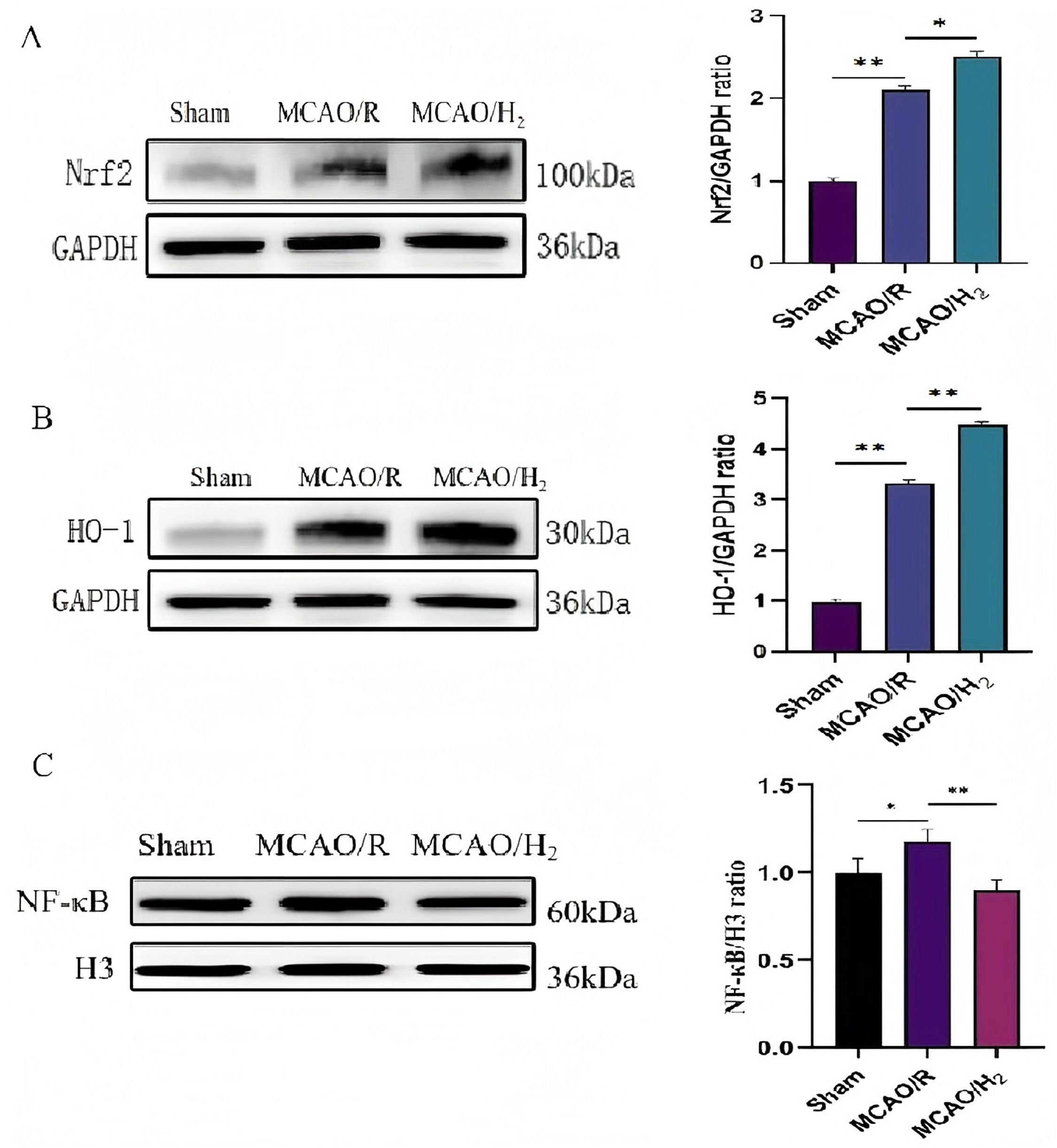
图4. 氢气在MCAO/R小鼠中激活Nrf2/HO‑1通路并抑制NF‑κB信号
蛋白质印迹法检测并统计Nrf2(A)、HO‑1(B)及细胞核NF‑κB(C)蛋白表达水平。数据以均数±标准差表示(每组n=3)。*P<0.05,P<0.01,MCAO/R组与假手术组或MCAO/H₂组比较。
既往研究表明,ROS可通过促进IκBα磷酸化激活NF‑κB,进而调控细胞NF‑κB信号通路活性。为探究氢气吸入是否影响NF‑κB活化,检测NF‑κB p65亚基的核转位。氢气处理可显著抑制MCAO/R诱导的NF‑κB p65核转位(P<0.01),提示其抑制NF‑κB介导的炎症信号(图4C)。上述结果证实,氢气通过激活Nrf2/HO‑1通路发挥抗氧化与抗炎作用。
氢气增强MCAO/R小鼠PINK1/Parkin介导线粒体自噬并抑制神经元凋亡
为探究线粒体自噬在氢气神经保护中的作用,检测关键线粒体自噬相关因子的蛋白表达。MCAO/R组线粒体自噬相关蛋白PINK1、Parkin及LC3‑II/LC3‑I比值升高(P<0.01、P<0.05),氢气处理可进一步显著升高(P<0.01、P<0.05),提示线粒体自噬增强(图5A‑5C)。TUNEL染色显示,MCAO/R组凋亡神经元显著增多(P<0.001,与假手术组比),氢气可使其明显减少(P<0.01)(图6A、6B)。蛋白质印迹显示,氢气显著下调促凋亡蛋白Bax、Caspase‑3,上调抗凋亡蛋白Bcl‑2(P<0.05或P<0.001,与MCAO/R组比)(图6C‑6E)。
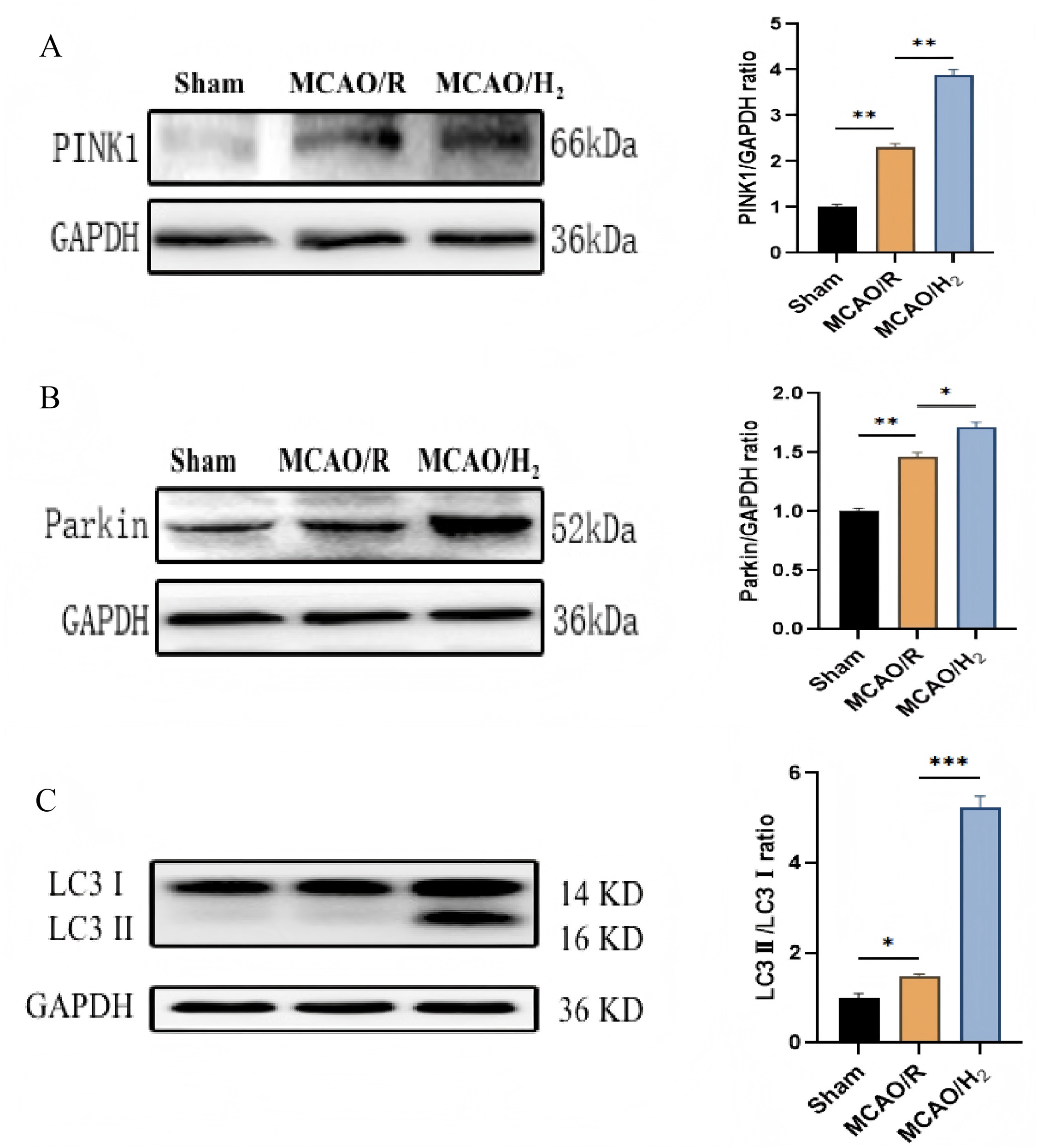
图5. 氢气增强MCAO/R小鼠PINK1/Parkin介导线粒体自噬
代表性蛋白质印迹条带与定量分析:PINK1(A)、Parkin(B)、LC3‑II/I(C)。数据以均数±标准差表示(每组n=3)。*P<0.05,P<0.01,*P<0.001,MCAO/R组与假手术组或MCAO/H₂组比较。
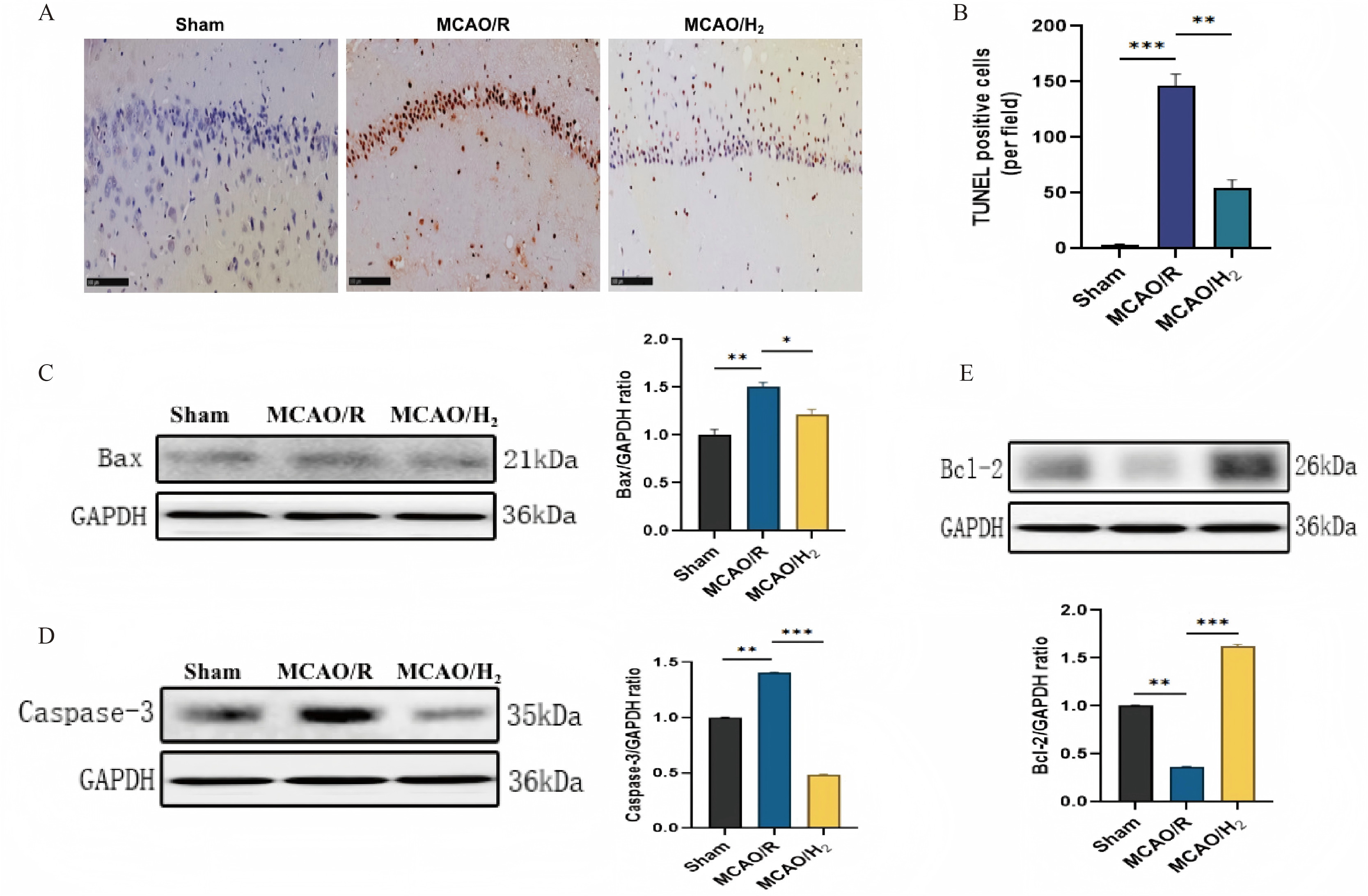
图6. 氢气吸入通过抑制神经元凋亡对MCAO/R小鼠发挥神经保护作用
(A、B)缺血侧海马区TUNEL染色代表性图像(放大倍数×200,标尺10μm)及TUNEL阳性凋亡细胞定量分析(每组n=3)。缺血脑组织中Bax(C)、Caspase‑3(D)、Bcl‑2(E)蛋白表达的代表性印迹与定量结果(每组n=3)。数据以均数±标准差表示。*P<0.05,P<0.01,*P<0.001,MCAO/R组与假手术组或MCAO/H₂组比较。
Nrf2抑制剂ML385逆转氢气对OGD/R损伤SH‑SY5Y细胞的神经保护作用
为进一步验证Nrf2参与氢气的神经保护作用,使用Nrf2特异性抑制剂ML385,体外检测线粒体自噬与凋亡相关标志物蛋白表达。ML385预处理可显著逆转氢气诱导的OGD/R细胞PINK1、Parkin上调及LC3‑II/LC3‑I比值升高(P<0.01,与OGD/R+H₂组比)(图7A‑7C)。ML385还阻断氢气的抗凋亡作用,使Bax、Caspase‑3表达回升、Bcl‑2表达下降(P<0.05,与OGD/R+H₂组比)(图7D‑7F)。以上结果证实,Nrf2信号是氢气诱导线粒体自噬与神经保护的关键上游介质。

图7. Nrf2抑制剂ML385逆转氢气对OGD/R损伤SH‑SY5Y细胞的神经保护作用
代表性蛋白质印迹条带与定量分析:PINK1(A)、Parkin(B)、LC3‑II/I(C)、Bax(D)、Caspase‑3(E)、Bcl‑2(F)。数据以均数±标准差表示,来自三次独立实验(每组n=3)。*P<0.05,P<0.01,*P<0.001,OGD/R组与空白对照组、OGD/R+H₂组,以及OGD/R+H₂组与OGD/R+H₂+ML385组比较。
细胞实验中,Nrf2抑制剂ML385实验加入DMSO溶剂对照组以进行严格对照分析,结果显示ML385显著抑制线粒体自噬(补充图1)。
综上所述,氢气吸入可显著减轻体内外MCAO/R与OGD/R诱导的神经元损伤,其机制部分依赖激活Nrf2/HO‑1通路并维持线粒体稳态(图8)。
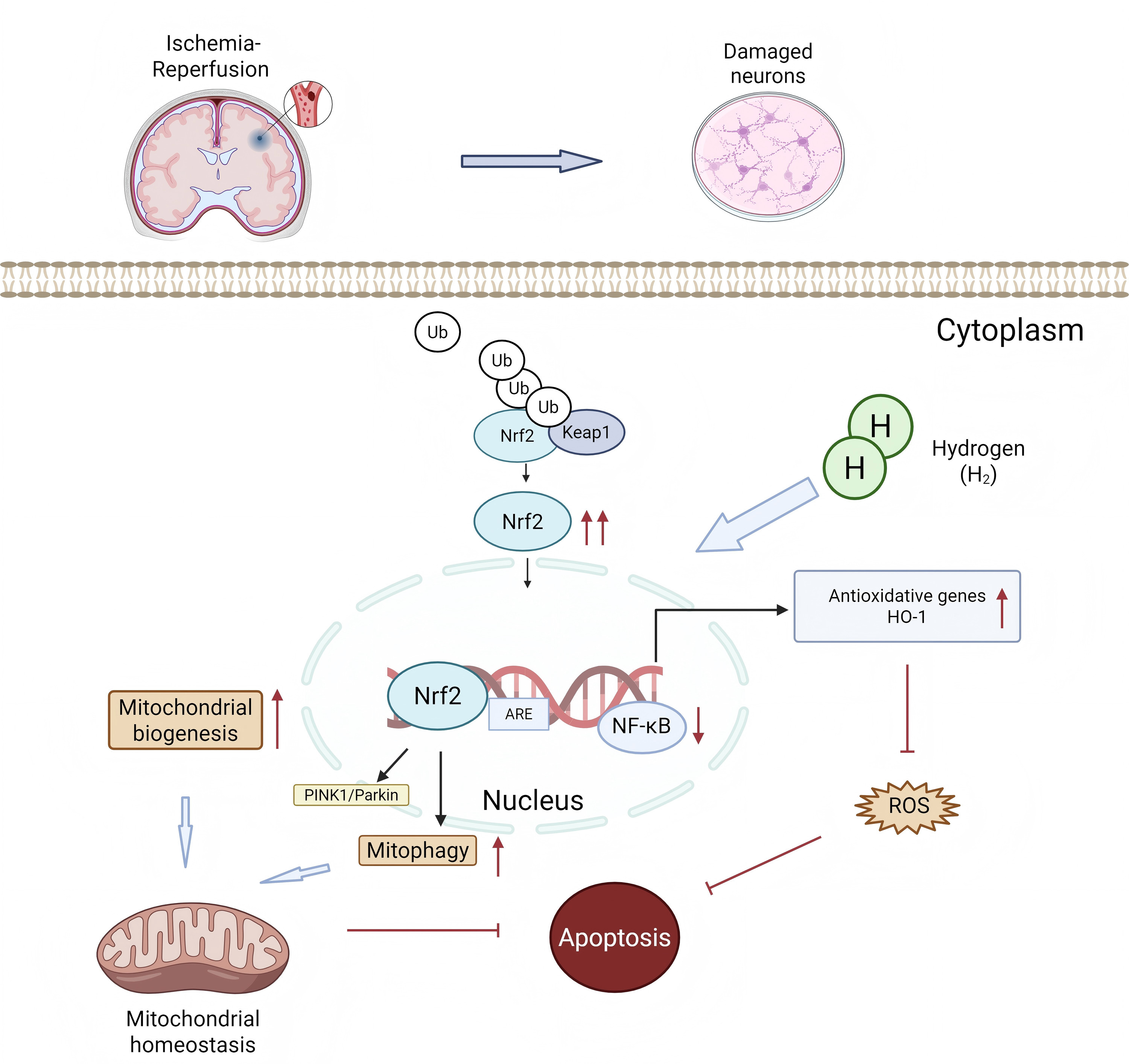
图8. 氢气抗脑缺血再灌注损伤神经保护机制模式图
氢气干预促进Nrf2核转位,抑制过量ROS生成,增强PINK1/Parkin介导线粒体自噬。上述效应共同改善线粒体功能、抑制神经元凋亡,最终减轻脑缺血再灌注损伤与神经功能缺损。
---
讨论
缺血性卒中是全球长期致残的主要原因,脑缺血再灌注损伤(CIRI)仍是临床有效再通治疗的主要障碍。线粒体功能障碍与过度氧化应激是CIRI核心病理机制,靶向调控线粒体自噬以维持线粒体稳态已成为极具前景的治疗策略。线粒体自噬可选择性清除受损线粒体,避免ROS堆积与凋亡信号激活,对缺血再灌注后神经元存活至关重要。
氢气因生物安全性高、可透过血脑屏障、具有选择性抗氧化能力,在神经领域研究中备受关注,但其抗CIRI的精确机制尚未完全阐明。氢气不仅可选择性清除内源性毒性ROS,还可作为细胞内信号分子与缓冲剂。自2007年发现氢气对脑缺血再灌注损伤具有神经保护作用以来,越来越多临床前证据证实其可抑制神经元凋亡、减轻氧化应激。
本研究证实,氢气吸入可在体内MCAO/R小鼠与体外OGD/R神经元模型中有效缓解CIRI,减小脑梗死体积、改善神经功能、抑制氧化应激与神经元凋亡、增强线粒体功能。本研究的创新点在于:证实Nrf2/PINK1/Parkin通路是氢气促进线粒体自噬的关键调控轴,这在既往氢气神经保护研究中尚未得到系统验证。
MCAO模型是CIRI研究的常用模型,可稳定产生可靠的梗死体积,使实验动物出现中度脑损伤。为排除激素干扰,所有体内实验均采用雄性小鼠,因雌性雌激素、孕激素等周期性波动可影响线粒体功能与自噬流,产生固有神经保护作用,可能掩盖氢气效果。TTC染色是评估脑缺血损伤药物疗效的金标准,MCAO/R组梗死体积稳定在约40%,证实模型构建成功;氢气治疗后梗死体积与神经功能评分显著改善。组织学(HE、尼氏染色)进一步证实,氢气可显著缓解CIRI所致病理损伤,包括皮层与海马神经元丢失、尼氏体耗竭、排列紊乱、核固缩与空泡化。
机制上,本研究拓展既往发现:氢气通过激活Nrf2通路发挥抗氧化作用,上调下游抗氧化酶HO‑1,并通过PINK1/Parkin信号级联增强线粒体自噬,揭示氢气神经保护中Nrf2信号与线粒体自噬的全新分子关联。
SH‑SY5Y细胞可模拟神经元形态与生理功能,用于体外机制验证。CCK‑8结果显示,OGD/R显著降低细胞活力,氢气可显著提高存活率;氢气还可显著抑制OGD/R细胞线粒体ROS生成,证实其强抗氧化能力。线粒体膜电位是线粒体结构完整与功能稳定的核心指标,OGD/R 12h后严重受损,氢气可有效维持。以上结果证实,氢气的神经保护作用与改善线粒体功能、减轻氧化损伤密切相关。
转录因子Nrf2通过诱导解毒与抗氧化酶基因表达,成为线粒体功能与细胞氧化还原稳态的重要调控因子,广泛参与缺血性卒中进程。氧化应激状态下,Nrf2与胞质抑制蛋白Keap1解离,转入细胞核并结合抗氧化反应元件(ARE),驱动下游保护性基因表达,调控氧化还原平衡、能量代谢与解毒。本研究蛋白质印迹显示,氢气显著提高Nrf2蛋白表达;HO‑1作为Nrf2靶基因,在维持线粒体功能、抑制氧化应激损伤与细胞凋亡中起关键作用。既往研究表明,Nrf2激活可影响线粒体稳态与自噬,可能通过调控HO‑1等下游靶点实现。Nrf2特异性抑制剂ML385可减弱氢气在SH‑SY5Y细胞中的抗氧化与线粒体保护作用,证实Nrf2通路与氢气缓解CIRI相关。
除直接抗氧化外,Nrf2激活可拮抗线粒体ROS过量生成与脂质过氧化,维持线粒体功能。过量ROS还可通过促进IκBα磷酸化与NF‑κB p65核转位驱动NF‑κB激活,加剧炎症与凋亡级联反应。本研究发现,MCAO/R损伤增强NF‑κB p65核聚集,氢气可显著逆转,提示氢气在CIRI中还具有抗炎作用。
越来越多证据表明,Nrf2可结合PINK1启动子内的ARE序列上调PINK1表达,建立Nrf2信号与PINK1/Parkin介导线粒体自噬的调控关联。本研究中,氢气升高PINK1、Parkin蛋白水平并提高LC3‑II/LC3‑I比值,证实其在OGD/R模型中增强线粒体自噬。重要的是,ML385抑制Nrf2可消除氢气诱导的PINK1/Parkin上调与线粒体自噬激活,证实Nrf2信号是氢气促进线粒体自噬的上游介质。
氧化还原平衡与线粒体完整性是神经元存活与凋亡的核心调控因素。体内TUNEL染色显示,氢气吸入显著减少MCAO/R诱导的皮层与海马神经元凋亡;分子检测进一步显示,氢气上调抗凋亡蛋白Bcl‑2,下调促凋亡蛋白Bax与活化Caspase‑3,恢复Bcl‑2/Bax平衡,该平衡对维持线粒体膜稳定、阻止细胞色素C释放与凋亡级联激活至关重要。ML385同样可消除氢气的抗凋亡作用,证实Nrf2通路激活是氢气抑制CIRI神经元凋亡的必需环节。
本研究存在若干局限性:结论为初步结果,基于雄性小鼠与单一神经元细胞系;氢气吸入虽产生可测量的神经保护作用,但梗死体积与神经功能改善程度中等;需在更大动物模型中开展临床前研究验证。尽管存在局限,本研究仍为氢气作为CIRI潜在治疗手段提供了可靠实验证据。
结论
总之,氢气吸入通过减轻氧化应激、抑制神经元凋亡、恢复线粒体稳态发挥显著抗CIRI神经保护作用,这些有益效应由Nrf2/PINK1/Parkin信号通路激活及后续线粒体自噬增强所介导。
https://blog.sciencenet.cn/blog-41174-1533065.html
上一篇:氢气吸入对脑血流的影响大【新进展】
下一篇:美国学者提出氢气吸入剂量计算方法