博文
类胰蛋白酶激活体温中枢参与过敏时超低体温反应
|
过敏能引起哮喘,过敏可以产生严重的皮肤瘙痒,过敏可以导致休克甚至致命。但许多人不了解的是,过敏可以导致严重低血压和低温。最近科学家发现,过敏反应中重要的肥大细胞释放的最常见分子,类胰蛋白酶能作用于体温调节中枢,对体温中枢产生欺骗,让身体误认为体温过高,引起降低体温的反射活动,导致体温迅速下降。这一发现可能对于寻找新的治疗药物指明方向。甚至于给脓毒症治疗带来新策略。
花生会引起某些人危险的,有时甚至是致命的过敏反应,其特征是体温和血压急剧下降,以及呼吸困难。这种过敏性休克通常归咎于免疫系统进入超速状态。但一项针对小鼠的新研究指出了另一个罪魁祸首:神经系统。
Nervous system may play role in severe allergic reactions | Science | AAAS
今天3月17日发表在《科学免疫学》(Science Immunology)上的研究结果“与人们的想法一致,但实际上没有人能够证明,”皇后大学神经免疫学家塞巴斯蒂安·塔尔博特(Sebastien Talbot)说,这项工作可以为治疗人类严重过敏反应开辟新的靶点。
在美国,每年约有50人中有一人患有过敏反应。除了花生,蜜蜂蜇伤和一些药物是常见的触发因素。这些过敏原导致免疫系统的肥大细胞释放出一连串的组胺和其他分子,这些分子扩散到全身,扩张血管并缩小气道。发生过敏反应时,体温也会下降,使人感到寒冷和潮湿,尽管为什么会发生这种情况还不太清楚。

小鼠也会出现过敏反应。当暴露于过敏原时,小鼠会趴在地上伸展。这种行为是由中枢神经系统控制的,这一现象让杜克大学的免疫学家索曼·亚伯拉罕(Soman Abraham)怀疑神经也可能在严重过敏反应中发挥作用。
为了找到答案,他和同事们给小鼠卵清蛋白,蛋清中发现的主要蛋白质和已知的过敏反应触发因素,并使用电极和显微镜来记录和测量神经元活动。与人类一样,啮齿动物的体温下降了约10°C。 但是老鼠的大脑并没有将此记录为突然冻结。相反,通常对热量做出反应的大脑区域具有更高水平的活动。这种虚假的温暖感解释了为什么即使体温下降,动物也会伸展身体,好像它们过热一样。
但是,是什么告诉老鼠它们首先过热呢?研究人员专注于脊髓中的一组神经元,这些神经元在过敏反应期间显得特别活跃。当研究小组操纵神经元上的受体以有效地关闭它们时,动物在过敏反应期间没有冷却下来。另一方面,激活神经元即使没有接触过敏原,也会重新产生过敏反应的症状。
在实际的过敏反应中,肥大细胞似乎是这种现象的关键。研究小组发现,除了组胺之外,细胞还会释放一种叫做类胰蛋白酶的化合物,它与连接到调节体温的大脑区域的神经元相互作用。当研究小组阻止类胰蛋白酶的释放时,动物不再降低体温以应对过敏原。
20世纪70年代以来,人们通过酶组织染色法,利用胰蛋白酶对肥大细胞(MC)进行染色,发现肥大细胞能够被染色,说明肥大细胞中一定含有胰蛋白酶活性物质。1981年Schwartz等进一步纯化这种酶后发现,它是由MC释放的,其活性90%以上来自一种酶,故命名为类胰蛋白酶。
Miller等在1989年克隆了第一种类胰蛋白酶cDNA,其后又有几种类胰蛋白酶被克隆。肥大细胞类胰蛋白酶是由四个非共价结合的亚单位组成的四聚体结 构,四个亚单位有共同的抗原性,各有个 活性中心。该酶是肥大细胞分泌颗粒的主要成分,占肥大细胞分泌颗粒总蛋白质量的 50 %以上,是肥大细胞内含量最多的蛋白质,并以活性形式储存在肥大细胞的脱颗粒中,在其脱颗粒时释出胞外,作为肥大细胞及其脱颗粒的标志。
Talbot说,免疫学家长期以来一直认为组胺是过敏反应的主要参与者,所以令他惊讶的是,类胰蛋白酶和神经系统似乎也起着重要作用。“找到一种新的介质,实际上触发了神经元和[免疫]细胞之间的串扰,这很酷。
该研究可以为治疗人类过敏反应提供新的靶点。患有严重过敏反应的人通常必须携带EpiPen,一旦反应开始,它就会提供肾上腺素注射以阻止反应。但一直缺乏预防性治疗。
通过靶向类胰蛋白酶或其激活神经元的受体来阻断免疫细胞和神经元之间通信的药物可能是帮助患有严重过敏反应的个体的一种方法,杜克大学的免疫学家Evangeline Bao说。因为这些将针对反应的根本原因,而不是像EpiPen那样仅仅缓解症状,这可能是一个更好的策略 - 而且是一个更具预防性的策略,她说。
Bao说,免疫系统和神经系统之间的串扰也可能在其他严重反应中发挥作用。她和她的同事现在正在研究这种沟通如何在败血症中发挥作用,败血症是身体对感染的过度反应。与全身过敏反应一样,脓毒症是对伤害的过度反应。在这种情况下,免疫细胞释放可能损害器官的炎症分子,在某些情况下导致死亡。
Talbot警告说,“应用还有很长的路要走。不过,这项研究肯定会引发该领域的大量研究。”
原论文摘要
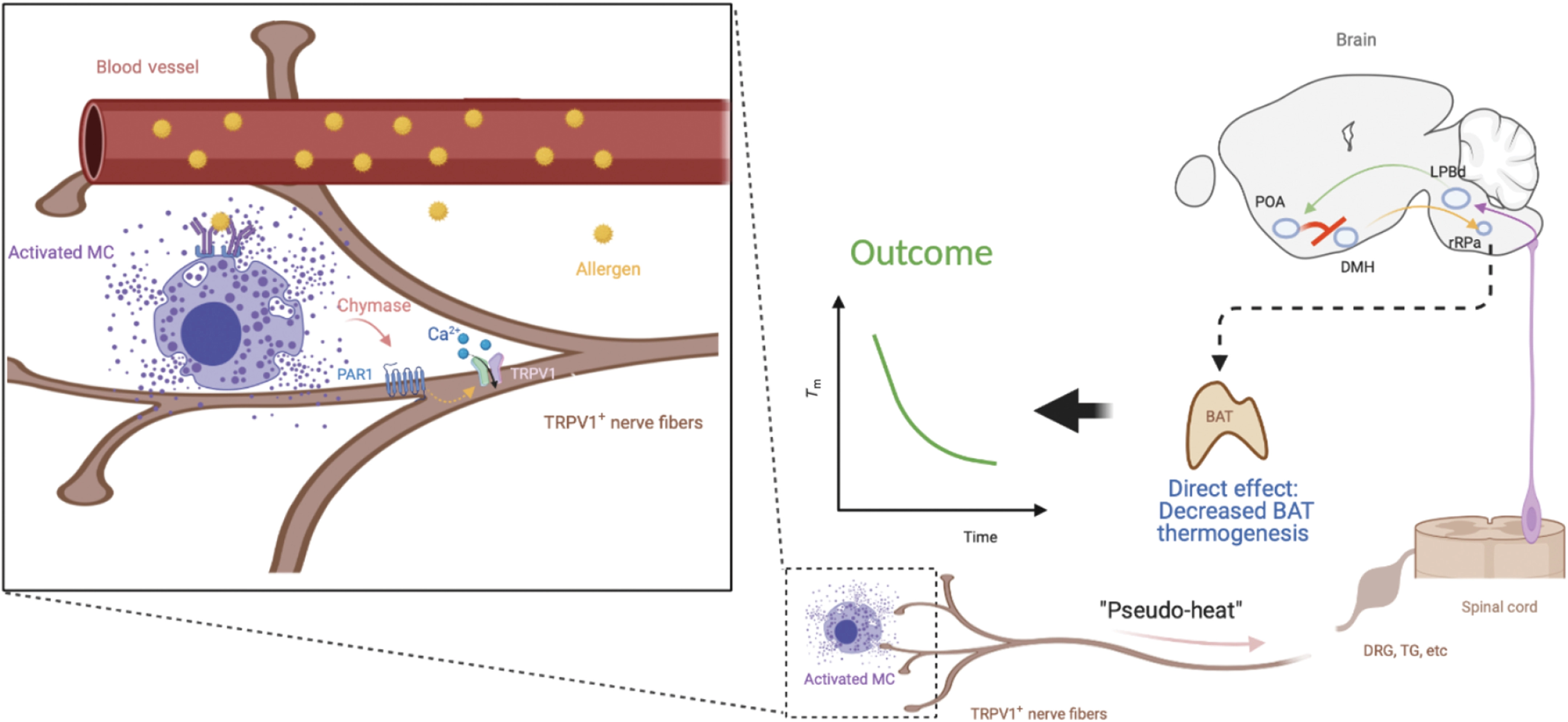
IgE 介导的全身性过敏反应是对变应原(包括某些食物和毒液)的一种危及生命的急性全身反应。当血源性变应原激活全身 IgE 结合的血管周围肥大细胞 (MC) 时,会触发全身性过敏反应,从而导致肥大细胞介质的广泛全身释放。通过诱发血管舒张和血管渗漏,这些介质被认为会引发人类血压和动物核心体温急剧下降。我们报告说,与过敏反应相关的小鼠IgE / 肥大细胞介导的体温下降也需要身体的体温调节神经回路。当来自肥大细胞的颗粒状类胰蛋白酶沉积在近端TRPV1感觉神经元上并通过蛋白酶激活的受体-1刺激它们时,该回路被激活。这会触发人体体温调节神经网络的激活,该神经网络会迅速减弱棕色脂肪组织产热以引起体温过低。缺乏类胰蛋白酶或TRPV1的小鼠表现出有限的IgE介导的过敏反应,并且在野生型小鼠中,过敏反应可以简单地通过全身激活TRPV1感觉神经元来概括。因此,除了对脉管系统的众所周知的作用外,肥大细胞产物,尤其是类胰蛋白酶,通过激活体温调节神经回路来促进IgE介导的过敏反应。
PAR2是胰酶受体,
蛋白酶激活受体(protease activated receptors, PARS)属于G蛋白偶联受体家族成员,胞外信号调节激酶(ERK1/2)信号转道通路, 引起细胞核反应, 激活多种细胞转录因子。它是细胞表面的一种G蛋白偶联受体,同样具有单链七次跨膜的共性。目前发现有4个受体即PAR1 ,PAR2,PAR3,PAR4.除了PAR2是胰酶受体,其他的三个都是凝血酶受体。它区别于其他G蛋白偶联受体的地方在于:一般的G蛋白偶联受体都是在被细胞外配体结合剪掉片段结合后引发G蛋白的磷酸化,然后自身也被磷酸化后进入细胞,再被磷酸化后和配体分离,再次运到细胞表面,重新使用。但是绝大多数PARs-配体复合物在进入细胞后被溶酶体消化降解,不再重新使用。
https://blog.sciencenet.cn/blog-41174-1380863.html
上一篇:慢性肾病患者的希望之光
下一篇:全扫描癌症突变的精准基因组编辑