博文
MCE 放射性核素rdc药物,开启肿瘤治疗新赛道_MedChemExpress
|
放射性核素-药物偶联物(RDCs)是核药物靶向治疗最有前景的发展方向之一。RDC 由靶向元素、连接体、螯合物和放射性同位素组成。RDC 在肿瘤早期诊断、治疗及术后肿瘤评估方面具有优势。同一配体可分别连接用于疾病诊断和治疗的核素,推动 RDC 药物诊疗一体化发展。
在肿瘤治疗进入精准化时代的今天,放射性核素偶联药物(Radionuclide Drug Conjugates, RDC)凭借“靶向导航+核素杀伤”的独特优势,成为继ADC药物之后,生物医药领域的又一研究热点,被医学界誉为抗癌“核导弹”,为晚期肿瘤患者带来了新的生存希望。
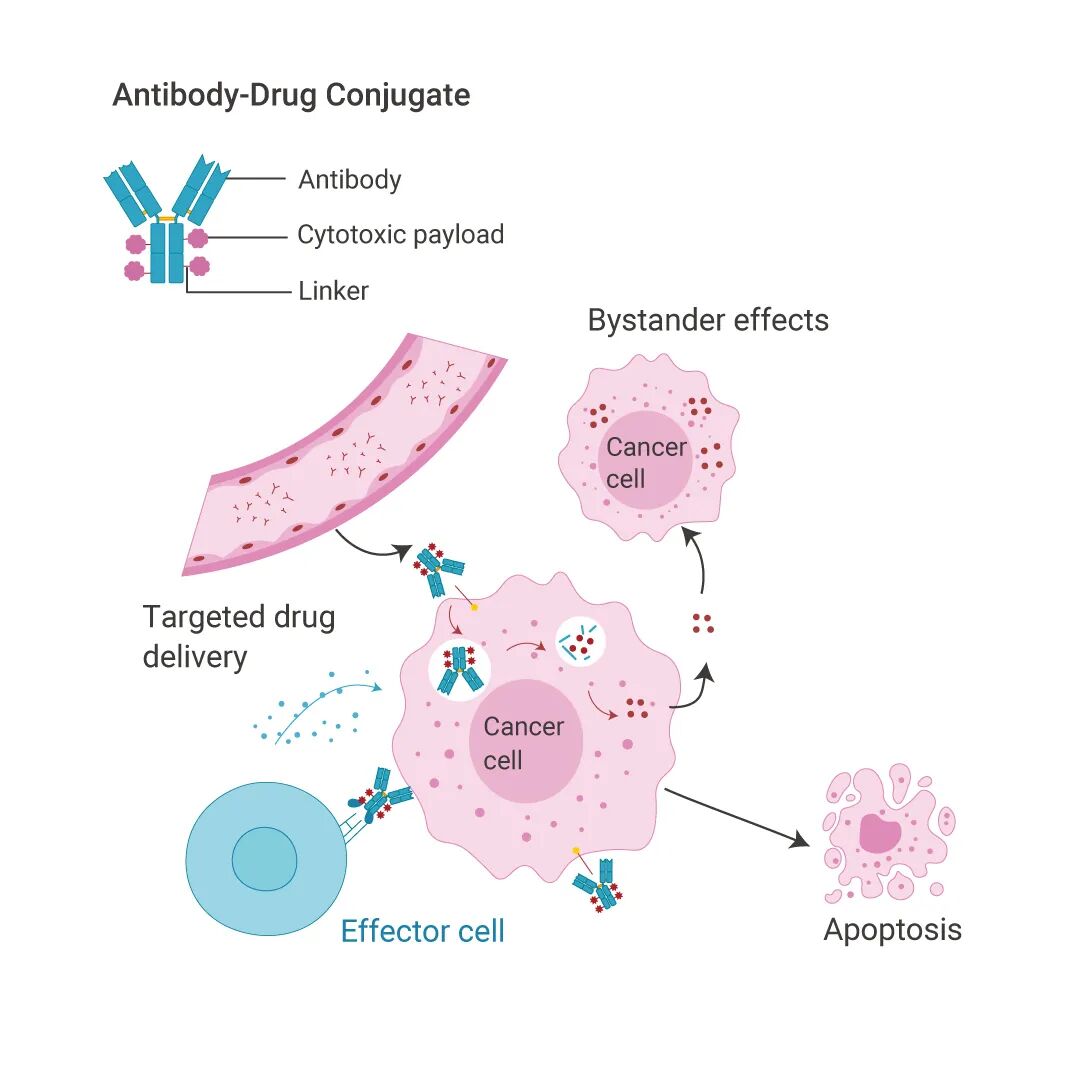
RDC药物的核心逻辑的是“精准投递、定向杀伤”,其结构由四大关键部分组成:介导靶向定位的载体(抗体、多肽或小分子)、连接臂、螯合物和放射性同位素,四者协同作用,实现对肿瘤细胞的精准打击而不损伤正常组织。与传统化疗的“地毯式轰炸”不同,RDC药物的靶向载体如同“GPS导航”,能精准识别肿瘤细胞表面的特异性靶点,将具有杀伤作用的放射性核素精准递送至肿瘤部位,再通过核素衰变释放的α射线、β射线或俄歇电子,利用电离辐射破坏肿瘤细胞DNA结构,从而抑制或杀死病变细胞,实现治疗目的。
根据功能差异,RDC药物可分为诊断用和治疗用两大类,完美实现“诊疗一体化”的临床需求。诊断用RDC主要利用单光子发射计算机断层成像(SPECT)或正电子发射体层成像(PET)技术,通过示踪核素(如68Ga、18F)揭示病变组织的位置、大小及代谢变化,为肿瘤诊断和治疗方案制定提供精准依据;治疗用RDC则选用具有强杀伤性的核素(如177Lu、锕-225),直接作用于肿瘤细胞,尤其适合晚期转移、化疗耐药的肿瘤患者,其中177LU-PSMA-617、锕-225-PSMA等药物在前列腺癌治疗中已展现出显著疗效。
相较于传统肿瘤治疗手段,RDC药物的优势尤为突出。其一,靶向性极强,能精准识别肿瘤细胞,减少对正常组织的损伤,大幅降低化疗、放疗带来的脱发、呕吐等副作用;其二,杀伤效率高,核素释放的射线射程短(仅几十微米),可集中作用于肿瘤细胞,实现“细胞级精准杀伤”,杀伤力是传统化疗的数百倍;其三,适配范围广,可针对不同肿瘤靶点(如PSMA、SSTR)设计专属药物,覆盖前列腺癌、神经内分泌瘤、肺癌等多种实体肿瘤,且能解决肿瘤异质性带来的耐药问题。
近年来,全球RDC药物研发迎来爆发期,多个药物已获得FDA批准上市,中国也在该领域加速追赶,研发进程成效显著。早在2005年,中国就成功上市国产RDC药物131I-chLym-1,用于中晚期肝癌治疗及术后复发预防;目前,国内已有8款RDC药物进入III期临床试验阶段,主要聚焦于前列腺癌、神经内分泌瘤等领域,其中ITM—11等创新药物还获得了FDA和EMA的孤儿药资格,有望快速实现临床转化。2026年,中国散裂中子源实现医用级阿尔法同位素居里级量产,彻底打破国外垄断,为RDC药物的国产化、规模化生产奠定了基础,也让这类精准抗癌药物有望降至亲民价格,惠及更多普通患者。
作为肿瘤精准治疗的重要方向,RDC药物不仅推动了核医学与肿瘤治疗的深度融合,更改写了晚期肿瘤的治疗格局。随着靶向载体优化、核素制备技术升级及联用策略的探索,RDC药物将在肿瘤诊疗一体化的道路上持续突破,有望成为更多晚期肿瘤患者的“救命稻草”,开启精准抗癌的全新篇章。
https://blog.sciencenet.cn/blog-3536222-1532303.html
上一篇:科研定制|MCE 实验动物饲料定制
下一篇:小分子精准抗癌新势力:多肽偶联药物PDC_MCE(MedChemExpress)
全部作者的其他最新博文
- • SMAD6抗体是IgG1 单克隆抗体_MCE(MedChemExpress)
- • Glepaglutide,914009-86-2 是一种 GLP-2R 激动剂_MCE(MedChemExpress)
- • Fmoc-Gly-OH-13C2,15N,285978-13-4 用于化合物合成_MCE(MedChemExpress)
- • Trimethylamine oxide-15N是 Trimethylamine N-oxide 的氘代物_MCE
- • L-Histidine-13C6 hydrochloride,L-组氨酸 13C6 , 201740-88-7_MCE
- • Citric acid-13C3,柠檬酸-13C3诱导 HaCaT 细胞凋亡_MCE(MedChemExpress)