博文
mLife |弯曲杆菌外排泵转运蛋白CmeB特定位点突变介导抗生素耐药的新机制
|

四川大学王红宁教授、唐艺芝副教授团队的文章“Antibiotic resistance mediated by site-specific mutations in the multidrug efflux transporter CmeB of zoonotic pathogen Campylobacter” 已在 mLife 上正式上线。该研究揭示了弯曲杆菌多重耐药外排泵转运蛋白 CmeB 通过特定位点突变介导抗生素耐药性的新机制。该团队通过自然转化及全基因组测序,鉴定出 CmeB 蛋白上的 T136A 和 M292I 突变。这些突变改变了药物结合口袋的结构,极大提升了细菌对氟苯尼考、环丙沙星等多种抗生素的排出效率,并能与 gyrA 突变协同作用,介导高水平耐药。该研究阐明了弯曲杆菌的适应性进化策略,为耐药性监测提供了新的潜在分子靶点。

弯曲杆菌(Campylobacter)是重要的食源性病原菌。随着抗生素在医疗和养殖领域的广泛使用,其耐药问题日益突出,已被美国疾病控制与预防中心(CDC)列为重点控制的公共卫生威胁。在弯曲杆菌中,CmeABC 多重耐药外排泵是介导抗生素外排的主要机制之一。已有研究表明,该外排泵的过表达或其天然变异体(如RE-CmeB)可导致耐药性产生,然而,关于其核心转运蛋白 CmeB 发生“获得性功能增强”点突变的研究仍较为有限。
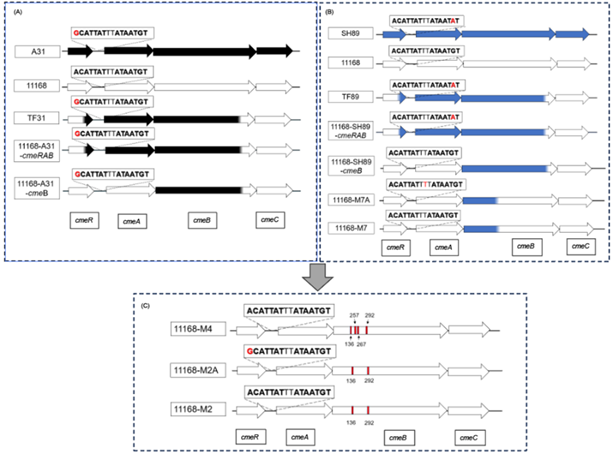
该研究在常规耐药性监测中,发现一株对氟苯尼考表现耐药、但缺乏已知耐药基因的弯曲杆菌天然分离株。通过自然转化和全基因组测序分析,鉴定出其 CmeB 药物结合口袋中存在两个关键氨基酸突变:T136A 和 M292I。功能验证表明,单独引入T136A 或 M292I 突变均无法介导耐药表型,而当二者同时存在时,可显著增强弯曲杆菌对氟苯尼考、环丙沙星、四环素等多种抗生素的耐药水平。进一步研究发现,该双突变与 gyrA 基因突变具有协同效应,可使环丙沙星的最小抑菌浓度(MIC)升高达512倍,导致极高水平的耐药。
蛋白质结构建模与分子动力学模拟显示,T136A 和M292I 突变不仅增强了 CmeB 与抗生素之间的疏水相互作用,稳定了结合复合物,同时减少了药物结合口袋的空间位阻,从而显著提升外排泵对药物的转运效率。基于NCBI数据库中对超过12万个基因组的深度挖掘,携带该双突变的弯曲杆菌分离株(共899株)已在全球35个国家广泛分布,宿主涵盖家禽、猪、牛及人类,提示该耐药机制已在全球多宿主环境中演化并传播。
引用本论文:Lin X, Zhao M, Gan J, Li H, He M, Yang F, et al. Antibiotic resistance mediated by site-specific mutations in the multidrug efflux transporter CmeB of zoonotic pathogen Campylobacter.mLife. 2026; 5: 83–98.
原文链接: https://doi.org/10.1002/mlf2.70051

mLife 期刊简介
mLife是由中国科学院主管、中国科学院微生物研究所主办(中国微生物学会为合作单位)的我国微生物学领域第一本综合性高起点英文期刊。mLife瞄准全球微生物学领域高水平科研成果和前沿进展,报道内容覆盖微生物学各个学科。mLife的办刊目标是打造微生物学领域综合性国际旗舰期刊。目前,mLife已被国内外重要数据库ESCI、PubMed、Scopus、CSCD、DOAJ、CAS、中国科技核心期刊等收录。mLife 2024年度JCR影响因子为4.5,位于微生物学科Q1区。
期刊网站:
https://wileyonlinelibrary.com/journal/mLife
https://www.sciopen.com/journal/2097-1699
投稿网站:
https://mc.manuscriptcentral.com/mlife
https://blog.sciencenet.cn/blog-3535224-1527911.html
上一篇:mLife | 生存博弈:原核生物防御系统的多样性与进化适应性
下一篇:mLife | 近两年mLife发表的文章哪些关注度高?