博文
生物类似药概述——医疗保健领域的开发、质量、监管问题和管理 | MDPI Pharmaceuticals
||
尽管目前对生物类似药的认识已显著提高,但关于其免疫原性、外推性、互换性、替代性和命名等方面仍存在诸多争议和误解。生物类似药的研发能够促进市场竞争,有助于医疗保健的可持续发展,并使更多患者获得治疗。然而,要最大限度地发挥生物类似药的优势,监管机构和研发者之间需要通力合作,以确保患者能够快速受益于这些新的治疗选择,同时保持高质量、安全性和有效性的标准。
葡萄牙科英布拉大学药学院药物技术系菲利帕·马斯卡雷尼亚斯-梅洛博士及其团队在Pharmaceuticals 发表的文章阐述了生物药品与生物类似药之间的区别,以及它们与预期仿制药、生物改良药和独立生物制剂之间的区别。我们将详细解释生物类似药获批所需的研发和监管方面的内容,包括分析相似性评估以及非临床和临床相似性评估。此外,它还重点关注生物类似药上市后的安全控制 (药物警戒) 以及仍然存在的与这些药物相关的争议 (免疫原性、外推性、互换性、替代性和命名)。
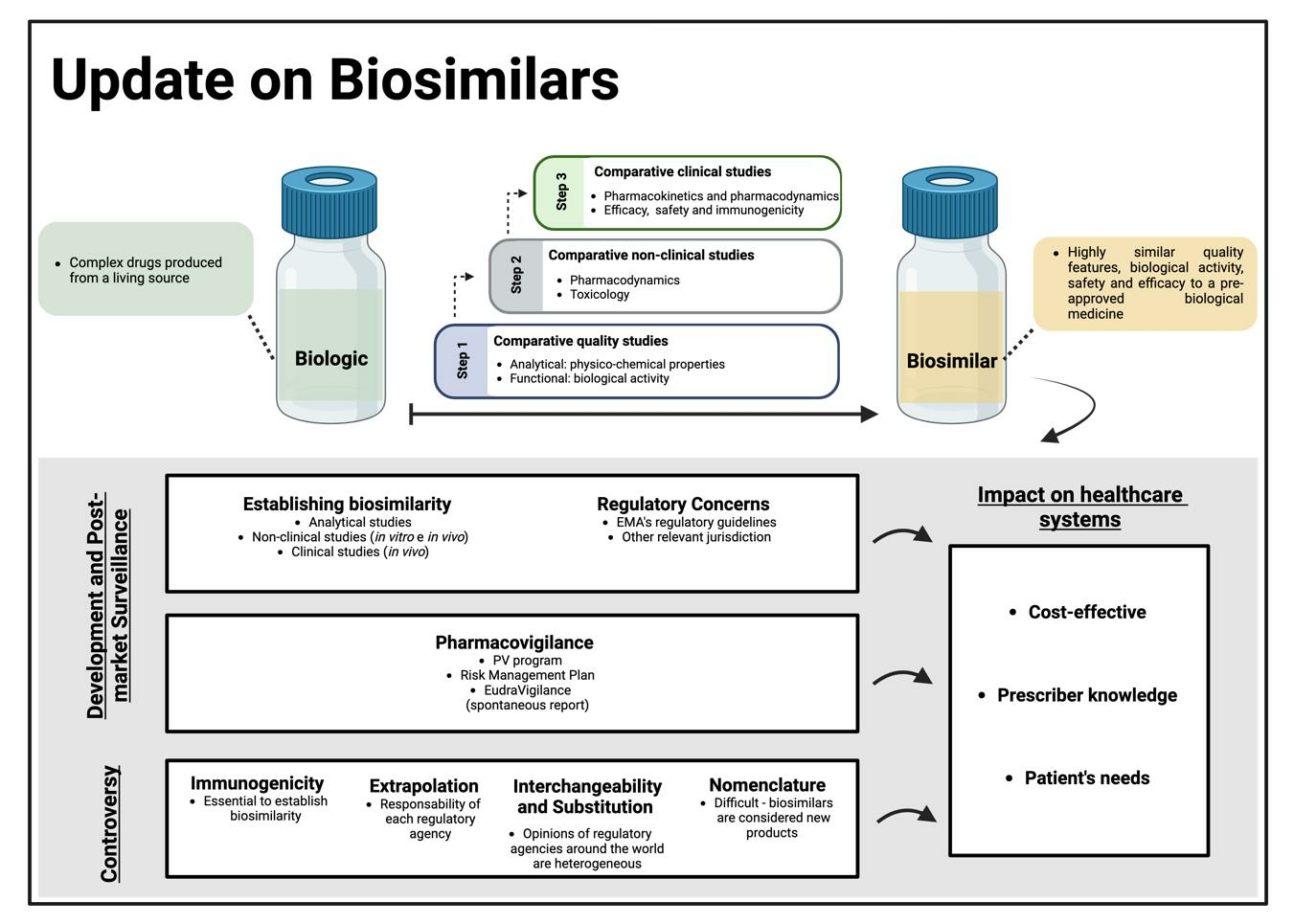
图1 图形摘要
研究过程与结果
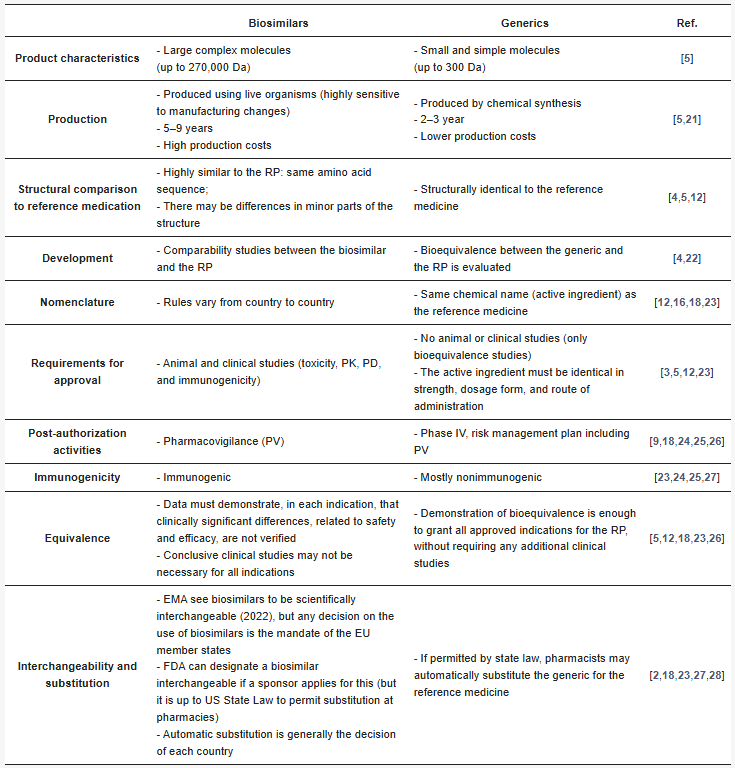
作者澄清说,生物类似药并非通用名药物的定义意义上的通用名药物——二者的区别见表1。通用名药物是化学合成的,与参考产品 (RP) 相同,而生物类似药是在活体生物中产生的大型复杂分子 (高达 270,000 DA)。生物类似药不应与仿制药、生物改良药和独立产品混淆,这些概念虽然相关,但完全不同。医生不应仅仅因为生物类似药价格低廉就推荐使用。这一决定应基于科学证据以及对二者差异的理解。本质上,这些药物是仿制药的生物对应物,可以归类为生物类似药。
表1. 生物类似药与仿制药的主要区别
如图2所示,生物类似药的研发和审批流程与新型创新药物 (化学或生物制剂) 的研发和审批流程存在显著差异。新型生物制剂侧重于通过大规模 III 期临床试验来验证其临床疗效,而生物类似药则侧重于分析方法上的相似性。
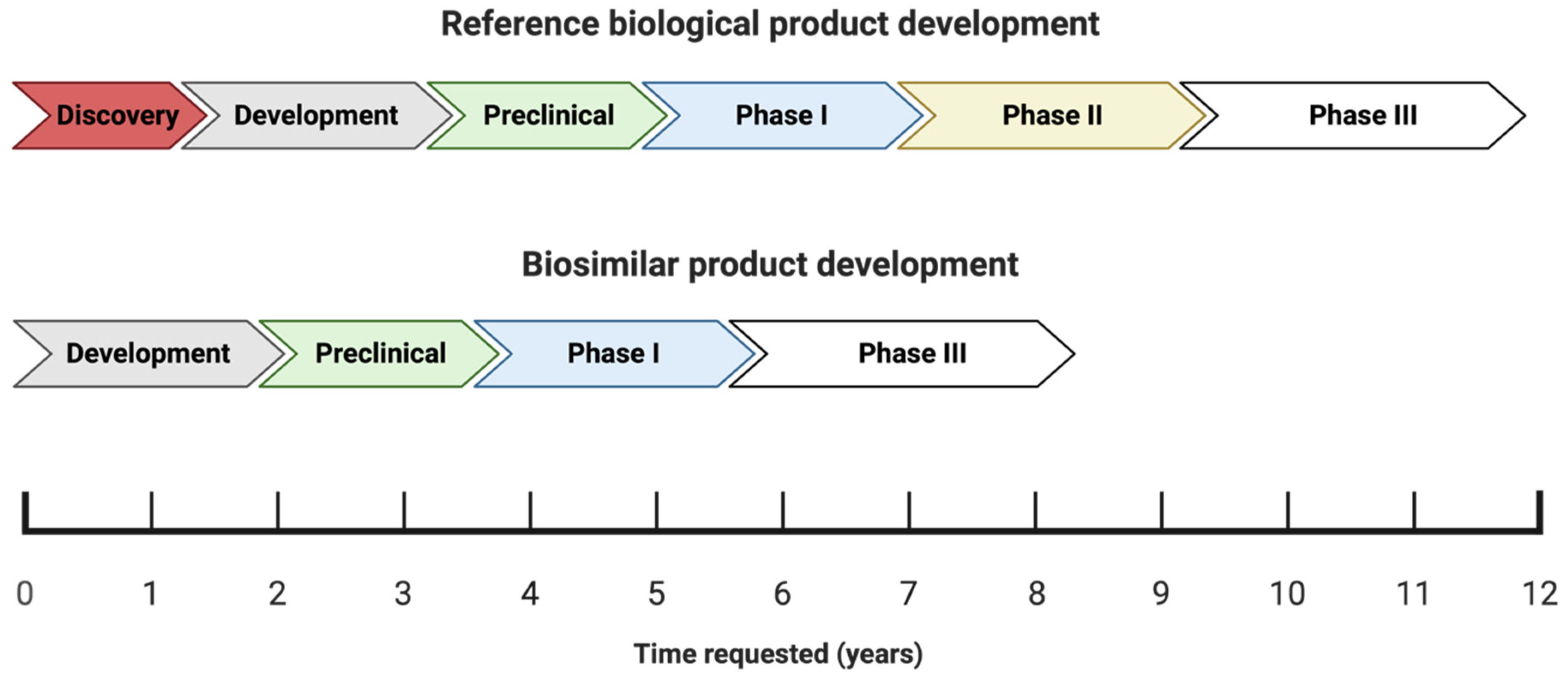
图2. 参考生物制剂与生物类似药的研发阶段及时间线 (以年为单位) 示意图
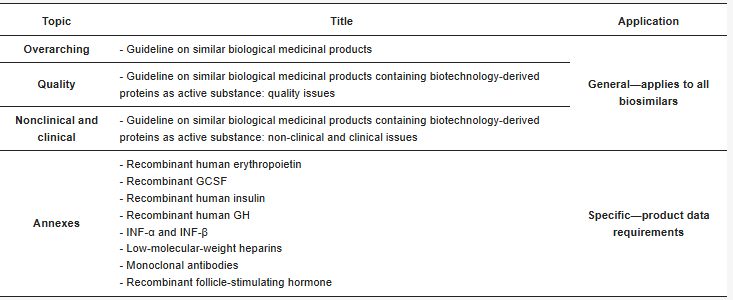
作者阐述,非临床可比性评估可以衡量生物类似药与参考药品在作用机制、功能活性和质量特性方面的相似程度。生物类似性的建立主要关注临床前研究,尤其是生物类似药的质量。因此,开展的临床研究的数量和范围取决于生物类似性的不确定性程度,而这种不确定性程度由先前的分析评估 (以及已开展的非临床体内试验,如有) 确定。欧洲药品管理局 (EMA) 和美国食品药品监督管理局 (FDA) 制定了具体且一致的监管指南,最终产品的批准必须遵循这些指南——EMA的指南见表2。然而,各监管机构之间存在差异,因此不同市场获批的生物类似药数量差异很大。欧洲药品管理局 (EMA) 于2003年率先建立了生物类似药审批体系。随后,在2006年,首个生物类似药 (Ominotrope®) 获得批准。近十年后,美国食品药品监督管理局 (FDA) 效仿EMA,采用了相同的原则,并于2015年批准了首个生物类似药。
表2. EMA关于生物类似药的开发和批准的监管指南
作者认为,从临床角度来看,上市后阶段必须持续监测产品的耐受性——这一点对于此类药物尤为重要,因为它们的疗效受多种因素影响,包括产生免疫反应的能力、超敏反应引起的不良反应、发生其他不良事件的可能性较高,以及生产工艺的易变性。因此,监测这些药物的耐受性至关重要,尤其是在儿科领域,因为儿童和成人的风险和合并症情况可能有所不同。
研究总结
本文基于现有报告,通过深入而严谨的讨论,更新并详细阐述了生物类似药的主要特性,以及其研发和审批过程中采用的监管与生产流程;同时探讨了生物类似药上市后的安全性监测及使用中存在的主要争议,为临床决策提供有价值的信息;此外,还提供了一个在医院环境中实施生物类似药的示例模式。全文汇集了有关生物类似药的最新且重要的内容与讨论。
阅读英文原文:https://www.mdpi.com/1424-8247/17/2/235
Pharmaceuticals 期刊介绍
主编:Amélia Pilar Rauter, Universidade de Lisboa, Portugal
期刊主题涵盖了药物化学、药理学、生物制药、药物递送、药物控释、药物制剂、天然产物、药代动力学和纳米医学等。目前期刊已被SCIE、Scopus和PubMed等数据库收录,位列JCR“药物化学”和“药理学与药学”两个学科领域Q1区。
2024 Impact Factor:4.8
2024 CiteScore:7.7
Time to First Decision:16 Days
Acceptance to Publication:3.4 Days
期刊主页:https://www.mdpi.com/journal/pharmaceuticals

https://blog.sciencenet.cn/blog-3516770-1530868.html
上一篇:Lubricants 中国矿业大学朱少禹博士和合肥工业大学孙军教授主持特刊:轴承润滑的多物理场建模
下一篇:从 “门槛”到“过程”:我们为什么要把发表挪到同行评审之前? | 预印本知多少(十七)
全部作者的精选博文
全部作者的其他最新博文
- • Metabolites 武汉纺织大学冯钰锜教授和朱泉霏教授主持特刊“质谱衍生化技术:解锁低丰度代谢组”
- • Nutrients:江苏大学陈震教授主持特刊"营养生物活性成分与脂质代谢疾病的综合探讨"
- • Processes:南京师范大学、西北工业大学、西安邮电大学学者共同创建特刊“电机及其驱动系统故障诊断与状态监测”
- • Electronics:西安交通大学、新疆大学、北京工业大学、西南交通大学学者共同创建特刊“下一代机器学习模型在状态监”
- • Cancers:苏州大学医学院程侠菊博士创建特刊"癌症治疗中的协同放疗和免疫疗法"
- • Information:重庆理工大学袁富江及其团队“联盟链PBFT共识算法的演化与优化策略”